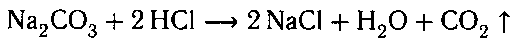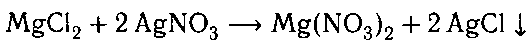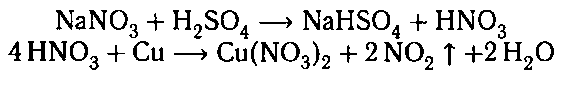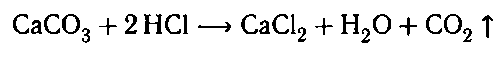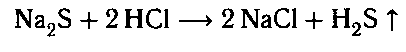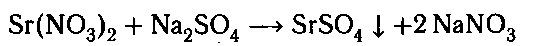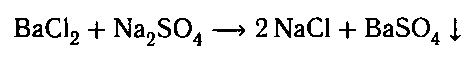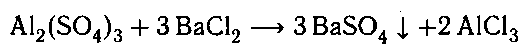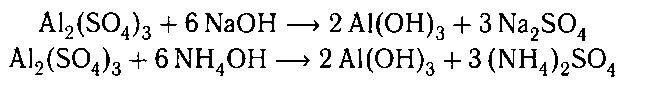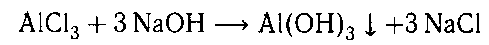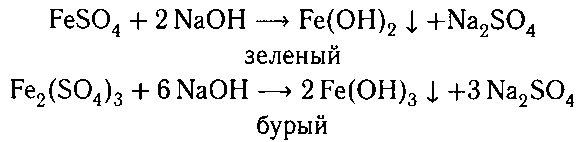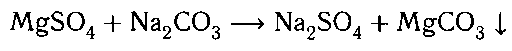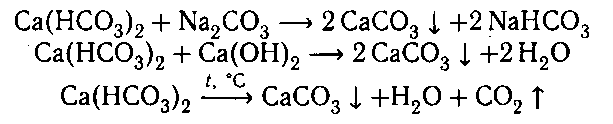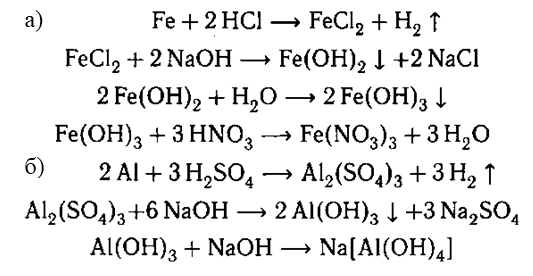- Сульфат алюминия способ распознавания
- Как написать хороший ответ?
- Сульфат алюминия способ распознавания
- Кто решил? Практическая работа 7 Химия 9 класс Рудзитис, Фельдман
- Сульфат алюминия, характеристика, свойства и получение, химические реакции
- Сульфат алюминия, характеристика, свойства и получение, химические реакции.
- Краткая характеристика сульфата алюминия:
- Физические свойства сульфата алюминия:
- Получение сульфата алюминия:
- Химические свойства сульфата алюминия. Химические реакции сульфата алюминия:
- Применение и использование сульфата алюминия:
Сульфат алюминия способ распознавания
Вопрос по химии:
Предложите способ распознавания солей: сульфат натрия, сульфат алюминия, сульфат железа(III). Приведите соответствующие уравнения реакций, укажите их признаки. Помогите пж.
Ответы и объяснения 1
Знаете ответ? Поделитесь им!
Как написать хороший ответ?
Чтобы добавить хороший ответ необходимо:
- Отвечать достоверно на те вопросы, на которые знаете правильный ответ;
- Писать подробно, чтобы ответ был исчерпывающий и не побуждал на дополнительные вопросы к нему;
- Писать без грамматических, орфографических и пунктуационных ошибок.
Этого делать не стоит:
- Копировать ответы со сторонних ресурсов. Хорошо ценятся уникальные и личные объяснения;
- Отвечать не по сути: «Подумай сам(а)», «Легкотня», «Не знаю» и так далее;
- Использовать мат — это неуважительно по отношению к пользователям;
- Писать в ВЕРХНЕМ РЕГИСТРЕ.
Есть сомнения?
Не нашли подходящего ответа на вопрос или ответ отсутствует? Воспользуйтесь поиском по сайту, чтобы найти все ответы на похожие вопросы в разделе Химия.
Трудности с домашними заданиями? Не стесняйтесь попросить о помощи — смело задавайте вопросы!
Химия — одна из важнейших и обширных областей естествознания, наука о веществах, их составе и строении, их свойствах, зависящих от состава и строения, их превращениях, ведущих к изменению состава — химических реакциях, а также о законах и закономерностях, которым эти превращения подчиняются.
Источник
Сульфат алюминия способ распознавания
В двух пробирках находился раствор сульфата алюминия. В первую пробирку добавили раствор вещества Х, а во вторую — раствор вещества Y. В обеих пробирках выпал осадок, но во второй пробирке он растворился при добавлении избытка вещества Y. В обоих опытах газ не выделялся.
Из предложенного перечня выберите вещества X и Y, которые могут вступать в описанные реакции.
1)
2)
3)
4)
5)
Запишите в таблицу номера выбранных веществ под соответствующими буквами.
Составим уравнения реакций.
При взаимодействии сульфата алюминия с раствором аммиака выпадает осадок гидроксида алюминия:
Веществом X является (5)
При взаимодействии сульфата алюминия с недостатком гидроксида калия также образуется осадок гидроксида алюминия:
В избытке гидроксида калия осадок растворяется:
Веществом Y является (3)
Источник
Кто решил? Практическая работа 7 Химия 9 класс Рудзитис, Фельдман
Решение экспериментальных задач.
1. В четырех пробирках даны следующие вещества в твердом виде: а) хлорид магния; б) гидроксид натрия; в) карбонат натрия; г) нитрат натрия. При помощи химических реакций определите, в какой пробирке находится каждое из этих веществ.
2. В четырех пробирках даны следующие твердые вещества: а) карбонат кальция; б) нитрат стронция; в) сульфат натрия; г) сульфид натрия. Определите, в какой пробирке находится каждое из перечисленных веществ.
3. При помощи характерных реакций докажите, что выданное вам вещество — сульфат алюминия.
4. В одной пробирке дан раствор хлорида натрия, во второй — раствор хлорида стронция, а в третьей — раствор хлорида алюминия. Определите, в какой пробирке находится каждое из выданных веществ.
5. Докажите, что кристаллы сульфата железа(II) частично окислились и содержат примеси ионов Fе 3+ .
6. В двух склянках дана вода. В одной из них вода содержит сульфат магния, а в другой — гидрокарбонат кальция. Проделайте опыты, при помощи которых можно устранить постоянную и временную жесткость.
7. Практически осуществите следующие превращения:
а) Fе → FеСl2 → Fе(ОН)2 → Fе(ОН)3 → Fе(NO3)3
б) Аl → Аl2(SO4)3 → Аl(ОН)3 → Na[Аl(ОH)4]
1. Добавляем раствор соляной кислоты. В пробирке с карбонатом натрия выделяется газ.
Оставшиеся вещества растворяем в воде и к
полученным растворам добавляем фенолфталеин.
В одной пробирке со щелочью раствор розовеет.
К оставшимся растворам добавляем раствор нит-
рата серебра. В пробирке с хлоридом магния обра-
зуется белый осадок.
К оставшемуся раствору добавляем концентри-
рованную серную кислоту и кусочек меди. Нагре-
ваем. Выделяется газ бурого цвета, что свидетель-
ствует о наличие нитрата натрия в пробирке:
2. Ко всем веществам добавляем раствор соляной
кислоты. В пробирке с карбонатом выделяется
углекислый газ:
В пробирке с сульфидом натрия выделяется газ
с запахом тухлых яиц — H2S.
После растворения оставшихся веществ в воде
добавляем раствор сульфата натрия.
В пробирке с нитратом стронция образуется
белый осадок.
К оставшемуся раствору добавляем раствор хло-
рида бария. Образуется белый осадок сульфата
бария:
3. К выданному веществу добавляем раствор
хлорида бария. Выпадает белый осадок, что свиде-
тельствует о наличии сульфат-иона.
При взаимодействии со щелочью или гидрокси-
дом аммония выпадает белый осадок гидроксида
алюминия:
4. Хлорид натрия окрашивает пламя горелки в
желтый цвет.
Хлорид стронция определяем по реакции с суль-
фатом аммония, в результате которой выделится
белый осадок: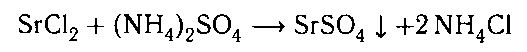
Хлорид алюминия доказываем реакцией с гид-
роксидом натрия
5. Растворяем кристаллы в воде и добавляем
раствор NaOH. Образуется зеленый и бурый осадки.
Если сульфат железа (II) содержал Fe3+, то в
зеленом осадке будут прожилки или пятна бурого
цвета.
6. В воду, содержащую MgSО4, добавляем рас-
твор Na2CО3. Образуется белый осадок.
Ионы Mg2+ обуславливают постоянную жест-
кость воды. Такую воду можно умягчить, добавив
раствор карбоната натрия, так как при этом проис-
ходит связывание ионов Mg2+.
В воду, содержащую Са(НСО3)2, добавляем:
раствор Na2CО3, известковое молоко, то есть насы-
щенный раствор Са(ОН)2; кипятим ее. Образуется
белый осадок.
Присутствие Са(НСО3)2 обуславливает времен-
ную жесткость воды. Эту воду можно умягчить
добавлением известкового молока, соды или кипя-
чением, так как все эти процессы сопровождаются
образованием СаСО3.
7.
Источник
Сульфат алюминия, характеристика, свойства и получение, химические реакции
Сульфат алюминия, характеристика, свойства и получение, химические реакции.
Сульфат алюминия – неорганическое вещество, имеет химическую формулу Al2(SO4)3.
Краткая характеристика сульфата алюминия:
Сульфат алюминия – неорганическое вещество белого цвета.
Химическая формула сульфата алюминия Al2(SO4)3.
Сульфат алюминия – неорганическое химическое соединение, соль серной кислоты и алюминия .
Хорошо растворяется в воде, этиленгликоле. Плохо растворим в этаноле.
С водой сульфат алюминия образует кристаллогидраты с различным содержанием воды Al2(SO4)3·nH2O, где n может быть вплоть до 18. Наиболее распространенными являются гексадекагидрат Al2(SO4)3·16H2O и октадекагидрат Al2(SO4)3·18H2O.
Устойчив при обычной температуре.
Сульфат алюминия пожаро- и взрывобезопасен. По степени воздействия на организм продукт относится к веществам 3-го класса опасности в соответствии с ГОСТ 12.1.005.
В земной коре сульфат алюминия находится как в свободном чистом состоянии, в форме кристаллогидратов, а также в составе двойных солей.
Сульфат алюминия в чистом состоянии распространён в природе в виде минерала миллозевичита. В форме кристаллогидратов сульфат алюминия встречается в природе в виде минерала алуногена Al2(SO4)3·17H2O.
Двойные соли сульфат алюминия образует с сульфатами ряда металлов, к которым, к примеру, относится и природный минерал алунит K2SO4·Al2(SO4)3·Al(OH)3.
В пищевой промышленности сульфат алюминия используется в виде добавки Е520.
Физические свойства сульфата алюминия:
| Наименование параметра: | Значение: |
| Химическая формула | Al2(SO4)3 |
| Синонимы и названия иностранном языке | aluminium sulphate (aluminum sulfate (англ.) |
алюминий сернокислый (рус.)
Получение сульфата алюминия:
В промышленности сульфат алюминия получается взаимодействием гидроксида алюминия с серной кислотой.
В лаборатории сульфат алюминия получают в результате следующих химических реакций:
- 1. взаимодействия сульфата меди и алюминия :
- 2. взаимодействия оксида алюминия и гидросульфата калия:
Химические свойства сульфата алюминия. Химические реакции сульфата алюминия:
Химические свойства сульфата алюминия аналогичны свойствам сульфатов других металлов . Однако, сульфат алюминия не реагирует с кислотами. Поэтому для него характерны следующие химические реакции:
1. реакция взаимодействия сульфата алюминия и гидроксида натрия :
В результате реакции образуются гидроксид алюминия и сульфат натрия.
2. реакция взаимодействия сульфата алюминия и гидроксида калия :
В результате реакции образуются гидроксид алюминия и сульфат калия.
3. реакция взаимодействия сульфата алюминия и гидроксида лития :
В результате реакции образуются гидроксид алюминия и сульфат лития.
4. реакция взаимодействия сульфата алюминия и нитрата бария:
В результате реакции образуются сульфат бария и нитрат алюминия .
5. реакция взаимодействия сульфата алюминия и нитрата свинца:
В результате реакции образуются сульфат свинца и нитрат алюминия.
6. реакция взаимодействия сульфата алюминия и фосфата натрия :
В результате реакции образуются фосфат алюминия и сульфат натрия.
7. реакция взаимодействия сульфата алюминия и фосфата калия :
В результате реакции образуются фосфат алюминия и сульфат калия.
8. реакция взаимодействия сульфата алюминия и гидрокарбоната натрия:
Al2(SO4)3 + 6NaHCO3 → 3Na2SO4 + 2Al(OH)3 + 6CO2.
В результате реакции образуются сульфат натрия, гидроксид алюминия и оксид углерода (IV).
9. реакция взаимодействия сульфата алюминия и гидрокарбоната кальция:
В результате реакции образуются сульфат кальция, гидроксид алюминия и оксид углерода (IV). Данная реакция используется для очистки воды. Гидроксид алюминия выпадает в осадок и его хлопья увлекают за собой различные примеси.
10. реакция взаимодействия сульфата алюминия и карбоната натрия и воды:
В результате реакции образуются сульфат натрия , гидроксид алюминия и оксид углерода (IV).
11. реакция термического разложения сульфата алюминия:
В результате реакции образуются оксид алюминия, оксид серы (IV) и кислород .
12. реакция термического разложения октадекагидрата сульфата алюминия:
Октодекагидрат сульфата алюминия разлагается на сульфат алюминия и воду.
Применение и использование сульфата алюминия:
Сульфат алюминия используется во множестве отраслей промышленности и для бытовых нужд:
– как коагулянт для очистки воды хозяйственно-питьевого и промышленного назначения;
– в фотографии входит в составы стабилизирующих растворов и дубящих фиксажей;
– как пищевая добавка Е520;
– в качестве морилки при крашении и печати текстильных изделий;
– в бумажной, текстильной, кожевенной и других отраслях промышленности.
Источник