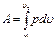Energy
education
сайт для тех, кто хочет изучать энергетику
Термодинамика и тепломассообмен
Идеальный газ
Идеальный газ — математическая модель газа, в которой предполагается, что потенциальной энергией молекул можно пренебречь по сравнению с их кинетической энергией. Между молекулами не действуют силы притяжения или отталкивания, соударения частиц между собой и со стенками сосуда абсолютно упруги, а время взаимодействия между молекулами пренебрежимо мало по сравнению со средним временем между столкновениями.
4. Процессы изменения состояния идеальных газов
К основным термодинамическим процессам относят следующие четыре процесса:
- изохорный – при постоянном объеме ($v = const$);
- изобарный – при постоянном давлении ($р = const$);
- изотермический – при постоянной температуре ($Т = const$);
- адиабатный – без теплообмена с внешней средой ($\mathrm
q = 0$).
В реальных условиях указанные ограничения практически не выполняются. В связи с этим в технической термодинамике существует понятие политропного процесса как общего случая термодинамического процесса. Предполагается, что политропный процесс обратим и теплоемкость рабочего тела (идеального газа) $с_n$ в ходе данного процесса не изменяется ($c_n=const$). Уравнение политропного процесса имеет вид:
где $n=\frac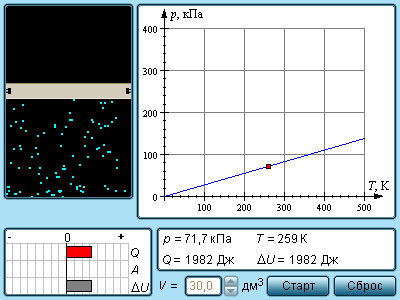
Изобарный процесс – термодинамический процесс, происходящий в системе при постоянном давлении. Параметры состояния идеального газа на изобаре связаны соотношением:
Отсюда следует, что чем выше температура газа, тем больше его удельный объем (т.е. тем меньше плотность). При этом величина v на изобаре при повышении температуры растет тем быстрее, чем меньше давление.
Работа расширения системы в изобарном процессе определяется следующим образом:
Для идеального газа работа расширения системы в изобарном процессе может быть представлена также в следующем виде:
Количество теплоты, сообщаемой системе при нагреве (или отдаваемой системой при охлаждении) в изобарном процессе, определяется следующим образом:
$$\mathrm
Изменение энтропии в изобарном процессе, т.е. разность энтропий, соответствующих состояниям 1 и 2, определяется из соотношения:
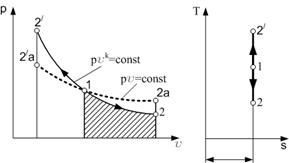
Изотермический процесс – процесс изменения состояния термодинамической системы при постоянной температуре.
Для идеального газа давления и объемы в любых точках на изотерме связаны уравнением Бойля—Мариотта, т.е. зависимость объема от давления на изотерме для идеального газа имеет характер гиперболы:
Работа расширения системы в изотермическом процессе между точками изотермы 1 и 2 определяется с помощью общего соотношения:
Количество теплоты , подводимой к системе (или отдаваемой системой) в изотермическом процессе, определяется из известного соотношения:
Количество работы, совершаемой идеальным газом в изотермическом процессе, равно количеству теплоты, подведенной к этому газу:
Изменение энтропии в изотермическом процессе, т.е. разность энтропий, соответствующих состояниям 1 и 2, вычисляется следующим способом:
Адиабатный процесс – такой термодинамический процесс, в котором к системе не подводится и от системы не отводится теплота. Термодинамическую систему, в которой протекает адиабатный процесс, можно представить себе в виде некоторого объема, ограниченного оболочкой, снабженной идеальной теплоизоляцией, абсолютно не пропускающей теплоту. В реальных условиях процесс является адиабатным в тех случаях, когда система снабжена хорошей теплоизоляцией или когда процесс расширения (сжатия) газа происходит настолько быстро, что не успевает произойти скольконибудь заметный теплообмен газа с окружающей средой.
Поскольку для обратимого процесса $\mathrm
Для любого состояния системы в изоэнтропном процессе справедливо соотношение Пуассона:
Если показатель изоэнтропы $k$ изменяется с изменением состояния системы и известен характер зависимости $k$ на изоэнтропе, то для расчета величины $p_2$ по известным $p_1$, $v_1$ и $v_2$ следует вычислить интеграл, стоящий в правой части по известным значениям $k$.
Для идеального газа показатель изоэнтропы $k$ можно определить:
Так как для идеального газа $c_p=c_v+µR$, тогда:
Как известно, теплоемкости идеального газа слабо изменяются с температурой, поэтому и величину $k$ с высокой степенью точности можно считать практически не зависящей от температуры. Известно, что мольная изохорная теплоемкость $μс_v$ идеального газа равна примерно $13$ кДж/(кмоль·К) для одноатомного идеального газа, $21$ кДж/(кмоль·К) для двухатомного и $29$ кДж/(кмоль·К) для трех- и многоатомного газа. Поскольку $µR≈8.3$ кДж/(кмоль·К), то получаем следующие примерные значения показателя изоэнтропы $k$ идеального газа: одноатомный $k=1.67$, двухатомный $k=1.40$, трех- и многоатомный $k=1.29$. Для воздуха показатель изоэнтропы в идеально-газовом состоянии равен примерно $1.40$.
Для изоэнтропного процесса в идеальном газе можно получить соотношения, связывающие между собой значения $p$, $Т$ и $v$:
Работа расширения системы в изоэнтропном процессе определяется следующим образом:
Таким образом, в адиабатном процессе работа расширения системы совершается за счет убыли внутренней энергии системы. Это и понятно – ведь в адиабатном процессе к системе нет притока теплоты извне и единственный источник энергии для совершения работы – внутренняя энергия самой системы.
В случае идеального газа уравнения для расчета работы расширения могут быть представлены также в иной форме:
Следует подчеркнуть, что уравнение выше пригодно для расчета в том случае, если в интервале параметров между точками 1 и 2 показатель изоэнтропы $k$ сохраняется постоянным.
Политропные процессы. Политропными называют термодинамические процессы, удовлетворяющие уравнению:
при произвольном, постоянном для данного процесса значении $n$.
Понятие о политропных процессах было введено в термодинамике по аналогии с понятием об адиабатных процессах. Уравнение политропного процесса по внешнему виду сходно с уравнением адиабаты, однако существенная разница между этими уравнениями состоит в том, что если показатель изоэнтропы (адиабаты) $k$ является в общем случае величиной переменной, то уже само понятие политропного процесса основано на предположении о том, что показатель политропы n является постоянной величиной. В политропном процессе к системе может подводиться (или отводиться от нее) теплота.
Понятие о политропных процессах широко используется главным образом при изучении процессов сжатия и расширения в газовых двигателях, зачастую политропные процессы оказываются удобными для аппроксимации действительных газовых процессов в двигателях. Реальные процессы сжатия в газовых двигателях и компрессорах часто не являются ни адиабатными, ни изотермическими, а занимают промежуточное положение между этими двумя видами процессов. Поэтому обычно встречаемые на практике значения показателя n политропного процесса лежат в интервале от $1$ до $k$.
Если политропный процесс осуществляется в идеальном газе, то нетрудно получить зависимости между начальными и конечными параметрами процесса:
Работа расширения системы в политропном процессе между точками 1 и 2 определяется с помощью уравнения:
Это уравнение можно преобразовать в вид:
Количество теплоты , подводимой к системе (или отводимой от нее) в политропном процессе можно определить с помощью уравнения первого закона термодинамики:
Тогда теплоемкость идеального газа в политропном процессе:
Изменение энтропии системы в политропном процессе, т.е. разность энтропий, соответствующих точкам 1 и 2 на политропе, определяется из соотношения:
Для того чтобы определить значение показателя политропы для того или иного конкретного газового процесса, надо располагать экспериментальными данными для этого процесса.
Администратор сайта: Колосов Михаил
email:
Copyright © 2011-2021. All rights reserved.
Источник
Процессы изменения состояния идеальных газов
Исследования термодинамических процессов, происходящих под влиянием тех или иных причин, проводятся по двум направлениям:
1) устанавливают закономерность изменения состояния газа;
2) выявляют особенности превращения энергии.
При изучении изменения состояния газа: 1 — выводят уравнение процесса и устанавливают соотношения между параметрами состояния газа; 2 — определяют количество теплоты, подводимой к газу, изменение его внутренней энергии и внешнюю работу, совершаемую газом.
Часто встречаются такие процессы изменения состояния газов, которые протекают в условиях, ограничивающих характер изменения их состояния, например процессы, происходящие:
1) при постоянном объеме рабочего тела (изохорный);
2) при постоянном давлении рабочего тела (изобарный);
3) при постоянной температуре рабочего тела (изотермический);
4) при отсутствии теплообмена между рабочим телом и внешней средой (адиабатный).
Изохорный процесс
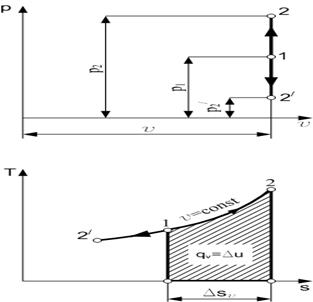
Примером изохорного процесса может быть нагревание или охлаждение газа в закрытом сосуде. Уравнение процесса будет иметь вид v = const. Если точка 1 характеризует начальное состояние газа, то при нагревании конечное состояние газа, в соответствии с законом Шарля, будет характеризоваться точкой 2, расположенной выше точки 1, а при охлаждении — точкой 2′, расположенной ниже точки 1 (рис. 1.2).
Рис. 1.2. Изохорный процесс изменения состояния газа в p-v- и T-s-диаграммах
Если v = const, то dv = 0, и тогда Аv определяется так:
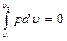
Это значит, что в изохорных процессах теплота, сообщаемая газу, идет только на увеличение его внутренней энергии, а отвод теплоты возможен только за счет уменьшения внутренней энергии, то есть
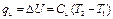
При наличии М, кг, или V, м 3 , газа
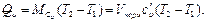
Изменение энтропии в изохорном процессе определяют по равенству
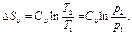
В T-s-диаграмме это уравнение изображается логарифмической кривой, направленной выпуклостью к оси абсцисс (рис. 1.2.). В процессе 1-2 энтропия возрастает, следовательно, теплота сообщается газу и он нагревается, а в процессе 1-2′ картина противоположная. Площадь под кривой процесса графически изображает количество теплоты qv.
Изобарный процесс
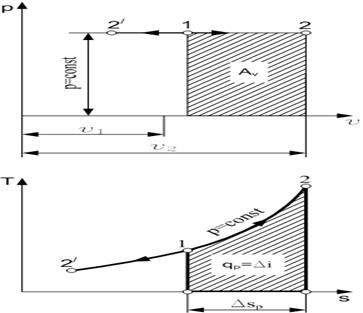
Уравнение изобарного процесса в p-v-координатах р = const, а его график в p-v-диаграмме — это горизонтальная прямая линия (рис. 1.3).
Если точка 1 характеризует начальное состояние газа, процесс изобарного расширения будет представлен линией 1-2, а изобарного сжатия — линией 1-2′.
В соответствии с законом Гей-Люссака для процесса 1-2 можно написать

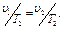
Изменение внутренней энергии идеального газа в изобарных процессах определяют по формуле (1.13), а внешнюю работу газа — по общей формуле для работы расширения газа
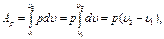
или 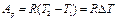
Если допустить, что в изобарном процессе 1 кг газа нагревается на 1 градус, то Ар = R.
Отсюда видно, что газовая постоянная R представляет собой работу, производимую в изобарном процессе 1 кг газа при его нагревании на 1 градус.
Теплота, сообщаемая газу в изобарном процессе, может быть выражена через теплоемкость cv уравнением
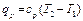
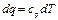
При наличии М, кг, или V, м 3 , газа
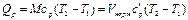
Рис. 1.3. Изобарный процесс изменения состояния газа в p-v- и T-s-диаграммах
Изменение энтропии для процесса р = const определяется по равенству
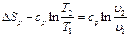
В T-s-диаграмме это уравнение изображается логарифмической кривой, направленной выпуклостью к оси абсцисс (рис. 1.3). В процессе 1-2 энтропия возрастает, т. е. теплота сообщается газу. Количество подведенной теплоты графически изображается площадью под кривой процесса.
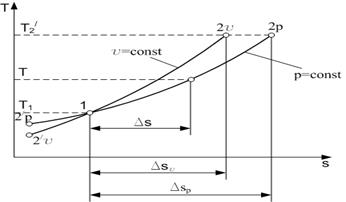
Из сопоставления уравнений (1.10) и (1.13) следует, что для одинакового интервала изменения температур (от Т1 до Т2) ∆sp > ∆sv, так как ср > сv.
Это означает, что в T-s-диаграмме изохора всегда круче изобары (рис. 1.4).
В соответствии с уравнением первого закона термодинамики 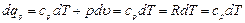
Сокращая на AT обе части равенства, получим уравнение Майера
Рис. 1.4. Изохорный и изобарный процессы в T-s-диаграмме.
Если уравнение первого закона термодинамики для процесса р = const написать в виде
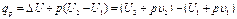
то получим 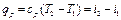
и 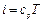
Формула (1.23) показывает, что теплота, сообщаемая идеальному газу в изобарном процессе, увеличивает его энтальпию. В дифференциальной форме уравнение для идеального газа принимает вид
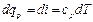
Это уравнение можно получить также исходя из математического определения энтальпии i.
Действительно, поскольку i = U + pv 
то, заменяя pv = RT, получим
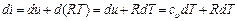
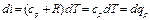
Уравнение (1.24) показывает, что di представляет собой элементарное количество теплоты, сообщаемой телу при нагревании в изобарном процессе, поэтому величину i назвали энтальпией (от греческого слова enthalpo — нагревание).
В теплотехнических расчетах всегда необходимо знать изменение энтальпии, поэтому начало ее отсчета не имеет значения. Вообще же его принимают при 0 К или 0 °С.
Изотермический процесс
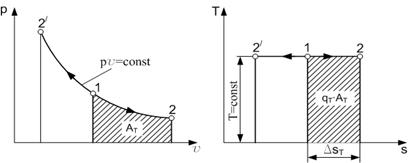
Уравнение этого процесса для идеального газа выражает закон Бойля-Мариотта (pv = const). График изотермического процесса в pv-диаграмме, как показывает его уравнение, будет изображаться равнобокой гиперболой, называемой изотермой. В T-s-диаграмме изотерма является прямой, параллельной оси абсцисс (рис. 1.5).
Процесс расширения 1-2 в T-s-диаграмме изображается прямой, идущей вправо, поскольку расширение газа при постоянной его температуре возможно лишь при подводе теплоты к газу.
Рис. 1.5. Изотермический процесс изменения состояния газа T-s-диаграммах.
Работа процесса Ат может быть определена из общего выражения для работы газа при его расширении
Заменяя по уравнению состояния газа р = RT/v, находим
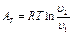
Количество теплоты qт в T-s-диаграмме изображается площадью прямоугольника с высотой Т и основанием ∆sт, т. е. q т = T∆sт, где изменение энтропии ∆sт можно найти из уравнений (1.28) и (1.29) при подстановке Т1 = Т2, что дает:
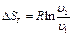
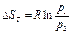
Тогда 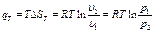
Так как изменение внутренней энергии ∆ U в изотермическом процессе идеального газа равно нулю, то Ат = qт .
Адиабатный процесс
Адиабатными, как уже отмечалось, называются процессы изменения состояния, происходящие без подвода и отвода теплоты от газа, т. е. когда dq = 0. При этом и q = 0. Однако не всякий процесс, для которого q = 0, будет адиабатичен. Есть процессы, на одной стадии которых теплота подводится, а на другой в том же количестве отводится.
Рис. 1.6. Адиабатный процесс изменения состояния газа
в p-v- и T-s-диаграммах.
Таким образом, необходимым и достаточным условием адиабатного процесса является аналитическое выражение dq = 0, означающее, что в процессе совершенно отсутствует теплообмен. При dq = 0 и Tds = 0, т. е. ds = 0, а это значит, что для обратимых адиабатных процессов s = const. Обратимый адиабатный процесс является в то же время изоэнтропным и в T-s-диаграмме обратимая адиабата будет графически изображаться прямой линией, параллельной оси Т. Площадь под кривой процесса будет отсутствовать, т. е. q = 0 (рис. 1.6).
Политропный процесс
Политропными называют процессы, в которых теплоемкость имеет любое, но постоянное на протяжении всего процесса значение. Следовательно, в любом политропном процессе распределение теплоты между значениями, характеризующими изменение внутренней энергии и работу газа, остается неизменным, т. е. отношение dU / dq = cvdT / cdT = cv / c = const, где с — постоянная для данного процесса теплоемкость газа. Уравнение для политропного процесса изменения состояния газа получают из уравнения первого закона термодинамики:
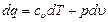
Уравнение политропного или обобщающего процесса изменения состояния газа
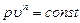
Величина n = (с — ср)/(с — с v ) называется показателем политропы. В том, что политропный процесс действительно является обобщающим, нетрудно убедиться, представив все рассмотренные ранее процессы как частные случаи процесса pv n = const. Например, для изобарного процесса уравнение политропы преобразуется в уравнение р = const при n = 0; для изотермы идеального газа n = 1 (pv = const при Т = const); для адиабатного процесса n = k (pv k = const) и, наконец, для изохорного процесса n = ± ∞.
3. Контрольные вопросы по первой теме
1. Что изучают в дисциплине «Теплотехника и энергетические машины»?
2. Что изучают в технической термодинамике?
3. Что такое термодинамическая система?
4. Перечислить основные термодинамические параметры.
5. Взаимосвязь плотности и удельного объема.
6. Назвать единицы измерения температуры.
7. Формула, показывающая взаимосвязь температуры в градусах Цельсия и градусах Кельвина.
8. Из чего состоит энергия рабочего тела, как ее вычисляют?
9. Назвать нормальные физические условия.
10. Написать уравнение Менделеева-Клапейрона для произвольной массы m.
11. Понятие об удельной теплоемкости, единицы ее измерения.
12. Как вычислить количество теплоты, подведенной к телу при изменении его температуры?
13. Понятие об идеальном газе и причинах его использования.
14. Что такое парциальное давление газа в смеси?
15. Математическое выражение закона Дальтона.
16. Какие процессы называют равновесными?
17. Какие процессы называют обратимыми?
18. Перечислить основные термодинамические процессы изменения состояния газа.
19. Что такое изохорный процесс изменения состояния газа, как выглядят графики для него в p-v- и T-s-диаграммах?
20. Что такое изобарный процесс изменения состояния газа, как выглядят графики для него в p-v- и T-s-диаграммах?
21. Что такое изотермический процесс изменения состояния газа, как выглядят графики для него в p-v- и T-s-диаграммах?
22. Что такое адиабатный процесс изменения состояния газа, как выглядят графики для него в p-v- и T-s-диаграммах?
23. Что такое политропный процесс изменения состояния газа, какая формула его описывает?
24. Что такое энтальпия?
25. Написать уравнение Майера. Что оно показывает?
26. Физический смысл универсальной газовой постоянной R .
Источник