- Микробиота, мукозальный иммунитет и антибиотики: тонкости взаимодействия
- Введение
- Мукозальный иммунитет и сигнальные рецепторы врожденного иммунитета
- Микробиота: иммунологические механизмы симбиоза
- Состав
- Функции
- Взаимодействие микробиоты и МАЛТ
- Антибиотики и иммуносупрессия
- Варианты преодоления иммуносупрессии, вызванной антибиотиками
- Трансплантация фекальной микробиоты (ТФМ)
- Использование пробиотиков
- МАМР и их минимальные биологически активные фрагменты (МБАФ)
- Заключение
Микробиота, мукозальный иммунитет и антибиотики: тонкости взаимодействия
*Пятилетний импакт фактор РИНЦ за 2020 г.
Читайте в новом номере
В барьерных тканях (слизистые и кожа) расположена многоуровневая система защиты организма от чужеродных инфекционных и химических агентов, получившая название «мукозоассоциированная лимфоидная ткань» (МАЛТ). Она включает в себя гуморальные факторы и клетки врожденного и адаптивного иммунитета, а также неиммунные механизмы защиты. Одним из важных компонентов защиты барьерных тканей является микробиота, комменсалы которой, с одной стороны, осуществляют метаболическую функцию и прямую противопатогенную активность, а с другой — постоянно стимулируют МАЛТ на разных уровнях и, таким образом, поддерживают иммунитет барьерных тканей в состоянии «тлеющей» активации и готовности к быстрому ответу на вторжение чужеродных организмов или веществ. Антибиотики, являясь одними из наиболее часто назначаемых лекарственных препаратов, нарушают количество, состав и активность симбиотических микроорганизмов. Как следствие, происходит ослабление иммунитета барьерных тканей, что способствует заселению слизистых и кожи патогенными микроорганизмами и, в частности, их антибиотикорезистентными штаммами. Осознание этого факта требует изменения тактики назначения антибиотиков и введения дополнительных лекарственных препаратов с целью поддержания активности МАЛТ. Препаратами — кандидатами на дополнение к этиотропной противоинфекционной терапии являются паттерны симбиотических микроорганизмов (microbial-associated molecular patterns (МАМР)) или, что более реально с точки зрения фармакологии, их минимальные биологически активные фрагменты (МБАФ).
Ключевые слова: мукозальный иммунитет, микробиота, антибиотики, иммуносупрессия, инфекции, антибиотикорезистентность, иммуномодуляция, заместительная терапия.
Для цитирования: Козлов И.Г. Микробиота, мукозальный иммунитет и антибиотики: тонкости взаимодействия. РМЖ. 2018;8(I):19-27.
Microbiota, mucosal immunity and antibiotics: the fineness of the interaction
I.G. Kozlov
D. Rogachev National Medical Research Center for Pediatric Hematology, Oncology and Immunology, Moscow
There is a multi-level system for protecting the body from foreign infectious and chemical agents, known as «mucosa-associated lymphoid tissue» (MALT), in the barrier tissues (mucosa and skin). It includes humoral factors and cells of congenital and adaptive immunity, as well as non-immune defense mechanisms. One of the important components of protecting barrier tissues is the microbiota, whose commensals, on the one hand, carry out metabolic function and direct anti-pathogenic activity, and, on the other hand, constantly stimulate MALT at different levels and, thus, support the immunity of barrier tissues in the state of «smoldering activation” and readiness for a rapid response to the invasion of foreign organisms or substances. Antibiotics, being one of the most frequently prescribed medications, disrupt the number, composition and activity of symbiotic microorganisms. As a consequence, the immunity of barrier tissues is weakened, which contributes to the colonization of mucous and skin by pathogenic microorganisms and, in particular, their antibiotic-resistant strains. Awareness of this fact requires a change in the tactics of prescribing antibiotics and the introduction of additional medications to maintain MALT activity. Candidate drugs to supplement etiotropic anti-infective therapy are microbial-associated molecular patterns (MAMP) or, that is more real from the pharmacologycal point of view, their minimal biologically active fragments (MBAF).
Key words: mucosal immunity, microbiota, antibiotics, immunosuppression, infections, antibiotic resistance, immunomodulation, replacement therapy.
For citation: Kozlov I.G. Microbiota, mucosal immunity and antibiotics: the fineness of the interaction // RMJ. 2018. № 8(I). P. 19–27.
Обзорная статья посвящена тонкостям взаимодействия микробиоты, мукозального иммунитета и антибиотиков
Введение
Мукозальный иммунитет и сигнальные рецепторы врожденного иммунитета
На протяжении всего развития иммунологии мукозальный иммунитет (иммунитет слизистых и кожи, иммунитет барьерных тканей) привлекал внимание исследователей и особенно врачей. Это обусловлено тем, что подавляющее большинство иммунных ответов происходит именно в барьерных тканях, которые находятся под непрерывной антигенной нагрузкой вследствие попыток проникновения в организм патогенных микроорганизмов и ксенобиотиков (посторонних или чужеродных веществ с иммуногенными свойствами).
При этом вполне физиологические иммунные реакции, направленные на поддержание гомеостаза организма, почти всегда сопровождаются воспалительным ответом (собственно воспаление является неотъемлемой частью успешной реализации иммунитета) и другой негативной с точки зрения пациента симптоматикой, что приводит его к необходимости искать помощи у врача. Насморк, кашель, боль в горле, диарея и диспепсия, воспаление кожных покровов, с одной стороны, и аллергические реакции, с другой, – возникновение всех этих проблем не обходится без участия мукозального иммунитета, они являются наиболее частыми причинами обращения к врачам различных специальностей. Как ни странно, несмотря на разную локализацию и достаточно разные проявления, в основе патогенеза всех этих состояний (и многих других) лежат одни и те же механизмы активации мукозального иммунитета.
Иммунитет слизистых реализуется через единую структурированную систему, получившую название «мукозоассоциированная лимфоидная ткань» (МАЛТ) (mucosa-associated lymphoid tissue — MALT). Структуризация МАЛТ идет по этажам в зависимости от того, где анатомически размещается та или иная барьерная ткань:
TALT — носоглотка, евстахиева труба, ухо.
NALT — носовая полость, рот и ротоглотка, конъюнктива.
BALT — трахея, бронхи, легкие, грудные железы (у женщин).
GALT — 1) пищевод, желудок, тонкий кишечник;
2) толстый кишечник и проксимальные отделы урогенитального тракта; дистальные отделы урогенитального тракта.
SALT — кожа (дерма).
МАЛТ — это самая большая часть иммунной системы, где на общей площади 400 м 2 располагаются около 50% иммунокомпетентных клеток. Здесь представлены клетки как врожденного иммунитета, так и приобретенного. Кроме клеток в МАЛТ сконцентрированы и другие механизмы защиты [1].
В любой части МАЛТ механизмы защиты имеют сходную организацию (хотя есть и различия между этажа-
ми) [2–6]:
Верхний «инертный» барьер представляет собой слой слизи или, в случае кожи, «сухой» слой, состоящий из кератина. Основные защитные факторы, представленные на этом уровне, — это физический барьер, противомикробные пептиды, секреторный IgA, компоненты системы комплемента и микробиота. Очевидно, что инертность этой структуры весьма условна, т. к. здесь постоянно протекают активные реакции киллинга микроорганизмов и множество биохимических процессов метаболической направленности.
Эпителиальный пласт долгое время рассматривался только как физический барьер. Сегодня подобное представление существенно изменилось. Во-первых, было установлено, что эпителиальные клетки экспрессируют отвечающие за взаимодействие с микроорганизмами рецепторы, которые способны запускать активацию этих клеток с последующей продукцией противомикробных пептидов, а также каскадом регуляторных молекул (цитокинов) и экспрессией на эпителиоцитах корецепторов для клеток иммунной системы. Во-вторых, в составе «непроницаемого» эпителиального пласта были обнаружены дендритные клетки (преимущественно ротовая полость, дыхательная система, урогенитальный тракт, кожа) и multifold, или М-клетки (тонкий кишечник, миндалины, аденоиды), осуществляющие контролируемый перенос через барьер внутрь организма чужеродного материала. Этот контролируемый «трафик» необходим для поддержания в «тонусе» барьерного иммунитета и оповещения иммунной системы об изменяющемся окружении (например, о дисбалансе микробиоты или о попадании на слизистые и кожу патогенных микроорганизмов). Иначе говоря, иммунная система барьерных тканей находится все время в состоянии «тлеющей» активации, что позволяет ей быстро и эффективно реагировать на агрессию [7].
Подэпителиальная рыхлая соединительная ткань lamina propria (собственная пластинка), где диффузно, в высокой концентрации располагаются клетки врожденного иммунитета: несколько популяций дендритных клеток, макрофаги, естественные киллеры, гранулоциты, лимфоциты врожденного иммунитета и т. д. [8–10].
Под эпителием в lamina propria находятся так называемые «изолированные лимфоидные фолликулы», которые являются представительством адаптивного иммунитета в барьерных тканях. Эти фолликулы имеют четкую организацию с Т- и В-клеточными зонами и герминативным центром. Т-клеточные зоны содержат практически все субпопуляции αβTCR CD4+ T-хелперов (Th1, Th2 и Th17), продуцирующие ИЛ-10 Т-регуляторные клетки, CD8+ T-эффекторы. В составе В-клеточных зон преобладают В-лимфоциты, секретирующие IgA. Именно в эти фолликулы дендритные клетки и М-клетки доставляют антигенный материал, инициируя адаптивный иммунный ответ. Адаптивная иммунная система барьерных тканей тесно связана с регионарными лимфатическими образованиями: пейеровыми бляшками, аппендиксом, миндалинами и т. д., которые позволяют перевести иммунный ответ с местного уровня на системный [8].
Таким образом, МАЛТ обеспечивает многоуровневую защиту организма от проникновения патогенов и чужеродных веществ: от «пассивной» гуморальной, через активный антиген-неспецифический врожденный иммунитет, к высокоспецифическому адаптивному иммунитету, с возможностью перехода с местного уровня на системный.
Помимо единой структурной организации, описанной выше, существует еще одна особенность, делающая МАЛТ отдельной (и даже почти автономной в некотором смысле) подсистемой в рамках общего иммунитета. Это так называемый «закон хоминга МАЛТ». В соответствии с этим законом активация адаптивного иммунитета в какойлибо части МАЛТ приводит к формированию пула антиген-специфических клеток, часть которого остается в месте начала иммунного ответа, а другая выходит в системный кровоток и расселяется (хоминг) только в другие компартменты МАЛТ. Например, если проникновение патогена произошло в кишечнике (GALT), то через некоторое время секретирующие патоген-специфические IgA В-лимфоциты можно будет обнаружить в бронхолегочных лимфатических фолликулах lamina propria (BALT). За счет этого механизма формируется глобальная защита всех барьерных тканей.
Интерес к открытию и характеристике сигнальных рецепторов врожденного иммунитета (signal pattern-recognizing receptor — sPRR) обусловлен не только Нобелевской премией в области биологии и медицины 2011 г., но и важными прикладными аспектами: от понимания, как в организме осуществляются первые события противоинфекционной защиты, до создания новых лекарств для терапии хронических воспалительных, аутоиммунных и аутовоспалительных заболеваний.
sPRR являются основными рецепторами, осуществляющими связь между клетками врожденного иммунитета и другими клетками организма, включая нелимфоидные клетки и клетки адаптивного иммунитета. Они объединяют воедино все компоненты иммунной системы и координируют ее деятельность. С помощью этих рецепторов врожденный иммунитет распознает высококонсервативные структурные молекулы, имеющиеся у больших таксономических групп микроорганизмов (табл. 1). 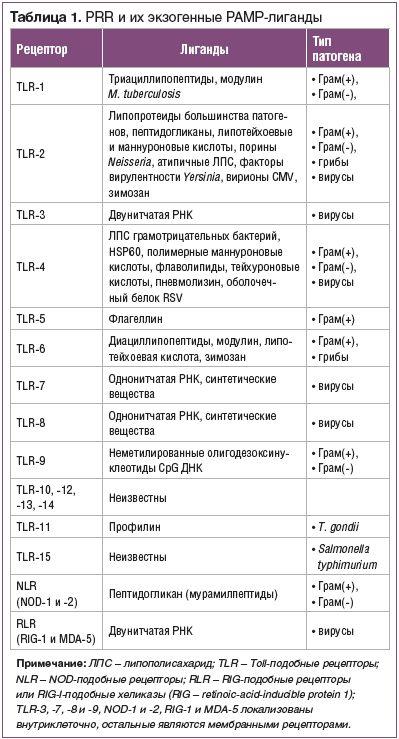
Эти молекулы получили название «патоген-ассоциированных молекулярных образов» (patogen-associated molecular patterns — PAMP). Наиболее известными PAMP являются бактериальный липополисахарид (ЛПС) (Грам(-) — грамотрицательные бактерии), липотейхоевые кислоты (Грам(+) — грамположительные бактерии), пептидогликан (ПГ) (грамотрицательные и грамположительные бактерии), маннаны, бактериальная ДНК, двуспиральная РНК вирусов, глюканы грибов и т. д. [11].
Рецепторы врожденного иммунитета, которые отвечают за распознавание РАМР, были названы «образ-распознающими» (pattern-recognition receptors — PRR) [11]. По функции их можно разделить на две группы: эндоцитозные и сигнальные. Эндоцитозные PRR (маннозные
рецепторы и рецепторы-мусорщики) в иммунологии известны достаточно давно — они обеспечивают процессы фагоцитоза с последующей доставкой патогена к лизосомам (начало адаптивного иммунного ответа).
Среди sPRR наибольшее значение имеют три семейства: Toll-подобные (TLR), NOD-подобные (NLR) и RIG-подобные рецепторы (RLR). Последние два семейства включают по 2 представителя PRR (NOD-1 и -2; RIG-1 и MDA-5), локализованных внутриклеточно и формирующих механизм «оповещения о несанкционированном прорыве» бактериального (NLR) или вирусного (RLR) патогена внутрь клетки или «побега» его из фаголизосомы [12, 13].
Наиболее изученными из sPRR являются Toll-подобные рецепторы (TLR). Данные рецепторы впервые были
описаны у дрозофил, у которых они, с одной стороны, отвечают за эмбриональное развитие, а с другой — обеспечивают антигрибковый иммунитет [14]. Сегодня у млекопитающих и человека охарактеризованы 15 TLR, которые расположены на мембране, в эндосомах или в цитоплазме клеток, осуществляющих первую линию защиты (нейтрофилы, макрофаги, дендритные, эндотелиальные и эпителиальные клетки кожных и слизистых покровов) [15–17].
В отличие от отвечающих за фагоцитоз эндоцитозных PRR, взаимодействие ТLR с соответствующим РАМР не сопровождается поглощением патогена, но приводит к изменению экспрессии большого количества генов и, в частности, генов провоспалительных цитокинов, которая опосредуется через последовательную активацию адапторных белков (например, MyD88), протеинкиназ (например, IRAK-4) и транскрипционных факторов (например, NF-κB) [18–20].
На уровне организма активация синтеза и секреции провоспалительных цитокинов (интерлейкины (ИЛ) -1, -2, -6, -8, -12, фактор некроза опухолей альфа (ФНО-α), интерферон-γ, гранулоцитарно-макрофагальный колониестимулирующий фактор) вызывает развитие воспалительной реакции с подключением всех имеющихся систем защиты от инфекционных агентов. На клеточном уровне эффект реализуется в трех направлениях. Во-первых, происходят активация самих клеток, несущих sPRR, и значительное усиление их защитного потенциала (продукция противомикробных пептидов и комплемента, фагоцитоз, переваривающая активность, продукция активных форм кислорода). Во-вторых, уже имеющиеся антиген-специфические клетки адаптивного иммунитета переходят в активированное состояние и усиливают свои эффекторные функции. В частности, зрелые В-лимфоциты увеличивают продукцию иммуноглобулинов (sIgA) и становятся более чувствительными к антигенной стимуляции, а Т-эффекторы наращивают киллерные функции. И, в‑третьих, происходят активация (прайминг) наивных лимфоцитов и подготовка их к началу адаптивного иммунного ответа [21, 22].
Именно через sPRR барьерный эпителий и мукозальные дендритные клетки распознают на ранних стадиях попытки инвазии микроорганизмов. Через эти же рецепторы клетки врожденного и адаптивного иммунитета подслизистого слоя или собственно дермы реагируют на уже проникшие через барьер патогены. Для реализации эффекта с sPRR не требуется пролиферации клеток и формирования антиген-специфического клона (необходимых при адаптивном иммунном ответе), и эффекторные реакции после распознавания данными рецепторами РАМР наступают немедленно. Этот факт объясняет высокую скорость врожденных иммунных механизмов элиминации патогена [23].
Микробиота: иммунологические механизмы симбиоза
Состав
Функции
Взаимодействие микробиоты и МАЛТ
Антибиотики и иммуносупрессия
Варианты преодоления иммуносупрессии, вызванной антибиотиками
Трансплантация фекальной микробиоты (ТФМ)
Использование пробиотиков
МАМР и их минимальные биологически активные фрагменты (МБАФ)
Заключение
Только для зарегистрированных пользователей
Источник





