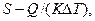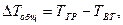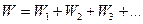Основные понятия. Способы выпаривания



Выпаривание — это процесс концентрирования растворов твердых нелетучих веществ путем удаления жидкого растворителя в виде паров. Сущность выпаривания заключается в переводе растворителя в парообразное состояние и отводе полученного пара от оставшегося сконцентрированного раствора. Выпаривание обычно проводят при кипении, т.е. в условиях, когда давление пара над раствором равно давлению в рабочем объеме аппарата. Различают следующие основные способы выпаривания:
• простое (однокорпусное), проводимое в непрерывном или периодическом режиме;
• многократное (многокорпусное), осуществляемое только в непрерывном режиме;
• с применением теплового насоса.
Все перечисленные способы выпаривания в зависимости от параметров греющего пара и свойств выпариваемых растворов реализуют как под давлением, так и в вакууме.
Простое выпаривание. Этот процесс осуществляют на установках небольшой производительности. Его проведение в периодическом режиме возможно с одновременной или порционной загрузкой исходного раствора.
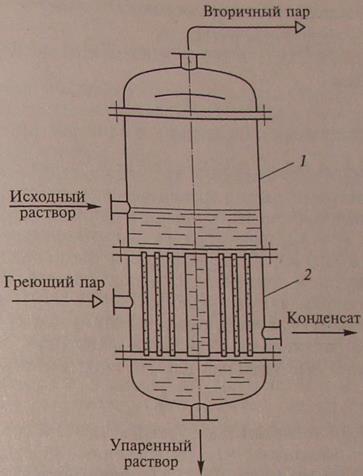
Схема однокорпусной выпарной установки непрерывного действия представлена на рис. 15.1. Аппарат состоит из сепаратора 1 и теплообменника 2. Греющий пар поступает в межтрубное пространство. Исходный раствор, подаваемый в аппарат, воспринимает теп-
Рис. 15.1. Схема однокорпусной выпарной установки непрерывного действия:
1 — сепаратор; 2 — теплообменник
лоту греющего пара, и растворитель испаряется. Образовавшийся вторичный пар и инертные газы освобождаются от брызг жидкости в сепараторе и отводятся через верхнюю часть аппарата. Упаренный раствор отбирается из штуцера, расположенного в нижней части аппарата.
Материальный баланс простого выпаривания может быть выражен двумя способами:
1)общий материальный баланс выпарного аппарата — с помощью уравнения
где GH, GK — массовый расход соответственно исходного и упаренного растворов, кг/с; W — массовый расход вторичного пара или выпариваемой воды, кг/с;
2)материальный баланс по сухому веществу, находящемуся в растворе, — с помощью уравнения
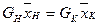
где 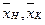
в исходном и упаренном растворах.
Из уравнений (15.1) и (15.2) найдем массовый расход выпариваемой воды:
( 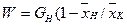
Уравнение теплового баланса имеет вид
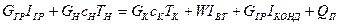
где 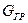
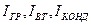
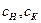
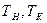
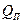
Под энтальпией (теплосодержанием) понимают сумму внутренней энергии и потенциальной энергии давления.
С учетом того, что удельная теплота конденсации пара
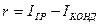
уравнение (15.3) позволяет определить массовый расход греющего пара. Расчет показывает, что для удаления 1 кг влаги из раствора может потребоваться 1,1. 1,2 кг греющего пара.
Площадь поверхности нагрева выпарного аппарата согласно основному уравнению теплопередачи (12.4) записывается в виде
где применительно к процессу выпаривания 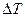
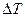
Общей разностью температур в выпарных установках называют разность температур греющего пара 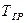
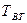
Полезная разность температур меньше общей на величину температурных потерь 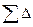
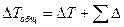
Различают три вида депрессий: температурную (физико-химическую), гидростатическую и гидравлическую.
Так как давление пара растворителя над раствором всегда ниже, чем над чистым растворителем, температура кипения раствора выше температуры кипения чистого растворителя при том же давлении. Например, в условиях, когда давление равно атмо-
сферному, вода кипит при температуре 100 °С, а 30%-ный раствор NaOH — при 117°С. Такая разность температур кипения раствора и чистого растворителя называется температурной депрессией 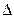

Значение температурной депрессии, зависящее от свойств растворенного вещества и растворителя, повышается с увеличением концентрации раствора и давления. Определить значение 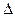
Большинство опытных данных относится к температурной депрессии 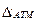
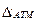
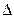
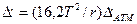
где Т — абсолютная температура кипения, К; r — удельная теплота испарения, Дж/кг, воды при данном давлении.
Повышение температуры кипения раствора обусловлено также гидростатической и гидравлической депрессиями.
Гидростатическая депрессия 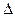
Гидравлическая депрессия 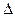
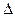
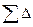
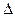
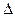
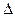
Проведение выпаривания в вакууме в большинстве случаев играет положительную роль: снижается температура кипения раствора, а это позволяет применять для нагревания выпарного аппарата пар низкого давления, который относится к тепловым отходам, образующимся при осуществлении других процессов.
Многократное выпаривание.Сущность этого способа выпаривания состоит в том, что его проводят в нескольких последовательно соединенных аппаратах, давление в которых поддерживают на таком уровне, чтобы вторичный пар предыдущего аппарата мог быть использован как греющий пар в последующем аппарате. Очевидно, что многократное выпаривание позволяет сократить расход теплоты на проведение процесса приблизительно пропорционально числу последовательно соединенных аппаратов (числу корпусов). Установки для многократного выпаривания всегда имеют несколько корпусов и поэтому называются многокорпусными.
Многокорпусные выпарные установки могут быть прямоточными, противоточными и комбинированными.
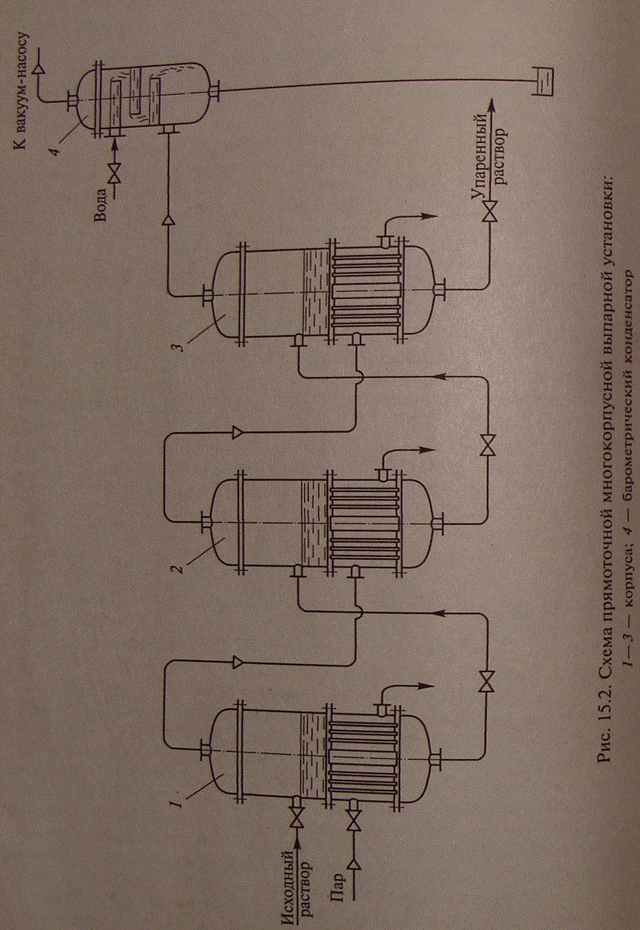
Схема прямоточной многокорпусной выпарной установки приведена на рис. 15.2. Исходный раствор подают в корпус 1, далее поступает в корпуса 2 и 3, а затем удаляется из корпуса 3 в виде готового продукта. Давление в установке уменьшается в направлении от корпуса 1 к корпусу 3, что обеспечивает перемещение раствора самотеком под действием перепада давлений.
Греющий пар перемещается в том же направлении, что и раствор: свежий пар вводится в корпус 1, а образовавшийся в этой корпусе вторичный пар направляется в качестве греющего пара в корпус 2. Образовавшийся в корпусе 2 вторичный пар применяется для обогрева корпуса 3, а вторичный пар из корпуса 3 поступает для конденсации в барометрический конденсатор 4.
Очевидным достоинством прямоточной схемы выпаривания является возможность перемещения раствора из корпуса в корпус без помощи насосов. К недостаткам этой схемы относится резкое снижение коэффициента теплопередачи от корпуса к корпусу.
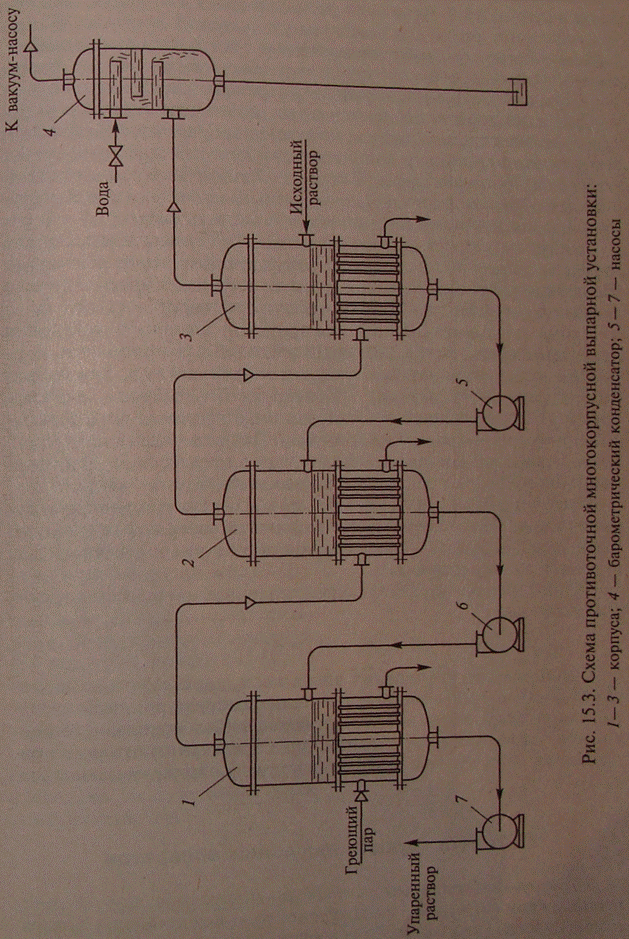
Схема противоточной многокорпусной выпарной установки представлена на рис. 15.3. Свежий греющий пар поступает в корпус 1, а вторичный пар уже в качестве греющего пара перемещается от корпуса 1 к корпусу 3. Выпариваемый раствор вводится вкорпус 3, перемещается в установке в направлении от корпуса 3 к корпусу 1 и отбирается из корпуса 1. Поскольку давление в каждом последующем корпусе меньше, чем в предыдущем, для перемещения раствора используются насосы 5— 7.
Преимуществом противоточной схемы выпаривания перед прямоточной является потребность в меньшей поверхности теплообмена, а недостатком — необходимость применения насосов для перекачивания растворов.
Общий массовый расход воды, выпариваемой в многокорпусной установке,
Очевидно, что увеличение числа корпусов ограничено вследствие уменьшения полезной разности температур, значения которых при этом возрастают. Оптимальное число корпусов установок многократного выпаривания, при определении которого принимаются во внимание и экономические соображения, составляет 3—4.
Источник
Способы разделения смесей
Для получения чистых веществ используют различные способы разделения смесей.
| Способы разделения смесей | |
|---|---|
| неоднородных (гетерогенных) | однородных (гомогенных) |
| — Отстаивание — Фильтрование — Действие магнитом — Центрифугирование | — Выпаривание. Кристаллизация. — Дистилляция (перегонка) |
Процессы разделения смесей основаны на различных физических свойствах компонентов, образующих смесь.
Отстаивание
Отстаивание — это разделение неоднородной жидкой смеси на компоненты, путём её расслоения с течением времени под действием силы тяжести.
Отстаиванием можно разделить смесь нерастворимых в воде веществ, имеющих разную плотность.
Пример. Смесь из железных и древесных опилок можно разделить, если высыпать её в сосуд с водой (1), взболтать и дать отстояться. Железные опилки опустятся на дно сосуда, а древесные будут плавать на поверхности воды (2), и их вместе с водой можно будет слить в другой сосуд (3):
На этом же принципе основано разделение смесей малорастворимых друг в друге жидкостей.
Пример. Смеси бензина с водой, нефти с водой, растительного масла с водой быстро расслаиваются, поэтому их можно разделить с помощью делительной воронки:
Отстаиванием также можно разделить вещества, которые осаждаются в воде с различной скоростью.
Пример. Смесь из глины и песка можно разделить, если высыпать её в сосуд с водой (1), взболтать и дать отстояться. Песок оседает на дно значительно быстрее глины (2):
Этот способ используется для отделения песка от глины в керамическом производстве (производство глиняной посуды, красных кирпичей и др.).
Центрифугирование
Центрифугирование — это разделение неоднородных жидких смесей путём вращения.
Пример. Если компоненты неоднородной жидкой смеси очень малы, такие смеси разделяют центрифугированием. Такие смеси помещают в пробирки и вращают с большой скоростью в специальных аппаратах — центрифугах.
Перед центрифугированием частицы смеси распределены по объёму пробирки равномерно. После центрифугирования более лёгкие частицы всплывают наверх, а тяжёлые оседают на дно пробирки.
С помощью центрифугирования, к примеру, отделяют сливки от молока.
Фильтрование
Фильтрование — это разделение жидкой неоднородной смеси на компоненты, путём пропускания смеси через пористую поверхность. В роли пористой поверхности может выступать бумажная воронка, марля, сложенная в несколько слоёв, или любой другой пористый материал, способный задержать один или несколько компонентов смеси.
Фильтрованием можно разделить неоднородную смесь, состоящую из растворимых и нерастворимых в воде веществ.
Пример. Чтобы разделить смесь, состоящую из поваренной соли и песка, её можно высыпать в сосуд с водой, взболтать и затем эту смесь пропустить через фильтровальную бумагу. Песок остаётся на фильтровальной бумаге, а прозрачный раствор поваренной соли проходит через фильтр:
При необходимости, растворённую поваренную соль из воды можно выделить выпариванием.
Действие магнитом
С помощью магнита из неоднородной смеси выделяют вещества, способные к намагничиванию.
Пример. C помощью магнита можно разделить смесь, состоящую из порошков железа и серы:
Выпаривание. Кристаллизация
Выпаривание — это способ разделения жидких смесей путём испарения одного из компонентов. Скорость испарения можно регулировать с помощью температуры, давления и площади поверхности испарения.
Пример. Чтобы растворённую в воде поваренную соль выделить из раствора, последний выпаривают:
Вода испаряется, а в фарфоровой чашке остаётся поваренная соль. Иногда применяют упаривание, т. е. частичное испарение воды. В результате образуется более концентрированный раствор, при охлаждении которого растворённое вещество выделяется в виде кристаллов. Этот процесс получил название кристаллизации.
Дистилляция (перегонка)
Дистилляция (перегонка) — это способ разделения жидких однородных смесей путём испарения жидкости с последующим охлаждением и конденсацией её паров. Данный способ основан на различии в температурах кипения компонентов смеси.
Пример. При нагревании жидкой однородной смеси сначала закипает вещество с наиболее низкой температурой кипения. Образующиеся пары конденсируются при охлаждении в другом сосуде. Когда этого вещества уже не останется в смеси, температура начнёт повышаться, и со временем закипает другой жидкий компонент:
Таким способом получают, к примеру, дистиллированную воду.
Источник