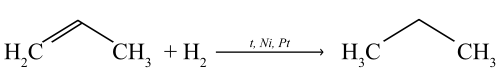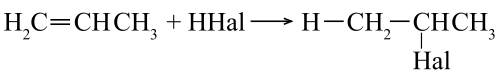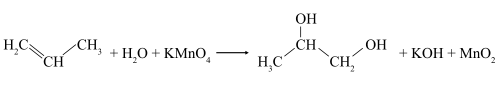- Пропилен
- Содержание
- Физические свойства
- Химические свойства
- Присоединение галогенов (галогенирование)
- Присоединение водорода (реакция гидрирования)
- Присоединение воды (реакция гидратации)
- Присоединение галогеноводородов (HHal)
- Горение на воздухе
- Полимеризация
- Окисление кислородом воздуха в пропиленоксид
- Получение
- В лаборатории
- В промышленности
- Применение
- Производство
- Источники
- Примечания
- Ссылки
- Полезное
- Смотреть что такое «Пропилен» в других словарях:
- Пропилен (пропен), получение, свойства, химические реакции
- Пропилен (пропен), получение, свойства, химические реакции.
- Пропилен (пропен), формула, газ, характеристики:
- Физические свойства пропилена (пропена):
- Химические свойства пропилена (пропена):
- Получение пропилена (пропена). Химические реакции – уравнения получения пропилена (пропена):
- Применение и использование пропилена (пропена):
- Мировая экономика
- Справочники
- Востребованные технологии
- Поиск технологий
- О чём данный сайт?
- О Второй индустриализации
Пропилен
| Пропилен | |
 | |
 | |
| Общие | |
|---|---|
| Химическая формула | C3H6 |
| Физические свойства | |
| Молярная масса | 42.08 г/моль |
| Плотность | 0.695@-47 °C г/см³ |
| Термические свойства | |
| Температура плавления | − 185.2 °C |
| Температура кипения | − 47.6 °C |
| Классификация | |
| Рег. номер CAS | 115-07-1 |
| SMILES | C=CC |
Пропиле́н (пропен) СН2=СН-СН3 — непредельный (ненасыщенный) углеводород ряда этилена, горючий газ, является изологом пропана. Вещество с наркотическим действием более сильным, чем у этилена. Класс опасности — четвертый. [1] .
Содержание
Физические свойства
Пропилен представляет собой газообразное вещество с низкой температурой кипения tкип= -47,7 °C и температурой плавления tпл= −187,6 °C, оптическая плотность d20 4 =0,5193.
Химические свойства
Обладает значительной реакционной способностью. Его химические свойства определяются двойной углерод-углеродной связью. p-связь, как наименее прочная и более доступная, при действии реагента разрывается, а освободившиеся валентности углеродных атомов затрачиваются на присоединение атомов, из которых состоит молекула реагента. Все реакции присоединения протекают по двойной связи и состоят в расщеплении π-связи алкена и образовании на месте разрыва двух новых σ-связей.
Чаще реакции присоединения идут по гетеролитическому типу, являясь реакциями электрофильного присоединения.
Присоединение галогенов (галогенирование)
Реакцию галогенирования обычно проводят в растворителе при обычной температуре. Галогены легко присоединяются по месту разрыва двойной связи с образованием дигалогенопроизводных. Легче идет присоединение хлора и брома, труднее — йода. Фтор взаимодействует со взрывом.
Присоединение водорода (реакция гидрирования)
Присоединяя водород в присутствии катализаторов (Pt, Pd, Ni), пропен переходит в предельный углеводород — пропан.
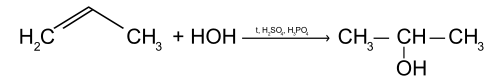
Присоединение воды (реакция гидратации)
Пропилен реагирует с водой с образованием одноатомного спирта изопропанола, при этом двойная связь раскрывается.
Присоединение галогеноводородов (HHal)
Происходит по правилу Марковникова. Водород кислоты HHal присоединяется к наиболее гидрированному атому углерода при двойной связи. Соответственно остаток Hal связывается с атомом углерода, при котором находится меньшее число атомов водорода.
Пример гидрогалогенирования — получение бромпроизводного пропана при реакции бромоводорода и пропилена.
Горение на воздухе
При поджигании горит на воздухе: 2СН2=СНСН3 + 9О2 → 6СО2 + 6Н2О.
С кислородом воздуха газообразный пропилен образует взрывчатые смеси.
В слабощелочной или нейтральной водной среде пропилен окисляется перманганатом калия, что сопровождается обесцвечиванием раствора KMnO4 и образованием гликолей (соединений с двумя гидроксильными группами при соседних атомах углерода). Эта реакция получила название реакции Вагнера.
Полимеризация
Условия реакции: нагревание, присутствие катализаторов. Соединение молекул происходит путем расщепления внутримолекулярных π-cвязей и образования новых межмолекулярных σ-cвязей.
Окисление кислородом воздуха в пропиленоксид
При нагревании в присутствии серебряных катализаторов:
Получение
В лаборатории
1. Отщепление галогеноводорода от галогеналкилов при действии на них спиртового раствора щелочи:
2. Гидрирование пропина в присутствии катализатора (Pd):
3. Дегидратация изопропилового спирта (отщепление воды). В качестве катализатора используют кислоты (серную или фосфорную) или Аl2O3:
4. Отщепление двух атомов галогена от дигалогеноалканов, содержащих галогены при соседних атомах С. Реакция протекает под действием металлов (Zn и др.):
В промышленности
Обычно пропилен выделяют из газов нефтепереработки (при крекинге сырой нефти в кипящем слое (процесс фирмы BASF), пиролизе бензиновых фракций) или попутных газов, а также из газов коксования угля. Существует несколько видов пиролиза пропилена: пиролиз в трубчатых печах, пиролиз в реакторе с кварцевым теплоносителем (процесс фирмы Phillips Petroleum Co.), пиролиз в реакторе с коксовым теплоносителем (процесс фирмы Farbewerke Hoechst), пиролиз в реакторе с песком в качестве теплоносителя (процесс фирмы Lurgi), пиролиз в трубчатой печи (процесс фирмы Kellogg), процесс Лавровского — Бродского, автотермический пиролиз по Бартоломе. В промышленности пропилен получают также дегидрированием алканов в присутствии катализатора (Сr2О3, Аl2О3).
Промышленным способом получения пропилена наряду с крекингом служит дегидратация пропанола над оксидом алюминия:
Применение
Для производства оксида пропилена, получения изопропилового спирта и ацетона, для синтеза альдегидов, для получения акриловой кислоты и акрилонитрила, полипропилена, пластмасс, каучуков, моющих средств, компонентов моторных топлив, растворителей.
Производство
Большая часть производственных мощностей по пропилену сосредоточена в Европе, Северной Америке и Азии. В настоящее время за год в мире производится более 50 миллионов тонн пропилена полимерного и химического сортов (PG/CG). Большая часть выпуска пропилена этих сортов приходится на долю установок пиролиза, где пропилен — побочный продукт производства этилена. Установками термического крекинга вырабатывается более 60 % такого пропилена. Нефтеперерабатывающими FCC-предприятиями выпускается 34 %. При дегидрогенизации или метатезисе пропана производится 3 % пропилена (в данном случае пропилен является целевым продуктом).
Пропилен нефтехимической чистоты (RG) производится на нефтеперерабатывающих предприятиях мира в количестве, равном 31,2 миллионам тонн. Большая часть такого пропилена вырабатывается на FCC-предприятиях, где пропилен — побочный продукт производства бензина и дистиллятов. Половина этих пропиленовых мощностей интегрирована с нефтехимическими предприятиями, на которых происходит алкилирование пропилена или смешивание LPG и пропана.
Источники
- http://www.ssa.ru
- http://chem.edu.ru
- А. И. Артеменко, Органическая химия, М.:Высшая школа — 1998
- Б. Д. Степин, А. А. Цветков, Органическая химия, М.:Высшая школа — 1994
Примечания
Ссылки
- http://www.xumuk.ru
- http://chemindustry.ru
 Углеводороды Углеводороды | |
|---|---|
| Алканы | Метан • Этан • Пропан • Бутан • Пентан • Гексан • Гептан • Октан • Нонан • Декан • Ундекан • Додекан • Тридекан • Тетрадекан • Гексадекан • Эйкозан . |
| Алкены | Этилен • Пропен • Бутен • Пентен • Гексен • Гептен • Октен . |
| Алкины | Ацетилен • Пропин • Бутин |
| Диены | Пропадиен • Бутадиен • Изопрен |
| Другие ненасыщеные | Винилацетилен • Диацетилен |
| Циклоалканы | Циклопропан • Циклобутан • Циклопентан • Циклогексан • Декалин • Индан |
| Ароматические | Бензол • Толуол • Диметилбензолы • Этилбензол • Пропилбензол • Кумол • Стирол • Фенилацетилен • Индан • Циклобутадиен • Дифенил • Дифенилметан • Трифенилметан • Тетрафенилметан |
| Полициклические | Нафталин • Антрацен • Пентацен • Фенантрен • Пирен • Бензпирен • Азулен • Хризен |
 |
Wikimedia Foundation . 2010 .
Полезное
Смотреть что такое «Пропилен» в других словарях:
ПРОПИЛЕН — Газообразное углеводородное тело, входящее в состав светильного газа. Словарь иностранных слов, вошедших в состав русского языка. Чудинов А.Н., 1910. ПРОПИЛЕН бесцветный газ углеводородного состава., находящейся в светильном газе; под сильным… … Словарь иностранных слов русского языка
Пропилен — – вещество, представляющее собой бесцветный горючий газ со слабым запахом. Химическая формула СH2=СН–CH3. Пропилен является одним из важнейших видов промышленного химического сырья. Содержится в газах крекинга нефтепродуктов. Широко… … Нефтегазовая микроэнциклопедия
ПРОПИЛЕН — (пропен) СН3СН=СН2, бесцветный газ, tкип ?47,7 .С. Получают пиролизом нефтепродуктов и дегидрогенизацией пропана. Важное сырье химической промышленности; применяется для синтеза глицерина, акрилонитрила, кумола, полипропилена и др … Большой Энциклопедический словарь
ПРОПИЛЕН — (пропен), бесцветный алифатический УГЛЕВОДОРОД, СН2СН:СН2, получаемый термическим КРЕКИНГОМ ЭТИЛЕНА. Используется в производстве широкого ряда химических веществ, включая виниловую и акриловую смолы. Свойства: температура кипения 48 °С;… … Научно-технический энциклопедический словарь
пропилен — сущ., кол во синонимов: 3 • олефин (5) • пропен (1) • углеводород (77) Словарь синонимов ASIS … Словарь синонимов
ПРОПИЛЕН — (пропен CH2 = CHCH3) непредельный (ненасыщенный) углеводород ряда этилена; бесцветный горючий газ со слабым запахом. Получают пиролизом нефтепродуктов и дегидрогенизацией пропана. Является важным сырьем химической промышленности … Российская энциклопедия по охране труда
пропилен — (C3Н6) [http://slovarionline.ru/anglo russkiy slovar neftegazovoy promyishlennosti/] Тематики нефтегазовая промышленность EN propylene … Справочник технического переводчика
ПРОПИЛЕН — (пропей), (СH2=CH СH3) ненасыщенный углеводород ряда этилена, горючий газ без цвета, но со слабым запахом; обладает высокой реакционной способностью. П. содержится в газах, образующихся при (см.) нефти; широко применяется для производства… … Большая политехническая энциклопедия
пропилен — а; м. Органическое соединение газ, выделяемый из попутных газов нефтедобычи и нефтепереработки (используется в производстве моторных масел). ◁ Пропиленовый, ая, ое. П ая смесь. * * * пропилен (пропен), СН3СН=СН2, бесцветный газ, tкип 47,7°C.… … Энциклопедический словарь
пропилен — propenas statusas T sritis chemija formulė CH₂=CHCH₃ atitikmenys: angl. propene; propylene rus. пропен; пропилен ryšiai: sinonimas – propilenas … Chemijos terminų aiškinamasis žodynas
Источник
Пропилен (пропен), получение, свойства, химические реакции
Пропилен (пропен), получение, свойства, химические реакции.
Пропилен (пропен), C3H6 – органическое вещество класса алкенов. Пропилен имеет двойную углерод-углеродную связь и поэтому относится к ненасыщенным или непредельным углеводородам.
Пропилен (пропен), формула, газ, характеристики:
Пропилен (пропен) – органическое вещество класса алкенов, состоящий из трех атомов углерода и шести атомов водорода . Пропилен имеет двойную углерод-углеродную связь и поэтому относится к ненасыщенным или непредельным углеводородам.
Химическая формула пропилена C3H6, рациональная формула H2CCHCH3, структурная формула CH2=CH-CH3. Изомеров не имеет.
Пропилен – бесцветный газ, без вкуса, со слабым запахом.
Пожаро- и взрывоопасен.
Плохо растворяется в воде . Зато хорошо растворяется в углеводородах.
Пропилен по токсикологической характеристике относится к веществам 4-го класса опасности (малоопасным веществам) по ГОСТ 12.1.007, но оказывает вредное воздействие на человека более сильным, чем этилен (этен).
Физические свойства пропилена (пропена):
| Наименование параметра: | Значение: |
| Цвет | без цвета |
| Запах | со слабым запахом |
| Вкус | без вкуса |
| Агрегатное состояние (при 20 °C и атмосферном давлении 1 атм.) | газ |
| Плотность (при 20 °C и атмосферном давлении 1 атм.), кг/м 3 | 1,184 |
| Плотность (при 0 °C и атмосферном давлении 1 атм.), кг/м 3 | 1,9149 |
| Температура плавления, °C | -185,25 |
| Температура кипения, °C | -47,6 |
| Температура вспышки, °C | 107,8 |
| Температура самовоспламенения, °C | 410 |
| Критическая температура*, °C | 91,4 |
| Критическое давление, МПа | 4,6 |
| Взрывоопасные концентрации смеси газа с воздухом, % объёмных | от 2,3 до 11,1 |
| Удельная теплота сгорания, МДж/кг | 45,694 |
| Молярная масса, г/моль | 42,08 |
* при температуре выше критической температуры газ невозможно сконденсировать ни при каком давлении.
Химические свойства пропилена (пропена):
Пропилен — химически активное вещество. Так как в молекуле между атомами углерода имеется двойная связь, то одна из них, менее прочная, легко разрывается, и по месту разрыва связи происходит присоединение, замещение, окисление, полимеризация молекул.
Химические свойства пропилена аналогичны свойствам других представителей ряда алкенов. Поэтому для него характерны следующие химические реакции:
- 1. каталитическое гидрирование (восстановление) пропилена:
В результате данной химической реакции образуется пропан.
- 2. галогенирование пропилена:
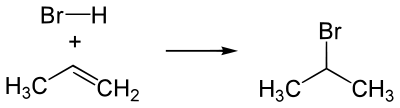
- 3. гидрогалогенирование пропилена:
Водород кислоты HBr присоединяется к наиболее гидрированному атому углерода при двойной связи. Соответственно остаток Br связывается с атомом углерода, при котором находится меньшее число атомов водорода.
- 4. гидратация пропилена:
Реакция происходит в присутствии минеральных кислот (серной, фосфорной). В результате данной химической реакции образуется изопропанол (изопропиловый спирт).
- 5. горение пропилена:
В результате горения пропилена происходит разрыв всех связей в молекуле, а продуктами реакции являются углекислый газ и вода.
- 6. полимеризация пропилена:
В результате образуется полипропилен.
Получение пропилена (пропена). Химические реакции – уравнения получения пропилена (пропена):
Пропилен получают как в лабораторных условиях, так и в промышленных масштабах.
Обычно пропилен получают при пиролизе углеводородного сырья и каталитическом крекинге нефтяных фракций.
В промышленных масштабах пропилен получают, например, в результате следующей химической реакции:
Пропилен в лабораторных условиях получается в результате следующих химических реакций:
- 1. дегидратация изопропилового спирта:
- 2. дегалогенирования дигалогенпроизводных пропана:
- 3. неполное гидрирование пропина:
- 4. дегидрогалогенирование галогенпроизводных алканов под действием спиртовых растворов щелочей:
Применение и использование пропилена (пропена):
– как сырье в химической промышленности для органического синтеза различных органических соединений: оксида пропилена, изопропилового спирта, ацетона, альдегидов, акриловой кислоты, акрилонитрила, полипропилена,
– в производстве полимеров , пластмасс , каучуков, моющих средств, компонентов моторных топлив, растворителей.
Примечание: © Фото //www.pexels.com, //pixabay.com

как получить пропилен реакция ацетилен пропен 1 2 вещество пропилен кислород водород связь является углекислый газ бромная вода
уравнение реакции масса объем полное сгорание моль молекула смесь превращение горение получение пропилена
напишите уравнение реакций пропилен
Мировая экономика
Справочники
Востребованные технологии
- Концепция инновационного развития общественного производства – осуществления Второй индустриализации России на период 2017-2022 гг. (106 543)
- Экономика Второй индустриализации России (102 550)
- Программа искусственного интеллекта ЭЛИС (27 763)
- Метан, получение, свойства, химические реакции (24 214)
- Этилен (этен), получение, свойства, химические реакции (23 986)
- Природный газ, свойства, химический состав, добыча и применение (21 577)
- Крахмал, свойства, получение и применение (20 896)
- Пропилен (пропен), получение, свойства, химические реакции (20 015)
- Целлюлоза, свойства, получение и применение (19 748)
- Прямоугольный треугольник, свойства, признаки и формулы (19 007)
Поиск технологий
О чём данный сайт?
Настоящий сайт посвящен авторским научным разработкам в области экономики и научной идее осуществления Второй индустриализации России.
Он включает в себя:
– экономику Второй индустриализации России,
– теорию, методологию и инструментарий инновационного развития – осуществления Второй индустриализации России,
– организационный механизм осуществления Второй индустриализации России,
– справочник прорывных технологий.
Мы не продаем товары, технологии и пр. производителей и изобретателей! Необходимо обращаться к ним напрямую!
Мы проводим переговоры с производителями и изобретателями отечественных прорывных технологий и даем рекомендации по их использованию.
О Второй индустриализации
Осуществление Второй индустриализации России базируется на качественно новой научной основе (теории, методологии и инструментарии), разработанной авторами сайта.
Конечным результатом Второй индустриализации России является повышение благосостояния каждого члена общества: рядового человека, предприятия и государства.
Вторая индустриализация России есть совокупность научно-технических и иных инновационных идей, проектов и разработок, имеющих возможность быть широко реализованными в практике хозяйственной деятельности в короткие сроки (3-5 лет), которые обеспечат качественно новое прогрессивное развитие общества в предстоящие 50-75 лет.
Та из стран, которая первой осуществит этот комплексный прорыв – Россия, станет лидером в мировом сообществе и останется недосягаемой для других стран на века.
Источник