- Этан: способы получения и свойства
- Гомологический ряд этана
- Строение этана
- Изомерия этана
- Химические свойства этана
- 1. Реакции замещения
- 1.1. Галогенирование
- 1.2. Нитрование этана
- 2. Дегидрирование этана
- 3. Окисление этана
- 3.1. Полное окисление – горение
- Получение этана
- 1. Взаимодействие галогеналканов с металлическим натрием (реакция Вюрца)
- 2. Декарбоксилирование солей карбоновых кислот (реакция Дюма)
- 3. Гидрирование алкенов и алкинов
- 4. Синтез Фишера-Тропша
- 5. Получение этана в промышленности
- Все возможные способы получения этана
- Характеристики и физические свойства этана
- Получение этана
- Химические свойства этана
- Применение этана
- Примеры решения задач
- Этан, получение, свойства, химические реакции
- Этан, получение, свойства, химические реакции.
- Этан, формула, газ, характеристики:
- Физические свойства этана:
- Химические свойства этана:
- Получение этана в промышленности и лаборатории. Химические реакции – уравнения получения этана:
- Применение и использование этана:
Этан: способы получения и свойства
Этан C2H6 – это предельный углеводород, содержащий два атома углерода в углеродной цепи. Бесцветный газ без вкуса и запаха, нерастворим в воде и не смешивается с ней.
Гомологический ряд этана
Все алканы — вещества, схожие по физическим и химическим свойствам, и отличающиеся на одну или несколько групп –СН2– друг от друга. Такие вещества называются гомологами, а ряд веществ, являющихся гомологами, называют гомологическим рядом.
Самый первый представитель гомологического ряда алканов – метан CH4. , или Н–СH2–H.
Продолжить гомологический ряд можно, последовательно добавляя группу –СН2– в углеводородную цепь алкана.
| Название алкана | Формула алкана |
| Метан | CH4 |
| Этан | C2H6 |
| Пропан | C3H8 |
| Бутан | C4H10 |
| Пентан | C5H12 |
| Гексан | C6H14 |
| Гептан | C7H16 |
| Октан | C8H18 |
| Нонан | C9H20 |
| Декан | C10H22 |
Общая формула гомологического ряда алканов CnH2n+2.
Первые четыре члена гомологического ряда алканов – газы, C5–C17 – жидкости, начиная с C18 – твердые вещества.
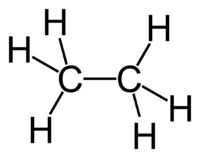
Строение этана
В молекулах алканов встречаются химические связи C–H и С–С.
Связь C–H ковалентная слабополярная, связь С–С – ковалентная неполярная. Это одинарные σ-связи. Атомы углерода в алканах образуют по четыре σ-связи. Следовательно, гибридизация атомов углерода в молекулах алканов – sp 3 :

При образовании связи С–С происходит перекрывание sp 3 -гибридных орбиталей атомов углерода:

При образовании связи С–H происходит перекрывание sp 3 -гибридной орбитали атома углерода и s-орбитали атома водорода:

Четыре sp 3 -гибридные орбитали атома углерода взаимно отталкиваются, и располагаются в пространстве так, чтобы угол между орбиталями был максимально возможным.
Поэтому четыре гибридные орбитали углерода в алканах направлены в пространстве под углом 109 о 28′ друг к другу:

Это соответствует тетраэдрическому строению молекулы.
| Например, в молекуле этана C2H6 атомы водорода располагаются в пространстве в вершинах двух тетраэдров, центрами которых являются атомы углерода |
Изомерия этана
Для этана не характерно наличие изомеров – ни структурных (изомерия углеродного скелета, положения заместителей), ни пространственных.
Химические свойства этана
Этан – предельный углеводород, поэтому он не может вступать в реакции присоединения.
Для метана характерны реакции:
Разрыв слабо-полярных связей С – Н протекает только по гомолитическому механизму с образованием свободных радикалов.
Поэтому для этана характерны радикальные реакции.
Этан устойчив к действию сильных окислителей (KMnO4, K2Cr2O7 и др.), не реагирует с концентрированными кислотами, щелочами, бромной водой.
1. Реакции замещения
В молекулах алканов связи С–Н более доступны для атаки другими частицами, чем менее прочные связи С–С.
1.1. Галогенирование
Этан реагирует с хлором и бромом на свету или при нагревании.
При хлорировании этана сначала образуется хлорэтан:
Хлорэтан может взаимодействовать с хлором и дальше с образованием дихлорэтана, трихлорэтана, тетрахлорметана и т.д.
1.2. Нитрование этана
Этан взаимодействует с разбавленной азотной кислотой по радикальному механизму, при нагревании и под давлением. Атом водорода в этане замещается на нитрогруппу NO2.
Например. При нитровании этана образуется преимущественно нитроэтан: 2. Дегидрирование этанаДегидрирование – это реакция отщепления атомов водорода. В качестве катализаторов дегидрирования используют никель Ni, платину Pt, палладий Pd, оксиды хрома (III), железа (III), цинка и др. При дегидрировании алканов, содержащих от 2 до 4 атомов углерода в молекуле, разрываются связи С–Н у соседних атомов углерода и образуются двойные и тройные связи.
3. Окисление этанаЭтан – слабополярное соединение, поэтому при обычных условиях он не окисляется даже сильными окислителями (перманганат калия, хромат или дихромат калия и др.). 3.1. Полное окисление – горениеЭтан горит с образованием углекислого газа и воды. Реакция горения этана сопровождается выделением большого количества теплоты. Уравнение сгорания алканов в общем виде: При горении этана в недостатке кислорода может образоваться угарный газ СО или сажа С. Получение этана1. Взаимодействие галогеналканов с металлическим натрием (реакция Вюрца)Это один из лабораторных способов получения этана из хлорметана или бромметана. При этом происходит удвоение углеродного скелета.
Рассчитаем количество вещества дихлорэтана (молярная масса равна – 99 г/моль): По уравнению реакции найдем количество вещества хлора. n(C2H4Cl2) : n(Cl2) = 1:2, т.е. n(Cl2) = 2 × n(C2H4Cl2) = 2 × 0,12 = 0,24 моль. Тогда объем хлора будет равен: Источник Этан, получение, свойства, химические реакцииЭтан, получение, свойства, химические реакции.Этан, C2H6 – органическое вещество класса алканов. В природе содержится в природном газе, добываемом из газовых и газоконденсатных месторождений, в попутном нефтяном газе. Образуется также при крекинге нефтепродуктов. Этан, формула, газ, характеристики:Этан (лат. ethanum) – органическое вещество класса алканов , состоящий из двух атомов углерода и шести атомов водорода. Химическая формула этана C2H6, рациональная формула H3CCH3. Изомеров не имеет. Этан – бесцветный газ, без вкуса и запаха. В природе содержится в природном газе , добываемом из газовых и газоконденсатных месторождений, в попутном нефтяном газе . Для выделения из природного и попутного нефтяного газа производят их очистку и сепарацию газа. Образуется также при крекинге нефтепродуктов ., в т.ч. сланцевой нефти. Пожаро- и взрывоопасен. Не растворяется в воде и других полярных растворителях. Зато растворяется в некоторых неполярных органических веществах (метанол, ацетон, бензол, тетрахлорметан, диэтиловый эфир и другие). Этан по токсикологической характеристике относится к веществам 4-го класса опасности (малоопасным веществам) по ГОСТ 12.1.007. Физические свойства этана:
* при температуре выше критической температуры газ невозможно сконденсировать ни при каком давлении. Химические свойства этана:Этан трудно вступает в химические реакции. В обычных условиях не реагирует с концентрированными кислотами, расплавленными и концентрированными щелочами, щелочными металлами, галогенами (кроме фтора), перманганатом калия и дихроматом калия в кислой среде. Химические свойства этана аналогичны свойствам других представителей ряда алканов. Поэтому для него характерны следующие химические реакции:
Реакция носит цепной характер. Молекула брома или йода под действием света распадается на радикалы, затем они атакуют молекулы этана, отрывая у них атом водорода, в результате этого образуется свободный этил CH3-CH2·, который сталкиваются с молекулами брома (йода), разрушая их и образуя новые радикалы йода или брома : Br2 → Br·+ Br· (hv); – инициирование реакции галогенирования; CH3-CH3 + Br· → CH3-CH2· + HBr; – рост цепи реакции галогенирования; CH3-CH2· + Br· → CH3-CH2Br; – обрыв цепи реакции галогенирования. Галогенирование — это одна из реакций замещения. В первую очередь галогенируется наименее гидрированый атом углерода (третичный атом, затем вторичный, первичные атомы галогенируются в последнюю очередь). Галогенирование этана проходит поэтапно – за один этап замещается не более одного атома водорода. Галогенирование будет происходить и далее, пока не будут замещены все атомы водорода .
При избытке кислорода: Горит бесцветным пламенем. При нехватке кислорода вместо углекислого газа (СО2) получается оксид углерода (СО), при еще меньшем количестве кислорода выделяется мелкодисперсный углерод (в различном виде, в т.ч. в виде графена , фуллерена и пр.) либо их смесь.
Получение этана в промышленности и лаборатории. Химические реакции – уравнения получения этана:Так как этан в достаточном количестве содержится в природном газе (до 30 % и более), попутном нефтяном газе и выделяется при крекинге нефтепродуктов , его не получают искусственно. Его выделяют при очистке и сепарации из природного газа , ПНГ и нефти при перегонке. Этан в лабораторных условиях получается в результате следующих химических реакций:
Суть данной реакции в том, что две молекулы галогеналкана связываются в одну, реагируя с щелочным металлом .
Применение и использование этана:– как сырье в химической промышленности для производства в основном этилена (этена). Источник |