Все способы производства вакцин
В мире сложилась тяжелая эпидемиологическая ситуация. Пандемия COVID-19 никуда уходить пока не собирается. Работа над лекарствами и вакцинами идет полным ходом практических во всех странах и Россия не исключение. Разберемся какие есть разработки и технологии на примере вакцин против коронавируса.
Из белков
Большая часть вакцинных препаратов, разрабатываемых для профилактики COVID-19 — субъединичные. Прививки разработанные по этой технологии самые безопасные: ни на одной стадии создания не используется живой вирус, а сама она содержит только вирусные белки. Для формирования полноценного иммунного ответа такие препараты вводятся несколько раз и требуют добавления компонентов, усиливающих иммунный ответ, например адъювантов или иммуностимуляторов.
Из частиц вирусов
Вакцины на основе вирусоподобных частиц также состоят только из вирусных белков, адъювантов и иммуностимуляторов. Для усиления иммунного ответа эти белки собираются в частицы, похожие на вирус. Они безопасны и способны вызывать иммунный ответ, но их создание для массовой вакцинации технологически сложно и дороже.
Из нуклеиновых кислот
ДНК- и РНК-вакцины — препараты на основе нуклеиновых кислот. Создание таких прививок осложняется тем, что технологии доставки генетического материала внутрь клетки организма еще разрабатываются. Это ограничивает использование ДНК- и РНК-вакцин: пока ни один препарат на основе нуклеиновой кислоты не применяется в клинической практике на людях.
С помощью других вирусов
Немалая часть разработок прототипов иммунобиологических препаратов основана на применении вирусных векторов: реплицирующихся — способных размножаться; нереплицирующихся — не способных размножаться. Технология создания этих двух видов одинакова: в геном вирусного вектора встраивается ген, кодирующий целевой белок другого вируса. Вектор — другой вирус, не вызывающий болезнь у человека. Например, для создания вакцины против COVID-19 в аденовирус встраивается ген, кодирующий белок коронавируса. Препятствие при использовании таких препаратов — присутствие у человека антител к вирусному вектору. В этом случае полноценный иммунный ответ может не сформироваться. Выбор вирусного вектора важный и определяющим этап при их разработке. Иммунитет при использовании реплицирующегося вектора формируется, как правило, уже после однократного введения, тогда как для вакцин на основе нереплицирующихся вирусных векторов чаще всего требуется несколько введений препарата.
Проверенные временем
Цельновирионные живые аттенуированные и инактивированные вакцины имеют самую продолжительную историю применения и являются классическими технологическими платформами. Инактивированные содержат нежизнеспособные вирусы, и для формирования иммунного ответа часто требуются повторные введения препарата. Для живых аттенуированных вакцин чаще требуется однократное введение, так как вирус сохраняет возможность размножаться в организме человека. Вирус в аттенуированной вакцине ослаблен, однако есть вероятность возврата к дикому типу, что приведет к вспышке при её использовании. Это приводит к необходимости регулярного проведения исследований по изучению генетической стабильности таких препаратов. Кроме того, технологическое создание вакцин этих типов медленнее в сравнении с производством ДНК- и РНК- или субъединичных вакцин. Кроме этого, при этом особых санитарных норм и требований биологической безопасности.
Где привиться
На данный момент созданные вакцины против коронавируса, к сожалению, доступны не всем. В первую очередь они используются для защиты людей, которые каждый день сталкиваются с вирусом, а также тех чьи профессии связаны с контактом с большим количеством людей, например учителя. Скоро привиться сможет и каждый желающий, а пока можно сделать прививку от гриппа и защитить себя и своих близких.
Подробнее о вакцинации читайте здесь «Коротко о вакцинации» и на сайте Роспотребнадзора.
Источник
Новые технологии производства вакцин: генетическая иммунизация и «обратная вакцинология»
Создавать вакцины против новых инфекций, используя старые испытанные технологии, удается не всегда. Некоторые микроорганизмы, например, вирус гепатита B, практически невозможно вырастить в культуре клеток, чтобы получить инактивированную вакцину. Во многих случаях вакцины на основе убитых микробов оказываются неэффективными, а живые вакцины — слишком опасными. Большие надежды возлагались на вакцины, полученные на основе рекомбинантных белков-антигенов (именно таким способом в 1980-е годы создали вакцину, защищающую от гепатита B). Но сейчас стало очевидным, что многие рекомбинантные вакцины вызывают слабый иммунный ответ. Вероятно, причина в том, что в таких препаратах содержится «голый» белок и отсутствуют другие молекулярные структуры, часто необходимые для запуска иммунного ответа. Чтобы рекомбинантные вакцины вошли в практику, нужны вещества-усилители (адъюванты), стимулирующие антигенную активность.
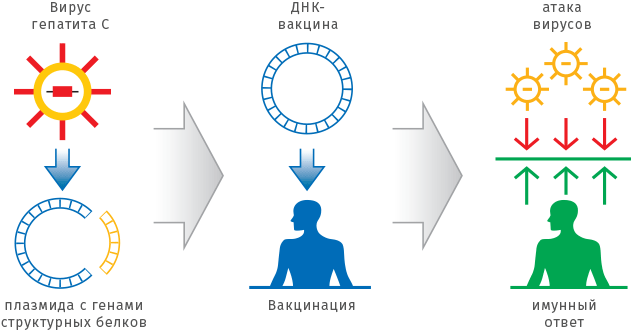
За последние 10 лет сформировалось новое направление — генетическая иммунизация. Его называют также ДНК-вакцинацией, поскольку в организм вводят не белок-антиген, а нуклеиновую кислоту (ДНК или РНК), в которой закодирована информация о белке. Реальная возможность использовать эту технологию в медицине и ветеринарии появилась в середине 90-х годов прошлого века. Новый подход достаточно прост, дешев и, самое главное, универсален. Сейчас уже разработаны относительно безопасные системы, которые обеспечивают эффективную доставку нуклеиновых кислот в ткани. Нужный ген вставляют в плазмиду (кольцо из ДНК) или в безопасный вирус. Такой носитель-вектор проникает в клетку и синтезирует нужные белки. Трансформированная клетка превращается в «фабрику» по производству вакцины прямо внутри организма. Вакцинная «фабрика» способна работать длительный период — до года. ДНК-вакцинация приводит к полноценному иммунному ответу и обеспечивает высокий уровень защиты от вирусной инфекции.
ДНК-вакцинация заключается в том, чтобы ввести фрагмент ДНК, кодирующий защитные антигены и цитокины, непосредственно в мышечную ткань. «Заразность» большинства вирусов во многом определяется их структурными белками. Плазмида (кольцевая молекула ДНК) с генами таких белков, введенная в мышцу, стимулирует иммунный ответ, который препятствует развитию заболевания.
Используя один и тот же плазмидный или вирусный вектор, можно создавать вакцины против различных инфекционных заболеваний, меняя только последовательность, кодирующую необходимые белки-антигены. При этом отпадает необходимость работать с опасными вирусами и бактериями, становится ненужной сложная и дорогостоящая процедура очистки белков. Препараты ДНК-вакцин не требуют специальных условий хранения и доставки, они стабильны длительное время при комнатной температуре.
Уже разработаны и испытываются ДНК-вакцины против инфекций, вызываемых вирусами гепатитов B и C, гриппа, лимфоцитарного хориоменингита, бешенства, иммунодефицита человека (ВИЧ), японского энцефалита, а также возбудителями сальмонеллеза, туберкулеза и некоторых паразитарных заболеваний (лейшманиоз, малярия). Эти инфекции крайне опасны для человечества, а попытки создать против них надежные вакцинные препараты классическими методами оказались безуспешными.
ДНК-вакцинация — одно из самых перспективных направлений в борьбе с раком. В опухоль можно вводить разные гены: те, что кодируют раковые антигены, гены цитокинов и иммуномодуляторов.
Вакцины «по расчету»: «обратная вакцинология»
Бурное развитие в последнее десятилетие геномики, биоинформатики и протеомики привело к совершенно новому подходу в создании вакцин, получившему название «обратная вакцинология» (reverse vaccinology). Этот термин четко выражает суть нового технологического приема. Если раньше при создании вакцин ученые шли по нисходящей линии, от целого микроорганизма к его составляющим, то теперь предлагается противоположный путь: от генома – к его продуктам. Такой подход основан на том, что большинство защитных антигенов — белковые молекулы. Обладая полными знаниями обо всех белковых компонентах любого возбудителя заболевания, можно определить, какие из них годятся в качестве потенциальных кандидатов на включение в состав вакцинного препарата, а какие — нет.
Чтобы определить нуклеотидную последовательность полного генома инфекционного микроорганизма, достаточно если не нескольких дней, то нескольких недель. Причем предварительная работа по получению «библиотек» клонов ДНК возбудителя уже давно выполняется с помощью стандартных наборов ферментов. Современные приборы для автоматического определения нуклеотидной последовательности в молекулах ДНК позволяют проводить в год до 14 млн реакций. Полная расшифровка генома и его описание со списком кодируемых белков занимают несколько месяцев.
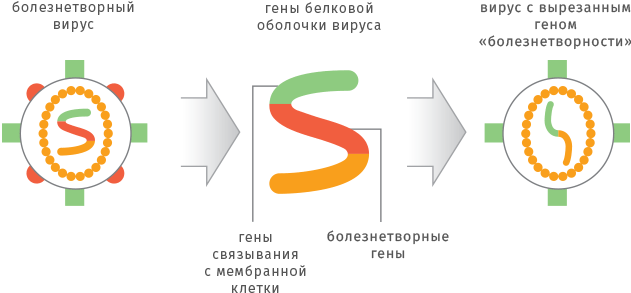
Рекомбинантные технологии позволяют получить ослабленный вирус за более короткое время. Для этого из генома вируса «вырезают» ген, который отвечает за вирулентность (болезнетворные свойства), но не влияет на размножение и иммуногенность. Получившийся безобидный вирусный штамм используют для изготовления вакцины.
Проведя компьютерный (in silico) анализ генома, исследователь получает не только список кодируемых белков, но и некоторые их характеристики, например, принадлежность к определенным группам, возможная локализация внутри бактериальной клетки, связь с мембраной, антигенные свойства.
Другой подход к отбору кандидатов в вакцины — определение активности отдельных генов микроорганизмов. Для этого одновременно измеряют уровень синтеза матричной РНК всех продуктов генов, производимых в клетке. Такая технология позволяет «вычислить» гены, вовлеченные в процесс распространения инфекции.
Третий подход основан на протеомной технологии. Ее методы дают возможность детализировать количественную и качественную характеристики белков в компонентах клетки. Существуют компьютерные программы, которые по аминокислотной последовательности могут предсказать не только трехмерную структуру изучаемого белка, но и его свойства и функции.
Используя эти три метода, можно отобрать набор белков и соответствующие им гены, которые представляют интерес для создания вакцины. Как правило, в эту группу входит около 20-30% всех генов бактериального генома. Для дальнейшей проверки нужно синтезировать и очистить отобранный антиген в количествах, необходимых для иммунизации животных. Очистку белка проводят с помощью полностью автоматизированных приборов. Используя современные технологии, лаборатория, состоящая из трех исследователей, может в течение месяца выделить и очистить более 100 белков.
Впервые принцип «обратной вакцинологии» использовали для получения вакцины против менингококков группы B. За последние годы таким способом разработаны вакцинные препараты против стрептококков Streptococcus agalactiae и S. pneumoniae, золотистого стафилококка, бактерии Porphyromonas gingivalis, вызывающей воспаление десен, провоцирующего астму микроорганизма Chlamydia pneumoniae и возбудителя тяжелой формы малярии Plasmodium falciparum.
Важно не только создать вакцину, но и найти наилучший способ ее доставки в организм. Сейчас появились так называемые мукозальные вакцины, которые вводятся через слизистые оболочки рта или носа либо через кожу. Преимущество таких препаратов в том, что вакцина поступает через входные ворота инфекции и тем самым стимулирует местный иммунитет в тех органах, которые первыми подвергаются атаке микроорганизмов.
Терапевтические вакцины
Обычные вакцины предназначены для предупреждения болезни: прививку делают здоровому человеку, чтобы заранее «вооружить» организм средствами борьбы с инфекцией (исключение — разработанная Пастером вакцина против бешенства, которую применяют после укуса бешеным животным; ее эффективность объясняется длительным инкубационным периодом этого вирусного заболевания). Но в последнее время отношение к вакцинам исключительно как к профилактическому средству изменилось. Появились терапевтические вакцины — препараты, которые индуцируют иммунный ответ у больных и тем самым способствуют выздоровлению или улучшению состояния. Такие вакцины нацелены на хронические заболевания, вызванные бактериями или вирусами (в частности, вирусами гепатитов B и C, вирусом папилломы, ВИЧ), опухоли (прежде всего, меланому, рак молочной железы или прямой кишки), аллергические или аутоиммунные болезни (рассеянный склероз, диабет I типа, ревматоидный артрит).
Существующие терапевтические вакцины для лечения хронических воспалительных заболеваний, вызванных бактериями или вирусами, получают классическими методами. Такие вакцины способствуют развитию иммунитета к входящим в их состав микроорганизмам и активизируют врожденный иммунитет.
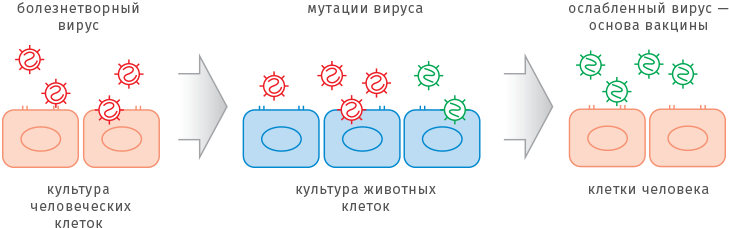
Один из традиционных методов ослабления вирусов — выращивание в животных клетках. Сначала болезнетворный вирус выделяют из культуры человеческих клеток. Выращивание вне человеческого организма само по себе ослабляет «заразность» вируса. Для некоторых заболеваний, например, краснухи, такой подготовки бывает достаточно, чтобы получить вакцинный штамм. Однако в общем случае для того, чтобы получить ослабленный штамм, вирус пересаживают в среду, приготовленную из клеток животных. Благодаря мутациям вирус приспособится к новой среде обитания. Для создания вакцины ученые отбирают те разновидности вирусов-мутантов, которые плохо растут на человеческих клетках, а значит, не могут вызвать болезнь.
Одна из важнейших целей разработчиков терапевтических вакцин — ВИЧ-инфекция. Уже проведена серия доклинических и клинических испытаний нескольких препаратов. Их способность вызывать развитие клеточного иммунитета у здоровых людей не вызывает сомнений. Однако убедительных данных о том, что вакцины подавляют размножение вируса у больных, пока нет.
Большие надежды в лечении нарушений иммунитета при раковых заболеваниях связаны с дендритными вакцинами. Их делают на основе дендритных клеток — особой разновидности лейкоцитов, которые занимаются поиском потенциально опасных микроорганизмов. Дендритные клетки «патрулируют», прежде всего, слизистые оболочки и кожу, то есть органы, контактирующие с внешней средой. Встретив патогенную бактерию или вирус, дендритные клетки поглощают «чужака» и используют его белки-антигены для того, чтобы активизировать иммунную систему на борьбу с врагом.
Схема изготовления дендритной вакцины такова: из крови больного выделяют клетки, которые дают начало дендритным клеткам, и размножают их в лабораторных условиях. Одновременно из опухоли пациента выделяют белки-антигены. Дендритные клетки некоторое время выдерживают вместе с опухолевыми антигенами, чтобы они запомнили образ врага, а затем вводят больному. Такая стимуляция иммунной системы заставляет организм активно бороться с опухолью.
Дендритные вакцины можно использовать для лечения как спонтанных опухолей, так и новообразований, ассоциированных с вирусами. Первые результаты испытания дендритных противораковых вакцин на людях (в небольших группах пациентов IV стадии заболевания) показали безвредность таких вакцин, а в ряде случаев зарегистрирован положительный клинический эффект.
У мышей дендритные вакцины помогают предупредить повторное развитие карциномы после удаления опухоли. Это позволяет надеяться, что они будут эффективны для продления безрецидивного периода онкологических больных после хирургического вмешательства.
В XX веке успехи вакцинологии определялись, прежде всего, победами над очередной опасной инфекцией. С развитием наших представлений о работе иммунной системы сфера применения вакцин постоянно расширяется. Есть надежда, что в XXI веке вакцины помогут снизить заболеваемость диабетом, миокардитом, атеросклерозом и другими «неинфекционными» болезнями. Полным ходом идет разработка препаратов для иммунопрофилактики и иммунотерапии онкологических заболеваний.
Источник