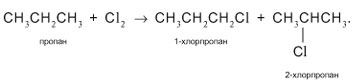
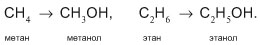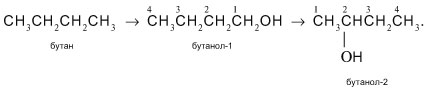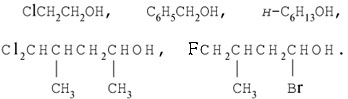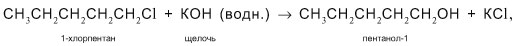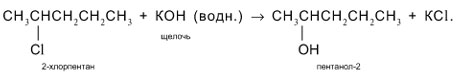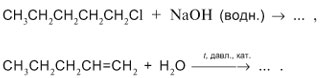- Одноатомные предельные спирты
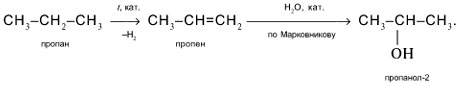
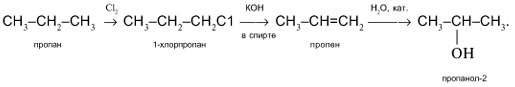
- Получение спиртов
- Пропанол-1: химические свойства и получение
- Строение пропанола-1
- Водородные связи и физические свойства спиртов
- Изомерия пропанола-1
- Структурная изомерия
- Химические свойства пропанола-1
- 1.1. Взаимодействие с раствором щелочей
- 1.2. Взаимодействие с металлами (щелочными и щелочноземельными)
- СН3–CH2–CH2–OK + H2O → СН3–CH2–CH2–OH + KOH
- 2. Реакции замещения группы ОН
- 2.1. Взаимодействие с галогеноводородами
- 2.2. Взаимодействие с аммиаком
- 2.3. Этерификация (образование сложных эфиров)
- 2.4. Взаимодействие с кислотами-гидроксидами
- 3. Реакции замещения группы ОН
- 3.1. Внутримолекулярная дегидратация
- 3.2. Межмолекулярная дегидратация
- 4. Окисление спиртов
- 4.1. Окисление оксидом меди (II)
- 4.2. Окисление кислородом в присутствии катализатора
- 4.3. Жесткое окисление
- 4.4. Горение спиртов
- 5. Дегидрирование спиртов
- Получение пропанола-1
- 1. Щелочной гидролиз галогеналканов
- 2. Гидрирование карбонильных соединений
Одноатомные предельные спирты
Спиртами называют производные углеводородов общей формулы RОН, где R – углеводородный радикал. Формула спирта получается из формулы соответствующего алкана заменой атома Н на группу ОН: RН 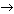
Вывести химическую формулу спиртов можно иначе, включая атом кислорода О между атомами
С–Н молекулы углеводорода:
RН 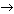
Гидроксильная группа ОН является функциональной группой спиртов. То есть группа ОН – особенность спиртов, она обусловливает главные физические и химические свойства этих соединений.
Общая формула одноатомных предельных спиртов – СnH2n+1OH.
Названия спиртов получают из названий углеводородов с таким же числом атомов С, как в спирте, добавлением суффикса —ол-. Например:
Название спиртов как производных соответствующих алканов характерно для соединений с линейной цепью. Положение группы ОН в них – при крайнем или при внутреннем атоме
С – указывают цифрой после названия:
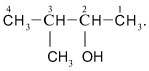
Названия спиртов – производных разветвленных углеводородов – составляют обычным образом. Выбирают главную углеродную цепь, которая должна включать атом С, соединенный с группой ОН. Нумеруют атомы С главной цепи таким образом, чтобы углерод с группой ОН получил меньший номер:
Название cоставляют, начиная с цифры, указывающей положение заместителя в главной углеродной цепи: «3-метил…» Затем называют главную цепь: «3-метилбутан. » Наконец добавляют суффикс —ол-(название группы ОН) и цифрой указывают атом углерода, с которым связана группа ОН: «3-метилбутанол-2».
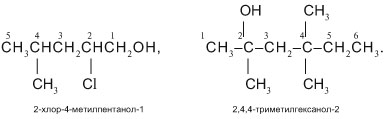
Если заместителей при главной цепи несколько, их перечисляют последовательно, указывая цифрой положение каждого. Повторяющиеся заместители в названии записывают с помощью приставок «ди-», «три-», «тетра-» и т.д. Например:
Изомерия спиртов. Изомеры спиртов имеют одинаковую молекулярную формулу, но разный порядок соединения атомов в молекулах.
Два вида изомерии спиртов:
1) изомерия углеродного скелета;
2) изомерия положения гидроксильной группы в молекуле.
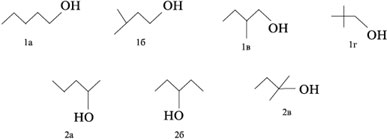
Представим изомеры спирта С5Н11ОН этих двух видов в линейно-уголковой форме записи:
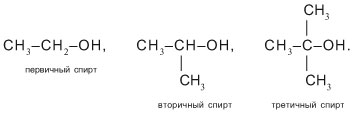
По числу атомов С, связанных со спиртовым (–С–ОН) углеродом, т.е. соседних с ним, спирты называют первичными (один сосед С), вторичными (два С) и третичными (три С-заместителя при углероде –С–ОН). Например:
Задача. Составьте по одному изомеру спиртов молекулярной формулы С6Н13ОН с главной углеродной цепью:
Решение
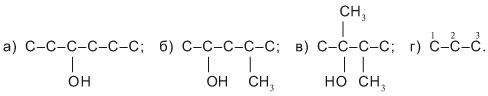
1) Записываем главные углеродные цепи с заданным числом атомов С, оставляя место для атомов Н (их укажем позже):
а) С–С–С–С–С–С; б) С–С–С–С–С; в) С–С–С–С; г) С–С–С.
2) Произвольно выбираем место присоединения группы ОН к главной цепи и при внутренних атомах С указываем углеродные заместители:
В примере г) нет возможности разместить три заместителя СН3– при атоме С-2 главной цепи. У спирта С6Н13ОН нет изомеров с трехуглеродной главной цепью.
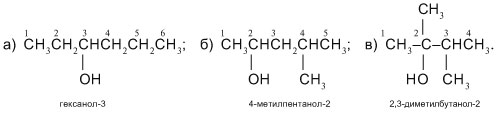
3) Расставляем атомы Н при углеродах главной цепи изомеров а)–в), руководствуясь валентностью углерода С(IV), и называем соединения:
УПРАЖНЕНИЯ.
1. Подчеркните химические формулы предельных одноатомных спиртов:
СН3ОН, С2Н5ОН, СН2=СНСН2ОН, СН
2. Назовите следующие спирты:
3. Составьте структурные формулы по названиям спиртов: а) гексанол-3;
б) 2-метилпентанол-2; в) н-октанол; г) 1-фенилпропанол-1; д) 1-циклогексилэтанол.
4. Составьте структурные формулы изомеров спиртов общей формулы С6Н13ОН:
а) первичного; б) вторичного; в) третичного. Назовите эти спирты.
5. По линейно-уголковым (графическим) формулам соединений запишите их структурные формулы и дайте названия веществам:
Получение спиртов
Низкомолекулярные спирты – метанол СН3ОН, этанол С2Н5ОН, пропанол С3Н7ОН, а также изопропанол (СН3)2СНОН – бесцветные подвижные жидкости со специфическим алкогольным запахом. Высокие температуры кипения: 64,7 °С – СН3ОН, 78 °С – С2Н5ОН, 97 °С – н-С3Н7ОН и 82 °С – (СН3)2СНОН – обусловлены межмолекулярной водородной связью, существующей в спиртах. Спирты С(1)–С(3) смешиваются с водой (растворяются) в любых соотношениях. Эти спирты, особенно метанол и этанол, наиболее широко используются в промышленности.
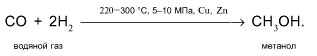
1. Метанол синтезируют из водяного газа:
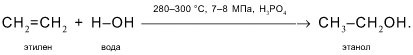
2. Этанол получают гидратацией этилена (присоединением воды к С2Н4):
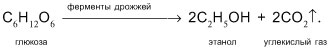
3. Другой способ получения этанола – сбраживание сахаристых веществ под действием дрожжевых ферментов. Процесс спиртового брожения глюкозы (виноградного сахара) имеет вид:
4. Этанол получают из крахмала, а также из древесины (целлюлозы) путем гидролиза до глюкозы ипоследующего сбраживания в спирт:
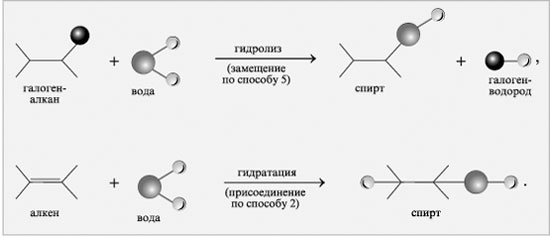
5. Высшие спирты получают из галогенпроизводных углеводородов гидролизом под действием водных растворов щелочей:
 | ||||||||||||||||||||||||||||||
| Электроотрицательность кислорода (ЭО = 3,5) больше электроотрицательности водорода (ЭО = 2,1) и углерода (ЭО = 2,4). |
Электронная плотность обеих связей смещена к более электроотрицательному атому кислорода:
| Атом кислорода в спиртах находится в состоянии sp 3 -гибридизации. |
В образовании химических связей с атомами C и H участвуют две 2sp 3 -гибридные орбитали, а еще две 2sp 3 -гибридные орбитали заняты неподеленными электронными парами атома кислорода.
Поэтому валентный угол C–О–H близок к тетраэдрическому и составляет почти 108 о .
Водородные связи и физические свойства спиртов
Спирты образуют межмолекулярные водородные связи. Водородные связи вызывают притяжение и ассоциацию молекул спиртов:
Поэтому спирты – жидкости с относительно высокой температурой кипения (температура кипения пропанола +92 о С).
Водородные связи образуются не только между молекулами спиртов, но и между молекулами спиртов и воды. Поэтому спирты очень хорошо растворимы в воде. Молекулы спиртов в воде гидратируются:
| Чем больше углеводородный радикал, тем меньше растворимость спирта в воде. Чем больше ОН-групп в спирте, тем больше растворимость в воде. |
Пропанол смешивается с водой в любых соотношениях.
Изомерия пропанола-1
Структурная изомерия
Для пропанола-1 характерна структурная изомерия – изомерия положения гидроксильной группы и межклассовая изомерия.
Структурные изомеры — это соединения с одинаковым составом, которые отличаются порядком связывания атомов в молекуле, т.е. строением молекул.
Межклассовые изомеры — это вещества разных классов с различным строением, но одинаковым составом. Спирты являются межклассовыми изомерами с простыми эфирами. Общая формула и спиртов, и простых эфиров — CnH2n+2О.
| Например. Межклассовые изомеры с общей формулой С3Н8О пропиловый спирт СН3–CH2–CH2–OH и метилэтиловый эфир CH3–O–CH2–CH3 |
| Пропиловый спирт | Метилэтиловый эфир |
| СН3–CH2–CH2–OH | CH3–O–CH2–CH3 |
Изомеры с различным положением группы ОН отличаются положением гидроксильной группы в молекуле. Такая изомерия характерна для спиртов, которые содержат три или больше атомов углерода.
| Например. Пропанол-1 и пропанол-2 |
| Пропанол-1 | Пропанол-2 |
 |  |
Химические свойства пропанола-1
Спирты – органические вещества, молекулы которых содержат, помимо углеводородной цепи, одну или несколько гидроксильных групп ОН.
Химические реакции гидроксисоединений идут с разрывом одной из связей: либо С–ОН с отщеплением группы ОН, либо связи О–Н с отщеплением водорода. Это реакции замещения, либо реакции отщепления (элиминирования).
Свойства спиртов определяются строением связей С–О–Н. Связи С–О и О–Н — ковалентные полярные. При этом на атоме водорода образуется частичный положительный заряд δ+, на атоме углерода также частичный положительный заряд δ+, а на атоме кислорода — частичный отрицательный заряд δ–.
Такие связи разрываются по ионному механизму. Разрыв связи О–Н с отрывом иона Н + соответствует кислотным свойствам гидроксисоединения. Разрыв связи С–О соответствует основным свойствам и реакциям нуклеофильного замещения.
С разрывом связи О–Н идут реакции окисления, а с разрывом связи С–О — реакции восстановления.
Таким образом, для спиртов характерны следующие свойства:
|
1. Кислотные свойства пропанола-1
| Спирты – неэлектролиты, в водном растворе не диссоциируют на ионы; кислотные свойства у них выражены слабее, чем у воды. |
1.1. Взаимодействие с раствором щелочей
При взаимодействии спиртов с растворами щелочей реакция практически не идет, т. к. образующиеся алкоголяты почти полностью гидролизуются водой.
Равновесие в этой реакции так сильно сдвинуто влево, что прямая реакция не идет. Поэтому пропанол-1 не взаимодействует с растворами щелочей.
1.2. Взаимодействие с металлами (щелочными и щелочноземельными)
Пропанол-1 взаимодействует с активными металлами (щелочными и щелочноземельными). При этом образуются алкоголяты. При взаимодействии с металлами спирты ведут себя, как кислоты.
| Например, пропанол-1 взаимодействует с калием с образованием пропилата калия и водорода . |
Алкоголяты под действием воды полностью гидролизуются с выделением спирта и гидроксида металла.
| Например, пропилат калия разлагается водой: |
СН3–CH2–CH2–OK + H2O → СН3–CH2–CH2–OH + KOH
2. Реакции замещения группы ОН
2.1. Взаимодействие с галогеноводородами
При взаимодействии спиртов с галогеноводородами группа ОН замещается на галоген и образуется галогеналкан.
| Например, пропанол-1 реагирует с бромоводородом. |
2.2. Взаимодействие с аммиаком
Гидроксогруппу спиртов можно заместить на аминогруппу при нагревании спирта с аммиаком на катализаторе.
| Например, при взаимодействии пропанола-1 с аммиаком образуется пропиламин. |
2.3. Этерификация (образование сложных эфиров)
Cпирты вступают в реакции с карбоновыми кислотами, образуя сложные эфиры.
| Например, пропанол-1 реагирует с уксусной кислотой с образованием пропилацетата (пропилового эфира уксусной кислоты): |
2.4. Взаимодействие с кислотами-гидроксидами
Спирты взаимодействуют и с неорганическими кислотами, например, азотной или серной.
| Например, при взаимодействии пропанола-1 с азотной кислотой образуется пропилнитрат. |
3. Реакции замещения группы ОН
В присутствии концентрированной серной кислоты от спиртов отщепляется вода. Процесс дегидратации протекает по двум возможным направлениям: внутримолекулярная дегидратация и межмолекулярная дегидратация.
3.1. Внутримолекулярная дегидратация
При высокой температуре происходит внутримолекулярная дегидратация и образуется соответствующий алкен.
| Например, из пропанола-1 под действием концентрированной серной кислоты при высокой температуре образуется пропилен: |
3.2. Межмолекулярная дегидратация
При низкой температуре происходит межмолекулярная дегидратация: ОН-группа в одной молекуле спирта замещается на группу OR другой молекулы. Продуктом реакции является простой эфир.
| Например, при дегидратации пропанола-1 при низкой температуре образуется дипропиловый эфир: |
4. Окисление спиртов
Реакции окисления в органической химии сопровождаются увеличением числа атомов кислорода (или числа связей с атомами кислорода) в молекуле и/или уменьшением числа атомов водорода (или числа связей с атомами водорода).
В зависимости от интенсивности и условий окисление можно условно разделить на каталитическое, мягкое и жесткое.
| Вторичные спирты окисляются в кетоны: в торичные спирты → кетоны |
Типичные окислители — оксид меди (II), перманганат калия KMnO4, K2Cr2O7, кислород в присутствии катализатора.
4.1. Окисление оксидом меди (II)
Cпирты можно окислить оксидом меди (II) при нагревании. При этом медь восстанавливается до простого вещества. Первичные спирты окисляются до альдегидов.
| Например, пропанол-1 окисляется оксидом меди до пропионового альдегида |
4.2. Окисление кислородом в присутствии катализатора
Cпирты можно окислить кислородом в присутствии катализатора (медь, оксид хрома (III) и др.). Первичные спирты окисляются до альдегидов.
| Например, при окислении пропанола-1 образуется пропаналь |
4.3. Жесткое окисление
При жестком окислении под действием перманганатов или соединений хрома (VI) первичные спирты окисляются до карбоновых кислот.
| При нагревании первичного спирта с перманганатом или дихроматом калия в кислой среде может образоваться также альдегид, если его сразу удаляют из реакционной смеси. |
| Например, при взаимодействии пропанола-1 с перманганатом калия в серной кислоте образуется пропионовая кислота |
4.4. Горение спиртов
Образуются углекислый газ и вода и выделяется большое количество теплоты.
| Например, уравнение сгорания пропанола-1: |
5. Дегидрирование спиртов
При нагревании спиртов в присутствии медного катализатора протекает реакция дегидрирования. При дегидрировании первичных спиртов образуются альдегиды.
| Например, при дегидрировании пропанола-1 образуется пропаналь. |
Получение пропанола-1
1. Щелочной гидролиз галогеналканов
При взаимодействии галогеналканов с водным раствором щелочей образуются спирты. Атом галогена в галогеналкане замещается на гидроксогруппу.
| Например, при нагревании 1-хлорпропана с водным раствором гидроксида натрия образуется пропанол-1 |
2. Гидрирование карбонильных соединений
Присоединение водорода к альдегидам протекает при нагревании в присутствии катализатора. При гидрировании альдегидов образуются первичные спирты.
Источник