- Технологии получения Н2
- ЭЛЕКТРОЛИЗ
- ИОНИЗАТОРЫ ВОДЫ
- ГЕНЕРАТОРЫ ВОДОРОДНОЙ ВОДЫ
- ОТЛИЧИЯ ОБЫЧНОГО ЭЛЕКТРОЛИЗА ОТ СОВРЕМЕННЫХ ПОЛИМЕРНЫХ МЕМБРАН
- ХИМИЧЕСКАЯ РЕАКЦИЯ МЕТАЛЛОВ С ВОДОЙ
- ЩЕЛОЧНЫЕ АЛКАЛИНОВЫЕ СТЕРЖНИ НЕ ВЫДЕЛЯЮТ ВОДОРОД.
- БАРБОТИРОВАНИЕ
- ВОДОРОДНАЯ ВОДА В ПРИРОДЕ
- ЦЕЛЕБНЫЕ ВОДОРОДНЫЕ ИСТОЧНИКИ В МИРЕ
- Разделяй и властвуй: совершенствование электролиза воды
- Основа исследования
- Результаты исследования
- Эпилог
- Немного рекламы 🙂
Технологии получения Н2
Существует несколько способов получения водородной воды, включая электролиз (например, ионизаторы воды или специальные водородные генераторы), химическая реакция щелочными металлами и воды (например, алюминий, магний) или просто барботирование газообразного H2 в воду.
ЭЛЕКТРОЛИЗ
На рынке существует множество приборов и устройств, способных изменять химические и физические показатели воды при помощи электрического тока. Современные технологии научилась определять какие именно показатели воды имеют полезные и терапевтические свойства.
В настоящее время для производства водородной воды используется 2 метода электролиза, это электрические системы, которые воздействуют электрическим током через минеральные соли в воде, а именно, ионизаторы щелочной воды и генераторы водородной воды с нейтральным рН.
ИОНИЗАТОРЫ ВОДЫ
Ионизатором воды является любое устройство или изделие, которое увеличивает концентрацию заряженных частиц — ионов и свободных электронов. В данном методе образуется щелочная среда с насыщением водорода на катоде и кислая среда с насыщением кислорода на аноде, где анод и катод разделены барьером.
Приборы ионизации воды существуют очень давно и в настоящее время ежегодно появляются новые приборы и изделия для изменения свойств воды.
Что такое ионизация воды?
Под ионом подразумевается электрически заряженная частица (положительная или отрицательная) в виде атома или молекулы, которые образовываются при присоединении или потери электронов. Поэтому любое устройство, которое увеличивает концентрацию ионов является ионизатором воды.
После научного открытия ионизации воды путем электролиза М.Фарадея были обнаружены и другие возможности ионизации воды. Процесс ионизации можно получить несколькими способами, но его эффективность и себестоимость будет существенно отличаться.
Важно обратить внимание на то, что ионизаторы щелочной воды были разработаны до того, как стало известно о терапевтических свойствах Н2. Таким образом, эти устройства были оптимизированы для щелочного pH, а не для высокой концентрации растворенного водорода.
Только после 2007 года ученые обнаружили, что терапевтическое свойство в щелочной ионизированной воде представляет собой газообразный водород Н2. Поэтому для терапевтического эффекта важна концентрация Н2 в воде.
Важно также отметить, что, хотя некоторые ионизаторы воды могут создавать очень высокую концентрацию Н2 за счет замедления потока воды, эта продуцируемая вода часто имеет очень высокий уровень рН, что может сделать воду неприемлемой. В этом случае легко снизить pH путем добавления нескольких капель лимонного сока (лимонной кислоты) для снижения рН при сохранении более высокого уровня, растворенного Н2.
ГЕНЕРАТОРЫ ВОДОРОДНОЙ ВОДЫ
Генераторы водорода изначально разработаны для производства водорода, где конструкция, электроды и поток воды сделаны для получения высокой концентрации Н2. Однако прогресс не стоит на месте и недавно появились современные протонообменные мембраны (PEM) на основе твердого полимерного электролита (SPE).
Протонообменная мембрана, это прорыв в электролизе воды, которая позволяет получить более высокую концентрацию чистого Н2 с отделением побочных продуктов электролиза кислорода (О2), озона (О3), и хлора (Cl2).
Как происходит электролиз в SPE/PEM мембране?
Вода проникает через поры мембраны в анодное пространство. На границе анода и мембраны происходит электроокисление воды с выделением кислорода:
2H2O + 4e» —► O2 + 4H+
Непроницаемость PEM мембраны для кислорода препятствует его проникновению в катодное пространство и образованию взрывоопасной гремучей смеси кислорода и водорода. В итоге, кислород удаляется из реакционной зоны.
Далее протоны Н+ движутся через мембрану к катоду, где происходит их восстановление с электронами с выделением газообразного водорода:
Протекание катодной и анодной реакций стимулируется введением на границе раздела электродов и полимерных катализаторов — мелкодисперсных платины и оксида иридия, что делает процесс электролиза более эффективным.
В результате вы получаете воду с высокой концентрацией чистого Н2 (более 1,2 мг/л всего за 5 мин) без примесей продуктов распада электролиза и ОВП до -500 мВ.
ОТЛИЧИЯ ОБЫЧНОГО ЭЛЕКТРОЛИЗА ОТ СОВРЕМЕННЫХ ПОЛИМЕРНЫХ МЕМБРАН
Современные полимерные мембраны SPE/PME сами являются электролитом, поэтому им не требуется вода с содержанием минералов для проводимости тока, в связи с чем они имеют огромное технологическое преимущество, долгий срок службы и способны производить высокую концентрацию чистого Н2.
Благодаря более низкому электрическому сопротивлению между анодом и катодом в полимерной мембране происходит меньшее падение напряжения и более эффективный электролитический выход H2. Увеличение срока службы мембраны связано с тем, что рН питьевой воды практически не меняется, соответственно не происходит образования минерального налета на электродах.
Почему это важно, что в приборе есть протонобменная мембрана/ Твердый полимерный электролит?
Вода в приборе не является электролитом, электролиз идет внутри мембраны, вода только насыщается чистым водородом. Рекомендуется использовать дистиллированную воду или воду обратного осмоса. Это позволяет долгое время сохранять работоспособность мембраны, без необходимости в промывках.
Бывают ли приборы, разделяющие при электролизе водород и кислород, но без протонобменной мембраны?
Да, даже самые в первых приборах для электролиза в виде U образной трубки водород и кислород получались отдельно. Но электролитом в них является раствор солей в воде и помимо водорода и кислорода будут выделяться другие соединения. Бывают также приборы с мембраной, отделяющей водород, но при этом мембрана не является твердым полимерным электролитом. Эти приборы требуют использования воды с солями, поэтому мембрана засоряется и требует частых промывок. Узнайте, может ли прибор работать с дистиллированной водой, чтобы понять используется ли в нем SPE/PEM мембрана.
ХИМИЧЕСКАЯ РЕАКЦИЯ МЕТАЛЛОВ С ВОДОЙ
Другой простой и удобный способ получения воды, насыщенной Н2 заключается на химической реакции щелочноземельных металлов и воды. Например, хорошо известно, что добавление металлического натрия или калия к воде приводит к огненному взрыву.
Обратите внимание, что это металлическая форма натрия, а не ионная соль (т.е. металлический натрий, а не хлорид натрия [Na+ Cl- ]). Причина, по которой происходит эта реакция, заключается в том, что металлы быстро отдают свой внешний валентный электрон воде, которая производит молекулярный водород и гидроксид натрия: (2Na + 2H2 O -> H 2 + 2NaOH). Полученный гидроксид натрия (NaOH) диссоциирует с образованием ионов натрия (Na+ ) и гидроксид-ионов (OH- ) в соответствии с: NaOH -> Na + + OH — . Эти металлы настолько бурно реагируют с водой, что выделяется достаточно тепла, чтобы воспламенить образовавшийся газообразный водород.
Самой безопасной химической реакцией металла с водой для получения Н2 является магний. Mg+2H2O->H2 +Mg(OH)2.
Гидроксид магния (Mg(OH-)2) диссоциирует на ионы магния (Mg2+) и гидроксид ионы (ОН-) в соответствии с равновесием:
Есть магниевые палочки, которые можно поместить в воду, таблетки магния, которые растворяются в воде, таблетки, которые можно употреблять (которые производят H2 в желудке), или устройства картриджного типа, которые можно поместить в воду, быстро производя 2-4 мг/кг. Концентрация LH 2 , а также фильтры для воды, содержащие залитую магниевую среду. Как и электролиз, все эти методы увеличивают pH воды, поскольку они снижают концентрацию ионов H +.
В нашем магазине Вы можете купить водородные таблетки «Шипучий магний Drink HRW» позволяют получать самые высокие концентрации растворенного водорода в воде (более 7,0мг/л) всего за 1 минуту.
ЩЕЛОЧНЫЕ АЛКАЛИНОВЫЕ СТЕРЖНИ НЕ ВЫДЕЛЯЮТ ВОДОРОД.
На рынке воды существует большое количество недорогих щелочных алкалиновых стержней либо минеральных солей (турмалин, шунгит, кремний, оксиды и соли Mg, K, Ca, Na,Fe). Алкалиновые стержни делают воду щелочной, за счет обмена ионами и не выделяют водород в достаточном количестве.
Такие изделия имеют более низкую стоимость, и они воздействуют только на кислотно-щелочной баланс организма, минимально влияя на свободные радикалы.
Важно! Обращайте внимание на состав изделия и названия минералов. Только металлический магний образует газообразный водород, который имеет терапевтический эффект!
БАРБОТИРОВАНИЕ
Еще одним из популярных методов обогащения воды газом Н2 является Барботирование.
Барботирование — это процесс пропускания газа или пара через слой жидкости. Газ продавливается через слой жидкости с помощью трубки с мелкими отверстиями.
Данный метод часто используется в промышленности и в быту, например насыщение кислородом аквариумов.
На качество насыщения воды водородом влияют следующие характеристики барботажа:
- Давление газа. Чем больше давление, тем лучше растворение.
- Размер пузырьков. Чем меньше размер, тем лучше растворяется.
- Время прохождения пузырьков через слой воды. Чем дольше пузыри находятся в воде, тем больше насыщение.
- Температура воды. В холодной воде растворение водорода происходит лучше.
Для уменьшения пузырьков используют специальные полимерные аэраторы, которые позволяют получить нано пузырьки, в результате насыщение воды водородом увеличится в разы.
Данный метод часто используется для водородных ванн и других больших емкостей с водой.
ВОДОРОДНАЯ ВОДА В ПРИРОДЕ
Известно, что в природе существует очень полезная вода. Например, из горных источников, а люди, живущие с ней рядом и постоянно употребляя ее, являются долгожителями.
Известный факт, что средняя продолжительность жизни мужчин и женщин на Северном Кавказе составляет 112 и 114 лет соответственно. В горных источниках присутствует «легкий водород» в питьевой воде и пониженное содержание кислорода в воздухе, что и является одними из главных источников долгожительства.
Польза такой воды обусловлена тем, что она проходит через земные минералы, в результате чего обогащается полезными свойствами. Эффективность такой воды имеет место только при употреблении ее из источника т.к. при длительном взаимодействии с атмосферным воздухом (10-12 часов) вода теряет свои целебные свойства.
ЦЕЛЕБНЫЕ ВОДОРОДНЫЕ ИСТОЧНИКИ В МИРЕ
На земле имеются, известные на весь мир, источники целебной воды, такие как Лурд во Франции, Норденау в Германии, Тлакота в Мексике и Надана в Индии.
Каждый год огромное количество людей с самыми разными заболеваниями приезжают к этим святым местам. Все они хотят испить целебной воды из святых источников, чтобы избавиться от своих заболеваний. Целебность этих источников подтверждена многими уникальными случаями.
Ученые стали изучать свойства этих вод и обнаружили единственное схожее свойство, делающее их уникальными – это большое содержание газообразного водорода. Концентрация Н2 в этих водах составляет 0,2 – 0,8 мг/л. Для сравнения, в обычной воде водородный показатель воды приблизительно равен 0,018 ppm. Поэтому такую воду стали называть – водородная вода.
Лурдская вода Франции
66 пациентов с неизлечимыми заболеваниями получили свидетельства об их выздоровлении. Концентрация водорода: 800ppb (0,8 мг/л)
Колодец Тлакота в Мексике
Он стал известен благодаря Magic Johnson, игроку NBA, о его СПИДе. Концентрация водорода: 200 ppb (0,2 мг/л)
Подземная вода рудника Норденауэр в Германии
Было зарегистрировано исцеления от рака крови и диабета. Концентрация водорода: 420 ppb (0,42 мг/л)
Колодец Наданы Индии
Это знаменитая достопримечательность для лечения кожных заболеваний, полиомиелита и т. д. Концентрация водорода: 180 ppb (0,18 мг/л)
Источник
Разделяй и властвуй: совершенствование электролиза воды
Одной из самых известных химических формул, которые нам известны еще со школьной скамьи, является H2O — оксид водорода, т.е вода. Без этого простого на первый взгляд вещества жизнь на нашей планете была бы совершенно иной, если вообще была бы. Помимо своих животворящих функций у воды имеется масса других применений, среди которых стоит выделить получение водорода (H). Одним из методов достижения этого является электролиз воды, когда ее разделяют на составляющие, т.е. на кислород и водород. Это достаточно сложный, затратный, но эффективный метод. Тем не менее, нет в мире такого, что ученые не хотели бы улучшить. Команда исследователей из университета штата Вашингтон и Лос-Аламосской национальной лаборатории нашли способ усовершенствовать электролиз воды, значительно снизив себестоимость его проведения без снижения результата. Какие изменения пришлось внедрить в электролиз воды, почему были использованы те или иные вещества, и какие результаты показывает обновленный метод добычи водорода? Об этом нам поведает доклад ученых. Поехали.
Основа исследования
Водород во многом уникальный элемент: он самый легкий среди элементов периодической таблицы, а его одноатомный вариант является самым распространенным веществом во Вселенной. Кроме того водород крайне дружелюбный элемент, с легкостью формирующий ковалентные связи с большинством неметаллов. В природе мы встречаем водород чаще в составе какого-то вещества, в том числе и в воде, нежели, так сказать, в одиночку.
При обычных условиях водород представляет собой газ без запаха и вкуса с химической формулой Н2. У него есть и жидкий эквивалент — жидкий водород, который хоть и не так популярен в массовой культуре, как жидкий азот, но не менее экстремален в аспекте температур: точка замерзания −259.14 °C; точка кипения −252.87 °C.
Для перечислений всех конкретных применений водорода понадобится немало времени, так как он принимает активное участие в самых разных сферах производства: пищевая промышленность, металлургия, производство электроники, производство аммиака и т.д. Не говоря уже об использовании водорода в качестве ракетного топлива.
Методов получения водорода также существует несколько: из природного газа, из угля и посредством электролиза воды. В год в мире по примерной оценке используется порядка 70 миллионов тонн, из которых лишь 100 000 тонн производится методом электролиза.
Такая методологическая «дискриминация» обусловлена сложностью и ценой электролиза в совокупности с получаемыми объемами водорода по сравнению с другими методами. Однако всегда есть возможность для совершенствования, о чем и пойдет речь далее, но обо всем по порядку.
Движущей силой электролиза воды для ее расщепления на кислород и водород является электричество. По словам ученых, низкотемпературный электролиз воды представляет особый интерес для сферы возобновляемой энергетики, так как этот метод может позволить хранить электроэнергию из возобновляемых источников в химических связях в форме водорода высокой чистоты.
При низкотемпературном электролизе воды в качестве электролита (проводящее ток вещество) используется концентрированный раствор KOH (гидроксид калия), протонообменная мембрана (PEM от proton-exchange membrane) или щелочная анионообменная мембрана (AEM от alkaline anion exchange membrane).
Основное преимущество AEM электролиза над другими вариантами заключается в его стоимости. То есть для его реализации нет необходимости использовать металлы платиновой группы (PGM от platinum-group metals) в качестве катализаторов. Однако всегда есть подвох, заключающийся в данном случае в нестабильности щелочного метода, ввиду чувствительности к перепадам давления и низкой скорости производства водорода.
В традиционных щелочных электролизерах (установка для электролиза) жидкий щелочной электролит (30–40 мас.% КОН) циркулирует через электроды, которые разделены пористой мембраной (1а).

Изображение №1: схема низкотемпературного электролиза воды.
Данный метод работает при плотности тока в 300–400 мА см -2 при температуре 60–90 °C и напряжении 1.7–2.4 В. Также ученые отмечают, что жидкий КОН очень чувствителен к CO2, которого предостаточно в воздухе, формируя в результате K2CO3. Этот процесс в свою очередь снижает анодную реакцию и ионную проводимость, а полученный K2CO3 осаждается в порах газодиффузионного слоя, блокируя перенос ионов. Вывод достаточно прост — производительность электролиза на базе КОН снижается из-за его свойств, которые крайне сложно контролировать.
В качестве альтернативы могут выступить электролизеры на основе ионообменных мембран, которые могут заменить жидкий электролит полимерным электролитом. PEM электролизеры обычно работают при более высоких плотностях тока (1–3 А см -2 при
2.0 В), чем у щелочных электролизеров, поскольку протонообменная мембрана имеет более высокую проводимость. (1b).
Использование твердых электролитов в PEM электролизе воды позволяет создать компактную систему с долговечными и устойчивыми структурными свойствами при высоких перепадах давления (200–400 psi). Но даже в этом методе есть свои недостатки, в частности высокая стоимость установки для электролиза, ввиду дорогостоящего кислотостойкого оборудования и необходимости в металлах платиновой группы.
В AEM электролизе за последние несколько лет произошло несколько изменений. Одним из самых важных является создание полимерных AEM (1с). Щелочной AEM-электролиз сочетает в себе многие преимущества других методов: возможность использовать катализаторы без PGM; возможность применять чистую воду или низкоконцентрированный щелочной раствор вместо концентрированных щелочных электролитов; низкие омические потери из-за высокой проводимости и тонких AEM. В дополнение к этому мембранная конструкция установки позволяет ей работать при значительных перепадах давления, а также снижает ее габариты и вес. Не говоря уже о снижении стоимости данного устройства.
Достоинств много, прям не успеваешь восхищаться, однако есть и недостатки. Весьма существенным минусом щелочного AEM электролиза является сам факт использования коррозионного концентрированного щелочного электролита. Если же использовать чистую воду, то производительность будет до смешного маленькой (400 мА см -2 при 1.8 В).
В своем исследовании ученые решили попытаться избавиться от некоторых недостатков данного метода, тем самым сделав его более привлекательным для массового производства водорода. Исследователи выяснили, что высокая концентрация четвертичных аммониевых соединений необходима для повышения активности реакций выделения водорода и кислорода в AEM электролизере. Также было установлено, что фенильные группы в основной цепи иономера* имеют негативный эффект, образуя кислые фенолы при высоких анодных потенциалах.
Иономер* — полимеры, состоящие из электрически нейтральных и ионизированных составных звеньев, ковалентно связанных с основной цепью полимера в виде боковых групп атомов.
Кватернизаця* — преобразование соединений элементов 15-ой группы (N, P, As, Sb), атомы которых имеют свободную электронную пару, в четвертичные соли при взаимодействии с реагентами типа RX (Х — анионоидная группа).
Результаты исследования
Прежде чем понять, на что способен усовершенствованный AEM электролизер, необходимо было установить, чего он не может, т.е выяснить факторы, ограничивающие его производительность. Для этого были проведены эксперименты с вращающимся дисковым электродом (RDE от rotating disk electrode). RDE эксперименты предоставляют информацию о различных требованиях к электролитам, используемым в топливных элементах и электролизерах, путем измерения реакции выделения кислорода (OER), реакции выделения водорода (HER), реакции восстановления кислорода (ORR) и реакции окисления водорода (HOR).

Изображение №2: влияние концентрации NaOH (гидроксид натрия) на активность электрокатализаторов.
На графиках выше показаны поляризационные кривые OER с использованием IrO2 и HER с использованием поликристаллического платинового электрода (Pt poly) в зависимости от концентрации NaOH. Активность OER и HER для AEM электролизера значительно увеличивалась при увеличении концентрации NaOH с 0.01 М (рН = 12) до 1 М (рН = 14). HOR активность Pt poly проявляет максимальную активность при концентрации NaOH в 0.02 М (вставка на 2b). Потеря активности HOR при более высокой концентрации NaOH (> 0.1 М) также сопровождалась более низкой плотностью тока, ограничивающей диффузию.
Более низкая HOR активность Pt poly с концентрированным раствором NaOH объясняется кумулятивной совместной адсорбцией катион-гидроксид-вода, что ограничивает доступ водорода к поверхности катализатора. Однако совместная адсорбция не влияет на активность HER и OER, поскольку адсорбция происходит от 0 до 0.9 В. Влияние концентрации NaOH на активность ORR Pt poly показало тенденцию, аналогичную HOR.
ORR-активность Pt поли увеличивалась при увеличении концентрации NaOH с 0,01 до 0.1 М, затем начинала уменьшаться при дальнейшем увеличении концентрации NaOH до 1 М.
Результаты экспериментов предполагают, что концентрация гидроксида аммония, необходимая для AEM электролизеров и AEM топливных элементов, может быть различной. Для AEM электролизеров предпочтительнее иономер с более высокой ионообменной емкостью (IEC от ionexchange capacity). Для AEM топливных элементов лучше подойдет иономер со средним IEC, так как иономеры с более высоким IEC вызывают ограниченный перенос газа из-за нежелательной совместной адсорбции катион-гидроксид-вода.
Далее ученые решили выяснить, каким должен быть иономер для AEM электролизеров. Эксперименты с RDE показали, что обеспечение условий с высоким pH (> 13) в электродах имеет важное значение для создания высокоэффективных AEM электролизеров.
На данный момент доступные анионообменные иономеры имеют две критические проблемы, которые могут ограничивать среду с высоким pH в AEM электролизерах.
Первая проблема заключается в наличии фенильных групп в основной цепи иономера. Ранее проведенное исследование показало, что фенильная группа в основной цепи иономера может окисляться при OER потенциалах и образовывать фенольное соединение, которое является кислым (pKa = 9.6). К сожалению, большинство стабильных щелочных иономеров содержат фенильные группы в своей структуре.
Следовательно, AEM электролизеры, использующие иономеры, содержащие фенильную группу, так или иначе подвержены образованию фенола.
В аспекте окисления фенильной группы было обнаружено несколько крайне важных особенностей. Скорость образования фенола связана с энергией адсорбции фенильной группы на поверхности OER катализаторов, а незамещенные фенильные группы в боковой цепи полимера оказывают более вредное воздействие по сравнению с замещенной аммонием фенильной группой.
Структура и размер фрагментов основной цепи в полиароматических соединениях сильно влияют на адсорбцию фенила, тогда как функционализированная боковой цепью фенильная группа демонстрирует гораздо более низкую энергию адсорбции из-за конкурирующей адсорбции с аммониевыми группами. Кроме того, биметаллические платиновые катализаторы (например, PtRu, PtNi и PtMo) могут эффективно снижать энергию адсорбции фенила.
Вторая проблема заключается в низкой концентрации функциональных групп гидроксида аммония в анионообменных иономерах. Значение IEC классических анионообменных иономеров, разработанных для AEM топливных элементов, обычно составляет около 1.5 мЭкв г -1 (мЭкв — миллиэквивалент). Для иономера предполагаемая концентрация аммония в наполненном водой электроде относительно низкая (
0.1 М). Неоднородное распределение иономера в электроде дополнительно снижает эффективность реакции и проводимость гидроксида. Следовательно, иономеры с более высоким IEC должны быть полезны для повышения производительности AEM электролизера.
Однако одно тянет за собой другое, так как для синтеза иономера с высоким IEC необходимо учитывать несколько критериев.
Во-первых, существует ограничение на максимальное количество аммониевых групп на полимерное составное звено (группа атомов, составляющих полимер).
Во-вторых, анионообменные иономеры с высоким IEC часто подвергаются реакции сшивания во время процесса функционализации, что затрудняет дальнейшую обработку.
И, в-третьих, когда анионообменные иономеры синтезируются с высоким IEC, они часто становятся растворимыми в воде, что непригодно для применения в электродах.
Как ни крути, а обойти все эти ограничения будет не так и просто. Тем не менее, взяв за основу вышеописанные данные, ученые подготовили несколько функционализированных триметиламмонием полистирольных иономеров (3а).

Изображение №3: химическая структура полимерных материалов, использованных в исследовании.
Созданные иономеры обладали достаточно уникальными характеристиками по сравнению с обычными иономерными связующими, разработанными для AEM топливных элементов.
Во-первых, основная алифатическая полимерная цепь не содержит фенильной группы. Отсутствие фенильной группы в основной цепи полимера исключает возможность адсорбции фенила и образования кислого фенола.
Во-вторых, основная цепь полимера не содержит длинных неионных алкильных цепей, которые могут снизить растворимость полимера.
В-третьих, все фенильные группы в боковых цепях имеют замещенные аммониевые или аминные группы, которые минимизируют адсорбцию фенильных групп и помогают поддерживать высокий рН.
По завершению синтеза иономеров было обнаружено, что их IEC варьируется в диапазоне от 2.2 до 3.3. Для AEM был подготовлен HTMA-DAPP, т.е. полифенилен Дильса-Альдера, функционализированный гексаметилтриметиламмонием (3b). Гидроксидная проводимость HTMA-DAPP составляла 120 мСм/см при 80 °C (мСм — миллисименс; сименс — единица измерения электрической проводимости).
Основная цепь полифенилена в высокомолекулярном полимере HTMA-DAPP обеспечивает превосходную механическую прочность (растягивающее напряжение > 20 МПа при относительной влажности 90% при 50 °C). А вот кватернизованный полистирол слишком хрупок для создания мембран и поэтому не подходит для применений с водным AEM электролизером, который требует механически стабильных AEM.
Щелочная стабильность HTMA-DAPP также достаточно высока: проявление минимального разложения в течение > 3000 часов в 4 М NaOH при 80 °C. Этот показатель гарантирует проведение испытаний AEM электролизера при рабочей температуре в 85 °C.
В условия использования чистой воды мембранный электрод демонстрирует плотность тока 107 мА см -2 при 1.8 В и 60 °C. Если же добавить в воду 0.1 М NaOH, то показатели увеличиваются в 3.5 раза до 376 мА см -2 при 1.8 В и 60 °С.
Если при использовании чистой воды увеличить рабочую температуру до 85 градусов, то плотность тока в электролизере возрастет до 224 мА см -2 .
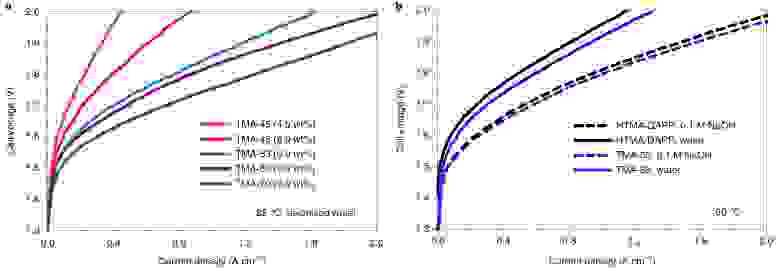
Изображение №4: влияние иономеров на производительность AEM.
На графике 4а продемонстрирован прогресс улучшения рабочих характеристик электролизера за счет исследуемого иономера.
Чтобы получить данное улучшение, необходимо было сначала точно определить необходимое содержание иономера. В результате плотность тока мембранного электрода с 9 мас.% иономера (в два раза выше от базового значения) составляла 405 мА см -2 при 1.8 В (красная кривая), что в 1.8 раза больше, чем базовый показатель мембранного электрода (MEA).
Далее была проведена интеграция мембранного электрода и иономеров триметиламина (CH3)3N, которые демонстрировали более высокие значения IEC при более высоком содержании иономеров. Производительность MEA с использованием TMA-53 (IEC = 2.6) значительно увеличилась (синяя кривая). При 1.8 В плотность тока составляла 791 мА см -2 , что в 2.0 раза больше, чем у MEA с TMA-45. Плотность тока при 1.8 В МЭС с TMA-62 (фиолетовая кривая) и TMA-70 (зеленая кривая) дополнительно увеличилась до 860 и 1360 мА см -2 соответственно. Плотность тока MEA с TMA-70, была в 1.7 раза выше, чем у MEA с TMA-53, и в 6 раз выше, чем у базового MEA при 1.8 В.
Помимо влияния иономеров на производительность электролизера, ученые также исследовали влияние фенильной группы в иономере (4b). Для этого были проведены эксперименты, в которых сравнивались два МЕА, которые были одинаковы, за исключением связующего электрода. Первый электрод — это MEA с HTMA-DAP, а второй — с TMA-53. Содержание иономера (9 мас.%) и значение IEC (2,6) для обоих электродов было также одинаковым.
При использовании 0.1 М NaOH электролита рабочие характеристики электролизера у обоих электродов были очень похожи: 954 мА см -2 для HTMA-DAPP MEA и 1.052 мА см -2 для TMA-53 MEA. Однако, если использовалась чистая вода, MEA с TMA-53 (630 мА см -2 ) показал заметно более высокую производительность по сравнению с MEA с DAPP-HTMA (484 мА см -2 ).
Подобные наблюдения указывают на то, что работа электролизера менее чувствительна к 0.1 М NaOH. Это может объясняться тем, что кислотные фенолы от окисления фенильной группы были нейтрализованы щелочным раствором.
Далее было проведено более детальное изучение характеристик MEA с TMA-70 посредством использования катализаторов, не содержащих металлов платиновой группы. В качестве анода был использован катализатор на основе нанопены NiFe.
Проверка характеристик MEA с разным содержанием иономеров в анодном NiFe катализаторе позволила определить, что 20 мас.% содержание иономера является наиболее эффективным.

Изображение №5: производительность AEM электролизера с анодным катализатором без применения металлов платиновой группы.
На графике выше показаны показатели производительности AEM электролизера с анодным NiFe катализатором в условиях подачи 1 М и 0.1 М растворов NaOH (60 °С) и чистой воды (85 °С) при 1.8 В: 5.3 А см -2 (1 М NaOH); 3.2 А см -2 (0.1 М NaOH); 2.7 А см -2 (чистая вода).
Далее для большей наглядности рабочие характеристики MEA с анодным NiFe катализатором сравнили с характеристиками электролизера с протонообменной мембраной (PEM), в которых используются катализаторы с металлами платиновой группы.
В кинетической области при напряжениях менее 1.58 В MEA с NiFe катализатором превзошел PEM электролизер (вставка на изображении №5). Если подробнее, то при 1.5 В плотность тока MEA составила 300 мА см -2 , а это в два раза выше, чем у PEM электролизера, где используется IrO2 (оксид иридия) и наноструктурированные тонкие пленки.
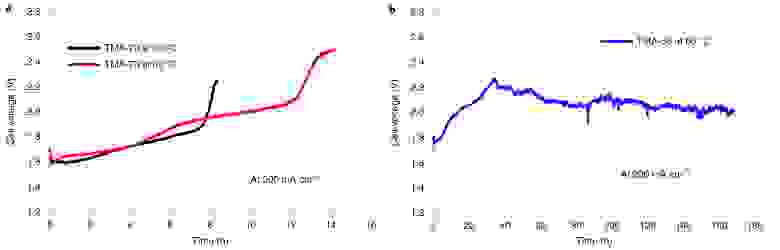
Изображение №6: показатели прочности AEM электролизеров с NiFe катализатором.
Помимо прочего ученые также решили проверить прочность AEM электролизера на чистой воде. На 6а показан кратковременный тест на прочность АЭМ электролизера с NiFe катализатором при постоянной плотности тока 200 мА см -2 . Как при 60, так и при 85 °С напряжение быстро увеличивалось в течение
Было обнаружено, что частицы катализатора были вымыты как из анодного, так и из катодного выходных потоков. Это может свидетельствовать о том, что иономер с высоким IEC (TMA-70) не удерживал частицы катализатора во время непрерывной работы.
Увеличение силы связывания иономера можно было достичь путем применения того же иономера с более низким IEC при 60 °C.
На 6b показан кратковременный тест на прочность AEM электролизера с использованием иономера TMA-53. По результатам четко видно, что система работает стабильно в течение более 100 часов после начального повышения напряжения с 1.75 до 2.1 В. Начальное повышение напряжения в течение первых 40 часов, вероятно, связано с окислением фенила.
Вывод достаточно печальный — система хоть и показывает отличные результаты по производительности, но не может похвастаться тем же в аспекте долговечности.
Для более подробного ознакомления с нюансами исследования рекомендую заглянуть в доклад ученых.
Эпилог
В данном труде исследователи продемонстрировали модель связующей системы для электродов, которая способна повысить производительность AEM электролизера. Такой вариант по своим характеристикам не уступает современным PEM электролизерам, при этом он не нуждается в металлах платиновой группы, что значительно снижает себестоимость всей системы.
Связующее для электродов было синтезировано на основе результатов экспериментов с вращающимся дисковым электродом, которые показали важность высокого локального pH для эффективной реакции выделения водорода и реакции выделения кислорода.
Удаление фенильных групп из основной цепи полимера позволяет предотвратить образование кислых фенолов, которые могут нейтрализовать гидроксид четвертичного аммония и снизить рН электролита. Кроме того, повышение рН электродов было достигнуто путем увеличения содержания иономера и IEC.
AEM электролизер, использующий кватернизованный иономер полистирола аммония, продемонстрировал отличную производительность даже без циркулирующего щелочного раствора.
Конечно не обошлось и без недостатков. В дальнейшем ученые намерены провести ряд дополнительных исследований для улучшения производительности разработанной системы и для повышения ее долговечности.
В совокупности все рассмотренные наблюдения являются дополнительными сведениями в области разработки высокоэффективных систем электролизеров, а также позволяют понять, как эффективнее хранить возобновляемую энергию.
Как говорят сами авторы исследования, суть заключается в том, что источники возобновляемой энергии весьма нестабильны. За одинаковый промежуток времени можно получить разный объем энергии, поскольку могут быть разные условия (например, ветрогенератор в безветренную погоду не особо эффективно работает). Тем не менее, порой имеется излишек энергии, которую необходимо эффективно утилизировать. Авторы сего труда считают, что использовать данную возобновляемую энергию нужно для производства водорода, необходимость в котором из года в год только растет.
Благодарю за внимание, оставайтесь любопытствующими и хорошей всем рабочей недели, ребята. 🙂
Немного рекламы 🙂
Спасибо, что остаётесь с нами. Вам нравятся наши статьи? Хотите видеть больше интересных материалов? Поддержите нас, оформив заказ или порекомендовав знакомым, облачные VPS для разработчиков от $4.99, уникальный аналог entry-level серверов, который был придуман нами для Вас: Вся правда о VPS (KVM) E5-2697 v3 (6 Cores) 10GB DDR4 480GB SSD 1Gbps от $19 или как правильно делить сервер? (доступны варианты с RAID1 и RAID10, до 24 ядер и до 40GB DDR4).
Dell R730xd в 2 раза дешевле в дата-центре Equinix Tier IV в Амстердаме? Только у нас 2 х Intel TetraDeca-Core Xeon 2x E5-2697v3 2.6GHz 14C 64GB DDR4 4x960GB SSD 1Gbps 100 ТВ от $199 в Нидерландах! Dell R420 — 2x E5-2430 2.2Ghz 6C 128GB DDR3 2x960GB SSD 1Gbps 100TB — от $99! Читайте о том Как построить инфраструктуру корп. класса c применением серверов Dell R730xd Е5-2650 v4 стоимостью 9000 евро за копейки?
Источник









