- Как разделить воду и спирт различными методами?
- Метод, о котором знает каждая бабка
- Как научились получать чистый спирт?
- Другие способы
- Как разделить спирт и воду
- Содержание:
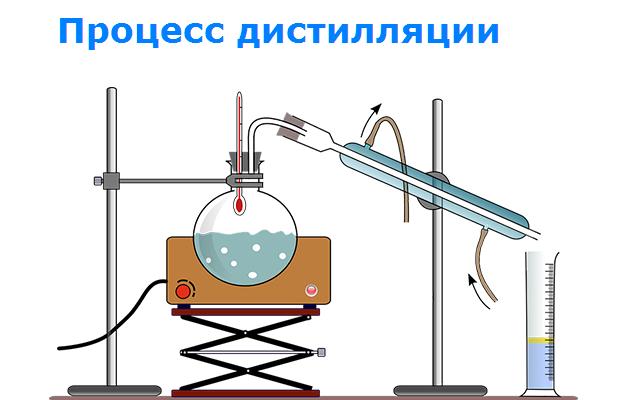
- Метод 1 из 3: дистилляция спирта из воды
- Метод 2 из 3: замораживание спиртовое замораживание
- Метод 3 из 3: «Посолить» спирт из воды
- Как можно разделить спирт и воду
- Как разделить спирт и воду?
Как разделить воду и спирт различными методами?
Вовсе не желание употребления спиртных напитков послужило толчком для зарождения спиртовой промышленности. Первыми, кто практически решил вопрос о том, как разделить воду и спирт, были не потребители и даже не производители зелья, а… медики. Спирт несравненно лучший по сравнению с водой растворитель, поэтому на его основе древние восточные лекари с успехом готовили свои снадобья. Метод дистилляции привезли в Европу, как один из трофеев, рыцари из своих крестовых походов. В Старом Свете метод прижился, правда, во Франции получил еще одно назначение – изготовление косметики. И лишь затем продукты перегона браги начали потихоньку завоевывать место под солнцем как напитки, с чем связано немало легенд и преданий.
Метод, о котором знает каждая бабка
Субстанция, из которой обычно получают спирт – это брага, а самогоноварение – самый древний способ как разделить смесь. Спирта и воды, правда, в чистом виде процесс не дает, зато дешев, надежен и отработан веками.
В процессе брожения из сахаросодержащих веществ дрожжи вырабатывают спирт, и при определенной его концентрации сами же в нем и погибают (спирт, оказывается, яд даже для производящих его дрожжей). Далее в дело вступает чистая физика: вода, как известно, при нормальном атмосферном давлении (около 760 мм.рт.ст.) превращается в пар при температуре 100 °C, а вот этиловый спирт – этанол, тот самый, что создает нам «праздничное» настроение, закипает при температуре порядка 78 °C.
Таким образом, способ, как разделить воду и спирт, очевиден. При нагревании первыми испаряются пары этанола и отводятся из зоны кипения. Затем пары поступают в охладитель и конденсируются, превращаются обратно в жидкость. Вода же остается в емкости.
Как научились получать чистый спирт?
Однако на деле не все так просто и легко. При 80 °C спирт интенсивно испаряется и покидает емкость. Вода, хоть и не достигает точки кипения при данной температуре, но часть ее все же испаряется и попадает в охладитель вместе с парами этанола. Если делать перегонку 3 и более раз, максимальная крепость, которой можно добиться – 80…85%. А как разделить воду и спирт полностью или почти полностью? Для этого в конце XIX века и была придумана ректификационная колонна.
Устройство ее отличается от обычного «бабкиного» самогонного аппарата наличием вертикальной шахты, куда поступают спиртосодержащие пары перед тем, как оказаться в холодильнике. В шахте пары проходят через ряд препятствий в виде тарелок, насыпных деталей произвольной формы и т. д. Задача этих препятствий в том, чтобы немного остудить пар и заставить его конденсироваться. В виде капель оседает и самотеком вновь попадает в емкость именно вода – как жидкость с более высокой температурой кипения. Пары же спирта продолжают свой путь к вершине колонны и лишь там они отбираются для охлаждения и конденсации.
Другие способы
Однако известны и другие способы, как разделить воду и спирт. Например, что выйдет, если исходную жидкость не нагревать, а наоборот – охлаждать? Именно так, по некоторым предположениям, поступали древние викинги со своим элем, чтобы сделать его крепче. В кувшине с элем, который выносили на ночь на лютый мороз, к утру образовывалась ледышка. Ее выбрасывали, а оставшийся в кувшине напиток оказывался крепче и забористее. Секрет метода прост – вода кристаллизуется при температуре 0 °C, чтобы заморозить этиловый спирт, его пришлось бы охладить до минус 115 °C.
Но если вообще отставить в сторону температуру? В этом случае как разделить спирт и воду? Химия также может помочь в решении задачи. Есть вещества, связывающие химически воду, нейтральные к спирту. Другие же, напротив, вступают в реакцию со спиртом, игнорируя Н2О. Это такие методы, как выщелачивание или высаливание. Однако на практике к таким способам прибегают чаще всего лишь в научных целях.
Источник
Как разделить спирт и воду
Есть несколько способов отделить спирт от воды. Самый распространенный способ — нагреть раствор. Поскольку он имеет более низкую температуру кипения, чем вода, спирт быстро превращается в пар. Затем э
Содержание:
Есть несколько способов отделить спирт от воды. Самый распространенный способ — нагреть раствор. Поскольку он имеет более низкую температуру кипения, чем вода, спирт быстро превращается в пар. Затем этот пар конденсируется (конденсируется) в отдельном контейнере. Можно также заморозить спиртовую смесь, чтобы удалить некоторые безалкогольные компоненты; оставшаяся жидкость будет иметь более высокое содержание алкоголя. Используйте обычную поваренную соль, чтобы отделить изопропиловый спирт от воды. В результате получится густой изопропиловый спирт, а не алкоголь для питья.
Метод 1 из 3: дистилляция спирта из воды
Создайте закрытую систему дистилляции. В простейших системах дистилляции используется стеклянная бутылка с круглым дном (или бутылка для кипячения), конденсатор и второй стеклянный контейнер для отдельных жидкостей. Мы рекомендуем использовать дробный столбец (или фракционирование), который вставляется между бутылью для кипячения и конденсаторным блоком для отделения спирта от воды.
- Простая система дистилляции требует двух жидкостей с очень большой разницей в точках кипения.
- Простые дистилляционные системы не потребляют много тепла и легко собираются, но точность отделения спирта от воды довольно низкая.
- Закрытая система дистилляции также известна как «по-прежнему«Что является производным от слова»дистилляция(Перегонка).
Метод 2 из 3: замораживание спиртовое замораживание
Начните с 5-15% алкоголя. Вам нужен контейнер, который можно безопасно заморозить и разморозить, и место (не знаю морозилка или наружная температура), где температура ниже 0 градусов Цельсия. Подобно методу дистилляции, который основан на разнице температур кипения, этот метод также использует разницу в точках замерзания спирта и воды.
- Этот древний метод отделения спирта от воды восходит к седьмому веку.
- Этот метод также известен как Монгольский по-прежнему (Монгольский НПЗ).
Налейте в емкость медицинский спирт. Так как вода при замерзании расширяется, убедитесь, что емкость достаточно велика, чтобы в ней не разбилась дополнительная замороженная жидкость. Содержание воды в жидкости увеличится, но количество алкогольного напитка уменьшится в результате отжима воды.
- Температура замерзания воды составляет 0 ° по Цельсию, а температура замерзания спирта -114 ° по Цельсию. Другими словами, алкоголь не замерзнет при нормальных условиях.
- Сифонируйте жидкость из замороженного вещества один раз в день. Чем дольше вы держите контейнер морозилка, содержание спирта в жидкости во льду будет выше.
- Если хотите больше алкоголя, используйте емкость большего размера. Убедитесь, что вы используете пластиковые контейнеры, специально предназначенные для хранения продуктов, так как обычный пластик может загрязнить ваши напитки.
Вынуть лед из емкости. Этот лед в основном состоит из воды, а спирт с более низкой температурой замерзания остается в емкости.
- В оставшейся жидкости будет более высокое содержание алкоголя, даже если это не чистый спирт.
- Вкус тоже будет сильнее. Поэтому этот метод популярен с крепким яблочным сидром (или яблочный джек), пиво, или пиво.
- название яблочный джек полученный из процесса замороженной дистилляции, ранее известный под названием подъемное (поднимается).
Метод 3 из 3: «Посолить» спирт из воды
Посыпьте изопропиловый спирт солью, чтобы начать азеотропную дистилляцию. Этот процесс дистилляции использует обезвоживание для отделения воды от спирта.Обезвоженный изопропил можно использовать в качестве топлива, средства от блох для домашних животных, антисептика для людей и домашних животных или в качестве средства для очистки льда (антиобледенитель) за лобовое стекло автомобиля.
- Обезвоженный изопропил — важная часть производства биодизельного топлива.
- Этот процесс также известен как «экстрактивная» дистилляция.
Подготовьте необходимые материалы. Вам понадобится смесь настоящего изопропилового спирта (смесь изопропилового спирта 50-70%) и контейнер для этой жидкости, когда все будет готово, банка с широким горлышком (размером 2 литра), 1 фунт (450 г) не йодированной поваренной соли и большая пипетка (Бастер) с конической насадкой.
- Убедитесь, что все материалы и инструменты чистые, включая емкости и пипетки.
- Изопропиловый спирт обычно продается в аптеках в емкостях по 30 мл (иначе 1 пинта). Вам понадобится 60 мл спирта, чтобы заполнить 2-литровую емкость для смешивания.
Заполните емкость для смешивания поваренной солью на ¼. Убедитесь, что вы не используете йодированную соль, поскольку она загрязняет процесс дистилляции. Обычно одной стандартной упаковки поваренной соли достаточно.
- Используйте предпочитаемую вами торговую марку, если соль не йодированная.
- Вы можете использовать столько алкоголя и соли, сколько хотите, при условии, что это 4/5 жидкости на 1/5 соли.
Добавьте спирт в емкость для смешивания и хорошо встряхните. Емкость для смешивания должна быть заполнена на ¾. Если его избыток, возможно, что оставшегося пространства в банке недостаточно для расширения из-за реакции смешивания спирта с солью.
- Перед встряхиванием убедитесь, что банка плотно закрыта.
- Прежде чем закончить взбалтывать, убедитесь, что соль равномерно смешана с жидкостью.
Позвольте силе тяжести разделить содержимое смеси. Обычно соль оседает на дно емкости за 15–30 минут. Жидкость, которая поднимается на поверхность, будет иметь более высокое содержание спирта. Это обезвоженный изопропиловый спирт.
- Не позволяйте двум смесям снова смешаться.
- Когда вы открываете банку, следите за тем, чтобы она не раскачивалась слишком сильно. Если он будет слишком сильно раскачиваться, он будет мешать соленой части банки, и процесс дистилляции придется повторить.
Используйте пипетку, чтобы извлечь дистиллированный спирт с поверхности банки. Возьмите емкость для алкоголя и назовите ее «дистиллированный изопропиловый спирт».
- Очень осторожно используйте пипетку, чтобы постепенно удалить жидкость из емкости для смешивания.
- Старайтесь не допускать тряски, проливания или опрокидывания емкости во время удаления дистиллированного спирта из емкости.
Источник
Как можно разделить спирт и воду
1. Разделить спирт и воду можно перегонкой — через змеевик (т. е. прогнать под воздействием высокой температуры через специальный аппарат) .
2. Спирт можно испарить из воды, т. к. он более летучий и испаряется при более низкой температуре — температура кипения воды 100 градусов по Цельсию, спирта — 78,37 градусов по Цельсию Поэтому пары спирта быстро испарятся, у вас останется лишь вода. Однако очевидно, что собрать пары спирта будет невозможно. Этим способом можно только очистить воду.
3. Или наоборот, заморозить. Вода превратится в лёд, а спирт останется жидким, т. к. у него температура кристаллизации (замерзания) t = −114 по Цельсию.
Способ, применяемый в Сибири: берут лом (железную палку или можно взять железный желоб) , выставляют на мороз, когда лом замёрзнет, его ставят в ведро и по нему сливают спирт. Вода примёрзнет, спирт останется в ведре.
4. Существуют специальные устройства для отделения спирта от воды, они различаются конструкциями узлов, деталями, приспособлениями для очищения спирта и повышения его концентрации. Аппараты устроены по принципу конденсационных отсекающих камер, в них входит испарительная емкость и ректификационные колонны. Емкость заполняется жидкостью, которая нагревается и испаряется. Разогретая жидкость поднимается верх в виде пара по камерам, где происходит конденсация воды, которая стекает обратно в емкость. Спирт в парообразном состоянии поступает в верхнюю камеру, остывает и виде капель поступает на выход в спиртоприемник. Когда спирта становится меньше, начинает подниматься вода, так как ей нужно больше времени для закипания и перехода в газообразное состояние. Полученный спирт нужно перегнать еще раз, тогда он получиться большей крепости.
Источник
Как разделить спирт и воду?
У спирта и воды разные температуры замерзания: у воды 0(ноль) градусов по Цельсию, у спирта -114,1 (минус сто четырнадцать целых и одна десятая) градусов по Цельсию. Поэтому можно просто заморозить. Вода преобразуется в свое твёрдое состояние — лёд, а спирт останется в жидком состоянии, в котором его можно собрать и разделить в разные ёмкости.
Обычно используют разгонку спирта и воды пользуясь разницей температур их кипения. Этот метод используется как в промышленности, так и в самогоноварении. В промышленности также используют перегонку при пониженном давлении и азеотропную перегонку, что позволяет получить спирт с концентрацией выше, чем 96%.
Вторым способом используемым в основном только химиками — это метод высаливания (например, карбонатом натрия). Здесь используется более высокая растворяющая способность воды к солям. При этом спирт вытесняется из раствора.
Третий способ — использование осушающих веществ. Обычно используется для доосушки остаточной воды из концентрированных растворов спирта. Для этого обычно используется оксид кальция или безводный сульфат меди.
Четвертый способ — использование веществ, более активно реагирующих с водой, чем со спиртом. Таким способом получают спирт до концентрации 99,99%. Обычно используют кипячение с магнием и этилформиатом.
Самый простой метод разделения спирта и воды -это метод перегонки (пример самогонный аппарат).
Температура кипения воды составляет 100 градусов,а температура кипения спирта равна 78 градусам,следовательно спирт испаряется быстрее воды.
Самый простой способ это сделать под воздействием высокой температуры через специальный аппарат методом перегона. И наоборот, через заморозку. При этом методе вода замёрзнет, а спирт останется жидким.
Качество водки, которая получится из спирта, в первую очередь зависит от самого этого спирта. Чем лучше спирт, тем качественнее водка получится. Также немаловажно и качество воды. В воде должно быть минимум солей, она должна быть истой, прозрачной и очищенной.
Для придания более мягкого вкуса водке используют лимонную кислоту, глюкозу, молоко, мёд, уксусную кислоту.
Наиболее оптимальная пропорция спирта и воды — это 2 к 3 соответственно.
Важным является и то, что именно спирт нужно влить воду.
При кипении жидкостей жидкость переходит из жидкого состояния в газообразное. Таким образом газ берётся из жидкости. Например при кипении воды из воды образуется газ называемый водяным паром.
Вообще концентрацию, «крепость» водки производят с помощью спиртометра или ареометра..
Приборчик опускают в раствор и по шкале смотрят..
Принцип основан на законе Архимеда..
Если нет такого прибора, то можно налить в мерную посуду например литр и взвесить..
А потом взвесить мерную посуду пустую..
Потом решаем систему линейных алгебраических уравнений:
r1,r2- плотности спирта, воды соответственно
V1,V2,V — объёмы спирта, воды и общий соответственно
M1,M2 — массы наполненной и пустой посуды соответственно
Находим отсюда объём спирта V1..
Отношение V1/V* 100% и есть объёмная концентрация спирта..
Этот способ может дать очень точные показания, если взять химическую мерную посуду и точные весы..
В лабораторных условиях получить воду можно многими способами.
Способ первый. Сжигаем водород (из баллона) в воздухе и в результате реакции, известной каждому школьнику: 2Н2 + О2 = 2Н2О, получаем пары воды. Если вода нужна в жидком состоянии, охлаждаем пары и получаем жидкую воду.
Способ второй. Сжигаем углеводородное топливо — метан, пропан-бутан, бензин и т.д. и т.п. Можно и парафин сжечь, только труднее добиться полного сгорания без копоти. В результате всех этих реакций горения образуется углекислый газ и вода. Например, в случае горения метана: СН4 + 2О2 = СО2 + 2Н2О. Углекислый газ выпускаем в воздух (а можно поглотить щелочью), а пары воды конденсируем.
Способ третий. Берем кристаллогидрат, например, медный купорос, алюмокалиевые квасцы, глауберову соль (10-водный сульфат натрия) и греем, обычно сильного нагревания не требуется. Вода отщепляется от кристаллов и ее легко отогнать и сконденсировать.
Наверное, можно припомнить еще несколько принципиально других методов, когда одним из продуктов химической реакции является вода.
Сейчас есть в продаже чистящие средства для бассейнов без использования хлорки , они правда дороговато стоят .
Я например чищу бассейн обычной пищевой содой и потом просто прогоняю воду через фильтр — она хорошо чистит и замедляет цветение — пачка на 2.5 тонны воды .
Источник