Разведение растворов по массе



План
1. Растворы. Определение.
2. Технологический процесс производства.
3. Стандартизация раствора.
4. Разведение растворов по массе.
5. Разведение раствора по объему.
6. Укрепление растворов.
7. Разведение растворов по плотности.
Растворы – это жидкие гомогенные системы, состоящие на растворителя и одного или нескольких, распределенных в нем в виде ионов или молекул. Растворение – массообменный процесс. Свойства истинных растворов приведены в таблице. В зависимости от растворителя различают растворы водные, спиртовые, масляные, глицериновые, на смешанных растворителях и др. Концентрацию растворов выражают в процентах по массе и массообъемных. Технологический процесс производства растворов в общем виде состоит из следующих стадий:
3. Освобождение раствора от механических включений нерастворимых примесей
5. Фасовка и упаковка готовой продукции
В промышленных условиях готовятся лишь стойкие при хранении водные растворы. Некоторые водные растворы (растворы формальдегида, перекиси водорода и др.) получают с добавлением стабилизаторов.
Водные растворы получают разными способами:
— растворением лекарственных веществ;
— химическим взаимодействием веществ, в т.ч. электрохимическим способом.
Схема производства растворов представлена в таблице.
Схема производства растворов для наружного и внутреннего применения
| Стадии и операции технологического процесса | Описание действия | Контроль |
| Подготовительная | Проводят расчеты в соответствии с НД. Подготавливают лекарственные вещества и растворитель (измельчают, отмеривают, взвешивают) | Подтверждают соответствие лекарственных веществ и растворителя требованиям НД |
| Растворение: — приготовление растворов путем механического перемешивания; — приготовление растворов химическим взаимодействием. | Водные растворы приготавливают массообъемным способом и по массе: — при приготовлении растворов массообъемным способом сухие лекарственные вещества взвешивают и доводят растворителем до требуемого объема или готовят по массе, но с учетом массообъемной концентрации и плотности раствора; — некоторые растворы готовят по массе (сахарный сироп, растворы кислот, щелочей и др.). Концентрированные растворы кислот и щелочей осторожно тонкой струйкой добавляют к воде при перемешивании. Приготовление растворов основного ацетата свинца, основного ацетата алюминия. Последний получают также электролизом | Соблюдение техники безопасности. Разбрызгивание жидкости недопустимо! Производство препаратов должно производиться со строгим соблюдением промышленного регламента. |
| Освобождение растворов от механических включений и нерастворимых примесей | Водные растворы фильтруют при атмосферном давлении, под вакуумом и избыточном давлении. | Раствор должен быть прозрачным. |
| Стандартизация | Определяют: — органолептические показатели; — подлинность; — количественное содержание действующих веществ; — отсутствие механических включений; — плотность раствора; — для некоторых растворов цветность (сахарный сироп); — рН и др. | Раствор должен быть стандартным в соответствии с НД |
| Фасовка и упаковка, хранение | Фасуют во флаконы равной емкости, снабжают этикетками «Наружное» или «Внутреннее» с указанием предприятия-изготовителя, торгового знака, названия препарата, даты изготовления и срока хранения. Хранят в прохладном, защищенном от света месте. | Раствор должен быть без осадка, не мутным, не гелеобразным. Исключение для жидкости Бурова |
Стадия растворения осуществляется в аппаратах-реакторах, снабженных мешалкой и теплообменником. Для ускорения растворения в большинстве случаев используют нагревание. Перемешивание осуществляется различными способами:
— механическим с помощью мешалок различной конструкции (якорных, рамных, планетарных, пропеллерных, турбинных и др.);
— гравитационным, основанным на различной плотности растворителя и раствора;
— циркуляционным и др.

Путем механического перемешивания получают водные растворы перекиси водорода, пергидроля, кальция хлорида, калия хлорида, аммиака, уксусной кислоты, сахарный сироп и др.
В результате химического взаимодействия получают раствор основного ацетата алюминия (жидкость Бурова), раствор основного ацетата свинца (свинцовый уксус).
Электрохимическим способом (электролизом) получают жидкость Бурова.
Отделение растворов от механических включений и нерастворимых примесей осуществляется отстаиванием, фильтрованием, центрифугированием.
Отстаивание основано на разделении фаз под действием сил тяжести. Для этого используют отстойники периодического и полунепрерывного действия. Отстаивание применяется для предварительной очистки растворов.
Фильтрование растворов основано на разделении твердой и жидкой фаз с помощью пористых перегородок (фильтров). Фильтрование может происходить при атмосферном давлении (под давлением гидростатического столба жидкости), при разрежении (под вакуумом), при избыточном давлении. Для фильтрования растворов используют нутч-фильтры, друг-фильтры, пресс-фильтры, фильтр-грибок и др.
Центрифугирование основано на разделении фаз под действием сил центробежного поля. Для разделения твердой и жидкой фаз применяют отстойные, фильтрующие и суперцентрифуги.
Стандартизация растворов.
Водные растворы стандартизуют:
— по количественному содержанию действующих веществ;
— по плотности и др. (например, ля сахарного сиропа определяют цветность и рН).
При несоответствии содержания действующих веществ в растворе его укрепляют или разбавляют по требуемым показателям согласно НД. Для получения раствора с заданной концентрацией или с заданной плотностью применяется правило смешения или соответствующие формулы, которые позволяют рассчитывать необходимое количество разбавителя, исходного раствора с заданной концентрацией или плотностью. Решение данных задач требует соблюдение определенных условий. Выбирается весовой или объемный способ расчета, т.е. ведут расчет в одной системе единиц. Когда имеется возможность, следует выбирать весовой способ разбавления растворов как наиболее точный, т.к. на определение массы раствора не влияет температура.
Для весового способа расчеты проводят по величинам m и Сm, а для объемного – V, r, CV, Cm/V, где
Cm – концентрация в процентах по массе;
CV – концентрация в процентах по объему;
Cm/V – массообъемная концентрация в процентах;
m – масса раствора в г, кг;
r – плотность раствора в г/мл;
V – объем раствора в мл, л.
Если вместо концентрации используется плотность, то количество разбавителя, исходного раствора и раствора требуемой концентрации берется по объему. Если в таких задачах дается масса раствора, то ее необходимо перевести в объем.
При установлении концентрации растворов (массой Сm. объемной СV или массообъемной Сm/V) руководствуются следующими правилами:
— в растворах кислот, щелочей, оснований и сахарном сиропе содержание лекарственного вещества обычно выражается в процентах по массе (Сm);
— в растворах, которые готовятся массообъемным способом, содержание растворенного вещества выражается в массообъемных процентах Сm/V;
При расчетах используют формулы и правило смешения («звездочки»).
Разведение растворов по массе
Источник
Способы приготовления растворов
Существует несколько способов приготовления растворов. По способу приготовления различают первичные и вторичные стандартные растворы.
1.
По точной навескеготовят первичные стандартные растворы, растворы стандартных установочных веществ, которые должны удовлетворять следующим требованиям:
а) состав их должен строго соответствовать химической формуле;
б) вещества должны быть устойчивыми при хранении в растворе и в сухом виде (не окисляться, не поглощать диоксид углерода, воду, не терять кристаллизационную воду);
в) величина молярной массы эквивалента должна быть по возможности наибольшей для уменьшения погрешности взвешивания и титрования.
При приготовлении растворов по точной навеске задаются концентрацией раствора и его объемом. Основные этапы работы:
- рассчитывают необходимую навеску для взвешивания с точностью до 0,0001 г по одной из формул:
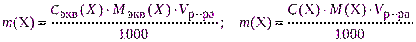
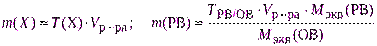
где Vр-ра – объем раствора, см 3 ;
- взвешивают точную навеску на аналитических весах;
- взвешенную навеску количественно переносят в мерную колбу вместимостью, равной Vр-ра, растворяют вещество, доводят до метки дистиллированной водой и перемешивают;
- если взятая навеска отличается от теоретически рассчитанной, то концентрацию раствора пересчитывают, используя указанные выше формулы, например:
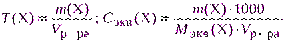
где Vр-ра – объем раствора, см 3 ; m(Х) – практическая навеска, г.
2.
По приблизительной навескеготовят растворы нестандартных веществ или растворы приблизительной концентрации. Этапы работы такие же, как и при приготовлении растворов по точной навеске, но навеску рассчитывают с точностью не более, чем до 0,01 г и берут ее на технических весах. Точную концентрацию такого раствора устанавливают титрованием (часто растворами первичных стандартов) и рассчитывают по закону эквивалентов:
Сэкв 1·V1 = Cэкв 2·V2 (2.16)
Приготовленные таким образом растворы с точно установленной концентрацией называются вторичными стандартами или титрованными.
3.
Из фиксанала (норма-дозы, стандарт-титра)готовят первичные стандартные растворы точной концентрации. Фиксанал – стеклянная ампула, в которой содержится точно известное количество nэкв вещества в кристаллическом виде или в виде раствора. Содержимое фиксанала количественно переносят в мерную колбу, доводят уровень раствора до метки, раствор перемешивают. Концентрация раствора должна быть задана, а вместимость мерной колбы рассчитывают, используя формулу (2.6).
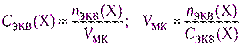
4.
Разбавлением концентрированных растворовготовят растворы многих веществ. В этом случае должны быть заданы объем разбавленного раствора, его концентрация и концентрация концентрированного раствора. Рассчитывают необходимый для разбавления объем концентрированного раствора, затем измеряют рассчитанный объем, переносят в мерную колбу или в мерный стакан, доводят уровень жидкости до метки дистиллированной водой и перемешивают. Если исходный раствор имел точную концентрацию и при его разбавлении использовали точную мерную посуду, то получают раствор точной концентрации. В противном случае получают раствор приблизительной концентрации, все расчеты ведут с точностью не более чем до 0,01, точную концентрацию устанавливают титрованием и рассчитывают по формуле (2.16).
Пример.Сколько грамм хлорида калия KCl потребуется для приготовления 2 дм 3 раствора:
а) с массовой долей, равной 30% и плотностью 1,110 г/см 3 ;
б) с титром, равным 0,001841 г/см 3 ;
в) с молярной концентрацией эквивалента, равной 0,2000 моль/дм 3 .
Решение.
| Дано: ω(KCl) = 30% | а) Массу хлорида калия рассчитаем, используя формулу (2.11): |
| Vр-ра= 2 дм 3 = 2000 см 3 ρ р-ра = 1,110 г/см 3 | 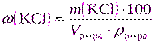 |
| Сэкв(KCl) = 0,2000 моль/дм 3 T(KCl) = 0,001841 г/см 3 |  |
| m(KCl) = ? |
б) Для расчета используем формулу (2.12):
в) Для расчета можно использовать формулу (2.7):
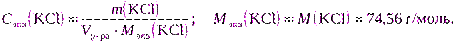
m(KCl) = Cэкв(KCl) · Vр-ра · Mэкв(KCl) = 0,2000·2·74,56 = 29,8240 г.
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Источник
Способы приготовления растворов
Содержание
Существует несколько способов приготовления растворов. По способу приготовления различают первичные и вторичные стандартные растворы.
Приготовление раствора по точной навеске
По точной навеске готовят первичные стандартные растворы, растворы стандартных установочных веществ, которые должны удовлетворять следующим требованиям:
а) состав их должен строго соответствовать химической формуле;
б) вещества должны быть устойчивыми при хранении в растворе и в сухом виде (не окисляться, не поглощать диоксид углерода, воду, не терять кристаллизационную воду);
в) величина молярной массы эквивалента должна быть по возможности наибольшей для уменьшения погрешности взвешивания и титрования.
При приготовлении растворов по точной навеске задаются концентрацией раствора и его объемом.
Основные этапы работы:
- рассчитывают необходимую навеску для взвешивания с точностью до 0,0001 г;
- взвешивают точную навеску на аналитических весах;
- взвешенную навеску количественно переносят в мерную колбу вместимостью, равной Vр-ра, растворяют вещество, доводят до метки дистиллированной водой и перемешивают;
- если взятая навеска отличается от теоретически рассчитанной, то концентрацию раствора пересчитывают.
Приготовление раствора по приблизительной навеске
По приблизительной навеске готовят растворы нестандартных веществ или растворы приблизительной концентрации. Этапы работы такие же, как и при приготовлении растворов по точной навеске, но навеску рассчитывают с точностью не более, чем до 0,01 г и берут ее на технических весах. Точную концентрацию такого раствора устанавливают титрованием (часто растворами первичных стандартов) и рассчитывают по закону эквивалентов:
Приготовленные таким образом растворы с точно установленной концентрацией называются вторичными стандартами или титрованными.
Приготовление раствора из фиксанала
Из фиксанала (норма-дозы, стандарт-титра) готовят первичные стандартные растворы точной концентрации. Фиксанал – стеклянная ампула, в которой содержится точно известное количество вещества (nэкв) в кристаллическом виде или в виде раствора. Содержимое фиксанала количественно переносят в мерную колбу, доводят уровень раствора до метки, раствор перемешивают. Концентрация раствора должна быть задана, а вместимость мерной колбы рассчитывают, используя формулу:
Приготовление раствора разбавлением концентрированного раствора
Разбавлением концентрированных растворов готовят растворы многих веществ. В этом случае должны быть заданы объем разбавленного раствора, его концентрация и концентрация концентрированного раствора. Рассчитывают необходимый для разбавления объем концентрированного раствора, затем измеряют рассчитанный объем, переносят в мерную колбу или в мерный стакан, доводят уровень жидкости до метки дистиллированной водой и перемешивают. Если исходный раствор имел точную концентрацию и при его разбавлении использовали точную мерную посуду, то получают раствор точной концентрации. В противном случае получают раствор приблизительной концентрации.
Все расчеты ведут с точностью не более чем до 0,01. Точную концентрацию устанавливают титрованием.
Установка титра
Установка титра – одна из важных операций лабораторной техники. От правильности приготовления титрованного раствора зависит и результат анализа. Так как каждый анализ почти всегда сопровождается титрованием, каждый работник лаборатории должен хорошо освоить технику проведения этой операции. Нужно помнить несколько правил, относящихся к титрованным растворам.
1. Титрованные растворы должны быть по возможности свежими. Длительное хранение их не должно допускаться. Для каждого раствора есть свой предельный срок хранения.
2. Титрованные растворы при стоянии изменяют свой титр, поэтому их следует иногда проверять. Если же делают особенно ответственный анализ, проверка титра раствора обязательна.
3. При приготовлении растворов марганцовокислого калия титр их следует устанавливать не ранее, чем через 3—4 дня после приготовления. То же относится ко всём другим растворам, способным изменяться со временем или при соприкосновении с воздухом, стеклом и пр.
4. Титрованные растворы щелочей лучше хранить в бутылях, покрытых внутри парафином, а также защищать их от действия двуокиси углерода воздуха (хлоркальциевая трубка с натронной известью или аскаритом).
5. Все бутыли с титрованными растворами должны иметь четкую надпись с указанием вещества, нормальности, поправки, времени изготовления раствора и даты проверки титра.
Во время титрования колбу нужно держать левой рукой, а правой рукой управлять краном бюретки, давая стекать жидкости равномерно. При титровании очень большое значение имеет скорость, поэтому, при повторном титровании одного и того же раствора, нужно, чтобы скорость добавления раствора из бюретки была по возможности одинаковой, т. е. в одно и то же время вытекало бы определенное количество жидкости. Для перемешивания титруемого раствора очень удобно применять магнитные мешалки. В этом случае титрование можно вести как в обычной конической колбе, так и в специальных, приспособленных для титрования темноокрашенных жидкостей.
Общие рекомендации
Подведем итог сказанному о приготовлении растворов.
1. Все водные растворы следует готовить только на дистиллированной воде. При приготовлении водных растворов солей заданной концентрации нужно учитывать также кристаллизационную воду.
2. Приготовляя точные растворы, нельзя наливать в мерную колбу сразу все нужное количество воды.
3. Мерные колбы калиброваны на определенный объем лишь при температуре, указанной на колбе. Поэтому точный объем жидкости можно получить только при стандартной температуре.
4. Так как приготовить растворы точно заданной концентрации трудно, то, прежде чем пользоваться раствором, надо установить его концентрацию или поправку на нормальность.
5. Необходимо наклеивать этикетки (или делать надпись специальным карандашом) на сосудах с растворами.
6. Все растворы следует готовить только в хорошо вымытой посуде. Надо заботиться о том, чтобы приготовленные растворы не загрязнялись каким-либо образом. Нельзя путать пробки от посуды, содержащей растворы разных веществ.
7. Растворы, которые могут портиться от действия света, такие, как марганцовокислый калий, азотнокислое серебро и др., нужно хранить только в темных склянках. Для некоторых веществ можно употреблять желтые склянки, для других же сосуды необходимо оклеивать черной бумагой, но не покрывать стекло черным лаком: лаковая пленка всегда немного пропускает свет. Если черной бумаги нет, бутыль или другой сосуд следует оклеить плотной бумагой и бумагу покрыть черным лаком.
8. Растворы щелочей нужно хранить так, чтобы на них не действовала двуокись углерода. Для этого в пробку вставляют хлоркальциевую трубку, наполненную натронной известью или другим твердым поглотителем двуокиси углерода.
9. Растворы щелочей следует готовить вначале очень концентрированными и разбавлять их до нужной концентрации только после отстаивания и фильтрования.
10. Надо быть осторожным с растворами, которые могут вредно действовать на кожу рук, одежду или обувь.
11. Все растворы нужно проверять. Точные растворы – путем установки титра, приблизительные – по плотности или иным путем.
12. Растворы (за исключением точных) после приготовления следует обязательно профильтровывать. Это относится одинаково и к водным растворам, и к растворам в органических жидкостях.
13. При приготовлении растворов в органических жидкостях надо применять только чистые растворители и, когда нужно, – безводные. Если растворитель чем-либо загрязнен, его следует перегнать или очистить от примесей каким-либо другим способом.
Источник