- Вещества состав которых не зависит от способа их получения углекислого газа
- Способы получения углекислого газа
- Содержание
- Получение углекислого газа из газов при брожении
- Схема получения углекислого газа на гидролизных заводах
- Углекислый газ в промышленности, его получение и применение
- Получение в промышленности
- Получение газообразной двуокиси углерода
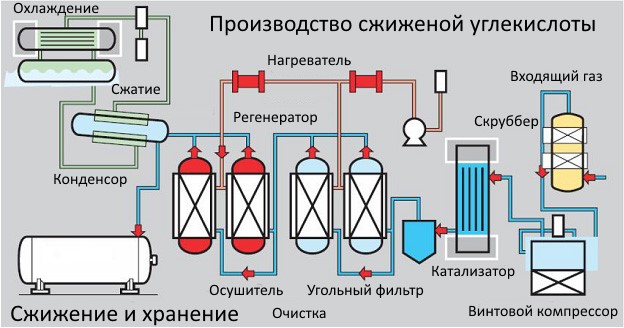
- Получение жидкой углекислоты
- Получение твердого диоксида углерода
- Применение в промышленности
- Химическая промышленность:
- Металлургия:
- Производство бумаги:
- Применение в других сферах деятельности
- Заключение
Вещества состав которых не зависит от способа их получения углекислого газа
FOR-DLE.ru — Всё для твоего DLE 😉
Привет, я Стас ! Я занимаюсь так называемой «вёрсткой» шаблонов под DataLife Engine.
На своем сайте я выкладываю уникальные, адаптивные, и качественные шаблоны. Все шаблоны проверяются на всех самых популярных браузерх.
Раньше я занимался простой вёрсткой одностраничных, новостных и т.п. шаблонов на HTML, Bootstrap. Однажды увидев сайты на DLE решил склеить пару шаблонов и выложить их в интернет. В итоге эта парочка шаблонов набрала неплохую популярность и хорошие отзывы, и я решил создать отдельный проект.
Кроме шаблонов я так же буду выкладывать полезную информацию для DataLife Engin и «статейки» для веб мастеров. Так же данный проект будет очень полезен для новичков и для тех, кто хочет правильно содержать свой сайт на DataLife Engine. Надеюсь моя работа вам понравится и вы поддержите этот проект. Как легко и удобно следить за обновлениями на сайте?
Достаточно просто зарегистрироваться на сайте, и уведомления о каждой новой публикации будут приходить на вашу электронную почту!
Задание 1
Какой состав имеет вода? Вода состоит из двух атомов водорода и одного атома кислорода (формула H2O) .
Зависит ли он от способа её получения? Не зависит, т.к. вода ― молекулярное вещество, а закон постоянства состава применим лишь к веществам, состоящим из молекул.
Почему вода из водопроводного крана, из колодца и из моря различается по вкусу? Содержит разное количество примесей (в основном растворённых в ней солей).
Задание 2
Выпишите вещества, состав которых не зависит от способа их получения: углекислый газ, этиловый спирт , кварц, уксусная кислота , алмаз.
Закон постоянства состава, а именно: состав вещества постоянен и не зависит от способа его получения, применим только к молекулярным веществам (углекислый газ, этиловый спирт, уксусная кислота). Алмаз и кварц ― немолекулярные вещества и могут содержать различные примеси (например, придающие им цвет) .
Источник
Способы получения углекислого газа
Углекислый газ не является редким и получают его как побочный продукт, что положительно сказывается на его стоимости. Поэтому он является самым дешевым газом, применяемым для защиты, метала сварного шва в процессе сварки. Кратко о способах производства углекислоты говорилось в статье о свойствах углекислого газа и теперь настало время рассмотреть их более подробно.
Содержание
В промышленном масштабе углекислый газ получают следующими способами:
- из известняка, в котором содержится до 40% СО2, кокса или антрацита до 18% CO2 путем их обжига в специальных печах;
- на установках, работающих по сернокислому методу за счет реакций взаимодействия серной кислоты с эмульсией мела;
- из газов, образующихся при брожении спирта, пива, расщепления жиров;
- из дымовых газов промышленных котельных, сжигающих уголь, природный газ и другое топливо. Дымовой газ содержит 12-20% СО2;
- из отходящих газов химических производств, в первую очередь синтетического аммиака и метанола. Отходящие газы содержат примерно 90% СО2.
На данный момент наиболее распространенным способом производства углекислоты является – получение из газов при брожении.
Получение углекислого газа из газов при брожении
Отходящий газ при брожении представляет собой почти чистый углекислый газ и является дешевым побочным продуктом производства.
На гидролизных заводах при брожении дрожжей с опилками выделяются газы, содержащие 99% CO2.
1 — бродильный чан; 2 — газгольдер; 3 — промывочная башня; 4 — предварительный компрессор; 5 — трубчатый холодильник; 6 — маслоотделитель; 7 — башня; 8 — башня; 9 — двухступенчатый компрессор; 10 — холодильник; 11 — маслоотделитель; 12 — цистерна.
Схема получения углекислого газа на гидролизных заводах
Газ из бродильного чана 1 подается насосами, а при наличии достаточного давления поступает самостоятельно в газгольдер 2, где происходит отделение от него твердых частиц. Затем газ поступает в промывочную башню 3, заполненную коксом или керамическими кольцами, где он омывается встречным потоком воды и окончательно освобождается от твердых частиц и растворимых в воде примесей. После промывки газ поступает в предварительный компрессор 4, где он сжимается до давления 400-550 кПа.
Так как при сжатии температура углекислого газа повышается до 90-100°С, то после компрессора газ поступает в трубчатый холодильник 5, где охлаждается до 15°С. Затем углекислота направляется в маслоотделитель 6, где отделяется масло, попавшее в газ при сжатии. После этого углекислый газ подвергается очистке водными растворами окислителей (KMnO4, K2Cr2P7, гипохромитом) в башне 7, а затем осушке активированным углем или силикагелем в башне 8.
После очистки и осушки углекислота поступает в двухступенчатый компрессор 9. На ступени I происходит сжатие его до 1-1,2 МПа. Затем углекислый газ поступает в холодильник 10, где охлаждается со 100 до 15°C, проходит маслоотделитель 11 и поступает на II ступень компрессора, где сжимается до 6-7 МПа, превращается в жидкую двуокись углерода и собирается в цистерну 12, из которой производится заправка стандартных баллонов или других емкостей (танков).
Принципиально процесс производства углекислого газа другими методами ничем не отличается от вышеуказанного: сначала газ очищается, потом производят осушку, а на последнем этапе охлаждение и сжатие для превращения в жидкость, поскольку в данном виде его удобно хранить и транспортировать.
Источник
Углекислый газ в промышленности, его получение и применение
Углекислый газ, имея универсальные свойства, используется в промышленности, медицине, сельском хозяйстве. Сегодня CO2 – это удобрение в сельском хозяйстве, медицинский инструмент, регулятор температуры и источник новой энергии.
Получение в промышленности
Получение диоксида углерода в промышленности методологически разнообразно. Он находится в дымовых отходах, выпускаемых в атмосферу ТЭЦ и электростанциями, получается при брожении спирта и выступает как продукт реакции с природными карбонатами.
Индустрия получения двуокиси углерода широка. Газ можно абсорбировать несколькими способами из одного источника. Во всех случаях это поэтапный процесс очистки от примесей (для достижения требований ГОСТа) и достижения нужной консистенции, агрегатного состояния.
Получение газообразной двуокиси углерода
Газообразный CO2 извлекают из промышленных (нефтяных) дымов путем адсорбции моноэтаноламина (коммерчески выгодно) и карбонатом калия (редко). Принцип сбора частиц углерода одинаков для обоих веществ. Они направляются по трубопроводу к отходам и собирают в себя углекислый газ. После сбора, насыщенные углекислотой газы направляются на очистку.
В специальных емкостях происходит реакция в при повышенной температуре или заниженном давлении. В процессе высвобождается чистая углекислота и продукты распада (аммиак и другие).

Схематически процесс выглядит так:
- Отходящий дым смешивается с адсорбентами (газообразным карбонатом калия или моноэтаноламином);
- Накопившие в себе двуокись углерода газы поступают в специальный газгольдер для очистки;
- В реакции с высокой температурой или низким давлением происходит отделение углекислого газа от адсорбента.
В лаборатории извлечь много CO2 не получается. Но это возможно в реакции с гидрокарбонатами и кислотами. В отдельности CO2 можно выделить на промышленных станках для получения кислорода, аргона или азота. Углекислый газ здесь выступает как побочный продукт. Хранится он в специальных баллонах, поставляемых потребителю.
Получение жидкой углекислоты
Добыча жидкой углекислоты поэтапно связана с получением ее из газа. Из летучего газообразного состояния, при обработке водородом, раствором перманганата калия и углем, образуется жидкая двуокись.
Сжижение происходит из-за низкого давления, сопровождающего реакцию. После многоступенчатой очистки, жидкий диоксид углерода попадает в компрессор. Там он сжимается и подается для сушки в 2 адсорбера, поочередно перенимающие работу для восстановления. Параллельно сжатая жидкость очищается от запахов и переводится в конденсатор, а оттуда – на хранение.
Этот метод сжижения применяется для газов спиртового брожения. Он актуален для пропана, бутана и т.д. Его используют на крупных пивоварнях, а получаемая очищенная углекислота имеет высокие показатели качества.
Получение твердого диоксида углерода
Твердый диоксид образуют из жидкого путем обработки низкой температурой (-56°). В промышленных условиях только 20% переходят в твердое состояние, а остальные – испаряются.

Порядок извлечения углекислотных кристаллов (сухого льда):
- Из емкости брожения газ переходит в емкость для промывки;
- В газгольдере после мытья он сжимается и сжижается;
- Многократно сжимаясь и нагреваясь, газообразный углерод охлаждается в специальных холодильниках;
- Жидкость очищается активированным углем;
- Поступает в холодильник, где охлаждается и дополнительно очищается от примесей;
- Охлажденный CO2 направляется на испарение и пресс, где комплектуется сухой лед.
Применение в промышленности
Применение углекислого газа в различных областях промышленности связано с химическими и физическими свойствами вещества. Он не горит, не опасен в минимальных концентрациях для человека и животных и является основным компонентом для жизнедеятельности растений.
Химическая промышленность:
- Участвует в синтезе искусственных химикатов;
- Регулирует температуру в реакциях;
- Нейтрализует щелочи;
- Очищает ткани животных и растений;
- Может восстанавливаться до метана.
Металлургия:
- Осаждение отходящего дыма;
- Регулирует направления течения воды при отводе шахт;
- Некоторые лазеры используют CO2 в качестве источника энергии (неон).
Производство бумаги:
- Регулирует водородный показатель в древесной массе или целлюлозе;
- Усиливает в мощности производственные машины.
Особую роль в промышленной и смежных индустриях играет сухой лед. Он применяется как:
- Источник охлаждения в морозильных камерах при перевозках;
- Охлаждение при затвердевании сплавов;
- Очистка сухим льдом оборудования (криобластинг).
Применение в других сферах деятельности
Человек также использует углекислоту в других областях деятельности и в быту. Доступность диоксида обуславливает его широкую распространенность, а свойства – востребованность даже среди обывателей.
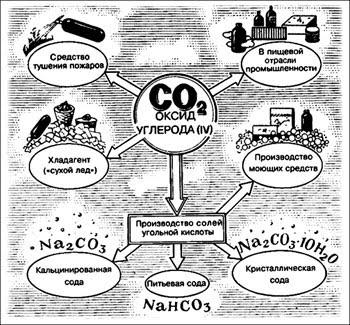
Где еще применяется углекислота:
- При сварке. Защищает металл от нагрева и окисления, обтекая электрическую дугу.
- В сельском хозяйстве. Углекислый газ в купе с солнечным светом – идеальный способ удобрить любые культуры. Распыление газа в парнике или теплице увеличивает урожайность в 2-3 раза;
- В медицине служит для создания атмосферы, близкой к реальной, при проведении искусственных операций на органах. Он применяется как стимулятор для восстановления дыхания пациента и при введении его в наркоз;
- Фармацевтика. Создает идеальную среду для синтеза химии и низкотемпературной транспортировки вод;
- Приборы и оборудование. Охлаждает оборудование и агрегаты без разбора на модули, выступает как абразивный элемент прочистки;
- Защита окружающей среды. Регулирует показатель водорода в стоках;
- Пищевая промышленность. Используется как консервант и разрыхлитель теста. Добавляется в напитки, делая их газированными;
- Для создания давления в пневматическом оружии.
Применение углекислого газа особенно востребовано в системах пожаротушения. Он заполняется в углекислотные газовые огнетушители и при возгорании позволяет изолировать очаг пожара от источника кислорода. Горение не может долго продолжаться без подпитки воздухом, а газификация углекислотой не даст ему проникнуть к огню.
Получаемый в малом количестве от спиртового брожения используется как способ газировки напитков. Он также уберегает муку, сухофрукты, арахис от насекомых, не влияя на качество и скорость их порчи.
Углекислый газ – первоклассная среда для разведения цветов, подкормки овощей и подводных растений. Он ускоряет фотосинтез и улучшает обменные процессы в растительных клетках. Главное – имеет доступную цену даже для обывателей.
Диоксид углерода может применяться и в криодеструкции, в качестве заморозки. Он сжигает холодом поверхность бородавок и родинок, заставляя их отваливаться, но не оставлять шрамов от скальпеля и швов.
Заключение
Углекислый газ – простое и распространенное по всей планете вещество, играющее практическую функцию в ключевых отраслях деятельности. Без него не обходится промышленность, медицина, пищевая отрасль и даже простой человеческий быт.
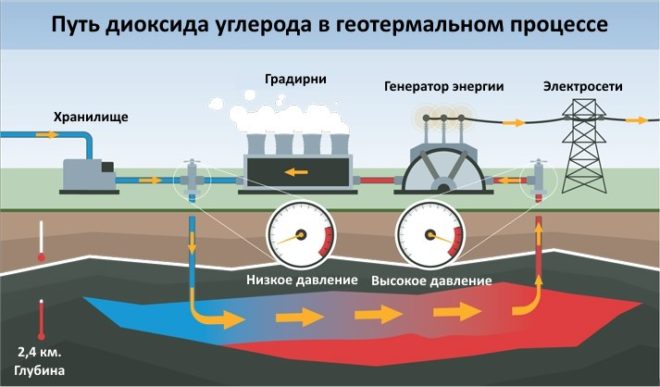
С недавних пор CO2 применяется как основа для производства источника топлива (метанола). Популярность набирает способ использования в качестве возобновляемого геотермального источника энергии, способного увеличить производство электроэнергии и сократить выбросы газа в атмосферу.
Источник