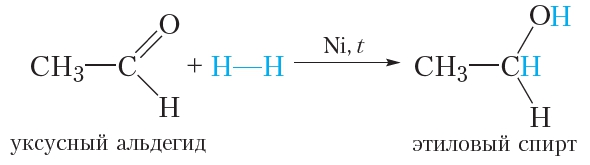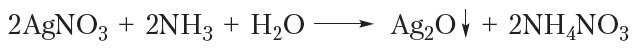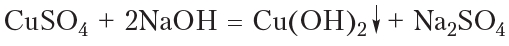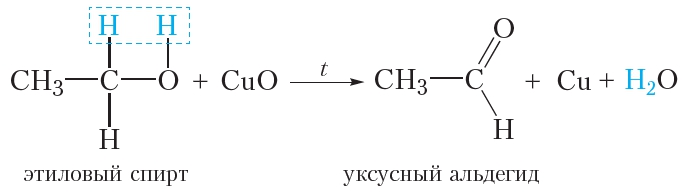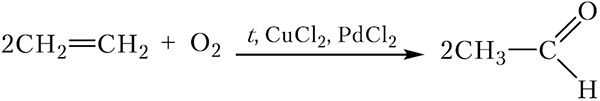- § 30. Химические свойства, получение и применение альдегидов
- Оглавление
- Химические свойства альдегидов
- Получение альдегидов
- Применение
- *Получение уксусного альдегида
- Вопросы и задания
- Уксусный альдегид: формула, свойства и получение
- Альдегиды и кетоны
- Как получить уксусный альдегид
- Общая формула альдегидов
- Классификация альдегидов
- Общая формула предельных альдегидов
- Гомологический ряд, изомерия, номенклатура
- Электронное строение молекул альдегидов
- Свойства альдегидов
- Физические свойства
- Химические свойства
- Способы получения
- Специфические способы получения формальдегида и ацетальдегида
- Применение альдегидов
§ 30. Химические свойства, получение и применение альдегидов
| Сайт: | Профильное обучение |
| Курс: | Химия. 10 класс |
| Книга: | § 30. Химические свойства, получение и применение альдегидов |
| Напечатано:: | Гость |
| Дата: | Суббота, 20 Ноябрь 2021, 15:14 |
Оглавление
Химические свойства альдегидов
Химические свойства альдегидов прежде всего обусловлены наличием в их молекулах альдегидной группы. По месту двойной связи альдегидной группы могут протекать реакции присоединения.
1. Гидрирование. Присоединение водорода
Молекула альдегида может присоединить по двойной связи молекулу водорода. Такая реакция сопровождаются разрывом π-связи в молекуле альдегида, так как она менее прочная, чем σ-связь:
Условия протекания данной реакции схожи с реакцией гидрирования алкенов: смесь водорода с парами альдегида пропускают над нагретым никелевым катализатором.
Продуктом присоединения водорода к альдегиду является первичный спирт.
В результате присоединения водорода молекула альдегида восстанавливается, поэтому реакцию с водородом также называют реакцией восстановления альдегидов.
2. Окисление
Альдегидная группа легко окисляется. В качестве окислителей могут выступать ионы металлов, расположенных в ряду активности правее водорода — ионы серебра (Ag + ) и меди (Cu 2+ ).
Окисление альдегидов аммиачным раствором оксида серебра
Если к разбавленному раствору нитрата серебра приливать раствор аммиака, то выпадает белый осадок оксида серебра:
Этот осадок сразу же растворяется в избытке аммиака. Образующийся прозрачный раствор называется аммиачным раствором оксида серебра. Если к этому раствору прибавить раствор уксусного альдегида и смесь осторожно нагреть, то вскоре на стенках пробирки образуется блестящий зеркальный налёт серебра, благодаря чему эта реакция называется реакцией «серебряного зеркала».
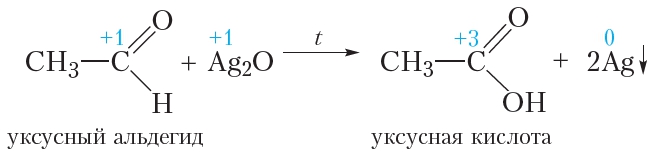
В протекающей реакции уксусный альдегид окисляется до уксусной кислоты, а оксид серебра восстанавливается с образованием металлического серебра:
Реакция «серебряного зеркала» является качественной реакцией на альдегиды.
Окисление альдегидов гидроксидом меди(II)
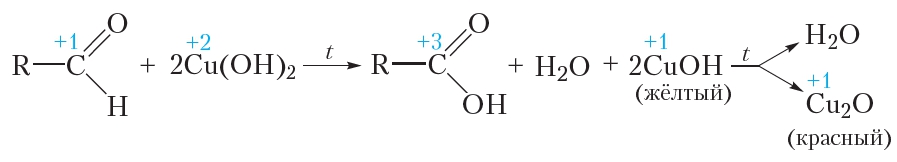
В качестве окислителя альдегидов до соответствующих кислот может быть использован также гидроксид меди(II). Для проведения такой реакции в пробирку помещают раствор сульфата меди(II), затем прибавляют раствор щёлочи. При этом выпадает голубой осадок гидроксида меди(II):
Затем в пробирку с осадком добавляют водный раствор альдегида и смесь нагревают. В процессе нагревания изначально голубой осадок становится жёлтым, а при дальнейшем нагревании — красным. Уравнение протекающей реакции:
Как видно из приведённого уравнения реакции, в результате восстановления гидроксида меди(II) образуется жёлтый осадок гидроксида меди(I), который при нагревании разлагается с образованием красного оксида меди(I).
Как и в случае реакции «серебряного зеркала», продуктом окисления альдегида является карбоновая кислота.
Реакция окисления альдегидов гидроксидом меди(II) так же, как и реакция «серебряного зеркала», является качественной реакцией на альдегиды.
Способность альдегидов окисляться до карбоновых кислот и восстанавливаться до спиртов особенно наглядно демонстрирует взаимосвязь между классами органических соединений, благодаря которой вещества одного класса могут быть получены из представителей других классов.
Получение альдегидов
1. Неполное окисление спиртов
Как вы уже знаете, альдегиды могут быть получены при неполном окислении первичных спиртов оксидом меди(II) (§ 24). Так, при окислении этилового спирта образуется уксусный альдегид:
Для проведения реакции медную проволоку прокаливают в пламени спиртовки, в результате поверхность проволоки покрывается чёрным оксидом меди(II). Затем проволоку погружают в этиловый спирт, при этом оксид меди(II) окисляет спирт до уксусного альдегида и образуется медь, поэтому проволока снова становится блестящей (видео 24.1).
2. Гидратация ацетилена
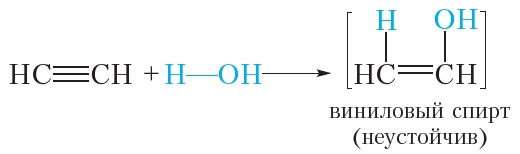
Уксусный альдегид можно получить по реакции присоединения воды к ацетилену в присутствии солей ртути и серной кислоты: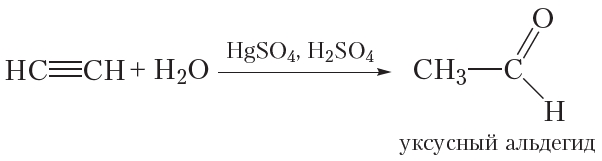
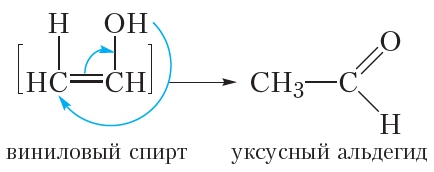
Рассмотрим подробнее, как протекает данная реакция. Сначала молекула воды присоединяется по одной π-связи молекулы ацетилена. При этом образуется неустойчивый виниловый спирт:
Напомним, что радикал CH2 



Применение
Наибольшее применение имеют муравьиный и уксусный альдегиды.
Некоторые области использования муравьиного альдегида основаны на его свойстве свёртывать белки. Он используется в медицине в качестве консерванта биологических тканей. Формальдегид широко применяется в кожевенном производстве, так как, оказывая влияние на белки кожи, он делает последнюю более твёрдой и устойчивой к гниению.
В результате взаимодействия формальдегида с аммиаком получают лекарственное средство — уротропин.
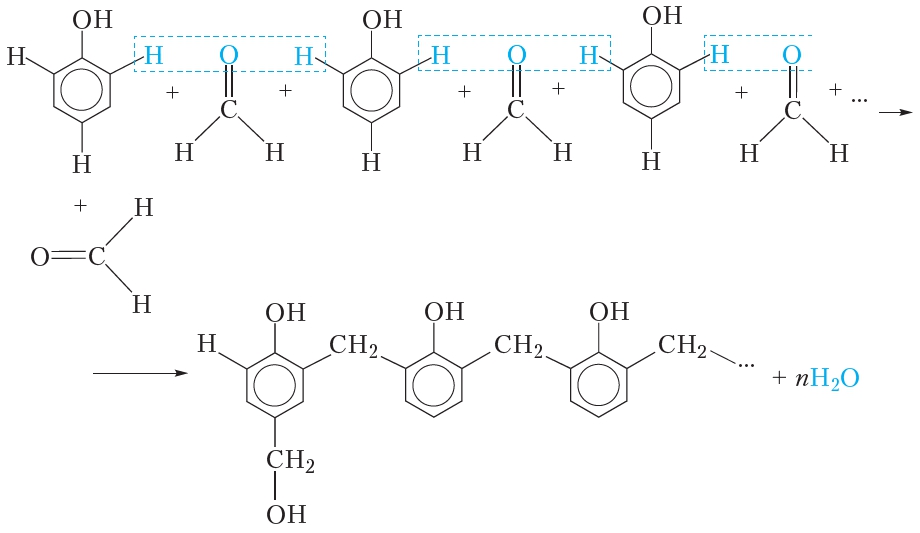
Кроме того формальдегид используется в производстве фенолформальдегидных пластмасс. Основу таких пластмасс составляет высокомолекулярное соединение — фенолформальдегидная смола. Она образуется при нагревании фенола с формальдегидом в присутствии катализатора. Механизм образования фенолформальдегидной смолы достаточно сложен и представлен схематически:
Как видно из приведённой схемы, в результате реакции образуется линейный полимер, в котором молекулы фенола соединены группами —CH2— через положения 2 и 6 бензольного кольца. Кроме этого, некоторые остатки фенола содержат в положении 4 бензольного кольца группы —CH2OH .
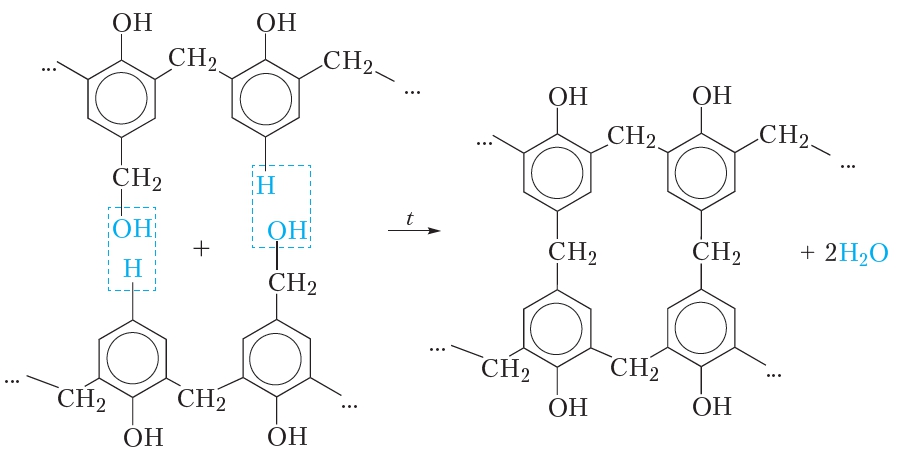
За счёт групп —CH2OH при нагревании до 130—150 °С такой полимер «сшивается», образуя очень твёрдую и прочную фенолформальдегидную смолу с «сетчатой» структурой:
Материалы на основе фенолформальдегидных смол обычно изготавливают, смешивая расплавленный полимер линейного строения с наполнителем (древесная мука, стружки, асбест и др.). Далее полученный материал прессуют при нагревании. При этом расплавленный полимер хорошо заполняет форму, а затем затвердевает, образуя «сетчатую» структуру. В результате получается монолитное твёрдое изделие. Некоторые материалы, в которых фенолформальдегидная смола выступает в качестве связующего, вам хорошо знакомы. Например, некоторые виды ДСП (древесностружечная плита) представляют собой смесь древесных стружек, скреплённых между собой фенолформальдегидным полимером.
В процессе образования фенолформальдегидной смолы из низкомолекулярных веществ — фенола и формальдегида — в результате отщепления воды образуется высокомолекулярное вещество. Такой процесс называется поликонденсацией. Следует различать процессы поликонденсации и полимеризации. В процессе поликонденсации наряду с высокомолекулярным соединением образуется побочный низкомолекулярный продукт. В рассмотренной реакции поликонденсации фенола с формальдегидом этим продуктом является вода.
В процессе полимеризации высокомолекулярное вещество (полимер) образуется в результате многократно повторяющейся реакции присоединения. Поэтому, в отличие от поликонденсации, процесс полимеризации не сопровождается образованием побочных низкомолекулярных продуктов.
Уксусный альдегид в больших количествах используется для производства уксусной кислоты, а также других органических веществ.
Альдегиды вступают в реакции присоединения по месту двойной связи C 
Альдегиды окисляются гидроксидом меди(II) и аммиачным раствором оксида серебра до карбоновых кислот. Эти реакции являются качественными реакциями на альдегидную группу.
Альдегиды могут быть получены окислением первичных спиртов оксидом меди(II).
Уксусный альдегид можно получить присоединением воды к ацетилену в присутствии солей ртути и серной кислоты.
Альдегиды используются для получения пластмасс, лекарственных препаратов, для синтеза органических веществ, а также в парфюмерии.
*Получение уксусного альдегида
В настоящее время уксусный альдегид получают в результате так называемого Вакер-процесса. Для этого газообразную смесь этилена с кислородом пропускают через водный раствор, содержащий хлориды палладия(II) и меди(II). Происходящие процессы можно выразить суммарным уравнением:
Вопросы и задания
1. Какие спирты образуются в результате восстановления водородом этаналя и 2-метилпропаналя? Напишите уравнения реакций, назовите образующиеся продукты.
2. Напишите уравнение реакции пропаналя с гидроксидом меди(II) при нагревании. Опишите наблюдаемые явления.
3. В результате нагревания водного раствора вещества А с аммиачным раствором оксида серебра образуется кислота Б, а стенки пробирки покрываются серебряным налётом.
При пропускании смеси вещества А с водородом над нагретым никелевым катализатором образуется спирт В. При нагревании спирта В с концентрированной серной кислотой получается углеводород Г, немного легче воздуха. Установите формулы веществ А—Г и приведите уравнения реакций, описанных в задании.
4. В результате окисления 2,15 г гомолога уксусного альдегида аммиачным раствором Ag2O было получено 5,4 г серебра. Установите молекулярную формулу альдегида.
5. Одним из современных промышленных методов получения уксусного альдегида является окисление этилена хлоридом палладия в присутствии хлорида меди(II) и кислорода воздуха (Вакер-процесс):
Для синтеза этаналя в промышленных условиях смесь этилена и кислорода пропускают через реактор, содержащий раствор хлоридов палладия и меди(II) при температуре 130 о С и давлении 400 кПа. Известно, что степень превращения веществ в реакторе в указанных условиях составляет 25 %. Укажите массу этаналя, образующегося из этилена объёмом (н. у.) 10 м 3 и достаточного количества кислорода.
6*. При действии воды на твёрдое вещество А образуется газ (н. у.) Б, легче воздуха. При пропускании Б через горячий водный раствор содержащий серную кислоту и сульфат ртути(II) образуется органическое вещество В. Вещество В можно также получить двухстадийным синтезом. Сначала вещество Б гидрируют на специальных катализаторах. При этом образуется газ (н. у.) Г, легче воздуха. Затем смесь газа Г и кислорода поглощают водным раствором, содержащим смесь CuCl2 и PdCl2. При этом образуется вещество В.
а) Приведите структурные формулы веществ А, Б, В и Г.
б) Напишите уравнения всех описанных в задаче реакций.
в) При гидрировании вещества В образуется вещество Д, имеющее только один изомер (вещество Е). Приведите формулы и названия веществ Д и Е, а также уравнение реакции гидрирования вещества В.
г) Температура кипения какого вещества (Д или Е) выше и почему?
7*. Напишите схемы реакций, с помощью которых можно получить в две стадии бромэтан, исходя из уксусного альдегида.
Источник
Уксусный альдегид: формула, свойства и получение
Альдегиды и кетоны
Альдегидами и кетонами называются производные углеводородов, содержащие карбонильную группу, или оксогруппу. В альдегидах, как правило, карбонильная группа связана одной из своих свободных валентностей с атомом водорода, другой – с каким-либо углеводородным радикалом. Все альдегиды содержат группу СОН, называемую альдегидной. В кетонах карбонильная группа двумя своими валентностями соединена с какими-либо углеводородными радикалами. Альдегиды и кетоны бывают насыщенными, ненасыщенными и ароматическими. Предельные альдегиды и кетоны с одинаковым числом углеродных атомов изомерны друг другу и имеют одну и ту же суммарную формулу.
Рисунок 3.3 – Строение карбонильной группы
Альдегиды называют или по кислотам, в которые они переходят при окислении (тривиальная номенклатура), или по названию предельных углеводородов с добавлением окончания -аль (систематическая номенклатура IUРАС). Кетоны по рациональной номенклатуре называют по названию радикалов, входящих в их молекулу, с добавлением окончания -кетон. По систематической номенклатуре IUРАС кетоны называют по названию соответствующего углеводорода с добавлением окончания -он и с указанием местонахождения карбонильной группы.
Наличие карбонильной группы обусловливает высокую реакционную активность альдегидов и кетонов и определяет их способность к многочисленным и разнообразным реакциям.
Альдегиды легко окисляются до карбоновых кислот с тем же углеродным скелетом.
1. Они могут окисляться даже кислородом воздуха и такими слабыми окислителями, как аммиачный раствор гидроокиси серебра:
2. Реакцию альдегидов с аммиачным раствором гидроокиси серебра называют «реакцией серебряного зеркала» – окисление аммиачным раствором оксида серебра (реактив Толленса). Ее используют для обнаружения альдегидов:
R–CH=O + 2[Ag(NH3)2]OH → RCOOH + 2Ag↓ + 4NH3 + H2O.
Кетоны не окисляются ни кислородом воздуха, ни слабыми окислителями, не восстанавливают аммиачный раствор гидроокиси серебра. Они окисляются лишь под действием более сильных окислителей, например, перманганата калия, причем окисление происходит иначе, чем окисление альдегидов. При окислении молекула кетона расщепляется с образованием молекул кислот или кислоты и кетона с меньшим числом углеродных атомов, чем первоначальный. Разрыв цепи углеродных атомов происходит рядом с карбонильным атомом углерода:
Если в молекуле кетона содержится два различных радикала, то распад молекулы при окислении может идти по двум возможным направлениям, например:
Таким образом, произведя окисление кетона и узнав, какие кислоты получились в результате окисления, можно определить строение кетона.
3. Реакция окисления гидроксидом меди(II):
а) в виде свежеприготовленного осадка Cu(OH)2 при нагревании;
б) в форме комплекса с аммиаком [Cu(NH3)4](OH)2;
в) в составе комплекса с солью винной кислоты (реактив Фелинга).
При этом образуется красно-кирпичный осадок оксида меди(I) или металлическая медь (реакция «медного зеркала», более характерная для формальдегида):
R–CH=О + 2Cu(OH)2 → RCOOH + Cu2O↓ + H2О;
H2C=О + Cu(OH)2 → HCOOH + Cu↓ + H2О;
R–CH=O + 2[Cu(NH3)4](OH)2 → RCOOH + Cu2O↓ + 4NH3 + 2H2O;
R–CH=O + 2Cu(OH)2/соль винной кислоты → RCOOH + Cu2O↓ + 2H2O.
При нагревании наблюдают появление осадка оксида меди(I) желтого цвета, переходящего в красный:
Муравьиный альдегид, в отличие от других альдегидов, восстанавливает оксиды меди, образуя «медное зеркало».
4. Реакция восстановления альдегидами реактива Фелинга.
Реакционную смесь нагревают. При этом раствор сначала окрашивается в зеленый, а затем в желтый цвет, и наконец, выпадает оксид меди (I) красного цвета:
5. Цветная реакция на альдегиды с фуксиксернистой кислотой: наблюдается постепенное появление красно-фиолетовой окраски. Если к смеси муравьиного альдегида с фуксинсернистой кислотой прибавлять концентрированную соляную кислоту, то появляется характерная синяя окраска. В смеси изовалерианового альдегида с фуксинсернистой кислотой под влиянием соляной кислоты окраска сравнительно быстро исчезает.
Рисунок 3.4 – Качественные реакции на альдегидную группу
Как альдегиды, так и кетоны могут присоединять водород, синильную кислоту, магний-органические соединения, гидросульфит натрия.
С гидроксиламином и фенилгидразином альдегиды и кетоны реагируют с образованием оксимов и фенилгидразонов; при действии пятихлористого фосфора атом кислорода в молекулах альдегидов и кетонов замещается двумя атомами хлора.
Однако между альдегидами и кетонами имеются и существенные различия. Так, в отличие от альдегидов кетоны не окрашивают бесцветный раствор фуксинсернистой кислоты, в мягких условиях не конденсируются под действием щелочей, за редкими исключениями, и дают со спиртами ацетали только в присутствии кислот Льюиса. Из кетонов с гидросульфитом натрия реагируют только те, которые содержат одну метильную или две метиленовые группы в непосредственном соседстве с карбонилом.
Окисляются кетоны труднее, чем альдегиды, причем при их окислении происходит разрушение молекулы, труднее для кетонов протекают и реакции конденсации.
Применение альдегидов и кетонов.
Метаналь (муравьиный альдегид) CH2=O: получение фенолформальдегидных смол; получение мочевино-формальдегидных (карбамидных) смол; полиоксиметиленовые полимеры; синтез лекарственных средств (уротропин); дезинфицирующее средство; консервант биологических препаратов (благодаря способности свертывать белок).
Этаналь (уксусный альдегид, ацетальдегид) СН3СН=О: производство уксусной кислоты; органический синтез.
Ацетон СН3–СО–СН3: растворитель лаков, красок, ацетатов целлюлозы; сырье для синтеза различных органических веществ.
Как получить уксусный альдегид
Реактивы и материалы: формальдегид, 40%-ный водный раствор; сульфат меди CuSO4, 0,2 н. раствор; едкий натр, 2 н. раствор.
В пробирку помещают 4 капли раствора едкого натра, разбавляют 4 каплями воды и добавляют 2 капли раствора сульфата меди (II). К выпавшему осадку гидроксида меди (II) прибавляют 1 каплю раствора формальдегида и взбалтывают содержимое пробирки.
Нагревают над пламенем горелки до кипения только верхнюю часть раствора так, чтобы нижняя часть оставалась для контроля холодной. В нагретой части пробирки выделяется желтый осадок гидроксида меди (I) (СuОН), переходящий в красный оксид меди (I) (Сu2О), а иногда на стенках пробирки выделяется даже металлическая медь.
CuSO4 + 2NaOH = Cu(OH)2 + Na2SO4
2Cu(OH)2 + HCOH = HCOOH + Cu2O + 2H2O
Повторите этот опыт, заменив раствор формальдегида раствором этаналя.
Общая формула альдегидов
(для простейшего альдегида R=H)
Классификация альдегидов
По строению углеводородного радикала:
Общая формула предельных альдегидов
Гомологический ряд, изомерия, номенклатура
Альдегиды изомерны другому классу соединений — кетонам
Альдегиды и кетоны содержат карбонильную группу ˃C=O, поэтому называются
Электронное строение молекул альдегидов
Атом углерода альдегидной группы находится в состоянии sp2-гибридизации, поэтому все σ-связи в этой группе располагаются в одной плоскости.
Облака р-электронов, образующих π-связь, перпендикулярны этой плоскости и легко смещаются к более электроотрицательному атому кислорода. Поэтому двойная связь C=O (в отличие от двойной связи C=C в алкенах) сильно поляризована.
Свойства альдегидов
Физические свойства
Химические свойства
Альдегиды — реакционноспособные соединения, вступающие в многочисленные реакции.
Наиболее характерны для альдегидов:
по карбонильной группе; реагенты типа НХ присоединяются следующим образом:
связи C-H альдегидной группы, в результате которых образуются карбоновые кислоты:
В избытке спирта в присутствии HCl полуацетали превращаются в ацетали:
II. уксусный альдегид cu oh 2
Эта реакция является (на стенках реакционного сосуда образуется зеркальный налет металлического серебра).
Эта реакция также являетсяу (выпадает красный осадок Сu2O).
Формальдегид окисляется различными O-содержащими окислителями сначала до муравьиной кислоты и далее — до Н2СO3(СO2 + Н2O):
III. Реакции ди-, три- и полимеризации
3. Полимеризация формальдегида
При длительном хранении формалина (40%-ный водный раствор формальдегида) в нем происходит полимеризация с образованием белого осадка параформа:
IV. Реакция поликонденсации формальдегида с фенолом
V. Превращение формальдегида в углеводы
VI. Взаимодействие формальдегида с аммиаком
Способы получения
1. Окисление алкенов
2. Каталитическое окисление первичных спиртов
3. Окисление первичных спиртов различными окислителями (КМnО4, K2Cr2О7 и др.)
4. Каталитическое дегидрирование первичных спиртов
5. Щелочной гидролиз дигалогеналканов, содержащих атомы галогена у первичного атома углерода.
При гидролизе дигалогеналканов, содержащих атомы галогена у вторичного атома углерода, образуются кетоны:
Специфические способы получения формальдегида и ацетальдегида
1. Каталитическое окисление метана
2. Гидратация ацетилена (реакция Кучерова)
Понятие о альдегиды. Состав молекулы, электронная и структурная формулы.
Функциональная карбонильная группа
Альдегидами называют органические вещества, молекулы которых содержат функциональную группу атомов 
Общая формула веществ этого класса CnH2n +1 COН или R-COН, в которой R — это атом водорода (в случае с Мурино альдегидом) или углеводородный радикал.
Группа атомов 
Сравнению со спиртами в составе молекул альдегидов на два атома водорода меньше.
Это отражается в названии «альдегиды», что происходит от слов «алкоголь» и «дегидрирования», т.е. дегидрований алкоголь.
Первый член гомологического ряда альдегидов — метаналь, или формальдегид, или Мурино альдегид.
Он формулу 
Следующий за ним — этаналь, или ацетальдегид, или уксусный альдегид. Его формула 
По номенклатуре, исторически сложилась, названия альдегидов происходят от названий тех кислот, на которые они превращаются при окислении. Например, Мурино альдегид — от Мурино кислоты, уксусный альдегид — от уксусной кислоты и т. д. По систематической номенклатуре, названия альдегидов образуют от названий соответствующих предельных углеводородов путем добавления суффикса-аль: метаналь, этаналь, пропаналя т.д..
Формальдегид СН2=О (муравьиный альдегид, метаналь).
Представляет собой бесцветное горючее вещество с острым раздражающим запахом. Растворим в воде, обычно используется в виде 33-40 % водного раствора, который называют формалином. Вырабатывают формальдегид в больших количествах.
Он применяется в производстве пластмасс. Полиформальдегид с большим молекулярным весом – ценный синтетический материал, используемый в качестве заменителя металлов. В кожевенной промышленности формальдегид применяется для дубления кожи, в медицине и санитарии – для дезинфекции.
В с/х формальдегид используется для протравливания семян перед посевом (уничтожают паразитические споры). Так как формальдегид образуется при неполном сгорании различных органических веществ, то он содержится в дыме угля, дерева; на этом основано консервирующее действие дыма при получении мясных и рыбных копченостей.
Ацетальдегид СН3—СН=О (уксусный альдегид, этаналь).
Представляет собой бесцветную легколетучую, легковоспламеняющуюся жидкость с сильным характерным запахом прелых яблок.
1. уксусный альдегид+ Ag₂O => (р. серебряного зеркала) 2. уксусный альдегид+2Cu(OH)₂ =>
Хорошо растворим в воде. Используют ацетальдегид для многих промышленных синтезов. Особенно важно окисление его в уксусную кислоту, превращение в этилацетат (по реакции Тищенко); может быть восстановлен в этиловый спирт.
Ацетон СН3—СО—СН3 (диметилкетон).
Бесцветная, легковоспламеняющаяся жидкость с довольно приятным запахом. Смешивается с водой. Ацетон является ценным растворителем (в производстве лаков, искусственного шелка, взрывчатых веществ) и исходным веществом в синтезе разнообразных органических соединений.
В последнее время в технике большое значение приобрело применение ацетона для получения так называемого кетена.
Кетен – газообразное вещество, очень реакционноспособное. Применяется для получения уксусного ангидрида и ряда других ценных продуктов, в частности, очень хорошего пищевого консерванта – сорбиновой кислоты.
Применение альдегидов
Из альдегидов наибольшее применение имеет формальдегид.
Особенности применения формальдегида: используется обычно в виде водного раствора – формалина; многие способы применения формальдегида основаны на свойстве свертывать белки; в сельском хозяйстве формалин необходим для протравливания семян; формалин применяется в кожевенном производстве; формалин оказывает дубящее действие на белки кожи, делает их более твердыми, негниющими; формалин применяется также для сохранения биологических препаратов; при взаимодействии формальдегида с аммиаком получается широко известное лекарственное вещество уротропин.
Основная масса формальдегида идет на получение фенолформальдегидных пластмасс, из которых изготавливаются: а) электротехнические изделия; б) детали машин и др.
Ацетальдегид (уксусный альдегид) в больших количествах используется для производства уксусной кислоты.
Восстановлением ацетальдегида в некоторых странах получают этиловый спирт.
Получение альдегидов:
1) общим способом получения альдегидов служит окисление спиртов;
2) если накалить в пламени спиртовки спираль из медной проволочки и опустить ее в пробирку со спиртом, то проволочка, которая покрывается при нагревании темным налетом оксида меди (II), в спирте становится блестящей;
3) обнаруживается также запах альдегида.
С помощью такой реакции получается формальдегид в промышленности.
Для получения формальдегида через реактор с раскаленной сеткой из меди или серебра пропускается смесь паров метилового спирта с воздухом;
4) при лабораторном получении альдегидов для окисления спиртов могут быть использованы и другие окислители, например перманганат калия;
5) при образовании альдегида спирт, или алкоголь, подвергается дегидрированию.
Особенности реакции гидратации ацетилена:
а) сначала идет присоединение воды к ацетилену по месту одной π-связи;
б) образуется виниловый спирт;
в) непредельные спирты, в которых гидроксильная группа находится у атома углерода, который связан двойной связью, неустойчивы и легко изомеризуются;
г) виниловый спирт превращается в альдегид:
д) реакция легко осуществляется, если пропускать ацетилен в нагретую воду, которая содержит серную кислоту и оксид ртути (II);
е) через несколько минут в приемнике можно обнаружить раствор альдегида.
В последние годы разработан и получает распространение способ получения ацетальдегида окислением этилена кислородом в присутствии хлоридов палладия и меди.
Свойства
В химическом отношении это высоко реакционноспособные вещества, что обусловлено наличием в их молекуле карбонильной группы.
Высокая реакционная способность альдегидов объясняется:
а) наличием поляризованной двойной связи
б) дипольным моментом карбонила
в) наличием частичного положительного заряда на атоме углерода карбонила
Двойная связь между С и О, в отличие от двойной связи между двумя углеродами, сильно поляризована, так как кислород обладает значительно большей электроотрицательностью, чем углерод, и электронная плотность π-связи смещается к кислороду.
Такая высокая поляризация определяет электрофильные свойства углерода карбонильной группы и его способность реагировать с нуклеофильными соединениями (вступать в реакции нуклеофильного присоединения). Кислород группы обладает нуклеофильными свойствами.
Характерны реакции окисления и нуклеофильного присоединения
Билет 7
1) Аминокислоты —органические бифункциональные соединения, в состав которых входят карбоксильные группы –СООН и аминогруппы -NH2.
Простейший представитель — аминоуксусная кислота H2N-CH2-COOH (глицин)
Некоторые представители аминокислот:
1) аминоуксусная кислота Н2N-СН2-СООН;
2) аминопропионовая кислота Н2N-СН2-СН2-СООН;
3) аминомасляная кислота Н2N-СН2-СН2-СН2-СООН;
4) аминовалериановая кислота Н2N-(СН2)4-СООН;
5) аминокапроновая кислота Н2N-(СН2)5-СООН.
Чем больше атомов углерода в молекуле аминокислоты, тем больше может существовать изомеров с различным положением аминогруппы по отношению к карбоксильной группе.
6. Чтобы в названии изомеров можно было указывать положение группы – NH2 по отношению к карбоксилу, атомы углерода в молекуле аминокислоты обозначаются последовательно буквами греческого алфавита: а) ?-аминокапроновая кислота; б) ?-аминокапроновая кислота.
Получение
Аминокислоты получают различными методами, нек-рые из них предназначены специально для получения тех или иных А.
Наиболее распространенными общими методами химического синтеза А. являются следующие.
1. Аминирование галоидопроизводных органических кислот. На галоидопроизводное (обычно бромзамещенную кислоту) действуют аммиаком, в результате чего галоид замещается на аминогруппу.
Получение А. из альдегидов путем обработки их аммиаком и цианистым водородом или цианидами. В результате такой обработки получается циангидрин, к-рый далее аминируется, образуя аминонитрил; омыление последнего дает А.
3. Конденсация альдегидов с производными глицина с последующим восстановлением и гидролизом.
Отдельные А. могут быть получены из гидролизатов белков в виде труднорастворимых солей или других производных. Напр., цистин и тирозин легко осаждаются в изо электрической точке; диаминокислоты осаждают в виде солей фосфорно-вольфрамовой, пикриновой (лизин), флавпановой (аргинин) и других кислот; дикарбоновые А.
осаждают в виде кальциевых или бариевых солей, глутаминовая к-та выделяется в виде гидрохлорида в кислой среде, аспарагиновая к-та — в виде медной соли и т. д. Для препаративного выделения ряда А. из гидролизатов белка применяют также методы хроматографии и электрофореза.
Для промышленных целей многие А. получают методами микробиологического синтеза, выделяя их из культуральной среды определенных штаммов бактерий.
Свойства аминокислот
Для любого спортсмена важны не только тренировки, но и теоретическая подкованность, благодаря которой можно получать высокие результаты тренировок.
Для этого стоит знать свойства аминокислот, ведь этот вид спортивного питания является одним из наиболее востребованных.
Источник