Синтез метилоранжа (гелиантина)
Уравнения основных реакций:
Реактивы.
Основные.
| Сульфаниловая кислота (кристаллогидрат) | 4,3 г |
| Азотистокислый натрий | 2,1 г |
| Диметиланилин | 3,2 г |
Вспомогательные
| Едкий натр, 2н раствор | 12,5 см 3 |
| Соляная кислота, 2н раствор | 12,5 см 3 |
| Соляная кислота, 1н раствор | 25 см 3 |
| Лед |
Посуда и приборы
| Стаканы химические (50, 100 и 500 см 3 ) | 3 шт. |
| Установка для вакуум-фильтрования | 1 шт. |
| Стеклянная палочка | 1 шт. |
Выполнение синтеза
В стакане емкостью 100 см 3 растворяют при легком нагревании 4,3 г кристаллической сульфаниловой кислоты в 12,5 см 3 2н раствора едкого натра. (Поскольку сульфаниловая кислота плохо растворима в воде, ее переводят в растворимую натриевую соль). После растворения всей кислоты жидкость должна иметь щелочную реакцию (по лакмусу). Полученный раствор охлаждают водой, добавляют 2,1 г натрия азотистокислого в 25 см 3 воды и перемешивают до полного его растворения. Далее раствор охлаждают льдом и приливают его при помешивании в стакан емкостью 500 см 3 , содержащий 12,5 см 3 2н раствора соляной кислоты. Через несколько минут выделяется белый порошкообразный осадок соли диазония в виде биполярного иона:
Полученный продукт не отделяют, а используют в виде взвеси. Он более устойчив, чем другие соли диазония, и может храниться несколько часов.
В маленьком стаканчике растворяют 3,2 см 3 свежеперегнанного диметиланилина в 25 см 3 1н раствора соляной кислоты. Необходимо следить, чтобы весь диметиланилин растворился, о чем свидетельствует отсутствие масляного слоя над раствором. Полученный раствор приливают к взвеси диазотированной сульфаниловой кислоты, находящейся в стакане емкостью 500 см 3 , и хорошо перемешивают. Через 5-10 минут образуется густая паста красной модификации красителя, устойчивой в кислоте. Для превращения красителя в натриевую соль к пасте добавляют 2н раствор едкого натра до резко щелочной реакции, хорошо перемешивают и нагревают до кипения; при этом большая часть красителя переходит в раствор.
Смесь охлаждают в ледяной воде, выделившиеся оранжевые кристаллы натриевой соли красителя отфильтровывают на установке для вакуум-фильтрования (Приложение В, рис. 4).
Продукт может быть сразу перекристаллизован из небольшого количества воды.
Можно убедиться в индикаторных свойствах метилоранжа. В щелочной среде гелиантин имеет желтый, в нейтральной — оранжевый, в кислой — красный цвет. Он изменяет цвет при рН = 3,2-4,4, вследствие превращения одной хромофорной группы в другую.
Красный гелиантин имеет хиноидную группировку:

при прибавлении к нему щелочи образуется желтый гелиантин с азогруппой:
G Техника безопасности.В синтезе красителя используют достаточно концентрированные растворы едкого натра, которые при попадании на кожу или слизистые оболочки могут вызвать сильное раздражение и даже химические ожоги. В этом случае места поражения следует промыть обильно струей воды, затем 1%-ным раствором уксусной кислоты (находится в уголке по технике безопасности) и опять обильно водой. Сульфаниловая кислота и диметиланилин также могут вызвать раздражение кожи при небрежном с ними обращении.
Жиры.
Липиды, их типы и основы номенклатуры. Воски, жиры и масла. Типы жиров в зависимости от происхождения, температуры плавления (консистенции), высыхаемости. Номенклатура глицеридов. Основные физико-химические характеристики: число омыления, эфирное, кислотное и иодное числа. Омыление, переэтерификация, переацилирование и гидрогенизация жиров. Понятие о прогоркании жиров. Окислительная порча жиров. Саломас, маргарин. Мыла, и их типы и моющая способность. Жесткость воды: типы и способы устранения. Понятие о синтетических моющих средствах.
Получение мыла
Процесс гидролиза жиров в присутствии щелочей называется омылением жиров. Обычные мыла представляют собой в основном смеси натриевых солей пальмитиновой, стеариновой и олеиновой кислот:
Если в качестве жира использовать растительное масло, то образуется глицерин и преимущественно олеиновокислый натрий:
Реактивы.
Основные
| Растительное масло | 30 г |
| Едкий натр, 5н раствор | 30 см 3 |
Вспомогательные.
| Натрий хлорид | 10 г |
Посуда и приборы:
| Чашка фарфоровая | 1 шт. |
| Палочка стеклянная | 1 шт. |
| Стакан химический (500 см 3 ) | 1 шт. |
| Электроплитка | 1 шт. |
| Сетка асбестовая | 1 шт. |
| Бумага фильтровальная |
Выполнение синтеза
В фарфоровой чашке на электроплитке с асбестовой сеткой предварительно нагревают до слабого кипения смесь из 10 см 3 5н раствора едкого натра и 10 см 3 воды, прибавляют 30 г жира (растительного масла) и продолжают нагревать при постоянном перемешивании реакционной смеси стеклянной палочкой.
Через час добавляют еще 10 см 3 раствора щелочи и продолжают все время перемешивать при слабом нагревании. Если при этом вода быстро испаряется, то ее компенсируют прибавлением новой порции так, чтобы постоянно была жидкая фаза.
По истечении второго часа прибавляют последнюю порцию раствора щелочи и добавляют снова 10 см 3 дистиллированной воды. После трех часов непрерывного нагревания к реакционной смеси прибавляют 30-40 см 3 воды и кипятят до образования густой гомогенной массы.
Для выделения мыла в свободном состоянии производят процесс высаливания, который сводится к увеличению концентрации ионов натрия:
Благодаря увеличению концентрации ионов натрия равновесие смещается в сторону образования недиссоциированных молекул мыла, которое выделяется в виде твердой, всплывающей на поверхность массы. Процесс высаливания дает возможность отделить мыло от глицерина, избытка щелочи и воды. С этой целью, в отдельном химическом стакане при нагревании на асбестовой сетке приготавливают раствор 10 г поваренной соли в 100-150 см 3 дистиллированной воды. Раствор доводят до кипения, переносят в него из фарфоровой чашки образовавшуюся однородную массу, энергично перемешивают и оставляют его на ночь.
Затвердевший и отделившийся слой мыла вынимают из стакана, удаляют с поверхности раствор щелочи, ополаскивая водой нижнюю поверхность мыла, помещают его на бумагу и оставляют на открытом воздухе на несколько дней до полного высушивания.
С полученным препаратом проделайте качественные реакции на мыло.
Источник
Метиловый оранжевый
| Метиловый оранжевый | |
 | |
 | |
 | |
| Общие | |
|---|---|
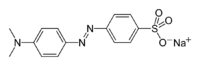
| Систематическое наименование | 4- (4 — диметиламинофенилазо ) бензолсульфонат натрия |
| Традиционные названия | метилоранж |
| Химическая формула | C14H14N3O3SNa |
| Физические свойства | |
| Молярная масса | 327.3359 г/моль |
| Плотность | 1.28 г/см³ |
| Термические свойства | |
| Химические свойства | |
| Растворимость в воде | (при 50°С) 0.2 г/100 мл |
| Растворимость в этанол | нерастворим г/100 мл |
Метиловый оранжевый(метилоранж гелиантин, 4-(4-диметиламинофенилазо)бензолсульфонат натрия) — известный кислотно-основной индикатор. Метилоранж является органическим синтетическим красителем из группы азокрасителей.
Содержание
Свойства
Внешний вид при обычных условиях: оранжево-жёлтые листочки или порошок, чешуйки. Метилоранж растворим в воде 0,2 г. на 100 г., лучше в горячей.
В растворах с рН 2 абсорбирует свет в λmax 505 нм.
Переход окраски в водных растворах от красной к оранжево-жёлтой наблюдается в области рН 3, 1 — 4, 4 (в кислой среде красный, в щелочной — жёлтый).
На интервал перехода окраски влияют: температура, наличие в растворе солей, органических растворителей, белковых веществ и других. Влияние температуры наиболее значительно для индикаторов, являющихся слабыми основаниями: например, для метилового оранжевого при комнатной температуре окраска изменяется в пределах рН 3, 1 — 4, 4, а при 100°С — в пределах рН 2, 5 — 3, 7.
Применение
| Метиловый оранжевый (pH индикатор) | ||
| нижний предел pH 3.1 | верхний предел pH 4.4 | |
| Red | ↔ | Yellow |
Применяется в качестве кислотно-основного индикатора, титранта при определении сильных окислителей, спектрофотометрическом определении окислителей (хрома, брома).
0,1%-ный водный раствор применяется в аналитической химии как индикатор.
Изменяет цвет от красного в кислотной среде (pH 3,1 до 4,4) к оранжевому в нейтральной и жёлтому в щелочной.
Получение
Лабораторный способ синтеза:
Метиловый оранжевый получают, диазотируя сульфаниловую кислоту, а затем сочетая полученное вещество с диметиланилином.
Навеску сульфаниловой кислоты растворяют в 25 мл 2 М раствора едкого натра (2 г NaOH в 25 мл раствора). В этом же растворе затем растворяют навеску нитрита натрия массой 4 г. После этого раствор охлаждают льдом и приливают к 25 мл 2 М раствора соляной кислоты, охлаждаемого льдом (кроме наружного охлаждения кусочки льда могут быть помещены в раствор). Навеску диметиланилина растворяют в 5 мл 1 М соляной кислоты, охлаждают льдом и к охлажденному раствору приливают полученный выше раствор диазобензолсульфокислоты. Происходит образование красителя. Приливают еще раствор едкого натра до сильнощелочной реакции. Из раствора выделяется натриевая соль красителя в виде оранжево-коричневых лепесткообразных кристаллов. Через несколько часов краситель отфильтровывают с отсасыванием и промывают на воронке 25 мл воды. Затем его тщательно отжимают на фильтровальной бумаге и сушат в фарфоровой чашке на водяной бане.
Мнемоническое правило
Для запоминания цвета индикатора метилового оранжевого в щелочах и кислотах служит мнемоническое стихотворение:
От щелочи я желт как в лихорадке,
Я розовею от кислот, как от стыда.
И я бросаюсь в воду без оглядки,
Здесь я оранжевый практически всегда.
Примечания
Ссылки
Wikimedia Foundation . 2010 .
Полезное
Смотреть что такое «Метиловый оранжевый» в других словарях:
метиловый оранжевый — (метилоранж, гелиантин), азокраситель. Водный раствор применяется в аналитической химии как индикатор кислотно основного титрования (переход окраски при рН = 3,1 4,4 от красной до оранжево жёлтой). * * * МЕТИЛОВЫЙ ОРАНЖЕВЫЙ МЕТИЛОВЫЙ ОРАНЖЕВЫЙ… … Энциклопедический словарь
метиловый оранжевый — metiloranžinis statusas T sritis chemija apibrėžtis Indikatorius. formulė (CH₃)₂NC₆H₄N=NC₆H₄SO₃Na atitikmenys: angl. helianthin; methyl orange rus. гелиантин; метиловый оранжевый ryšiai: sinonimas – heliantinas sinonimas – natrio 4 [4… … Chemijos terminų aiškinamasis žodynas
Метиловый оранжевый — 24. Метиловый оранжевый 4 Диметиламиноазобензол 4¢ сульфокислоты натриевая соль C14H14O3N3SNa Источник: ГОСТ 4919.1 77: Реактивы и особо чистые вещества. Методы приготовления растворов индикаторов … Словарь-справочник терминов нормативно-технической документации
Метиловый оранжевый — метилоранж, гелиантин (n диметиламиноазобензолсульфонат натрия), органический синтетический краситель группы азокрасителей (См. Азокрасители). Применяют как кислотно основной индикатор при титровании растворами сильных кислот, а также для … Большая советская энциклопедия
МЕТИЛОВЫЙ ОРАНЖЕВЫЙ — (метилоранж, гелиантин), краситель. Вод. р р применяется в аналитич. химии как индикатор кислотно основного титрования (переход окраски при рН = 3,1 4,4 от красной до оранжево жёлтой) … Естествознание. Энциклопедический словарь
метиловый оранжевый — метилоранж, гелиантин … Cловарь химических синонимов I
МЕТИЛОВЫЙ ОРАНЖЕВЫЙ Водный — МЕТИЛОВЫЙ ОРАНЖЕВЫЙ (метилоранж гелиантин), азокраситель. Водный раствор применяется в аналитической химии как индикатор кислотно основного титрования (переход окраски при pH = 3,1 4,4 от красной до оранжево желтой) … Большой Энциклопедический словарь
метилоранж — метиловый оранжевый, гелиантин … Cловарь химических синонимов I
Реактивы и растворы — 5.2 Реактивы и растворы Натрий углекислый по ГОСТ 83. Кремния двуокись по ГОСТ 9428. Кислота азотная по ГОСТ 4461, разбавленная 1:4. Аммоний углекислый по ГОСТ 3770. Метиловый оранжевый индикатор, водный раствор с массовой концентрацией 1 г/дм3.… … Словарь-справочник терминов нормативно-технической документации
ГОСТ 4919.1-77: Реактивы и особо чистые вещества. Методы приготовления растворов индикаторов — Терминология ГОСТ 4919.1 77: Реактивы и особо чистые вещества. Методы приготовления растворов индикаторов оригинал документа: 26. 1 Нафтолфталеин (альфа нафтолфталеин) С28Н18O4 Определения термина из разных документов: Нафтолфталеин 10. 2,4… … Словарь-справочник терминов нормативно-технической документации
Источник













