- Вода в нашей жизни
- 1. Термический способ умягчения воды
- 2. Реагентное умягчение воды.
- 2.1.Известковый метод.
- 2.2.Известково-содовый
- Термическое умягчение воды, эффективен ли метод?
- Термическое умягчение воды – что это такое?
- За счет чего происходит термическое умягчение воды?
- Каким образом осуществляется термический метод умягчения воды?
- Уменьшение жесткости с применением подручных средств
- Каким образом осуществляется термическое умягчение воды в промышленных установках?
- Альтернативные решения
- Выводы и дополнительные рекомендации
Вода в нашей жизни
Продолжение. Начало см. в № 3, 4, 5, 6, 7, 8, 9, 10, 12, 13, 14, 15/2009
§ 12. ЖЕСТКОСТЬ ВОДЫ И СПОСОБЫ Ее УСТРАНЕНИЯ
Цель. Расширить и углубить представления учащихся о реакциях обмена, используя сведения о способах устранения жесткости воды. Воспитывать бережное отношение к водным ресурсам.
Форма занятия. Беседа, рассказ. Демонстрационный эксперимент.
Оборудование и реактивы. Прибор для получения газов, стеклянная трубка, пробирки, пробиркодержатель; известковая вода, растворы хлорида кальция, соляной кислоты, карбоната натрия, кусочки мрамора.
Виды жесткости воды.
Способы устранения жесткости воды.
Понятие о жесткости воды
Абсолютно чистой воды в природе не существует. Она всегда содержит различные примеси как в растворенном, так и во взвешенном состоянии, от их концентрации и природы зависит пригодность воды для бытовых и промышленных нужд. Для питьевой воды установлены строгие стандарты по содержанию элементов, цвету, вкусу и др. Так, рН – показатель кислотности или щелочности среды – может находиться в пределах от 6,5 до 9,5.
Определенные требования предъявляются к воде, используемой в промышленности. Например, она не должна портить продукцию, вызывать коррозию металлических деталей и механизмов, засорять насосы и трубы. В настоящее время все больше предприятий стремятся создать замкнутые циклы (очистка – производство – очистка – производство и т.д.).
Вода, в которой растворены соли кальция и магния, обладает особым свойством – жесткостью. Известно, что она образует плотные слои накипи (в основном карбонат и сульфат кальция и карбонат магния) на стенках паровых котлов, кипятильников, чайников. Солевой нарост имеет плохую теплопроводность, поэтому вызывает местный перегрев стенок котла и коррозию корпуса. Случайное отделение части накипи от раскаленной стенки может вызвать быстрое испарение воды и даже взрыв котла.
В жесткой воде плохо растворяются некоторые пищевые продукты, хуже развариваются овощи, снижается качество приготовленной пищи. При стирке белья в такой воде увеличивается расход моющих средств. На ткани осаждаются кальциево-магниевые соли высших карбоновых кислот, входящих в состав мыла. Ими пропитываются нити, изделия теряют былую мягкость. Поэтому для стирки мылом в жесткой воде требуется предварительное умягчение воды – устранение жесткости. Синтетические моющие средства обеспечивают более эффективный и экономичный процесс стирки даже в морской воде, т.к. они не образуют нерастворимых солей кальция и магния.
Технологи на фармацевтических и пищевых фабриках особенно тщательно контролируют качество воды. При проведении количественных анализов принято выражать жесткость воды в миллимоль эквивалентах ионов кальция и магния, содержащихся в 1 л воды:
1 ммоль экв/л Са 2+ соответствует 20,04 мг/л;
1 ммоль экв/л Mg 2+ соответствует 12,16 мг/л.
В аналитической практике пользуются и другими способами выражения концентрации, например молярной (моль/л). По этому показателю жесткости воды ее подразделяют на три группы:
– мягкая вода, имеющая жесткость до 2 ммоль экв/л;
– среднежесткая – от 2 до 10 ммоль экв/л;
– жесткая – более 10 ммоль экв/л;
(ммоль – миллимоль, тысячная доля моль).
Виды жесткости воды
Разные соли кальция и магния обусловливают разную жесткость воды (см. схему).
Способы устранения жесткости
Во многих сферах деятельности человека нужна вода с определенным содержанием растворенных в ней солей. На водоочистительных предприятиях используют различные методы очистки воды и ее умягчения.
Устранение жесткости, или умягчение, воды заключается в удалении ионов кальция и магния, которое осуществляется тремя методами: термическим, химическим и физико-химическим.
1. Термический метод – кипячение воды.
При кипячении воды происходит разложение гидрокарбонатов кальция и магния с образованием углекислого газа и карбонатов этих металлов, которые выпадают в осадок:
Сa(HCO3)2 


Mg(HCO3)2 


Таким образом, в результате кипячения воды устраняется жесткость, обусловленная присутствием именно гидрокарбонатов. Это так называемая устранимая (временная) жесткость.
Благодаря этому методу мы легко можем приготовить душистый чай или вкусный компот. Витамины и другие полезные соединения мягкой водой лучше извлекаются из натуральных или засушенных фруктов. Многие хозяйки об этом знают и для приготовления компотов, лечебных настоев пользуются предварительно прокипяченной водой, ее аккуратно сливают, не взмучивая карбонатный осадок.
Для некоторых химических целей требуется достаточно полная очистка воды от солей, которые создают жесткость. Для ее устранения используют химические реагенты, такие, как карбонат натрия, гидроксид кальция, ортофосфат натрия.
а) Известково-содовый метод основан на обработке воды гашеной известью, при этом устраняется временная жесткость, а также связываются ионы Fe 2+ .
При добавлении соды происходит устранение постоянной жесткости:
Учащимся предлагается самостоятельно дописать схемы реакций.
Использование соды при стирке позволяет экономить моющие средства, а отсутствие хлопьевидных осадков улучшает качество ручной и машинной стирки, особенно легко удаляются пятна различных видов технических загрязнений.
б) Фосфатный метод базируется на образовании нерастворимых ортофосфатов кальция и магния, выпадающих в осадок:
3CaSO4 + 2Na3PO4 = 3Na2SO4 + Ca3(PO4)2
Реагенты, составляющие основу химического метода умягчения воды, входят в состав средств, предотвращающих образование накипи на стиральных машинах-автоматах. Антинакипины значительно продлевают срок службы дорогостоящей техники, экономят энергию за счет увеличения теплоотдачи нагревательных элементов и улучшают качество стирки, усиливая действие стирального порошка.
Учащимся можно предложить роль экспертов, которые оценивают состав реагентов – антинакипинов, указываемый на упаковках. При внимательном прочтении можно убедиться, что сода, фосфаты и полифосфаты натрия входят в качестве основных реагентов, предотвращающих образование накипи.
3. Физико-химический метод.
Он основан на использовании ионообменных смол – ионитов. Они представляют собой твердые полиэлектролиты, у которых ионы одного знака заряда закреплены на твердой матрице, а противоионы способны переходить в раствор.
Иониты, используемые в ионообменных установках, достаточно компактны и применяются в большинстве современных фильтров для очистки и умягчения воды, ими оснащены, например, пищеблоки морских лайнеров, подводных лодок.
Способность к ионному обмену проявляется у ряда природных алюмосиликатов. Например, при взбалтывании воды с небольшим количеством глины между ними происходит обмен ионами. Данный эффект используется в лечебных целях, глиняные аппликации эффективны в профилактике заболеваний кожи, в ней восстанавливается водно-электролитный баланс.
Широкое применение находят синтетические ионообменники, они включают и полимерные материалы. В зависимости от того, какие ионы переходят в раствор с поверхности, различают катиониты и аниониты.
Катиониты содержат ионы Na + или Н + – это сульфоугли или алюмосиликаты. Аниониты включают подвижные гидроксид-ионы, это так называемые искусственные смолы.
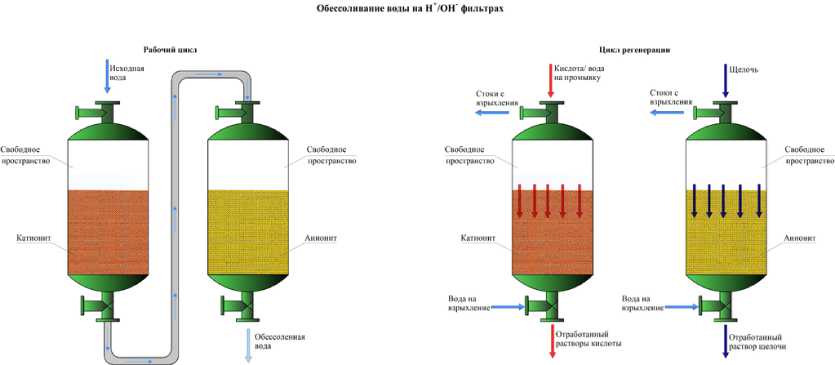
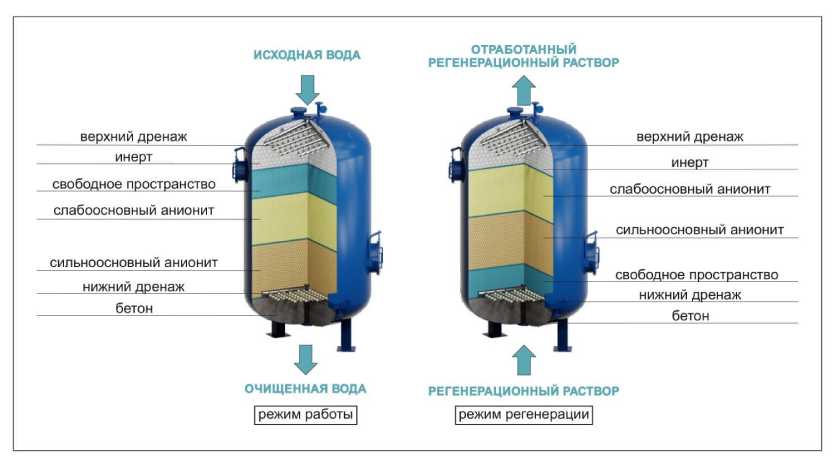
Умягчение воды в промышленных ионообменниках производится фильтрованием через слой катионита толщиной 2–4 м, его поверхность достаточно велика, т.к. полимерная основа состоит из маленьких гранул диаметром 0,5–1,5 мм. В порах этих частичек остаются ионы кальция, вместо них в воду поступают ионы натрия, и вода становится мягкой.
Катионит периодически регенерируют, промывая его концентрированным раствором хлорида натрия, при этом кальций вынужден покидать ранее занятые «позиции» в ионообменнике, его место занимают ионы натрия. Так обновляют адсорбент в фильтре для воды «Гейзер». Для Н + -катионитов промывку ведут раствором соляной кислоты, аниониты регенерируют раствором гидроксида натрия.
Демонстрационный эксперимент заключается в получении жесткой воды (учитель пропускает углекислый газ через раствор известковой воды до растворения получившегося осадка), и устранении ее жесткости при нагревании или добавлении раствора соды. Аналогично демонстрируется устранение постоянной жесткости воды, содержащей растворы хлорида кальция.
Вопросы для беседы и закрепления материала
1. Какими ионами обусловлена жесткость воды и в каких единицах она измеряется?
2. Назовите виды жесткости воды.
3. Почему необходимо устранять жесткость воды?
4. Как влияют соли, придающие воде жесткость, на организм человека?
5. Как понизить жесткость природной воды в быту?
6. Какие способы устранения жесткости воды вы знаете? Подтвердите ответ уравнениями химических реакций.
7. Почему мыло плохо мылится в жесткой воде?
Источник
1. Термический способ умягчения воды
Временная или карбонатная жесткость, устраняется нагреванием воды до 70—80°С и последующей фильтрацией. При нагревании протекают реакции:
Однако полностью устранить карбонатную жёсткость термическим методом нельзя, т. к. СаСО3, хотя и незначительно, но растворим в воде. Растворимость МgСО3 достаточно высока, поэтому гидрокарбонат магния сразу же взаимодействует с водой, т.е. наблюдается процесс гидролиза и вместо МgСО3, в осадок выпадает Mg(ОН)2:
Термическое умягчение воды связано со значительными затратами, поэтому применяется лишь в том случае, когда вода должна подвергаться соответствующему нагреву.
2. Реагентное умягчение воды.
Реагентное умягчение воды состоит в том, что при введении в воду специальных реагентов катионы кальция и магния, растворенные в ней, переходят в практически нерастворимые соединения, которые выпадают в осадок. В зависимости от используемых реагентов методы водоумягчения классифицируют на известковый, известково-содовый, щелочной, фосфатный и бариевый.
2.1.Известковый метод.
Данный метод используют для частичного устранения из воды карбонатной жесткости.
При введении в воду гашёной извести в виде известкового молока гидрокарбонат кальция соли осаждаются в виде карбонатов:
Дальнейшее введение в воду извести приводит к гидролизу магниевых солей и образованию малорастворимого гидроксида магния, который при рН≥ 10,2…10,3 выпадает в осадок:
Известкованием устраняют из воды и некарбонатную магниевую жесткость при условии, что рН воды будет не ниже 10,2 (при других значениях рН воды гидроксид магния не выпадает в осадок):
Приведенные уравнения показывают, что магниевая жесткость устраняется, но значение общей жесткости остается неизменным, так как магниевая жесткость заменяется кальциевой, некарбонатной. Поэтому данный способ можно применять только для умягчения воды с большим значением карбонатной жесткости.
Устранение временной жесткости нейтрализацией гидрокарбонатов гашеной известью применяется крайне редко, т. к. а) мелкодисперсные осадки плохо осаждаются, и требуется укрупнение частиц; б) большое количество мелкодисперсных органических веществ препятствует образованию осадка.
2.2.Известково-содовый
Этот метод используют для одновременного понижения карбонатной и некарбонатной жесткости, когда не требуется глубокого умягчения воды.
Химизм процесса описывается реакциями:
(Уравнения реакций устранения карбонатной жесткости с помощью извести смотри выше в п.2.1.).
После добавления в воду реагентов происходит мгновенное образование коллоидных соединений СаСОз и Mg(OH)2, однако их переход от коллоидного состояния в грубодисперсное, т.е. в то состояние, при котором они выпадают в осадок, занимает длительное время. Поэтому часто известково-содовый способ сочетают с термическим. Например, такое сочетание используют при умягчении воды, которая используется для питания котлов низкого давления, для подпитки теплосети и т.д.
Глубина умягчения воды при известково-содовом методе соответственно равна: без подогрева воды жесткость понижается до 1…2мэкв/л;
при подогреве воды до 80…90 о С жесткость понижается до 0,2…0,4мэкв/л.
Источник
Термическое умягчение воды, эффективен ли метод?
Удаление солей жесткости предотвращает образование накипи. Эту обработку применяют в быту и для решения производственных задач. Термическое умягчение воды подразумевает поддержание определенного температурного режима. Изучение технологического процесса поможет без лишних сопутствующих затрат использовать данный способ на практике.
Термическое умягчение воды – что это такое?
Если отсутствуют вредные для здоровья компоненты, для питья специальная подготовка не требуется. Минералы в концентрации, не превышающей санитарных норм, необходимы организму для формирования костных тканей и естественных обменных процессов. Однако даже минимальное содержание соединений кальция и магния опасно для котлов и другой техники. Образующаяся при нагреве накипь засоряет протоки, нарушает расчетный теплообмен, провоцирует аварийные ситуации.
Удаление солей можно выполнить с помощью термического метода умягчения воды. Также применяют:
- вымораживание;
- дистилляцию;
- ионный обмен;
- обработку реагентами;
- обратный осмос.
Предотвращают образование накипи полифосфатными фильтрами, либо электромагнитным преобразованием. Для повышения эффективности применяют различные комбинации специализированных методов.
Решающее значение для выбора подходящей технологии имеет исходный состав примесей. Для питьевой воды установлена допустимая концентрация солей – 7 мг-экв/литр. Этот уровень ощущается вкусовыми рецепторами по характерному горькому привкусу. В соответствии с особенностями подключаемого оборудования формулируют требования к параметрам на выходе. Для питания промышленных котлов барабанного типа, например, жесткость уменьшают до 0,05 мг-экв/литр.
За счет чего происходит термическое умягчение воды?
Для изучения технологического процесса можно использовать формулы преобразований. Нагревом смещают химическое равновесие, уменьшая растворимость кальциевых соединений. В результате исходные примеси распадаются на чистую воду и углекислый газ. Твердые частицы (карбонаты) формируют накипь на стенках. Если процедура выполняется в проточной емкости – шлам вымывается в дренаж потоком воды.
Формула термического умягчения воды: Ca (HCO3)2 -> CaCO3 + CO2 + H2O. Следует отметить, что часть карбоната кальция способна растворяться в воде.
Аналогичным образом удаляют соединения магния: Mg (HCO3) -> MgCO3 + CO2 + H2O. Надо учитывать хорошую растворяемость MgCO3, которая препятствует завершению преобразования в твердый осадок. Чтобы получить необходимый результат, кипячение продолжают. Такое воздействие трансформирует полученное соединение в гидроксид, который не способен создать концентрацию в смеси более 8,5 мг на литр: MgCO3 + H2O -> MgOH2 + CO2.
Описание поясняет, что это такое «временная жесткость». Специфическим термином обозначают наличие примесей, которые можно удалить кипячением. Как правило, учитывают кальциевые и магниевые соединения. Остаток растворенных солей определяет значение постоянной жесткости. Для устранения этих компонентов надо применять иные методы ионного обмена.
Каким образом осуществляется термический метод умягчения воды?
Чтобы создать благоприятные условия для формирования осадка, повышают температуру. Необходимые реакции заметно ускоряются от +60°С. Кипячение улучшает эффективность процесса. Обработка в таком режиме увеличивает площадь контакта с воздухом, а термический метод умягчения воды ускоряет удаление образующегося углекислого газа.
Уменьшение жесткости с применением подручных средств
Выяснив, за счет чего происходит термическое умягчение воды, не сложно подобрать без ошибок функциональные компоненты технологической установки. Чтобы углекислый газ беспрепятственно выходил из рабочей зоны, оставляют щель или применяют крышку с регулятором отверстия в рукоятке. Если оставить емкость открытой, вода будет слишком быстро испаряться. В этом случае увеличатся энергетическое затраты, повысится уровень влажности в помещении. В меньшем количестве оставшейся жидкости увеличиться общая концентрация солевых примесей, что ухудшит органолептические параметры.
Эксперты рекомендуют не применять термическое умягчение при жесткости менее 3-4 мг-экв/ литр. При таком содержании примесей формирование осадка происходит очень медленно при одновременном испарении большого количества воды.
Следующий важный параметр – общая площадь контакта стенок и донной части с водой. На соответствующих поверхностях осаждается накипь. В крупной посуде умягчение происходит быстрее.
Сложно определить точную длительность процесса. На этот параметр оказывает влияние комплекс исходных условий:
- содержание кальция, углекислого газа, других примесей;
- температурный режим;
- форма посуды;
- размеры выходного отверстия.
Для приблизительных расчетов можно использовать интервал кипячения 4-5 минут при жесткости 6-8 мг-экв/литр.
Пользователи рекомендуют применять экспериментальный способ уточнения вкусовых параметров:
- последовательно кипятят 3-4 порции воды в одинаковой посуде;
- используют разные временные интервалы;
- пробы разливают в герметичную тару, охлаждают до комнатной температуры;
- выполняют сравнение с исходным образцом (без высокотемпературной обработки).
Дегустацию рекомендуется повторить 2-3 раза для определения мелких оттенков органолептических ощущений. Результаты оценивают в баллах. Содержание солей можно выяснить с применением специализированного прибора. Электронный TDS-метр показывает общую концентрацию соответствующих примесей. Эксперты советуют приобретать модели с встроенной температурной компенсацией, которые обеспечивают высокую точность измерений.
Для увеличения эффективной площади размещают на дне емкости гальку, осколки фаянса, иные химически нейтральные материалы. Применяют пропорцию 250г засыпки на литр воды. После кипячения по этой методике отстаивают воду 4-5 минут для осаждения нерастворимых частиц.
Каким образом осуществляется термическое умягчение воды в промышленных установках?
Для обработки больших объемов жидкости применяют термическое умягчение воды и непрерывные технологические операции. В крупной промышленной колонне устанавливают распределяющее устройство, которое обеспечивает равномерное распределение жидкости в рабочем объеме. Специальным подогревателем увеличивают температуру. Образованный шлам извлекают через патрубок в нижней части. Закрепление накипи на функциональных частях предотвращают технологической продувкой.
Альтернативные решения
Представленное выше описание объясняет, какой метод умягчения воды называют термическим. Но для удаления солей жесткости можно применить другие технологии. Следующая таблица поможет сделать общий сравнительный анализ:
Общие параметры рабочего процесса
В жидкость добавляют известь либо другие химические соединения.
Гранулированный наполнитель накапливает соединения жесткости, насыщает жидкость солями натрия.
Рулонная преграда с микроскопическими отверстиями пропускает воду, но задерживает вредные примеси.
Типичное целевое назначение
Сравнительно слабое умягчение, удаление взвесей.
Снижение уровня жесткости до безопасного уровня.
Качественное удаление примесей с эффективностью фильтрации до 99%.
Технологический расход воды в %
Максимальная исходная (остаточная) жесткость в мг-экв/литр
8-10 (0,01 и менее)
Допустимая температура, °C
Каждый реагентный метод умягчения воды отличается характерными преимуществами и недостатками. Для корректной оценки надо проверять оснащение определенного объекта недвижимости. Следующие выводы относятся к воспроизведению технологического процесса в домашних условиях.
Выяснив, какой метод умягчения воды называют термическим, не сложно сделать заключение о следующих минусах:
- продолжительное время обработки;
- существенная зависимость от настроек рабочих режимов;
- загрязнение атмосферы помещения паром;
- необходимость регулярной очистки посуды.
Реагентную технологию применяют только для обработки технической жидкости. Для выполнения санитарных требований к питьевой воде нужна специальная подготовка. Качественные дозирующие устройства стоят дорого.
Ионный обмен – стандартное инженерное решение в области бытовой водоподготовки. В торговой сети предлагают широкий ассортимент специализированного оборудования данной категории. Компактные модели «кабинетного» типа приобретают для оснащения квартир. Наборы из двух раздельных емкостей устанавливают в коттеджах. При выборе этой технологии нужно учесть:
- необходимость предварительного удаления песка, хлора, других вредных примесей;
- сложную настройку;
- дополнительные затраты на подводку канализации, других сетей;
- регулярное пополнение запаса таблетированной соли;
- сильный шум в процессе регенерации.
Мембранные технологии обеспечивают высшее качество фильтрации! Но типичная бытовая установка рассчитана на обработку 160-180 литров жидкости за сутки. Этого недостаточно для полноценного водоснабжения. Недостаток устраняют комплектом из нескольких рабочих блоков, установленных параллельно. Насосом повышают давление. Раствором кислоты выполняют периодическую промывку. Для автоматизации рабочих циклов применяют микропроцессорное управление. Производительное хорошо оснащенное оборудование этой категории стоит более 100000 руб., поэтому использование метода сопряжено со значительными финансовыми затратами.
Выводы и дополнительные рекомендации
Термическая обработка подойдет для умягчения нескольких литров воды с применением обычной посуды. Чтобы удалить из жидкости вредные примеси с надежными гарантиями без лишних проблем, пользуются установкой обратного осмоса. Для защиты всего оборудования в квартире (частном доме) от накипи применяют ионный обмен.
Вместо сложного извлечения солей можно блокировать образование накипи. Эту задачу решают с помощью электромагнитного преобразователя АкваЩит. Экономичные модели действуют на расстоянии до 700 м при уровне жесткости 17 мг-экв/л. Мощные модификации обеспечивают защиту на дистанции до 2 км, сохраняют эффективность при концентрации солей кальция и магния до 21 мг-экв/л. Аппараты не надо настраивать. Для монтажа придется потратить не более 10-15 мин. Производитель установил официальную гарантию 7 лет, что косвенно подтверждает надежность и долговечность оборудования.
Источник