Тепловое движение температура способы измерения температуры
Тепловые явления – это явления, связанные с нагреванием или охлаждением тел, а также с изменением их агрегатного состояния.
Все тепловые явления связаны с температурой.
Все тела характеризуются состоянием своего теплового равновесия. Главной характеристикой теплового равновесия является температура.
Температура – это мера «нагретости» тела.
Поскольку температура является физической величиной, то её можно и нужно измерить. Для измерения температуры используется прибор, который называется термометр (от греч. термо – тепло, метрео – измеряю).
Первый термометр (а, точнее, его аналог) изобрёл Галилео Галилей. Изобретение Галилея, которое он представил своим студентам на лекциях в университете в конце XVI века (1597 г.), было названо термоскопом.
Любой термометр основан на следующем принципе: изменение физических свойств веществ в зависимости от температуры.
Опыт Галилея
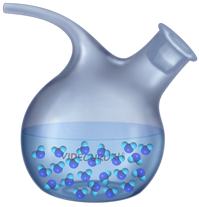
Рис. 1. Опыт Галилея
Опыт Галилея (см. Рис. 1) состоял в следующем: он взял колбу с длинной ножкой и наполнил её водой. Затем взял стакан с водой и перевернул колбу ножкой вниз, поставив в стакан. Часть воды, естественно, вылилась, однако, в результате, в ножке остался определённый уровень воды. Если теперь нагревать колбу (в которой находится воздух), то уровень воды будет опускаться, а если охлаждать, то, наоборот, повышаться. Это связано с тем, что при нагревании вещества (в частности, воздух) имеют свойство расширяться, а при охлаждении – наоборот, сужаться (именно поэтому рельсы делают несплошными, а провода между столбами иногда немного провисают).
Эта идея и легла в основу первого термоскопа, который позволял оценивать изменение температуры (точно измерить температуру таким термоскопом нельзя, так как его показания будут сильно зависеть от атмосферного давления).
В это же время была введена так называемая градусная шкала. Само слово «градус» в переводе с латинского означает «ступень».
На сегодняшний день сохранились три основные шкалы.
1. Шкала Цельсия
Наибольшее распространение получение шкала, которая с детства известна каждому – шкала Цельсия.
Андерс Цельсий – шведский астроном, который предложил следующую шкалу температур: 0 о С – температура кипения воды; 100 о С – температура замерзания воды. В настоящее время все мы привыкли к перевёрнутой шкале Цельсия.
Примечание: сам Цельсий говорил, что такой выбор шкалы вызван простым фактом: зато зимой не будет отрицательной температуры.
2. Шкала Фаренгейта
В Англии, США, Франции, Латинской Америке и некоторых других странах популярностью пользуется шкала Фаренгейта.
Габриель Фаренгейт – немецкий исследователь – инженер, который впервые применил свою собственную шкалу для изготовления стекла. Шкала Фаренгейта более тонкая: по размерности градус шкалы Фаренгейта меньше градуса шкалы по Цельсию.
3. Шкала Реомюра
Техническая шкала придумана французским исследователем Р. А. Реомюром. По этой шкале 0 соответствует температуре замерзания воды, а вот в качестве температуры кипения воды Реомюром была выбрана температура в 80 градусов.
В физике, в основном, используется так называемая абсолютная шкала – шкала Кельвина. 1 градус по Цельсию равен 1 градусу по Кельвину, однако температура в 0 о С соответствует приблизительно 273 К .
Кем и
когда
введена.
А. Цельсия
шведский
астроном, физик
1742 г.
Фаренгейт
стеклодув из Голландии
1724 г.
Реомюр французский физик
1726 г.
Томсон
(лорд Кельвин)
английский физик
1848 г.
Наличие положительных и отрицательных температур
0 о C
– температура таяния льда,
100 о C
– температура кипения воды.
32F
– температура таяния льда,
212F
– температура кипения воды.
0R
– температура таяния
льда,
80R
– температура кипения воды.
0K – абсолютный нуль,
273К
– температура таяния льда
Т = t + 273
Самая высокая температура.
Она получена в центре взрыва термоядерной бомбы – около 300. 400 млн °C. Максимальная температура, достигнутая в ходе управляемой термоядерной реакции на испытательной термоядерной установке ТОКАМАК в Принстонской лаборатории физики плазмы, США, в июне 1986г., составляет 200 млн °C.
Самая низкая температура.
Абсолютный нуль по шкале Кельвина (0 K) соответствует –273,15°С или –459,67° F . Самая низкая температура, 2·10 –9 K выше абсолютного нуля, была достигнута в двухступенчатом криостате ядерного размагничивания в Лаборатории низких температур Хельсинкского технологического университета, Финляндия, группой учёных под руководством профессора Олли Лоунасмаа (род. в 1930 г.), о чём было объявлено в октябре 1989 г.
Напомним, что при изменении температуры тела изменяются его линейные размеры (при нагревании – расширяются, при охлаждении – сужаются). Это связано с поведением молекул. При нагревании увеличивается скорость движения частиц, соответственно, они начинают чаще взаимодействовать, и объём увеличивается.
Из этого можно сделать вывод, что температура связана с движением частиц, из которых состоят тела (это относится и к твёрдым, и к жидким, и к газообразным телам).
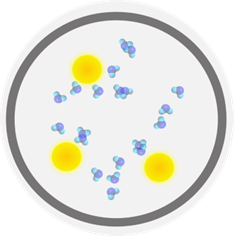
Движение частиц в газах является беспорядочным (так как молекулы и атомы в газах практически не взаимодействуют).
Движение частиц в жидкостях является «скачкообразным», то есть: молекулы ведут «осёдлый образ жизни», но способны «перепрыгивать» с одного места на другое. Этим определяется текучесть жидкостей.
Движение частиц в твёрдых телах называется колебательным.
Таким образом, все частицы находятся в непрерывном движении. Это движение частиц называется тепловым движением (беспорядочное, хаотическое движение).
Это движение никогда не останавливается (до тех пор, пока у тела есть температура).
Подтвердил наличие теплового движения в 1827 году английский ботаник Роберт Броун, по имени которого данное движение называют броуновским движением.
На сегодняшний день известно, что самая низкая температура, которая может быть достигнута, составляет приблизительно -273 о С . Именно при такой температуре замирает движение частиц (однако не замирает движение внутри самих частиц).
Рассмотрим в заключении ещё один опыт – опыт французского учёного Гильома Амонтона, который в 1702 году изобрёл так называемый газовый термометр. С небольшими изменениями этот термометр дошёл и до наших дней.
Опыт Амонтона
Рис. 2. Опыт Амонтона
Возьмём колбу с водой и заткнём её пробкой с тонкой трубкой (см. Рис. 2). Если теперь нагревать воду, то за счёт расширения воды, её уровень в трубке будет повышаться. По уровню поднятия воды в трубке можно сделать вывод об изменении температуры. Преимущество термометра Амонтона состоит в том, что он не зависит от атмосферного давления.
На этом уроке мы рассмотрели такую важную физическую величину, как температура. Изучили способы её измерения, характеристики и свойства. На дальнейших уроках мы изучим такое понятие, как внутренняя энергия.
Источник
Тепловое движение. Температура
Урок 1. Физика 8 класс (ФГОС)
В данный момент вы не можете посмотреть или раздать видеоурок ученикам
Чтобы получить доступ к этому и другим видеоурокам комплекта, вам нужно добавить его в личный кабинет, приобрев в каталоге.
Получите невероятные возможности
Конспект урока «Тепловое движение. Температура»
Из химии и физики 7 класса вы знаете, что все вещества имеют дискретное строение. Иными словами, они состоят из мельчайших частиц — атомов и молекул, между которыми существуют промежутки.
Размеры атомов и молекул настолько малы, что увидеть их без сильных электронных микроскопов не удаётся. Но большое количество разнообразных наблюдаемых явлений подтверждают дискретность веществ. Среди них и хорошо знакомое вам явление диффузии — самопроизвольное проникновение одного вещества в другое.
Диффузия в жидкости
Однако самым убедительным доказательством дискретного строения вещества является броуновское движение. Давайте посмотрим, в чем его суть.
Броуновское движение — это беспорядочное движение малых частиц вещества, взвешенных в жидкости или газе.
Взвешенными называются частицы, плотность вещества которых сравнима с плотностью среды, в которой они находятся. При этом размеры этих частиц в тысячу с лишним раз превышают размеры молекул.
Впервые такое движение наблюдал английский ботаник Р. Броун в 1827 г. Он рассматривал движение частиц цветочной пыльцы в воде под микроскопом. Каждая частица пыльцы совершала причудливое зигзагообразное движение.
Постепенно становилось понятным, что мельчайшие частички вещества испытывают со всех сторон удары ещё более мелких частиц, которые в микроскоп уже не видны.
Открытое Р. Броуном движение неоспоримо доказало факт того, что все вещества состоят из атомов и молекул. И самое главное, что эти мельчайшие частицы вещества находятся в непрерывном беспорядочном движении, интенсивность которого зависит от температуры вещества. Чем выше температура, тем быстрее двигаются молекулы вещества, и наоборот. Именно поэтому броуновское движение ещё называют тепловым движением.
А что такое температура?
Многие из вас наверняка приведут примеры того, что температура горячей воды больше чем холодной. А кто-то скажет, что температура на улице зимой ниже, чем летом.
Стакан с холодной и горячей водой
Температура — это физическая величина, которая характеризует тепловое состояние тела (степень его «нагретости»).
Однако наши с вами ощущения неоднозначны и зависят от состояния человека и окружающей среды. Так, например, в одной и той же комнате металлические предметы всегда кажутся более холодными, чем деревянные или пластмассовые.
Или вот ещё один пример — опыт, который вы можете провести в домашних условиях. Погрузим на некоторое время одну руку в горячую воду, а другую — в холодную. Теперь, если мы обе руки поместим в воду при комнатной температуре и попытаемся на основании своих ощущений установить, какая в сосуде вода — холодная или горячая, то, на удивление, у нас ничего не получится, поскольку наши ощущения будут разными: рука, которая находилась в горячей воде, будет чувствовать холод, а рука, находившаяся в холодной воде, будет ощущать тепло.
Поэтому, для того, чтобы сделать те или иные выводы о температуре тела, её необходимо измерить. Для измерения температуры используется специальный измерительный прибор — термометр. Его действие основано на зависимости свойств тела от температуры (расширение тел при нагревании и их сжатие при охлаждении).
Единицей измерения температуры является градус Цельсия.
Эта единица была названа в честь шведского учёного А. Цельсия, предложившего использовать стоградусную шкалу температур. За 0 о С в ней принимается температура тающего льда, а за 100 о С — температура кипения воды при нормальных условиях.
Помимо шкалы Цельсия, существуют и другие температурные шкалы. Например, термометры со шкалой Фаренгейта до сих пор применяют в Англии и Америке. За 0 о в этой шкале была принята температура самой холодной зимы в Голландии в 1709 г., а вторая точка соответствовала нормальной температуре человеческого тела — 98 о F.
Во Франции долгое время использовалась шкала Реомюра, которая в настоящее время вышла из употребления.
В физике, в частности в термодинамике, используется шкала Кельвина. В ней температура отсчитывается от абсолютного нуля — то есть от минимальной теоретически возможной температуры тела. В нашей привычной шкале — шкале Цельсия, эта температура равняется −273,15 о С.
Вы конечно знаете, что при любой температуре вещество, например, вода, состоит из одних и тех же молекул. Иными словами, молекулы холодной воды ничем не отличаются от молекул воды горячей. Но что же тогда меняется в воде при изменении её температуры?
Изменяется скорость движения молекул. Чем быстрее двигаются молекулы в веществе, тем более высокой является температура вещества, и наоборот. Т. е., температура зависит от скорости движения молекул.
Но только ли от скорости молекул зависит температура тела? Например, при средней скорости движения молекул в 440 м/с кислород имеет температуру 20 о С, а азот — 16 о С. Это обусловлено тем, что молекулы азота легче молекул кислорода. Следовательно, температура зависит и от массы молекул.
В 7 классе вы познакомились с величиной, которая также зависела от скорости и массы — это кинетическая энергия.
Поэтому можно утверждать, что температура является мерой средней кинетической энергии молекул тела.
Теперь выясним каковы особенности броуновского движения в различных агрегатных состояниях вещества.
Вы уже знаете, что расстояние между молекулами у газов достаточно большое, и намного больше чем у жидкостей и твёрдых тел. Но силы взаимодействия между молекулами газа ничтожно малы. Поэтому молекула в газе двигается свободно до момента столкновения с другой молекулой. При столкновении молекула меняет направление своего движения и вновь движется свободно до следующего столкновения. Именно поэтому газы не сохраняют своей формы и занимают весь предоставленный им объём.
Расположение молекул в газе
Тепловое движение молекул жидкости другое. Расстояния между молекулами жидкости намного меньше, чем в газах, а сами молекулы связаны друг с другом силами притяжения и отталкивания. Поэтому они совершают беспорядочные колебания и вращения в одном положении, а также могут перемещаться относительно друг друга.
Расположение молекул в газе
Наличие сил притяжения между молекулами обеспечивает жидкости сохранение объёма, а перемещения — текучесть. Поэтому жидкость и сохраняет свой объем, но не сохраняет форму, а принимает форму того сосуда, в котором она находится.
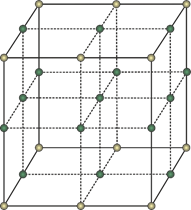
В твёрдых телах частицы связаны между собой сильнее, чем в жидкостях. Поэтому их тепловое движение главным образом сводится к хаотичному колебанию около своего положения равновесия.
Расположение молекул в газе
Сильное взаимодействие в твёрдом веществе частиц друг с другом, и отсутствие у них подвижности, приводит к тому, что твёрдые тела сохраняют свою форму и объём.
Источник