Перенос электронов и окислительное фосфорилирование



Баланс одного оборота цикла Кребса
Окисление малата до оксалоацетата
Cукцинат Фумарат Малат Оксалоацетат
Фумараза
Сукцинатдегидрогеназа
Окисление сукцината катализируется сукцинатдегидрогеназой – флавопротеидом, в молекуле которого с белком ковалентно связан флавинадениндинуклеотид. Этот способный восстанавливаться кофермент действует как акцептор водорода:
Сукцинат + Е–ФАД ↔ Фумарат + Е–ФАДН2
Сукцинатдегидрогеназа прочно связана с мембраной митохондрий, имеет сложную структуру и состоит из нескольких субъединиц. Сукцинатдегидрогеназа обладает некоторыми свойствами аллостерического фермента.
Обратимая реакция фумарата, продуктом которой является малат, катализируется ферментом фумаразой.
Фумарат + Н2О ↔ Малат
Изменение свободной стандартной энергии невелико, поэтому эта реакция является легко обратимой. Молекула состоит из 4 субъединиц. Кофермента для реакции не требуется.
СОО — СОО — СОО — СОО —
| ФАД | Н2О | НАД + |
CH2 ↓ C – H ↓ HO – C – H ↓ C = O
CH2 ↓ Н– C H – C – H ↓ CH2
| ФАДН2| | НАДН|
COO — COO — COO — COO —
В последней реакции цикла Кребса НАД-зависимая малатдегидрогеназа катализирует окисление малата в оксалоацетат:
Малат + НАД + ↔ Оксалоацетат + НАДН + Н +
Хотя реакция носит эндергонический (без выделения энергии) характер, в клетке она идет только в прямом направлении, так как продукты реакции быстро удаляются.
Два атома углерода выводятся из цикла в виде двуокиси углерода, т.е. ровно столько же, сколько поступает в цикл в виде ацетильной группы, однако это не те самые, а другие атомы. В реакциях ферментативного дегидрирования образуется также 4 пары атомов водорода – 3 пары используются для восстановления НАД + , а одна – для восстановления ФАД сукцинатдегидрогеназы. В конечном счете все 4 пары атомов водорода превращаются в ионы Н + и соответствующее число электронов переносится по дыхательной цепи на кислород.
Рассмотрим вопрос о том, каким образом пары электронов, отдаваемые промежуточными продуктами цикла трикарбоновых кислот, переходят через длинную цепь ферментов – переносчиков электронов, опускаясь на все более низкие энергетические уровни до тех пор, пока они не восстановят молекулярный кислород – конечный акцептор электронов в процессе дыхания. Значительная часть свободной энергии электронов запасается при этом в форме энергии фосфатной связи АТФ. Этот процесс называется окислительным фосфорилированием. Процессы переноса электронов и окислительного фосфорилирования происходят почти во всех аэробных клетках. В эукариотических клетках ферменты, катализирующие эти реакции, локализованы во внутренней мембране митохондрий, в прокариотических клетках они локализованы в клеточной мембране.
2.7.6. Путь переноса электронов – дыхательная цепь
Пары водородных атомов, отщепляемые от промежуточных продуктов в реакциях дегидрирования при гликолизе и в цикле Кребса, окисляются молекулярным кислородом до Н2О с одновременным фосфорилированием АДФ до АТФ. Происходит это, когда водород, отделившийся от НАДН или ФАДН2, передается по цепи, включающей по меньшей мере 5 переносчиков – флавопротеид, кофермент Q и несколько разных цитохромов. В конце цепи электроны соединяются с молекулярным кислородом с образованием аниона О 2– . Соединяясь с протонами водорода, эти анионы образуют воду. Промежуточные переносчики водорода претерпевают при этом ряд окислительно-восстановительных реакций. Переносчики сгруппированы таким образом, что в трех пунктах цепи при переходе водородных атомов от одного переносчика к другому, небольшое количество энергии высвобождается и включается в молекулу АТФ.
НАДН + Н + + Е1 – ФАД → НАД + + Е1 – ФАДН2
2E2 – Fe(11) + 2H + + KoQ → 2E2 – Fe(111) + KoQH2
KoQ H2 + 2 Цит.b(111) → KoQ + 2H + + 2 Цит.b(111)
2Цит.b(11) + 2 Цит.с(111) → 2Цит.b(111) + 2Цит.с(11)
2Цит.с(11) + 2 Цит. а (111) → 2Цит.с(111) + 2Цит.а(11)
2Цит.а(11) + 2Цит.а3(111) → 2Цит.а(111) + 2Цит.а3(11)
Считается, что на участке НАДН и КоQ (убихинон — вездесущий хинон) осуществляется двухэлектронный перенос, а на участке между цитохромом b и кислородом – одноэлектронный. Молекулы–переносчики электронов, составляющие цепь переноса электронов, сгруппированы в надмолекулярные структуры – дыхательные ансамбли. Эти дыхательные ансамбли встроены в структуру внутренней митохондриальной мембраны. Переносчики, располагающиеся рядом в цепи переноса, ориентируются, вероятно, таким образом, что их простетические группы могут контактировать друг с другом благодаря определенным колебательным и вращательным движениям.

Процесс переноса электронов через всю дыхательную цепь, от НАДН к молекулярному кислороду, сопровождается очень большим уменьшением свободной энергии, а именно на 52,7 ккал. Для образования АТФ из АДФ и фосфата необходимо только 7,3 ккал. Очевидно, что уменьшение свободной энергии при переносе одной пары электронов от НАДН до кислорода достаточно велико для того, чтобы обеспечить возможность синтеза нескольких молекул АТФ из АДФ и фосфата в стандартных условиях при условии наличия соответствующего механизма сопряжения. Изменение свободной энергии, сопровождающее перенос пары электронов от НАД*Н к кислороду, можно разбить на 3 части, каждая из которых соответствует определенному участку дыхательной цепи и достаточна для того, чтобы обеспечить фосфорилирование АДФ до АТФ в сопряженной реакции. Эти реакции окислительного фосфорилирования сохраняют около 40% энергии.
Идея о наличии сопряжения между фосфорилированием АДФ и аэробным дыханием была впервые высказана в Советском Союзе Энгельгардтом еще в начале 30 годов. В настоящее время общепризнанно, что необходимым условием окислительного фосфорилирования является целостность структуры внутренней мембраны митохондрий.
Суммарное уравнение процесса фосфорилирования в дыхательной цепи:
НАДН + 2Н + + 3 АДФ + Фн + 1/2 О2 → НАД + + 4 Н2О + 3 АТФ
НАДН + 2Н + + 1/2 О2 → НАД + + Н2О DG¢ = – 52,7 ккал
3 АДФ + 3 Фн → 3 АТФ +3 Н2О DG¢ = + 21,9 ккал
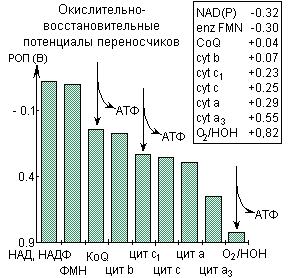
Рис.14. Окислительно-восстановительные потенциалы переносчиков электронов в электрон-транспортной цепи митохондрий и места сопряжения окисления и фосфорилирования
Очевидно, что при сопряженном фосфорилировании, в результате которого образуется 3 молекулы АТФ, запасается 21,9/52,7*100, т.е. около 40% всей энергии, освобождающейся от переноса электронов от НАДН к кислороду. Окисление всех связанных с НАД субстратов, происходящее в митохондриях за счет молекулярного кислорода, сопровождается образованием 3 молекул АТФ. Была установлена также примерная локализация трех участков дыхательной цепи, в которых происходит запасание энергии, основанная на термодинамических расчетах и экспериментальных данных (рис.14): 1) один из флавопротеидов цепи, 2) место, в котором пара электронов переходит от цитохрома b к цитохрому с, 3) место, где пара электронов переходит от цитохрома а к кислороду. Таким образом, дыхательная цепь напоминает каскадное устройство, поставляющее клетке свободную энергию удобными для нее порциями.
Источник
Параграф 21. Цикл трикарбоновых кислот
Автор текста – Анисимова Елена Сергеевна.
Авторские права защищены. Продавать текст нельзя.
Курсив не зубрить.
Замечания можно присылать по почте: exam_bch@mail.ru
https://vk.com/bch_5
Параграф учебника по биохимии 21:
«Цикл трикарбоновых кислот».
См. п.20, 22, файл «21 формулы ЦТК».
Содержание параграфа 21:
21. 1. Цикл трикарбоновых кислот:
реакции,
ферменты и их коферменты,
витамины, необходимые для их работы.
21. 2. Субстратное фосфорилирование в 4-й и 5-й реакции ЦТК.
21. 3. Регуляция ЦТК.
21. 4. Биологические функции цтк.
21. 4. 1. Катаболически-энергетическая функция ЦТК:
21. 4. 2. Анаболическая функция ЦТК.
21. 4. 3. Регуляторная функция ЦТК.
21. 1. ЦИКЛ трикарбоновых кислот:
реакции, ферменты и их коферменты,
витамины, необходимые для их работы.
Необратимые реакции катализируются ключевыми ферментами,
а обратимые реакции – не ключевыми ферментами.
Знать названия ферментов, если они не являются ключевыми или ДГ, не обязательно.
Ключевыми ферментами ЦТК являются все ДГ,
кроме последней –
то есть ИЦДГ, КГДГ, СДГ ключевые, а МДГ – не ключевой.
Еще один ключевой фермент ЦТК – цитрат/синтаза, то есть самый 1 фермент.
Всего ключевых – 4.
Порядок основных метаболитов ЦТК:
ацетилКоА + оксалоацетат ;
цитрат ; изоцитрат ; кетоглутарат ;
сукцинилКоА ; сукцинат ;
фумарат ; малат ; оксалоацетат.
Формулы этих метаболитов нужно знать очень хорошо.
В формуле ацетилКоА 2 С,
в формуле цитрата и (его изомера) изоцитрата по 6 С,
в формуле кетоглутарата 5 С,
а в остальных формулах – по 4 С.
Оксалоацетат – это (почти) сукцинат с кетогруппой (=О),
малат – это сукцинат с гидроксильной группой (ОН),
фумарат – это сукцинат без 2-х атомов водорода и с двойной связью.
1-я реакция ЦТК (необратимая).
Образование цитрата
при взаимодействии ацетилКоА и оксалоацетата.
Схема 1-й реакции ЦТК:
ацетилКоА + оксалоацетат + Н2О ;
цитрат + КоА.
Катализируется ферментом цитрат/синтазой*
(фермент регуляторный = ключевой,
как часто и бывает у первых ферментов метаболических путей – п.7).
Источник энергии для реакции –
расщепление макроэргической связи ацетилКоА.
Нужно знать, но не нужно учить, так как все это легко вычисляется
при сравнении формул субстратов и продуктов:
1) из двух углеродов ацетилКоА
и 4-х углеродов оксалоацетата
образуется шести-углеродный скелет цитрата (2+4=6),
2) второй углерод ацетилКоА
присоединяется ко второму углероду оксалоацетата,
3) в реакцию вступает также молекула воды,
а среди продуктов есть КоА.
2-я реакция ЦТК (обратимая).
Превращение цитрата в изоцитрат (путем изомеризации).
Схема 2-й реакции ЦТК:
цитрат ; изоцитрат.
Сравнение формул цитрата и изоцитрата показывает,
что формула изоцитрата отличается от формулы цитрата
только расположением -ОН группы.
Превращение происходит путем отщепления от цитрата воды
(ОН от 3-го С и Н – от 2-го С)
и последующего присоединения воды обратно,
но при этом ОН присоединяется ко 2-му С, а Н – к 3-му С.
Фермент – цитрат/изомераза (аконитаза).
3-я реакция ЦТК (необратимая).
Превращение изоцитрата в кетоглутарат
путем окислительного декарбоксилирования
под действием фермента изоцитрат/ДГ* (ключевой фермент).
Схема 3-й реакции ЦТК:
изоцитрат + НАД+ ;
кетоглутарат + СО2 + НАДН и Н+.
Сравнение формул изоцитрата и кетоглутарата показывает,
что формула кетоглутарата отличается от формулы изоцитрата
отсутствием атомов СОО карбоксильной группы при 3-м атоме С
и пары атомов водорода во втором положении (при С и при О).
Это подсказывает следующее:
происходит отщепление от изоцитрата (от 3-го С)
карбоксильной группы
(в виде СО2 – это декароксилирование)
и отщепление пары атомов водорода (2-х протонов и 2х электронов –
это окисление).
Поэтому процесс называется окислительным декарбоксилированием.
Фермент называется дегидрогеназой
потому, что катализирует дегидрирование –
отщепление атомов водорода.
Отщепленный СО2 в основном попадет в легкие для выдоха – п.122.
Отщепленный водород переносится на кофермент
для переноса в ДЦ и выработки АТФ (2,5 молекул АТФ).
В данном случае водород переносится на кофермент НАД+,
который превращается при этом в НАДН и Н+
(восстановленную форму кофермента).
В этой реакции происходит укорочение углеродного скелета изоцитрата на 1С.
Это один из двух атомов углерода, которые входили в состав ацетилКоА.
В следующей реакции происходит отщепление еще одного атома углерода.
И в итоге оба атома молекулы ацетил КоА превращаются в СО2.
А углеродный скелет из двух атомов углерода молекулы ацетил КлА
распадается на две одноуглеродных молекулы СО2.
Тем самым завершается разрушение углеродных скелетов, начатое ранее – п.20.3.
Для этой реакции нужен витамин РР в составе кофермента НАД.
4-я реакция ЦТК (необратимая).
Превращение кетоглутарата в сукцинилКоА
под действием фермента кетоглутарат/ДГ*
(кетоглутарат/дегидрогеназного комплекса),
путем окислительного декарбоксилирования.
Схема 4-й реакции ЦТК:
кетоглутарат + НАД+ + КоА ;
сукцинилКоА + СО2 + НАДН и Н+.
Сравнение формул кетоглутарата и сукцинилКоА показывает,
что одна из карбоксильных групп кетоглутарата
замещается коферментом А
и что два атома Н
«не вошли в состав» продукта реакции сукцинилКоА,
а это значит, что они отщепились от субстратов.
Отщепленная карбоксильная группа выделяется в виде СО2,
а отщепленные атомы водорода переносятся на кофермент НАД+,
в результате чего он превращается в НАДН
и далее отдаст атомы водорода в ДЦ.
В этой реакции происходит укорочение углеродного скелета кетоглутарата на 1С. Это еще один из двух атомов углерода, которые входили в состав ацетилКоА (укорочение на один атом С происходит и в предыдущей реакции).
Для этой реакции нужен витамин В2 в составе кофермента ФАД.
А также – витамин РР в составе кофермента НАД,
Витамин пантотенат в составе кофермента А и витамин В1.
Точно такой же набор витаминов и коферментов нужен
и для превращения пирувата в ацетилКоА
(для окислительного декарбоксилирования пирувата) – п.32.
При этом роль НАД и КоА ясна уже из схемы реакции,
а про В1 и В2 нужно просто запомнить,
что они нужны в тех же реакциях ЦТК, где участвует КоА.
5-я реакция ЦТК (обратимая).
Превращение сукцинилаКоА в сукцинат
(под действием фермента сукцинилКоА/синТЕтазы).
Схема 5-й реакции ЦТК:
сукцинилКоА + ГДФ + фосфат ;
сукцинат + ГТФ;
Далее:
ГТФ + (АДФ + фосфат) ;
(ГДФ + фосфат) + АТФ.
Из названий субстрата и продукта понятно,
что КоА отщепляется от сукцинила,
сравнение формул сукцинилКоА и сукцината показывает,
что на месте КоА появляются ОН атомы.
При отщеплении КоА происходит разрушение макроэргической связи,
что сопровождается выделением энергии.
За счет этой энергии происходит образование другой макроэргической связи –
связи между ГДФ и фосфатом.
В результате присоединения фосфата к ГДФ образуется ГТФ.
ГТФ может расщепляться на ГДФ и фосфат,
что сопровождается выделением энергии.
За счет этой энергии (которая выделяется при расщеплении ГТФ на ГДФ и фосфат)
может синтезироваться АТФ из АДФ и фосфата.
В результате пятая реакция ЦТК приводит к образованию 1 молекулы АТФ.
При расщеплении сукцинилКоА происходит присоединение воды, но это обычно не отмечают,
так как вода выделяется при образовании ГТФ.
6-я реакция ЦТК (необратимая)
Превращение сукцината в фумарат
под действием фермента сукцинат/дегидрогеназа*.
Схема 6-й реакции ЦТК:
сукцинат + ФАД ;
фумарат + ФАДН2.
Сравнение формул сукцината и фумарата показывает,
что формула фумарата отличается от формулы сукцината
отсутствием двух атомов водорода.
То есть при превращении сукцината в фумарат
происходит отщепление двух атомов водорода – дегидрирование.
Поэтому фермент называется сукцинат/дегидрогеназой*.
Отщепленные от сукцината атомы водорода
присоединяются к коферменту ФАД
(который превращается при этом в ФАДН2),
для передачи атомов водорода в ДЦ и выработки 1,5 АТФ.
Для этой реакции нужен витамин В2 в составе кофермента ФАД.
7-я реакция ЦТК (обратимая):
Превращение фумарата в малат.
Схема 7-й реакции ЦТК:
фумарат + НОН ;
малат.
Сравнение формул фумарата и малата показывает,
что формула малата отличается от формулы фумарата
наличием атомов Н и ОН.
Это подсказывает, что при превращении фумарата в малат
происходит присоединение НОН, то есть гидратация.
Катализируется ферментом гидратазой (фумарат-гидратазой = фумаразой). Название фермента можно не учить.
8-я реакция ЦТК (обратимая):
Превращение малата в оксалоацетат
под действием фермента малат/дегидрогеназа.
Схема 8-й реакции ЦТК:
Малат + НАД+ ;
оксалоацетат + НАДН и Н+.
Сравнение формул малата и оксалоацетата показывает,
что формула оксалоацетата отличается от формулы малата
отсутствием двух атомов водорода.
Из этого следует, что при превращении малата в оксалоацетат
происходит отщепление двух атомов водорода – дегидрирование.
Поэтому фермент называется малат/дегидрогеназой.
Отщепленные от малата атомы водорода
присоединяются к коферменту НАД+
для передачи атомов водорода в ДЦ и выработки 2,5 АТФ.
Для этой реакции нужен витамин РР в составе кофермента НАД.
21. 2. Субстратное фосфорилирование в 4-й и 5-й реакции ЦТК.
См.п.23.
В этом примере происходит синтез ГТФ (а в итоге и АТФ)
способом, который называется субстратным фосфорилированием (СФ).
Имеется в виду фосфорилирование ГДФ
(то есть присоединение фосфата к ГДФ)
за счет энергии, которая выделяется
при расщеплении макроэргической связи сукцинилКоА
(который называется первичным макроэргом).
Макроэргическая связь сукцинилКоА
образована за счет энергии,
которая выделилась при окислении кетоглутарата;
кетоглутарат называют субстратом
в этом примере субстратного фосфорилирования.
ГТФ и АТФ называют вторичными макроэргами.
Другие примеры (два) субстратного фосфорилирования встречаются в гликолизе.
Кроме субстратного фосфорилирования,
есть окислительное фосфорилирование (ОФ).
При окислительном фосфорилировании
синтез АТФ происходит за счет энергии,
которая выделяется при работе ДЦ.
Поэтому ОФ может происходить только при наличии кислорода, то есть в аэробных условиях.
Субстратное фосфорилирование не требует наличия кислорода,
то есть может происходить в анаэробных условиях.
Но что касается СФ в ЦТК,
то это СФ не происходит в анаэробных условиях,
потому что в анаэробных условиях не работает ЦТК.
ЦТК не работает в анаэробных условиях потому,
что без кислорода не работает ДЦ.
Без работы ДЦ, освобождающей коферменты НАДН и ФАДН2
от переносимых ими атомов водорода,
эти коферменты не могут передавать водород в ДЦ,
молекулы этих коферментов находятся в восстановленном состоянии
(то есть нагружены переносимыми ими атомами водорода),
а для работы ЦТК нужны окисленные коферменты.
21. 3. Регуляция ЦТК. См. таблицы в п.22.
1). Регуляция работы ЦТК осуществляется путем регуляции активности ключевых ферментов:
ЦТК – цитрат/синтазы, ИЦДГ, КГДГ, СДГ.
Ускорение активности ферментов приводит к ускорению реакций и наоборот.
Увеличивают активность ЦТК:
— гормоны
— — катехоламины (адреналин и норадреналин)
— и глюкагон,
— — вторые посредники (п.92) цАМФ и ионы кальция
— и метаболиты АДФ, НАД+.
Инсулин поддерживает ЦТК (п.102).
Уменьшают активность ЦТК:
метаболиты АТФ, НАДН,
главные продукты ЦТК –
это аллостеричекое ингибирование (п.6)
по принципу отрицательной обратной связи.
Значение регуляции ЦТК –
приспособление работы ЦТК к потребностям организма.
Например, адреналин и норадреналин (катехоламины) –
это гормоны стресса,
при котором увеличивается потребность в выработке АТФ
(так как увеличиваются затраты АТФ).
ЦТК необходим для выработки АТФ
(так как ЦТК поставляет для ДЦ восстановленные коферменты),
поэтому катехоламины увеличивают активность ЦТК.
цАМФ и ионы кальция (п.95)
участвуют в передаче сигнала катехоламинов и глюкагона в клетку
(эти гормоны связываются со своими рецепторами на поверхности клетки).
НАДН и АТФ снижают активность ЦТК потому,
что при наличии этих веществ в клетке в достаточных количествах
необходимость в работе ЦТК снижается,
так как эти вещества образуются за счет работы ЦТК,
то есть эти вещества являются продуктами ЦТК.
Если НАДН в клетке достаточно,
то ДЦ получит достаточно водорода
и сможет работать достаточно активно для того, чтобы был синтезирован АТФ.
НАД+ и АДФ повышают активность ЦТК,
когда их много в клетке.
Потому что накопление в клетке АДФ
означает дефицит в клетке АТФ
(АДФ образуется при расходе, использовании АТФ).
Накопление в клетке НАД+ означает, что НАДН в клетке мало,
ДЦ не получает достаточного количества водорода
и не может работать достаточно активно для того, чтобы был синтезирован АТФ.
И ингибиторы ЦТК (АТФ и НАДН),
и активаторы ЦТК (НАД+ и АДФ) являются (по механизму)
аллостерическими регуляторами ЦТК.
21. 4. Биологические ФУНКЦИИ ЦТК.
21. 4. 1. Катаболически-энергетическая функция ЦТК:
21. 4. 2. Анаболическая функция ЦТК.
21. 4. 3. Регуляторная функция ЦТК:
ЦТК необходим для выработки основного количества АТФ
(в большинстве клеток: кроме ЭЦ, в которых нет ЦТК).
Один оборот ЦТК, в котором происходит катаболизм одной молекулы АцетилКоА,
дает 10 молекул АТФ:
1 молекула АТФ образуется путем СФ
при превращении сукцинилКоА в сукцинат (реакции ЦТК 4 и 5).
9 молекул АТФ образуются путем ОФ с помощью ДЦ
1) в ЦТК от метаболитов отщепляются атомы водорода
(дегидрирование метаболитов),
2) атомы Н переносятся на 3 НАД+ и 1 ФАД,
образуя 3 НАДН (Н+) и 1 ФАДН2,
3) которые отдают водород в ДЦ для переноса на О2 и образования НОН.
В ЦТК АцетилКоА превращается в 2 молекулы СО2,
при этом происходит распад углеродного (катаболизм) скелета ацетилКоА:
двух/углеродная молекула ацетилКоА
превращается в две одноуглеродных молекулы СО2.
Поскольку ацетилКоА образуется
при катаболизме углеводов (гликолиз и ПДГ), жиров и белков,
то, превращая ацетилКоА в СО2,
ЦТК завершает катаболизм веществ разных классов.
Эта функция ЦТК, связанная с разрушением ацетилКоА
и выработкой АТФ, называется КАТАБОЛИЧЕСКИ-ЭНЕРГЕТИЧЕСКОЙ.
21. 4. 2. Анаболическая функция ЦТК.
Метаболиты ЦТК могут использоваться
для синтеза ряда веществ, для анаболизма.
Эта функция ЦТК называется анаболической.
Примеры:
1). Из ОА синтезируется ГЛЮКОЗА (в процессе ГНГ, п.33) –
это позволяет жить без пищи более 12 часов.
2). Из ОА и кетоглутарата
синтезируются заменимые аминокислоты
(Асп, АсН, Глу, ГлН, аргинин и др.) для синтеза белков
(Глу является еще нейромедиатором
и субстратом для синтеза другого медиатора – ГАМК). П.67.
3). Из сукцинилКоА
синтезируется порфирин для синтеза ГЕМА
для синтеза гемоглобина, цитохрома и ряда других белков. П.121.
4). П.46 и 48.
Из цитрата образуется ацетилКоА
для синтеза жирных кислот
(для синтеза липидов МЕМБРАН, жира),
кетоновых тел (питание тканей при голоде стрессе и др.)
и холестерина (для мембран, гормонов и др.).
Снижение работы ЦТК
из-за дефицита его витаминов, приема алкоголя (п.26) и т.д.
— приводит к снижению всех перечисленных синтезов,
— к гипогликемии при перерыве в питании или при голоде (риск обморока),
— к снижению деления клеток
(т.к. мало материала для мембран,
особенно при дефиците в питании жиров и белков,
а главное – мало АТФ),
— дистрофии (снижен синтез белка,
особенно при дефиците аминокислот в пище).
21. 4. 3. Регуляторная функция ЦТК:
метаболиты ЦТК регулируют активность других процессов.
Цитрат
ингибирует гликолиз
и активирует синтез жирных кислот.
АцетилКоА
ингибирует ПДГ
и активирует ГНГ (облигатный активатор).
НАДН ингибирует многие катаболические процессы (но не ДЦ).
Не путайте регуляторную роль ЦТК с регуляцией самого ЦТК.
См. таблицу «Регуляторная роль Ц Т К» в отдельном файле.
Источник