Способы выражения состава фаз
Весовой и молярный состав
В технике состав выражают обычно в весовых долях (или весовых процентах), т. е. в виде отношения массы компонента в данной фазе к массе всей фазы. Если масса фазы 




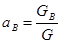

причем 
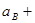


Во многих случаях состав выражают в молярных долях, т. е в виде отношения числа киломолей компонента в данной фазе к общему числу киломолей в этой фазе. Если всего в фазе 
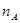





причем 


Пересчет весового состава в молярный, или обратный пере-счет, производится следующим образом. Пусть весовой состав смеси 



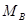
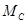
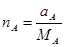
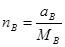

а общее число кмоль составляет:





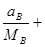
по формуле (16-2) находим молярный состав смеси:



или в общем виде для 
 |
Если задан молярный состав смеси 




и общую ее массу:


По формуле (16-1) находим весовой состав смеси:


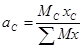
или в общем виде для 
 |
Знаменатель этой формулы, представляющий собой массу 1 кмоль смеси, называется средней молекулярной массой смеси:




Состав смеси двух компонентов (двойные смеси) полностью характеризуется содержанием в ней лишь одного из компонентов. Пусть весовая и молярная доли этого компонента 


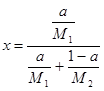

где 

Пример 1-1.Определить молярный состав и среднюю молекулярную массу смеси бензола и толуола, содержащей 30 вес. % бензола.
Р е ш е н и е. Молекулярные массы компонентов: 

Молярная доля толуола (1—х) = 0,664. Эту же величину можно найти и по формуле (1-6), подставляя в нее весовую долю толуола а — 0,7, при этом М\ = 92 и М2 = 78.
Средняя молекулярная масса смеси по формуле (1-5):
Мср. = 78 • 0,336 + 92 • 0,664 = 87,2
Пример 1-2.Определить весовой состав смеси, содержащей 20 мол % этана, 35 мол % пропана, 15 мол. % бутана и 30 мол % изобутана.
Решение. Весовой состав определяем по формуле (1-4) и сводим результаты расчета в табл. 22.
Результаты расчета весового состава смеси
| Компоненты | Молекулярная Масса (Mk) | Молярная Доля (Xk) | м к х к | Весовая доля 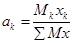 |
| Этан | 0,20 | 6,0 | 0,126 | |
| Пропан | 0,35 | 15,4 | 0,325 | |
| Бутан | 0,15 | 8,7 | 0,183 | |
| Изобутан | 0,30 | 17,4 | 0,366 |
Состав выражают также через массу компонента, содержащегося в 1 м 3 смеси (объемная концентрация). Объемная концентрация С имеет размерность кг/м 3 .
Сумма объемных концентрации всех компанентов ΣС равна массе 1 м 3 смеси, т. е. плотности ρ. Таки образом, весовая доля k-го компанента смеси:
Парциальное давление компанентов газовых смесей
Содержание компонентов газообразной смеси часто выражают через парциальное давление. Под парциальным давлением компанента понимают давление, под которым находился бы данный компанент, если в отсутствие других компанентов он занимал весь объем смеси при ее температуре.
Согласно закону Дальтона, полное давление Р газовой смеси равно сумме парциальных давлений компанентов pА, рВ, рс, …:
Как не трудно убедиться, отношение парциального давления компонента к полном давлению равно объемной доле компонента в смеси. В самом деле, если парциальное давление k-го компонента pk, а объем газовой смеси V, то объем Vk, занимаемый этим компонентом при давлении P, определиться из соотношения pkV=PVk, откуда Vk=рkV/Р, а объемная доля компонента в смеси
Так как 1 кмоль любых компонента занимает при одинаковой температуре один и тот же объем, то объемная доля ϑk равна молярной доле уk компонента в газовой смеси.
Напишем уравнение состояния для 1 кг каждого компонента газовой смеси:
где pk – парциальное давление k-го компонента, н/м 2 ;
R — газовая постоянная (8314 Дж/кмоль · град);
Mk — молекулярная масса компонента.
Отсюда определяем объем V смеси, в котором находится 1 кг k-го компонента:
Объемная концентрация компонента Сk=1/V, или
Уравнение (1-9) устанавливает связь между парциальным давлением и молярной долей, уравнение (1-10) – между парциальным давлением и объемной концентрацией.
Пример 1-3. Смесь двуокиси углерода с воздухом содержит 15 объемн. % СО2. Определить содержание СО2 в смеси в вес. %, парциальное давление СО2 в смеси и объемную концентрацию СО2 при 25°С и общем (абсолютном) далении Р=19,6 бар (20 ат).
Решение. Для газовых смесей объемная доля компонента равна его молярной; следовательно, молярная доля двуокиси углерода у=0,15. Молекулярные массы составляют: М1=44 (для СО2) , М2=29 (для воздуха).
Весовую долю СО2 находим по формуле (1-7).
a=44 · 0,15/ 44 · 0,15 + 29 (1-0,15)=0,212, или 21,2 вес. %
Парциальное давление СО2 определяем по уравнению (1-9)
Р = 19,6 · 0,15 = 2,94 бар (3 ат)
Объемная концентрация СО2 по уравнению (1-10) составит,
С=44 · 2,94 · 10 5 /8314(273+25)=5,23 кг/м 3
Относительный весовой состав
Состав двойной смеси можно выразить в виде отношения массы распределяемого компонента к массе носителя. Это отношение называется относительным весовым составом. Связь между относительным весовым составом Х и весовой долей а выражается следующим соотношением:
Х=а/1-а, или а=Х/1+Х (1-11)
При расчете состава газовой смеси, выраженный через парциальное давление компонента р, часто приходиться пересчитывать в относительно весовой состав. Это может быть сделано следующим образом. Если общее давление смеси Р, то парциальное давление носителя (Р — р); тогда уравнение состояние для компонента будет иметь вид
где V – объем смеси, м 3 ;
GK и GH – количества компонента и носителя в объеме V, кг;
МK и МH – молекулярные массы компонента и носителя.
Деля первое уравнение на второе, получим:
Отсюда находим относительный весовой состав:
Пример 1-4. Найти относительный весовой состав смеси, рассмотренной в примере 1-3.
Решение. По формуле (1-11) находим
Y=0,212/ (1-0,212)=0,27 кг CO2 на 1 кг воздуха
Если весовая доля не рассчитывалась, можно использовать формулу (1-12):
Y=44/29 · 2,94/(19,6-2,94)=0,27 кг СО2 на 1 кг воздуха
Равновесие между фазами
Подобно тому как передача тепла протекает лишь при отклонении от состояния равновесия, т. е. при наличии разности температур между теплоносителями, так и переход вещества из одной фазы в другую происходит при отсутствии равновесия между фазами.
Пусть имеются две фазы 






Скорость обратного перехода будет увеличиваться по мере повышения концентрации распределяемого вещества в фазе 





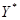






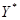


Опора деревянной одностоечной и способы укрепление угловых опор: Опоры ВЛ — конструкции, предназначенные для поддерживания проводов на необходимой высоте над землей, водой.
Организация стока поверхностных вод: Наибольшее количество влаги на земном шаре испаряется с поверхности морей и океанов (88‰).
Папиллярные узоры пальцев рук — маркер спортивных способностей: дерматоглифические признаки формируются на 3-5 месяце беременности, не изменяются в течение жизни.
Источник