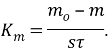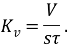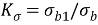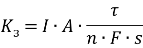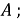Способы выражения скорости коррозии. Способы защиты металлов от коррозии
Лекция 2.
Скорость коррозии может быть выражена в различных единицах.
-по потере металла, отнесенной к единице поверхности и к единице времени, например, г (см 2 . ч) или г (м 2 . год);
-по глубинному показателю, т.е. по уменьшению толщины металла вследствие коррозии, выраженному в линейных единицах и отнесенному к единице времени, например, ммгод;
-по коррозии, связанной с разрушением кристаллической решетки металла, при этом учитывается механически показатель, т.е. относительное изменение прочности металла за определенный период, например, уменьшение временного сопротивления на разрыв, кг(см 2 . год).
Коррозионная стойкость металлов в настоящее время оценивается по десятибалльной шкале с учетом глубинного показателя.
Кроме массовых способов измерения потерь металла нередко используют объемные способы. Это возможно в тех случаях, когда окисление металла сопровождается расходом или выделением газа.
Так, при атмосферной коррозии расходуется кислород, а при кислотной – выделяется водород.
Объем израсходованного кислорода или выделившегося водорода пропорционален массе окислившегося металла.
Измерения объема менее точно, чем взвешивание, но при массовом методе необходимо прервать испытание, удалить продукты коррозии и лишь тогда определять уменьшение массы образца.
За изменением объема газа в некоторой замкнутой системе можно следить не прерывая испытания, что дает более содержательную информацию о кинетике процесса коррозии.
Массовые потери металла (в г) в первом случае определяются по формуле:
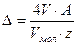
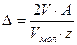
где V, Vмол — объем израсходованного кислорода (объем выделившегося водорода) и их молярные объемы в условиях опыта;
А – атомная масса металла;
z- валентность металла в продуктах коррозии.
Массовый показатель скорости коррозии при этом определяется по формуле:
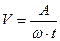
где 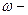
Массовый показатель скорости коррозии 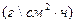
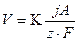
где К- коэффициент, учитывающий в каких единицах выражена плотность тока (если j выражена в Асм 2 , 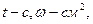
j- плотность тока;
F- константа (число Фарадея).
Применение этих методов оценки массового показателя скорости иногда затруднительно из-за того, что неизвестна валентность (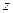
Однако эти методы нашли широкое применение в практике научно- исследовательских работ.
В связис тем, что коррозия — естественный процесс, обусловленный термодинамической нестойкостью металлов в эксплуатационных условиях, срок службы металлических изделий часто бывает относительно коротким. Продлитьего можно в основном четырьмя способами, которые широко используются в практике:
— изоляция поверхности металлических изделий от агрессивной среды;
— воздействие на металл с целью повышения его коррозионной устойчивости;
— воздействие на окружающую среду с целью снижения ее агрессивности;
— поддержание такого энергетического состояния металла, при котором окисление его термодинамически невозможно или сильно заторможено.
Первый способ носит название пассивной защиты. К нему относятся следующие методы:
1. Нанесение на поверхность металла слоя химически инертного относительно металла и агрессивной среды вещества с высокими диэлектрическими свойствами. Этот метод является наиболее распространенным. Он предполагает использование различного рода мастик, красок, лаков, эмалей и пластмасс, жидких в момент нанесения, а затем образующих твердую пленку, которая обладает прочным сцеплением (адгезией) с поверхностью металла. К этому методу следует отнести также и специальные методы укладки, часто используемые для защиты подземных сооружений на территории городов и заводов (например, коллекторная прокладка, при которой подземные трубопроводы располагают в специальных каналах, изолирующим слоем в данном случае является воздушный зазор между стенкой трубопровода и каналом).
2. Обработка изделий специальными окислителями, в результате которой на поверхности металла образуется слой малорастворимых продуктов коррозии. Примером может служить образование нерастворимых фосфатов на поверхности стальных изделий (фосфатирование) или окиси алюминия на изделиях из алюминиевых сплавов.
3. Нанесение на изделия из малостойкого металла тонкого слоя другого металла, обладающего меньшей скоростью коррозии в данной среде (например, оцинкование, хромирование или никелирование стальных изделий).
4. Обработка металлических изделий растворами окислителей (пассиваторов) для перевода поверхностного слоя металла из активного состояния в пассивное, при котором резко уменьшается переход ионов металла в раствор и тем самым снижается интенсивность коррозионного процесса.
Второй способ защиты — введение в металл компонентов, повышающих его коррозионную стойкость в данных условиях, или удаление вредных примесей, ускоряющих коррозию. Он применяется на стадии изготовления металла, а также при термической и механической обработке металлических деталей. Общую теорию коррозионного легирования предложил Н. Д. Томашов. Во многих случаях легирование металла, мало склонного к пассивации, металлом, легко пассивируемым в данной среде, приводит к образованию сплава, обладающего той же (или почти той же) пассивируемостью, что и легирующий металл. Таким путем получены многочисленные коррозионностойкие сплавы, например нержавеющие стали, легированные хромом и никелем.
Третий способ защиты предусматривает дезактивационную обработку агрессивной среды путем введения ингибиторов (замедлителей) коррозии. Действие ингибиторов сводится в основном к адсорбции на поверхности металла молекул или ионов ингибитора, тормозящих коррозию. К этому способу можно отнести и удаление агрессивных компонентов из состава коррозионной среды (деаэрации водных растворов, очистка воздуха от примесей и осушка его).

Обработкой коррозионной среды различными ядохимикатами достигается значительное снижение интенсивности деятельности микроорганизмов, что уменьшает опасность биокоррозии металлов.
При борьбе с подземной коррозией осуществляется обработка агрессивного грунта с целью его гидрофобизации (несмачиваемости водой), нейтрализации и частичной замены на менее агрессивный грунт или специальную засыпку. Последнее мероприятие может быть квалифицировано также как изоляция металла от прямого воздействия среды.
Четвертый способ носит название активной защиты. К нему относятся следующие методы:
1. Постоянная катодная поляризация изделия, эксплуатирующегося в среде с достаточно большой электропроводностью. Такая поляризация, осуществляемая от внешнего источника электрической энергии, носит название катодной защиты. В некоторых случаях катодная поляризация может осуществляться не постоянно, а периодически, что дает ощутимый экономический эффект. При катодной защите изделию сообщается настолько отрицательный электрический потенциал, что окисление металла становится термодинамически невозможным.
2. Катодная поляризация, вызванная электрическим контактом изделия с металлом, обладающим более отрицательным электродным потенциалом, например стального изделия с магниевой отливкой. Более электроотрицательный металл в среде с достаточно высокой электропроводностью подвергается окислению, а следовательно, разрушается. Его следует периодически заменять. Такой металл называется протектором, а метод — протекторной защитой.
К этому методу можно отнести мероприятия по борьбе с блуждающими токами, которые ведутся по двум основным направлениям: предупреждение или уменьшение возможности возникновения блуждающих токов на самом источнике тока и проведение специальных работ на защищаемом подземном сооружении. Мероприятия первого направления — обязательная, но только начальная мера. Независимо от их результатов следует проводить работы по защите самих подземных сооружений, к которым относятся использование высокоизолирующих совершенных покрытий, устройство электрических экранов, установка изолирующих соединений (фланцев) на трубопроводах, укладка трубопроводов в подземных коллекторах и каналах, электродренажная защита, катодная поляризация и др.
3. Анодная поляризация, которая в некоторых случаях способствует поддержанию пассивного состояния металла в средах, не пассивирующих металл и являющихся весьма агрессивными.
К способам защиты от коррозии часто относят использование неметаллических материалов, обладающих высокой химической стойкостью (асбоцемента, бетона, керамики, стекла, пластмассы и т. д.).
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Источник
Лабораторные методы измерения и приборы контроля коррозии
Рубрика: Технические науки
Дата публикации: 07.06.2016 2016-06-07
Статья просмотрена: 3759 раз
Библиографическое описание:
Яхяев, Н. Ш. Лабораторные методы измерения и приборы контроля коррозии / Н. Ш. Яхяев, А. К. Камолов. — Текст : непосредственный // Молодой ученый. — 2016. — № 12 (116). — С. 455-458. — URL: https://moluch.ru/archive/116/29791/ (дата обращения: 20.11.2021).
Для количественного выражения скорости коррозии служат показатели коррозии: массометрический, объёмный механический, токовый и др. Массометрический показатель скорости коррозии — это изменение массы метелла в результате коррозии отнесённое к единице его поверхности, в единицу времени вычисляется по формуле.
Где 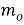
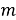
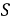
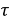
Методы определения скорости коррозии по потерям массы применяют для оценки равномерной. Этими методами невозможно оценивать неравномерную коррозию межкристаллитное и транскристаллитное коррозионные разрушения.
Объёмный показатель коррозии характеризует объем V выделенного или поглощенного в процессии коррозии газа, приведенный к нормальным условиям (T= 273 К, 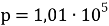
Где -объём поглощенного или выделенного газа, см 2 ; 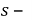
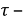
При переходе металла в продукты коррозии и кислых средах выделяется эквивалентное количество водорода. В нейтральных кислородсодержащих средах при образовании продуктов коррозии поглощенного эквивалентное количество кислорода. Объем выделенного водорода или поглощенного кислорода измеряется с помощью эвдиометра.
Глубинный показатель скорости коррозии учитывать уменьшение толщины металла вследствие коррозии, выраженное в линейных единицах и отнесенное к единице времени. Среднее значение глубины коррозионного поражения при равномерной коррозии можно вычислить с помощью массометрического показателя скорости коррозии 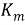
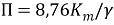
Где 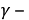
Это показатель удобен для сравнения скорости коррозии металлов с различным плотностями.
Механический показатель коррозии характеризует изменение какого — либо показателя механических свойств металла (%) за определенное время испытаний.
Например показатель изменения предела прочности определяют по формуле
Где 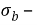
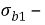
Токовый показатель коррозии позволяет количество прокорродировавщего металла по формуле Фараден, если известна сила коррозионного тока
Где 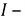
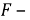
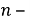
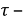
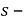
При качественной и количественной оценке коррозионной стойкости металлов рекомендуется пользоваться десятибалльной шкалой (ГОСТ 13819–68) (табл.1)
Десятибалльная шкала коррозионной стойкости металлов (ГОСТ 13819–68)
Группа стойкости
Скорость коррозии металлов, мм/год
Балл
От 0,001 до 0,005
Химический состав и механические свойства некоторых конструкционных материалов. Наибольшие применение для изготовления оборудования нефтяной и газовой промышленности получили стали и чугуны. Среди сталей наиболее часто встречаются углеродистые, низколегированные и нержавеющие.
Конструкционные углеродистые стали делятся на углеродистую сталь обыкновенного качества и сталь качественную.
Сталь углеродистая обыкновенного качества подразделяется в зависимости от назначения и гарантируемых характеристики на три группы: группа А- сталь с гарантируемыми механическими свойствами (применяется для несварных нагруженных элементов конструкций); группа Б- сталь с гарантируемым химическом составе (применяется для сварных элементов неответственных конструкций); группа В-сталь с гарантируемыми механическими свойствами и химическим составом (применяется для сварных элементов ответственных конструкций).
Химический состав углеродистой стали обыкновенного качества
Марки стали
Содержание элементов,%
Углерод
Марганец
Кремний
Лабораторные методы измерений
Лабораторные испытания — это обычно ускоренные испытания, проводимые в определенных, контролируемых условиях, которые могут отличаться от существующих на практике.
Лабораторные коррозионные испытания применяют: при изучении механизма; для оценки стойкости конструкционных материалов и эффективности различных методов защиты от коррозии.
Подготовка образцов. Для гравиметрических коррозионных испытаний размеры образцов ограничивают так, чтобы их можно было взвешивать на аналитических весах. Обычно размеры образцов принимают 40х20х2 или 50х20х2 мм. Для крепления образцов во время испытания в одном из краев пластины сверлят отверстий диаметром 5 мм.
Подготовленные образцы испытывают по методике предусмотренной программой смачивание поверхности образца после погружение его готовить не мене трех образцов. Увеличение число параллельно испытываемых образцов позволяет повысить надежность результатов, особенно в том случае, когда требуется установить относительно небольшое различие в характеристике материала.
Для получения надежной информации об изменении скорости коррозии во времени необходима устанавливать на испытание такое число комплектов образцов, чтобы обеспечивать по крайней мете три периода испытаний.
Удаление продуктов коррозии. Продукты коррозии удаляют после выдержки образцов в растворах, взаимодействующих преимущественно с продуктами коррозии
Визуальное наблюдение коррозионных поражений позволяет фиксировать изменение внешнего вида поверхности металла при этом отмечают время начала появления продуктов коррозии. Их распределение по поверхности металла можно регистрировать последовательным фотографированием.
Для наблюдение распределением катодных и анодных участков по поверхности металла в электролиты вводят специальные реагенты. С помощью K 3 Fe(CN)6 * 2H2O можно фиксировать анодные участки поверхности по синему окрашиванию прилегающего к ним раствора. Фенолфталеин, введенный в раствор, под действием щелочной реакции на катодных металлической поверхности окрашивается в разовый цвет.
Глубину точечного поражения определяют при помощи оптического микроскопа наведением его на резкость сначала по неповрежденной поверхности, а затем по дну питтинга.
Гравиметрический метод — один из наиболее распространенных методов определения скорости коррозии. Самый простой и доступный способ испытания в электролитах — это испытание в открытом сосуде. В лабораторных исследованных обычно используют минимум 150 мл раствора на 1 см 2 поверхности образца.
Подготовленные к испытаниям образцы подвешивают на стеклянных крючках или капроновой нити, опускают в сосуды со средой и испытывают при полном частичном или переменном погружении в неподвижный или перемешиваемый электролит, через который можно пропускать воздух, кислород азот или другой газ.
Рис. 1. Схема коррозионных испытаний образцов в открытом сосуде при полном (а), частичном (б), погружении и неподвижный и перемешиваемый (в) раствор; 1-испытаемый образец; 2-подвеска; 3- стеклянный стакан с коррозионным раствором; 4- мешалка.
Рис. 2. Схема работы потенциостата в режиме поддержания постоянного поляризующего тока: 1-источник задающего напряжения; 2-усилитель; 3- миллиамперметр; 4- катукна; 5- рабочий электролит; 6-вспомогательный электрод; 7- вольтметр; 8- электрохимическая ячейка; 9- электрод сравнения.
- Саакиян Л. С., Ефремон А. П. и др. Зашита нефтепромыслового оборудования от коррозии. М.:- Недра, 1985 г, 206 с.
- Кац Н. Г., Стариков В. П., Парфенов С. Н. Химическое сопротивление Материалов и защита оборудования нефтегазопереработки от коррозии. М.: Машиностроение. -2011 г.
- Жук Н. П. Курс теории коррозии и защита металлов: учеб. Пособие/ Жук Н. П. -2-е изд., стереотипное. Перепечатка издания 1976.-М:. ООО ТИД «Альянс», 2006.-472.
Источник