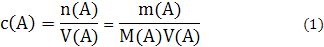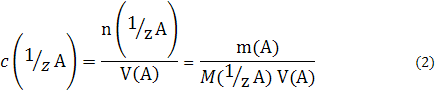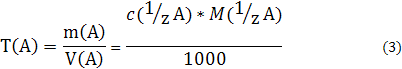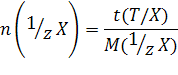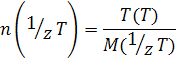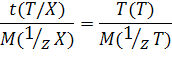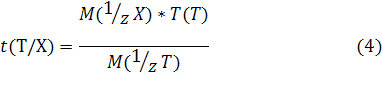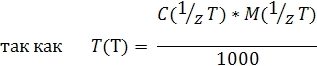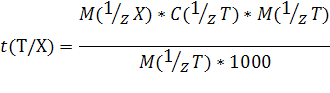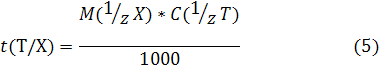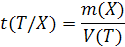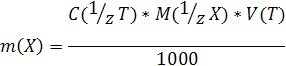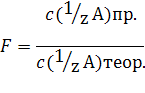Расчёты в титриметрическом анализе
I. Способы выражения концентраций в титриметрическом анализе.
В титриметрическом анализе используют следующие основные способы выражения концентраций растворов.
1) Молярная концентрация c(A)— количество растворенного вещества А в молях, содержащееся в одном литре расвора:
где n(А) — количество растворенного вещества А, моль; V(A) — объем раствора, л; m(A) — масса растворенного вещества А, г; М(А) — молярная масса растворенного вещества А, г/моль. Молярная концентрация измеряется в моль/л.
2) Молярная концентрация эквивалента c( 1 /zA), или нормальность (старое название) — количество растворенного вещества А в молях, соответствующее эквиваленту вещества А, содержащееся в одном литре раствора:
где 1 /z — фактор эквивалентности; рассчитывается для каждого вещества на основании стехиометрии реакции, n( 1 /zA) — количество вещества, равное эквиваленту А в растворе, моль; M( 1 /zA) — молярная масса эквивалента растворенного вещества А, г/моль.
Молярная концентрация эквивалента измеряется в моль/л.
3) Титр Т(А) растворенного вещества А — это масса растворенного вещества А, содержащаяся в одном миллилитре раствора:
где объем раствора V(A) измеряется в мл.
Титр измеряется в г/мл; в некоторых случаях — в мкг/мл. Иногда титр обозначают символом t(А).
4) Титр раствора по определяемому веществу X, или Титриметрический фактор пересчета t(T\X) — масса титруемого вещества X, взаимодействующая с одним миллилитром титранта Т:
Вывод формулы для t(Т/Х)
Пусть при титровании протекает реакция:
X + T = продукты реакции
Согласно закону эквивалентов вещества X и T реагируют в эквивалентных количествах
Измеряется, как и титр раствора, в г/мл.
Титр по определяемому веществу используется при расчете массы определяемого компонента по результатам титриметрического анализа лекарственных препаратов и других веществ.
Пусть, например, на титрование анализируемого раствора, содержащего определяемый компонент X, израсходован объем титранта V(T) мл с молярной концентрацией эквивалента c( 1 /zТ).
5) Поправочный коэффициент F(или K) — число, выражающее отношение действительной (практической) концентрации c( 1 /zA)пр. вещества А в растворе к его заданной (теоретической ) концентрации c( 1 /zA)теор.:
Пусть, например, требуется приготовить раствор с заданной (теоретической) концентрацией 0,1000 моль/л. Практически приготовлен раствор с близкой (но не точно равной 0,1000 моль/л) концентрацией 0,1056 моль/л. Тогда поправочный коэффициент равен
F = 0,1056/0,1000 = 1,056
В дальнейшем при применении приготовленного раствора можно во всех расчетах использовать теоретическую концентрацию, вводя поправочный (для данного раствора) коэффициент, что упрощает проведение расчетов.
Отечественная Государственная Фармация рекомендует готовить стандартные растворы с поправочным коэффициентом в пределах 0,98—1,02.
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Источник
Способы выражения концентраций в титриметрическом анализе
В титриметрическом анализе используют следующие основные способы выражения концентраций растворов.
Молярная концентрация с(А) —- количество растворенного вещества А в молях, содержащееся в одном литре раствора:

где m(А) — масса растворенного вещества А, г
М(А.) — молярная масса растворенного вещества А, г/моль.
Молярная концентрация эквивалента с(1/Z А), или нормальность (старое название),— количество растворенного вещества А в молях, соответствующее эквиваленту А, содержащееся в одном литре раствора:

где 1/Z — фактор эквивалентности; рассчитывается для каждого вещества на основании стехиометрии реакции;
M(1/ZА) — молярная масса эквивалента растворенного вещества А, г/моль.
Титр T(А) растворенного вещества А — это масса растворенного вещества А в граммах, содержащаяся в одном миллилитре раствора:

где объем раствора V измеряется в мл.
Титр раствора по определяемому веществу X, или титриметрический фактор пересчета t (Т/ Х), — масса титруемого вещества, взаимодействующая с одним миллилитром титранта Т:

Поправочный коэффициент К — число, выражающее отношение действительной (практической) концентрации c(1/zA) вещества А в растворе к его заданной (теоретической) концентрации с(1/zА)теор:
К = c(1/zA)пр/c(1/zA)теор
Лабораторная работа № 1
Определение содержания Na 2 CO 3 и NaHCO 3
При их совместном присутствии
Для своего варианта рассчитать навеску вещества с заданной концентрацией в требуемом объеме.
| № | Соединение | mн, г | См | Сн | % | Т×10 3 | r, г/см 3 | V, л или m, кг |
| 1 | NaHCO3 Na2CO3 | 0,05 0,05 | 0,5 | |||||
| 2 | NaHCO3 Na2CO3 | 0,03 0,06 | 0,5 | |||||
| 3 | Na2CO3 NaHCO3 | 0,4 0,5 | 3,0 6,0 | 0,5 кг | ||||
| 4 | Na2CO3 NaHCO3 | 5,0 5,0 | 0,25 | |||||
| 5 | NaHCO3 | 7,0 | 0,25 | |||||
| 6 | Na2CO3 | 0,6 | 0,25 кг | |||||
| 7 | NaHCO3 | 0,05 | 0,25 | |||||
| 8 | NaHCO3 Na2CO3 | 0,06 0,05 | 0,25 | |||||
| 9 | NaHCO3 Na2CO3 | 0,055 0,045 | 0,25 | |||||
| 10 | NaHCO3 Na2CO3 | 0,2 0,8 | 0,25 кг | |||||
| 11 | Na2CO3 NaHCO3 | 8,0 2,0 | 0,2 | |||||
| 12 | Na2CO3 NaHCO3 | 4,0 6,0 | 0,25 | |||||
| 13 | Na2CO3 NaHCO3 | 7,0 3,0 | 0,25 | |||||
| 14 | Na HCO3 | 0,45 | 0,25 кг | |||||
| 15 | NaНCO3 | 0,1 | 0,25 | |||||
| 16 | Na2CO3 | 0,1 | 0,25 | |||||
| 17 | NaHCO3 Na2CO3 | 0,01 0,09 | 0,2 | |||||
| 18 | NaHCO3 | 0,38 | 0,25 кг | |||||
| 19 | NaHCO3 Na2CO3 | 1,0 6,0 | 0,25 | |||||
| 20 | Na2CO3 NaHCO3 | 3,0 7,0 | 0,25 | |||||
| 21 | Na2CO3 NaHCO3 | 1,5 6,5 | 0,5 | |||||
| 22 | Na2CO3 | 0,42 | 0,25 кг | |||||
| 23 | NaHCO3 | 0,1 | 0,25 | |||||
| 24 | Na2CO3 | 0,08 | 0,2 | |||||
| 25 | NaHCO3 | 7,0 | 0,25 | |||||
| 26 | Na2CO3 | 0,6 | 0,25 кг | |||||
| 27 | NaHCO3 | 0,05 | 0,25 | |||||
| 28 | NaHCO3 Na2CO3 | 0,06 0,05 | 0,25 | |||||
| 29 | NaHCO3 | 0,38 | 0,25 кг |
Результаты занести в таблицу и показать преподавателю. После его разрешения приступить к приготовлению раствора.
| Соединение | mн, г | См | Сн | % | Т, г/мл | r, г/см 3 | V, л или m, кг |
| NaHCO3 Na2CO3 |
Приготовление раствора солей нужной концентрации
Рассчитанную навеску солей (или одной соли) взвешивают на аналитических весах и количественно переносят в мерную колбу заданного объема (200 мл, 250 мл или 500 мл). Мерную колбу заполняют наполовину дистиллированной водой и растворяют навеску путем перемешивания. После растворения солей (или одной соли) доливают дистиллированную воду до метки мерной колбы и тщательно перемешивают.
Раствор переливают в пластмассовую бутылку и подписывают.
Содержание солей определяют путем титрования приготовленного раствора соляной кислотой, используя два индикатора: фенолфталеин и метиловый оранжевый. При титровании наблюдаются две точки эквивалентности: первая, когда «наполовину» нейтрализован Na2CO3, вторая, когда нейтрализован NaHCO3, содержащийся в исходной смеси и полученный в результате нейтрализации Na2CO3. В этот момент наступает полная нейтрализация смеси Na2CO3.
NaHCO3 + HCl ® NaCl + CO2 + H2O (метиловый оранжевый)
Кислота хлористоводородная, НСl 0,1н раствор;
Индикаторы: фенолфталеин, метиловый оранжевый.
В бюретку до значения «0» заливают 0,1 н раствор HCl.
В коническую колбу емкостью 250 мл пипеткой переносят аликвотную часть приготовленного раствора, добавляют 2-3 капли фенолфталеина (раствор окрашивается в малиновый цвет) и по каплям приливают из бюретки 0,1 н раствор HCl до полного обесцвечивания раствора. Записывают объем раствора НС1, пошедший на титрование V ф. Затем в эту же колбу добавляют 2-3 капли метилового оранжевого (раствор окрашивается в желтый цвет) и продолжают тировать 0,1 н НС1 до перехода окраски в красновато-оранжевый цвет. Записывают объем раствора соляной кислоты, пошедший на титрование V мо.
Проводят три параллельных опыта. В формулу для расчета подставляют среднее арифметическое значение трех параллельных определений: 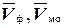
Содержание карбоната натрия и гидрокарбоната натрия определяют по формулам:


где NHCl — нормальность раствора соляной кислоты;
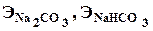
Vк и Vп — объемы соответственно мерной колбы и мерной пипетки, мл.
Принято экспериментальные данные и результаты расчетов выражать только значащими цифрами. Значащими называют все достоверно известные цифры плюс первая из недостоверных, т.е. все результаты следует округлять до первой недостоверной цифры.
Например, объем титранта, пошедший на титрование V = 12,5 мл.
Содержание определяемого вещества (г) записывают до трех значащих цифр. Например, 0,204; 0,0258 или 1,23. Нули, стоящие в начале числа всегда незначимы и служат лишь для указания места запятой в десятичной дроби.
Лабораторная работа № 2
Определение содержания Na ОН и Na 2 CO 3
Дата добавления: 2019-09-13 ; просмотров: 434 ; Мы поможем в написании вашей работы!
Источник
Концентрация растворов. Способы выражения концентрации растворов.
Концентрация раствора может выражаться как в безразмерных единицах (долях, процентах), так и в размерных величинах (массовых долях, молярности, титрах, мольных долях).
Концентрация – это количественный состав растворенного вещества (в конкретных единицах) в единице объема или массы. Обозначили растворенное вещество — Х, а растворитель — S. Чаще всего использую понятие молярности (молярная концентрация) и мольной доли.
Способы выражения концентрации растворов.
1. Массовая доля (или процентная концентрация вещества) – это отношение массы растворенного вещества m к общей массе раствора. Для бинарного раствора, состоящего из растворённого вещества и растворителя:

ω – массовая доля растворенного вещества;
mв-ва – масса растворённого вещества;
Массовую долю выражают в долях от единицы или в процентах.
2. Молярная концентрация или молярность – это количество молей растворённого вещества в одном литре раствора V:

C – молярная концентрация растворённого вещества, моль/л (возможно также обозначение М, например, 0,2 М HCl);
n – количество растворенного вещества, моль;
V – объём раствора, л.
Раствор называют молярным или одномолярным, если в 1 литре раствора растворено 1 моль вещества, децимолярным – растворено 0,1 моля вещества, сантимолярным – растворено 0,01 моля вещества, миллимолярным – растворено 0,001 моля вещества.
3. Моляльная концентрация (моляльность) раствора С(x) показывает количество молей n растворенного вещества в 1 кг растворителя m:

С (x) – моляльность, моль/кг;
n – количество растворенного вещества, моль;
4. Титр – содержание вещества в граммах в 1 мл раствора:

T – титр растворённого вещества, г/мл;
mв-ва – масса растворенного вещества, г;
5. Мольная доля растворённого вещества – безразмерная величина, равная отношению количества растворенного вещества n к общему количеству веществ в растворе:

N – мольная доля растворённого вещества;
n – количество растворённого вещества, моль;
nр-ля – количество вещества растворителя, моль.
Сумма мольных долей должна равняться 1:
Иногда при решении задач необходимо переходить от одних единиц выражения к другим:
ω(X) — массовая доля растворенного вещества, в %;
М(Х) – молярная масса растворенного вещества;
ρ= m/(1000V) – плотность раствора. 6. Нормальная концентрация растворов (нормальность или молярная концентрация эквивалента) – число грамм-эквивалентов данного вещества в одном литре раствора.
Грамм-эквивалент вещества – количество граммов вещества, численно равное его эквиваленту.
Эквивалент – это условная единица, равноценная одному иону водорода в кислотоно-основных реакциях или одному электрону в окислительно – восстановительных реакциях.
Для записи концентрации таких растворов используют сокращения н или N. Например, раствор, содержащий 0,1 моль-экв/л, называют децинормальным и записывают как 0,1 н.

СН – нормальная концентрация, моль-экв/л;
z – число эквивалентности;
Растворимость вещества S — максимальная масса вещества, которая может раствориться в 100 г растворителя:
Коэффициент растворимости – отношение массы вещества, образующего насыщенный раствор при конкретной температуре, к массе растворителя:
Источник