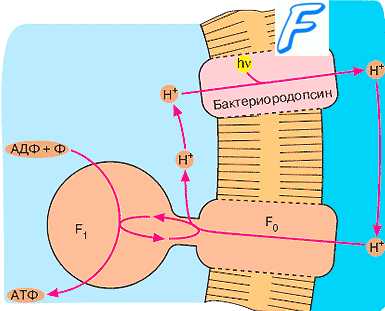
Способы синтеза атф у бактерий
Синтез АТФ осуществляется тремя способами: фотосинтетическое фосфорилирование, окислительное фосфорилирование (сопряжённое с транспортом электронов по дыхательной цепи) и субстратное фосфорилирование.
В первых двух процессах преобразование поступившей с потоком электронов энергии в энергию фосфоэфирных связей АТФ осуществляет особый фермент — АТФ-синтетаза. Этот фермент присутствует во всех мембранах, участвующих в преобразовании энергии (мембраны бактерий, митохондрий и хлоропластов). АТФ-синтетаза катализирует присоединение неорганического фосфата (Фн) к АДФ, образование которого осуществляет аде-нилаткиназа (АМФ + АТФ = 2 АДФ). Активность АТФ-синтетазы можно обнаружить по обратной реакции гидролиза АТФ: АТФ + Н20 = АДФ + Фн + Н+. Благодаря обратимости реакции фосфорилирования, накопившийся АТФ может быть использован для создания протонного градиента, обеспечивающего энергией движение жгутиков и осмотическую работу. Энергия также направляется для обратного переноса электронов, необходимого для восстановления никотинамидадениндинуклеотида (НАД) при использовании бактериями неорганических доноров электронов (S03, N03, Fe2+ и др.).
Получение энергии в процессе фотосинтеза. Бактерии фототрофы. Реакции фотосинтеза.
Получение энергии в процессе фотосинтеза. Основной источник энергии для жизни на Земле — Солнце, но непосредственно утилизировать энергию инсоляции в мире бактерий способны лишь немногочисленные бактерии фототрофы [от греч. photos, свет, + trophe, питание]. Фотосинтезирующие бактерии, подобно растениям, превращают энергию видимого света в протонный потенциал на энергопреобразующей мембране. В последующем с помощью АТФ-синтетазы энергия консервируется в АТФ. Основной признак, отличающий фотосинтегические реакции у пурпурных и зелёных бактерий от таковых у растений и цианобактерий, — отсутствие выделения кислорода (так как в качестве донора электронов они используют не воду, a H2S или органические вещества). У бактерий аналог хлоропластов растительных клеток — хроматофоры, содержащие хлорофилл и каротиноидные пигменты.
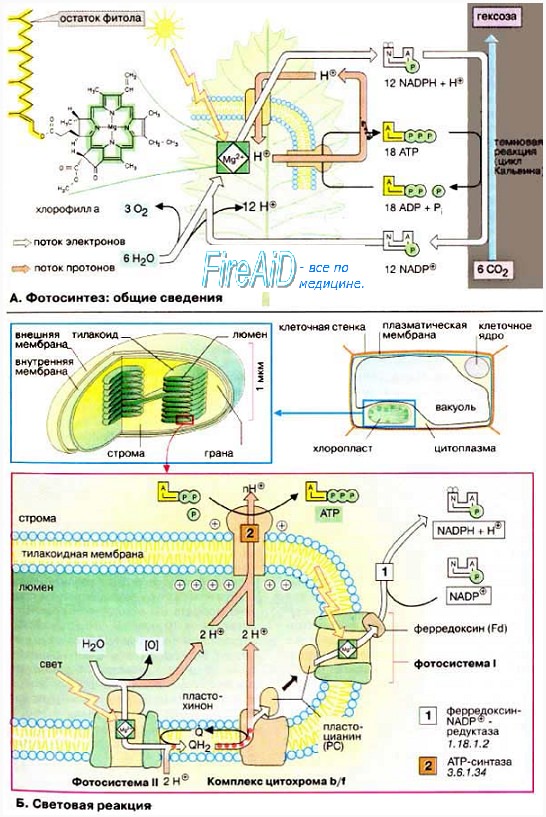
Таким образом, под фотосинтезом понимают происходящее в клетках фототрофных организмов преобразование световой энергии в биохимически доступную энергию (протонный градиент на мембране тилакоидов и хлоропластов, АТФ) и восстановительную силу НАДФН+, а также связанный с этим синтез клеточных компонентов. Реакции фотосинтеза протекают в две стадии (световая и темновая фазы).
Световая фаза фотосинтеза. Под действием фотонов электрон хроматофора активируется, затем он возвращается в исходное состояние. При этом высвобождается энергия, используемая для создания протонного градиента, а затем синтеза АТФ и восстановления никотинамидадениндинуклеотидфосфата (НАДФ) до НАДФН+. Последнее может происходить за счёт обратного транспорта электронов с затратой АТФ.
Темновая фаза фотосинтеза. Образовавшиеся макроэргические соединения используются для ассимиляционного восстановления С02 в глюкозу. Глюкоза содержит значительное количество энергии (около 690 ккал/моль), что и используют гетеротрофные бактерии, разлагая глюкозу и запасая энергию в универсальном хранителе — АТФ.
Источник
Метаболизм прокариот. Катаболизм и анаболизм. Брожение
» data-shape=»round» data-use-links data-color-scheme=»normal» data-direction=»horizontal» data-services=»messenger,vkontakte,facebook,odnoklassniki,telegram,twitter,viber,whatsapp,moimir,lj,blogger»>
МЕТАБОЛИЗМ ПРОКАРИОТ
ПРОЦЕССЫ КАТАБОЛИЗМА И АНАБОЛИЗМА
Метаболизм прокариот, так же как и эукариот, складывается из двух противоположно направленных процессов — катаболизма и анаболизма.
Катаболизм — это совокупность реакций окисления различных восстановленных органических и неорганических соединений, сопровождающихся выделением энергии, аккумулируемой клеткой л-форме фосфатных связей (АТФ).
Анаболизм — это совокупность реакций биосинтеза конституционных и запасных компонентов клетки за счет веществ питательного субстрата и промежуточных продуктов, образующихся при катаболизме. Анаболизм осуществляется за счет энергии, аккумулированной в фосфатных связях в форме АТФ или других богатых энергией соединений.
Процессы катаболизма и анаболизма в клетке протекают одновременно и тесно взаимосвязаны между собой. Совокупность последовательных ферментативных реакций обоих процессов можно подразделить на 3 этапа.
Начальный этап предусматривает ферментативное превращение веществ исходного субстрата и носит название периферического метаболизма (СО2).
Промежуточный этап объединяет ферментативные реакции, сопровождающиеся образованием промежуточных продуктов, нередко одинаковых для процессов катаболизма и анаболизма (ПВК).
Конечный этап характеризуется образованием конечных продуктов анаболизма, идущих на построение структурных элементов клетки, и конечных продуктов катаболизма, выделяемых клеткой в среду.
ФЕРМЕНТЫ ПРОКАРИОТНОЙ КЛЕТКИ
Ферменты – это белки, биологические катализаторы всех биохимических реакций.
- Ферменты – это белки,
- Ферменты участвуют в реакциях в небольших количествах.
- Ферменты не входят в состав конечных продуктов реакции,
- Ферменты катализируют много реакций,
- Ферменты обладают специфичностью,
Ф могут быть простые (состоят из Б), и сложные ( Б+ небелковая часть). Небелковая часть может быть прочно связана – простетическая группа, и непрочно связаны – кофермент.
По времени образования ферменты прокариотной клетки можно подразделить на 2 группы.
Конститутивные ферменты, синтез которых идет с достоянной скоростью независимо от веществ субстрата; в клетке они находятся в более или менее постоянной концентрации. Примером конститутивных ферментов могут служить гликолитические ферменты.
Индуцибельные ферменты, скорость синтеза которых в клетке резко возрастает в ответ на появление в среде субстрата-индуктора. К индуцибельным ферментам относится большинство гидролаз.
Ключевые позиции в процессах метаболизма занимают алло-стерические ферменты. Последние чутко реагируют на потребности клетки в конечных продуктах метаболизма. Избыточное количество конечного продукта тотчас же ингибирует активность первого фермента в системе собственного биосинтетического пути.
- оксидоредуктазы – О-В,
- Лигазы – катализируют соединение молекул,
- гидролазы – катализируют расщепление между атомами С и О2, N,S. И катализируют присоединение молекул воды.,
- лиазы – катализируют отсоединение атомов от одних веществ и присоединение к другим.,
- Изомеразы – катализируют внутирмолекулярный перенос.
- Эндоферменты – все вышеуказанные Ф,
- Экзоферменты – выделяются из прокариотной клетки в окружающую среду.
Биосинтез углеводов.
- Для прокариот-автотрофов исходным продуктом для синтеза углеводов является СО2. Фотосинтезирующие автотрофные микроорганизмы фиксируют СО2 и осуществляют биосинтез углеводов так же, как растения при фотосинтезе, через цикл Кальвина.
- Сначала идет синтез триозофосфатов по циклу Кальвина, а затем на их основании синтезируются другие углеводы.
Прокариоты-гетеротрофы получают сахара с пищей.
- На основании этих сахаров идет реакция полимеризации.
- Синтез идет путем реакции карбоксилирования:
Биосинтез Белков.
Большинство прокариот способны синтезировать все аминокислоты, входящие в состав их клеточных белков. Предшественниками для синтеза аминокислот служат промежуточные продукты метаболизма, такие, как а-кетоглутаровая, щавелевоуксусная, пировиноградная, Источником азота обычно является аммиак или нитраты, нитриты, молекулярный азот.
Биосинтез аминокислот происходит различными путями.
Наиболее простой путь — прямое аминирование кетокислот аммиаком. Образуется 3 а/к
ЩУК+ NH3— аспорагиновая ,
А-кетоглутаровая+ NH3— глутаминовая.
Остальные а/к образуются в результате переаминирования. Донором амино-групп является глутаминовая а/к.
У гетеротрофов – а/к получают с пищей и из них синтезируют Б.
Биосинтез нуклеотидов.
Нуклеотиды являются исходным материалом для биосинтеза нуклеиновых кислот н многих коферментов.
По химической природе нуклеотиды — сложные соединения, состоящие из азотистых оснований — производных пурина или пиримидина, углеводов типа пентоз и фосфорной кислоты. Однако, несмотря на сложность химической природы, большинство прокариот способны синтезировать нуклеотиды, используя низкомолекулярные предшественники.
Основным звеном биосинтеза нуклеотидов считается синтез пуриновых и пиримидиновых азотистых оснований.
- Начальной стадией синтеза пуриновых нуклеотидов является взаимодействие фосфорибозил-1-пирофосфата с глутамином с образованием фосфорибозиламина. Затем в реакцию включаются другие соединения-предшественники и. ряд последовательных ферментативных реакций завершается образованием инозиновой кислоты — пуриновото нуклеотида. Она служит исходным продуктом для синтеза других нуклеотидов — адениловой и гуаниловой кислот, необходимых для синтеза РНК.
2. Первым пиримидиновым нуклеотидом, синтезируемым из низкомолекулярных соединений, является
1- оротидиловая кислота – СО2= уридиловая кислоты.
2 – уридиловая кислота + NH3 —цитидиловая кислота — нуклеотид, содержащий цитозич.
3. цитидиловая кислота путем ферментативного метилирования — тимидиловая кислота — нуклеотид, содержащий тимин.
Биосинтез липидов.
Липиды в клетке прокариот представлены химическими соединениями различной природы (триглицериды, фосфолипиды, гликолипиды, воска), выполняющими разные функции. Они входят в состав клеточных мембран, являются компонентами пигментных систем и транспорта электронов, выполняют роль запасных веществ.
Исходными продуктами для биосинтеза липидов служат жирные кислоты, спирты, углеводы, фосфаты. Пути биосинтеза липидов сложны и протекают с затратой значительного количества энергии при участии многочисленных ферментов. Наиболее важны для жизнедеятельности клетки триглицериды и фосфолипиды.
1. Биосинтез жирных кислот с четным числом атомов углерода происходит в результате последовательного присоединения к молекуле ацетил-KnA двууглеродного остатка от малонил-КоА. Так, при биосинтезе пальмитиновой кислоты 1 молекула ацетил-КоА конденсируется с 7 молекулами малонил-КоА.
Важную роль в реакциях биосинтеза жирных кислот играет ацилпереносящий белок (АПБ) — переносчик ацильных групп. Последовательное наращивание двууглеродных остатков через ряд промежуточных продуктов приводит к образованию C16 — С18-соединений.
В клетках прокариот компонентами липидов могут являться ненасыщенные жирные кислоты, содержащие одну двойную связь. Образование двойной связи у аэробных микроорганизмов происходит при участии кислорода и специфического фермента десатуразы.
Исходным субстратом для синтеза фосфолипидов служит фосфодиоксиацетон — промежуточное соединение гликолитического цикла. Восстановление его приводит к образованию З-фосфоглицерина, который, соединяясь с двумя остатками жирных кислот, продуцирует фосфатидную кислоту. Присоединение к ее фосфатной группе серина, инозита, этаноламина, холина заканчивается синтезом фосфатидилсерина, фосфатидилинозита, фосфатидилэтано-ламина- (кефалина) и фосфатиДилхолина (лецитина).
Для прокариот характерны весьма различные способы получения энергии. Так, наиболее древняя группа анаэробных прокариот довольствуется химической энергией процессов брожения. Большинство прокариот получают энергию в реакциях аэробного окисления самых различных органических соединений. Однако среди них имеются факультативные анаэробы, способные переходить от аэробного окисления органических веществ субстрата к анаэробному нитратному или сульфатному дыханию.
Энергия, получаемая прокариотами, аккумулируется клеткой в высокоэнергетических соединениях с фосфатной связью: производные фосфорной кислоты — аденозинтрифосфат (АТФ),
При отщеплении одного из остатков фосфорной кислоты от молекулы АТФ с образованием АДФ освобождается значительное количество энергии.
И наоборот, присоединение фосфорной кислоты к АДФ в реакциях фосфорилирования с образованием АТФ (АДФ + Фн = АТФ) сопровождается аккумуляцией энергии.
Энергия, аккумулированная в АТФ, расходуется клеткой на биосинтез веществ, связанный с активным ростом культуры. Часть энергии постоянно потребляется на поддержание жизнедеятельности организма – на активный транспорт питательного субстрата в клетку, на обновление клеточного материала (белки ферментов, иРНК, вещества клеточной стенки и цитоплазматической мембраны), на движение организма и т. д.
Ферменты цепи переноса электронов.
Отщепление и перенос водорода или электронов от окисляемого субстрата на конечный акцептор осуществляется через последовательную цепь дыхательных ферментов, получившую название цепи переноса электронов (ЦПЭ) или дыхательной цепи (рис. 24).
Общая характеристика процессов брожения.
Брожение — эволюционно наиболее древний и примитивный способ получения энергии, характерный для некоторых групп прокариот. Основные типы брожений — спиртовое, молочнокислое и маслянокислое – открыты
Л. Пастером в 1861 г., хотя продукты брожений были известны
человеку с незапамятных времен.
Процессы брожения протекают в анаэробных условиях без участия молекулярного кислорода за счет окислительно-восстановительных превращений органических соединений субстрата и сопровождаются выделением незначительного количества энергии. Так, в процессе молочнокислого брожения образуются всегда 2 молекулы АТФ на 1 молекулу сброженной глюкозы, в то время как при аэробном окислении 1 молекулы глюкозы синтезируются 38 молекул АТФ.
В качестве исходного субстрата в процессах брожения микроорганизмы используют самые разнообразные органические вещества – углеводы, спирты, органические кислоты, аминокислоты, пурины, пиримидины. Конечными продуктами брожений обычно являются органические кислоты (молочная, уксусная, янтарная и др.), спирты (этиловый, пропиловый, бутиловый), ацетон, ССЬ и Н^. По выходу основного конечного продукта выделяют различные типы брожений: молочнокислое, спиртовое, маслянокислое, пропионо-вокислое и др.
В любом процессе брожения можно выделить две стадии: окислительную и восстановительную.
Первая, окислительная стадия большинства процессов брожения заключается в серии последовательных реакций, ведущих к образованию пировиноградной кислоты из углевода. У различных групп микроорганизмов установлены три пути превращения глюкозы в пировиноградную кислоту. Первый, наиболее распространенный путь, характерный для дрожжей и многих бактерий, получил название гликолиза.
Второй, пентозофосфатный путь также показан для многих бактерий.
Гликолиз
включает ряд реакций, каждая из которых катализируется специфическим ферментом. Исходными продуктами гликолиза служат моносахариды или дисахариды, которые ферментативным путем расщепляются до моносахаридов.
В реакциях гликолиза из одной молекулы глюкозы образуются 2 молекулы пировиноградной кислоты, 2 молекулы НАД ■ Н2 и 4 молекулы АТФ, из которых 2 синтезируются при окислении двух молекул 3-ФГА и 2 при дегидратации двух молекул 2-ФГК. Из четырех синтезированных молекул АТФ 2 молекулы АТФ затрачиваются на фосфорилирование глюкозы во фруктозо-1,6-дифосфат. Поэтому общий энергетический эффект реакций гликолиза составляет 2 молекулы АТФ на 1 молекулу сброженной глюкозы.
Пентозофосфатный путь растщепления углеводов,
Конечными продуктами сбраживания гексоз в пентозофосфатном цикле являются рибозо-5-фосфат и 3-ФГА. Последний гликолитическим путем превращается в пировиноградную кислоту и гексозофосфаты, которые снова включаются в цикл (рис. 25).
Эволюционное значение возникновения пентозофосфатного пути сбраживания углеводов заключается прежде всего в обеспечении прокариотной клетки пентозами как исходными веществами для процессов биосинтеза. В частности, образующаяся рибоза является предшественником иуклеотидов, нуклеиновых
С энергетической стороны этот путь сбраживания углеводов в два раза менее эффективен, чем гликолитический, так как на 1 молекулу глюкозы образуется только 1 молекула АТФ.
Молочнокислое брожение.
Молочнокислое брожение считается эволюционно одним из самых древних и примитивных типов брожения. По характеру самого процесса и образующимся конечным продуктам различают гомо- и гетероферментативное молочнокислое брожение.
1. В основе гомоферментативного молочнокислого брожения лежит гликолитический цикл сбраживания гексозы с образованием двух молекул пировиноградной кислоты. Последняя, выступая конечным акцептором водорода, восстанавливается до единственного продукта — молочной кислоты.
Энергетической выход гомоферментатипного молочнокислого брожения всего 2 молекулы АТФ на 1 молекулу сброженной глюкозы.
Процесс ведут гомоферментативные молочнокислые бактерии. Морфологически они представлены кокками, спор не образуют, неподвижны. 2- В основе гетероферментативного молочнокислого брожения лежит пентозофосфатный путь сбраживания гексоз или пентоз с образованием молочной кислоты и ряда других продуктов – уксусной кислоты, этилового спирта, глицерина и углекислого газа.
По морфологическим, культуральным и многим физиологическим признакам гетероферментативные молочнокислые бактерии близки к гомоферментативньтм. Различные виды молочнокислых бактерий способны развиваться в широких температурных пределах от 7—10 до 40—42 °С, имея оптимум 25—30 “С.
Значение молочнокислого брожения
1. С незапамятных времен молочнокислые бактерии находят применение в различных отраслях хозяйственной деятельности человека — для приготовления кисломолочных продуктов, сливочного масла, сыра, квашения овощей, в хлебопекарном производстве для заквасок ржаного и пшеничного хлеба, в сельском хозяйстве для силосования кормов.
2. Для производства кисломолочных продуктов в разных географических широтах используют различные виды молочнокислых бактерий.
3. Молочнокислые бактерии играют важную роль в приготовлении сыров. В основе сыроварения лежит коагуляция казеина молока под действием сычужного фермента, получаемого из желудка жвачных животных.
4. Многие молочнокислые бактерии способны синтезировать вещества, обладающие антибиотическими свойствами (лактолин, низин, бревин, диплококкцин и др.). На этом свойстве молочнокислых бактерий основано их антагонистическое действие на гнилостные и болезнетворные микроорганизмы в кишечнике человека и животных.
Спиртовое брожение.
этапы
1– Окислительный этап. Процесс спиртового брожения проходит по гликолитическому пути до образования пировиноградной кислоты.
2- Восстановительный этап. Далее при участии ключевого фермента спиртового брожения — пируватдекарбоксилазы — происходит декарбоксилирование пировиноградной кислоты. В результате образуются ацетальдегид и углекислый газ
3. Образовавшийся ацетлъдегид выступает конечным акцептором водорода и под действием
НАд-зависимой алкогольдегидрогеназы восстанавливается до этилового спирта. Донором водорода, как и при молочнокислом брожении, служит 3-фосфоглицерино-вый альдегид
Энергетический выход процесса составляют 2 молекулы АТФ на I молекулу сброженной глюкозы. Отличие спиртового брожения от молочнокислого заключается в различной природе конечного акцептора водорода.
Значение
Спиртовое брожение лежит в основе ряда промышленных производств — виноделия, получения спирта, пивоварения, хлебопечения.
Возбудители
- -дрожжи – аэробы, клетки округлой формы, неподвижны
- бактерии – сарцины
Маслянокислое брожение.
Маслянокислое брожение проходит в строго анаэробных условиях и ведут его облигатно-анаэробные бактерии рода Clostridium.
Характерной особенностью маслянокислого брожения является реакция конденсации с образованием C4-соединения (масляной кислоты). В результате ряда последовательных реакций из пировиноградной кислоты образуются уксусный альдегид, муравьиная и уксусная кислоты, нередко этиловый спирт. Муравьиная кислота почти тотчас же распадается до СО2 и Н2, а реакция конденсации ацетальдегида приводит к образованию масляной кислоты. Суммарно процесс маслянокислого брожения можно выразить следующим уравнением:
Энергетический выход данного процесса составляет 3,3 молекулы АТФ на 1 молекулу сброженной глюкозы. Это наибольший выход энергии, получаемый во всех вышерассмотренных типах брожений,
Маслянокислые бактерии рода Clostridium многочисленны и ге-терогенпы. Морфологически они представлены крупными палочками. В молодой культуре палочки подвижны, тип жгутикования перитрихиальный. По мере старения клетки формируют эндоспоры.
Масляно-кислое брожение
1 этап – окисление (гликолиз)
Значение
- минерализуют органическое вещество
- молочно-кислые бактерии фиксируют атм азот.
- Используются для получения парфюмерного масла.
1 –вызывают порчу кисломолочных продуктов
2- являются возбудителями заболеваний
Ввозбудители столбняка проникают через поврежденные покровы.
Аэробное окисление органического и неорганического субстрата.
Большая часть аэробных прокариотных организмов потребляет в качестве источника энергии различные органические соединения, окисляя их до конечных продуктов СО2 и Н2О. Аэробное окисление органических веществ в прокариотной клетке проходит подобно аэробному дыханию эукариот. В основе его лежит окисление пировиноградной кислоты по циклу трикарбоновых кислот (ЦТК—цикл Кребса).
Собственно цикл Кребса начинается с реакции конденсации ацетил-КоА с молекулой щавелевоуксусной кислоты (ЩУК). В результате реакции образуются свободный KоA и лимонная кислота.
Лимонная кислота под действием фермента аконитазы превращается в цис-аконитовую и далее в изолимонную кислоту. Последняя подвергается дегидрированию, в результате которого образуется щавелево-янтарная кислота и НАД-Н2. Щавелевоянтарная кислота, легко декарбоксилируется и превращается в а-кетоглутаровую кислоту. Далее а-кетоглутаратдегидрогеназный комплекс катализирует реакцию окислительного декарбоксилирования а-кетоглутаровой кислоты, в результате чего образуется сукцинил-КоА, содержащий высокоэнергетическую тиоэфирную связь. Это единственная необратимая реакция цикла Кребса.
При участии фермента сукцинилтиокиназы из сукцинил-КоА образуется янтарная кислота. Освобождающаяся при разрыве тиоэфирной связи энергия запасается в фосфатной связи АТФ. Янтарная кислота окисляется в фумаровую, которая далее гидратируется с образованием яблочной кислоты. Последующее дегидрирование яблочной кислоты завершает цикл трикарбоновых кислот, образуя щавелевоуксусную кислоту.
Цикл Кребса выполняет две важные функции для клетки.
В реакциях этого цикла осуществляется полное окисление органического субстрата с отщеплением водорода и переходом его на
фермент,
Исходным субстратом служат – углеводы, жирные кислоты, аминокислоты.
Цикл Кребса сопряжен с дыхательной цепью.
В целом энергетический выход аэробного окисления прокариотных организмов значительно выше энергетического эффекта процессов брожения. На одну молекулу глюкозы, окисленной до конечных продуктов CO2 и Н2О, образуется 38 молекул АТФ.
Источник