- Способы регуляции мышечного сокращения
- Молекулярные механизмы мышечного сокращения
- Молекулярные особенности сократительных нитей
- Видео физиология мышц и мышечного сокращения — профессор, д.м.н. П.Е. Умрюхин
- Способы регуляции мышечного сокращения
- Видео физиология мышц и мышечного сокращения — профессор, д.м.н. П.Е. Умрюхин
- Способы регуляции мышечного сокращения
- Видео физиология гуморальной регуляции и ее отличие от гормональной — профессор, д.м.н. П.Е. Умрюхин
Способы регуляции мышечного сокращения
Выделяют несколько последовательных этапов запуска и осуществления мышечного сокращения.
1. Потенциал действия распространяется вдоль двигательного нервного волокна до его окончаний на мышечных волокнах.
2. Каждое нервное окончание секретирует небольшое количество нейромедиатора ацетилхолина.
3. Ацетилхолин действует на ограниченную область мембраны мышечного волокна, открывая многочисленные управляемые ацетилхолином каналы, проходящие сквозь белковые молекулы, встроенные в мембрану.
4. Открытие управляемых ацетилхолином каналов позволяет большому количеству ионов натрия диффундировать внутрь мышечного волокна, что ведет к возникновению на мембране потенциала действия.
5. Потенциал действия проводится вдоль мембраны мышечного волокна так же, как и по мембране нервного волокна.
6. Потенциал действия деполяризует мышечную мембрану, и большая часть возникающего при этом электричества течет через центр мышечного волокна. Это ведет к выделению из саркоплазматического ретикулума большого количества ионов кальция, которые в нем хранятся.
7. Ионы кальция инициируют силы сцепления между актиновыми и миозиновыми нитями, вызывающие скольжение их относительно друг друга, что и составляет основу процесса сокращения мыщц.
8. Спустя долю секунды с помощью кальциевого насоса в мембране саркоплазматического ретикулума ионы кальция закачиваются обратно и сохраняются в ретикулуме до прихода нового потенциала действия. Удаление ионов кальция от миофибрилл ведет к прекращению мышечного сокращения.
Далее мы обсудим молекулярные механизмы этого процесса.
Молекулярные механизмы мышечного сокращения
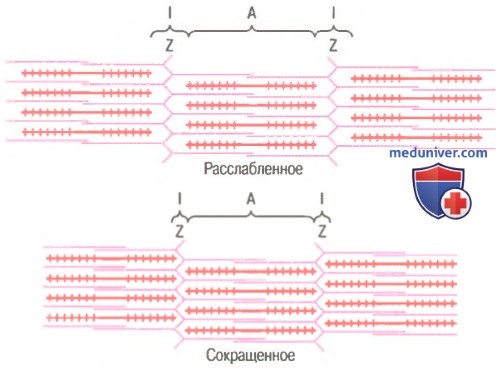
Механизм скольжения нитей для мышечного сокращения. На рисунке показан основной механизм мышечного сокращения. Показано расслабленное состояние саркомера (вверху) и сокращенное состояние (внизу). В расслабленном состоянии концы актиновых нитей, отходящие от двух последовательных Z-дисков, лишь незначительно перекрываются. Наоборот, в сокращенном состоянии актиновые нити втягиваются внутрь между миозиновыми так сильно, что их концы максимально перекрывают друг друга. При этом Z-диски притягиваются актиновыми нитями к концам миозиновых. Таким образом, мышечное сокращение осуществляется путем механизма скольжения нитей.
Что заставляет нити актина скользить внутрь среди нитей миозина? Это связано с действием сил, генерируемых при взаимодействии поперечных мостиков, исходящих от нитей миозина, с нитями актина. В условиях покоя эти силы не проявляются, однако распространение потенциала действия вдоль мышечного волокна приводит к выделению из саркоплазматическо-го ретикулума большого количества ионов кальция, которые быстро окружают миофи-бриллы. В свою очередь, ионы кальция активируют силы взаимодействия между нитями актина и миозина, в результате начинается сокращение. Для осуществления процесса сокращения необходима энергия. Ее источником являются высокоэнергетические связи молекулы АТФ, которая разрушается до АДФ с высвобождением энергии. В следующих разделах мы приведем известные детали молекулярных процессов сокращения.
Молекулярные особенности сократительных нитей
Миозиновая нить. Она состоит из множества молекул миозина, молекулярная масса каждой составляет около 480000. На рисунке показана отдельная молекула; и также — объединение многих молекул миозина в миозиновую нить, а также взаимодействие одной стороны этой нити с концами двух актиновых нитей.
В состав молекулы миозина входят 6 полипептидных цепей: 2 тяжелые цепи с молекулярной массой около 200000 каждая и 4 легкие цепи с молекулярной массой около 20000 каждая. Две тяжелые цепи спирально закручиваются вокруг друг друга, формируя двойную спираль, которую называют миозиновым хвостом. С одного конца обе цепи изгибаются в противоположных направлениях, формируя глобулярную полипептидную структуру, называемую миозиновой головкой. Таким образом, на одном конце двойной спирали молекулы миозина образуются 2 свободные головки; 4 легкие цепи также включены в состав миозиновой головки (по 2 в каждой). Они помогают регулировать функцию головки во время мышечного сокращения.
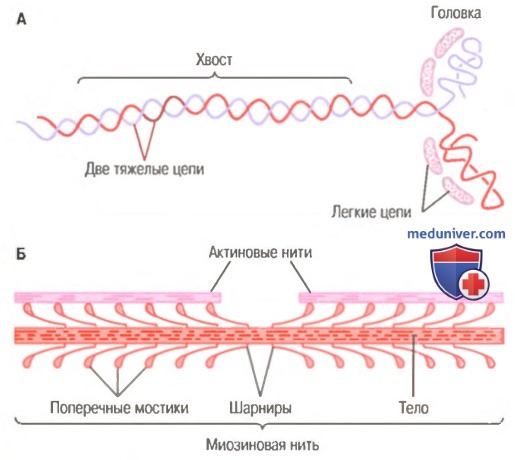
Б. Объединение многих молекул миозина в одну миозиновую нить.
Показаны также тысячи миозиновых поперечных мостиков и взаимодействие их головок с прилежащими актиновыми нитями.
Миозиновая нить состоит из 200 или более отдельных молекул миозина. Видно, что хвосты молекул миозина объединяются, формируя тело нити, а многочисленные головки молекул выдаются наружу по сторонам тела. Кроме того, наряду с головкой в сторону выступает часть хвоста каждой миозиновой молекулы, образуя плечОу которое выдвигает головку наружу от тела, как показано на рисунке. Выступающие плечи и головки вместе называют поперечными мостиками. Каждый поперечный мостик может сгибаться в двух точках, называемых шарнирами. Один из них расположен в месте, где плечо отходит от тела миозиновой нити, а другой — где головка крепится к плечу. Движение плеча позволяет головке или выдвигаться далеко наружу от тела миозиновой нити, или приближаться к телу. В свою очередь, повороты головки участвуют в процессе сокращения, что обсуждается в следующих разделах.
Общая длина каждой миозиновой нити остается постоянной и равна почти 1,6 мкм. В самом центре миозиновой нити на протяжении 0,2 мкм поперечных мостиков нет, поскольку снабженные шарнирами плечи отходят в стороны от центра.
Сама миозиновая нить сплетена таким образом, что каждая последующая пара поперечных мостиков смещена в продольном направлении относительно предыдущей на 120°, что обеспечивает распределение поперечных мостиков во всех направлениях вокруг нити.
АТФ-азная активность миозиновой головки. Есть и другая особенность миозиновой головки, необходимая для мышечного сокращения: миозиновая головка функционирует как фермент АТФ-аза. Как объясняется далее, это свойство позволяет головке расщеплять АТФ и использовать энергию расщепления высокоэнергетической связи для процесса сокращения.
Актиновая нить. Актиновая нить состоит из трех белковых компонентов: актина, тропомиозина и тропонина.
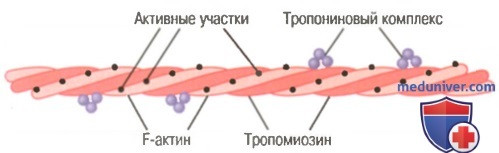
К одному концу каждой молекулы тропомиозина прикреплен тропониновый комплекс, который запускает сокращение.
Основой актиновой нити являются две цепи белковой молекулы F-актина. Обе цепи закручиваются в спираль так же, как и молекула миозина.
Каждая цепь двойной спирали F-актина состоит из полимеризованных молекул G-актина с молекулярной массой около 42000. К каждой молекуле G-актина прикреплена 1 молекула АДФ. Полагают, что эти молекулы АДФ являются активными участками на актиновых нитях, с которыми взаимодействуют поперечные мостики миозиновых нитей, обеспечивая мышечное сокращение. Активные участки на обеих цепях F-актина двойной спирали расположены со смещением таким образом, что вдоль всей поверхности актиновой нити встречается один активный участок примерно через каждые 2,7 нм.
Длина каждой актиновой нити — около 1 мкм. Основания актиновых нитей прочно встроены в Z-диски; концы этих нитей выступают в обоих направлениях, располагаясь в пространствах между миозиновыми молекулами.
Молекулы тропомиозина. Актиновая нить также содержит другой белок — тропомиозин. Каждая молекула тропомиозина имеет молекулярную массу 70000 и длину 40 нм. Эти молекулы спирально оплетают спираль из F-актина. В состоянии покоя молекулы тропомиозина располагаются поверх активных участков актиновых нитей, препятствуя их взаимодействию с миозиновыми нитями, лежащему в основе сокращения.
Тропонин и его роль в мышечном сокращении. По ходу молекул тропомиозина к ним периодически прикреплены другие белковые молекулы, называемые тропонином. Они представляют собой комплексы трех слабосвязанных белковых субъединиц, каждая из которых играет специфическую роль в регуляции мышечного сокращения. Одна из субъединиц (тропонин I) имеет высокое сродство к актину, другая (тропонин Т) — к тропомиозину, третья (тропонин С) — к ионам кальция. Считают, что этот комплекс прикрепляет тропомиозин к актину. Высокое сродство тропонина к ионам кальция, как полагают, инициирует процесс сокращения, о чем говорится в следующей статье.
Видео физиология мышц и мышечного сокращения — профессор, д.м.н. П.Е. Умрюхин
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
— Вернуться в оглавление раздела «Физиология человека.»
Источник
Способы регуляции мышечного сокращения
Как и в скелетной мышце, пусковым стимулом для сокращения большинства гладких мышц является увеличение количества внутриклеточных ионов кальция. В разных типах гладких мышц это увеличение может быть вызвано нервной стимуляцией, гормональной стимуляцией, растяжением волокна или даже изменением химического состава окружающей волокно среды.
Однако в гладких мышцах нет тропонина (регуляторного белка, который активируется кальцием). Сокращение гладкой мышцы активируется совершенно другим механизмом, изложенным далее.
Соединение ионов кальция с кальмодулином. Активация миозинкиназы и фосфорилирование головки миозина.
Вместо тропонина гладкомышечные клетки содержат большое количество другого регуляторного белка, называемого кальмодулином. Хотя этот белок похож на тропонин, он отличается способом запуска сокращения. Кальмодулин делает это путем активации миозиновых поперечных мостиков. Активация и сокращение осуществляются в следующей последовательности.
1. Ионы кальция связываются с кальмодулином.
2. Комплекс кальмодулин-кальций соединяется с фосфорилирующим ферментом миозинкиназой и активирует ее.
3. Одна из легких цепочек каждой головки миозина, называемая регуляторной цепочкой фосфорилируется под действием миозинкиназы. Когда эта цепочка не фосфорилирована, циклического прикрепления и отделения миозиновой головки по отношению к актиновой нити не происходит. Но при фосфорилировании регуляторной цепочки головка приобретает способность к повторному связыванию с актиновой нитью и осуществлению всего циклического процесса периодических «подтягиваний», лежащих в основе сокращения, как и в скелетной мышце.
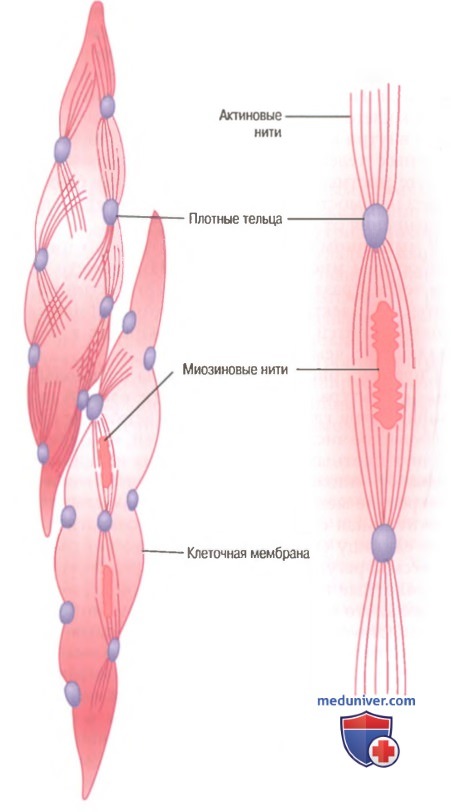
Прекращение сокращения. Роль миозинфосфатазы. Когда концентрация ионов кальция падает ниже критического уровня, изложенные процессы автоматически развиваются в обратном направлении, кроме фосфорилирования головки миозина. Для обратного развития этого состояния нужен другой фермент — миозинфосфатаза, который локализуется в жидкостях гладкомышечной клетки и отщепляет фосфатазу от регуляторной легкой цепочки. После этого циклическая активность, а значит и сокращение, прекращается.
Следовательно, время, необходимое для расслабления мышцы, в большой степени определяется количеством активной миозинфосфатазы в клетке.
Возможный механизм регуляции механизма «защелки». В связи с важностью механизма «защелки» в функции гладких мышц предпринимаются попытки объяснить это явление, поскольку оно делает возможным долговременное поддержание тонуса гладких мышц многих органов без значительных энергетических затрат. Среди многих предложенных механизмов приводим один из простейших.
Когда сильно активированы и миозинкиназа, и миозинфосфатаза, частота циклов миозино-вых головок и скорость сокращения высокие. Затем, когда активация ферментов снижается, частота циклов уменьшается, но в то же время деактивация этих ферментов позволяет миози-новым головкам оставаться прикрепленными к актиновым нитям в течение все более длительной части цикла. Следовательно, число головок, прикрепленных к актиновой нити в любой данный момент времени, остается большим.
Поскольку число прикрепленных к актину головок определяет статическую силу сокращения, напряжение удерживается, или «защелкивается». Однако энергии при этом используется мало, поскольку расщепления АТФ до АДФ не происходит, за исключением тех редких случаев, когда какая-нибудь головка отсоединяется.
Видео физиология мышц и мышечного сокращения — профессор, д.м.н. П.Е. Умрюхин
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Источник
Способы регуляции мышечного сокращения
Волокна скелетной мышцы стимулируются исключительно нервными сигналами, но сокращения гладкой мышцы могут вызываться множеством типов сигналов: нервными, гормональными, растяжением мышцы и некоторыми другими. Основная причина различий состоит в том, что гладкомышечная мембрана содержит много типов рецепторных белков, способных запустить сократительный процесс. Кроме того, есть и другие рецепторные белки, тормозящие сокращение гладкой мышцы, что также отличает ее от скелетной мышцы. Обсудим сначала нервную регуляцию гладкомышечного сокращения, а затем гормональный контроль и другие способы управления.
Физиологическая анатомия нервно-мышечных соединений гладких мышц. Сложно организованные нервно-мышечные соединения, обнаруживаемые на волокнах скелетных мышц, в гладких мышцах не встречаются. Вместо этого вегетативные нервные волокна, иннервирующие гладкие мышцы, обычно диффузно разветвляются на наружной поверхности пласта мышечных волокон. В большинстве случаев эти волокна не входят в непосредственный контакт с клеточными мембранами гладкомышечных волокон, а формируют так называемые диффузные соединения, которые секретируют медиаторы в матрикс, покрывающий гладкую мышцу, часто на расстоянии от нескольких нанометров до нескольких микрометров от мышечных клеток; затем медиатор диффундирует к клеткам.
Более того, при наличии многих слоев мышечных клеток нервные волокна часто иннервируют только наружный слой, и возбуждение распространяется от этого наружного слоя к внутренним слоям путем проведения потенциалов действия по мышечной массе или путем дополнительной диффузии медиатора.
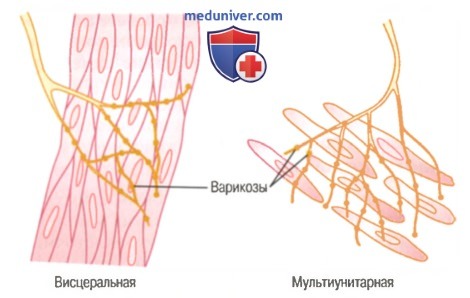
Аксоны, иннервирующие гладкомышечные волокна, не имеют типичных ветвящихся окончаний, характерных для двигательной концевой пластинки волокон скелетной мышцы. Вместо этого большинство тонких концевых частей аксонов имеют множество варикозных расширений (варикозов), распределенных вдоль их осей. В этих местах связь между шванновскими клетками, окутывающими аксоны, прерывается, и медиатор может секретироваться через стенки варикозов. В варикозах находятся везикулы, которые подобно везикулам в концевой пластинке скелетных мышц содержат медиатор. Но в противоположность везикулам в соединениях скелетных мышц, которые всегда содержат ацетилхолин, везикулы окончаний вегетативных нервных волокон содержат ацетилхолин в одних волокнах и норадреналин — в других, а иногда и другие вещества.
В некоторых случаях, особенно в гладких мышцах мультиунитарного типа, варикозы отдалены от мембраны мышечных клеток на 20-30 нм, что равно ширине синаптической щели в соединении скелетной мышцы. Такие соединения называют контактными, и они функционируют во многом так же, как нервно-мышечные соединения скелетных мышц. Скорость сокращения этих гладкомышечных волокон значительно больше, чем у волокон, стимулируемых диффузными соединениями.
Возбуждающие и тормозящие медиаторы, секретируемые в нервно-мышечных соединениях гладких мышц. Самыми важными медиаторами, которые секретируются вегетативными нервами, иннервирующими гладкие мышцы, являются ацетилхолин и норадреналин, однако они никогда не выделяются одними и теми же нервными волокнами. Ацетилхолин для гладких мышц одних органов является возбуждающим медиатором, а на гладкие мышцы других органов действует как тормозящий агент. Если ацетилхолин возбуждает мышечное волокно, норадреналин обычно тормозит его. И наоборот, если ацетилхолин тормозит волокно, норадреналин, как правило, его возбуждает.
Но почему возникают такие разные реакции? Ответ заключается в том, что ацетилхолин и норадреналин возбуждают или тормозят гладкую мышцу, связываясь сначала с рецепторным белком на поверхности мембраны мышечной клетки. Некоторые из этих рецепторных белков являются возбуждающими рецепторами, тогда как другие — тормозящими рецепторами. Следовательно, тип рецептора определяет, как будет реагировать гладкая мышца — торможением или возбуждением, а также какой из двух медиаторов (ацетилхолин или норадреналин) будет проявлять возбуждающее или тормозящее действие.
Видео физиология гуморальной регуляции и ее отличие от гормональной — профессор, д.м.н. П.Е. Умрюхин
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Источник




