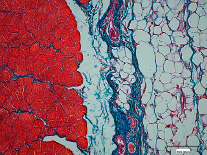
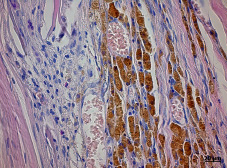
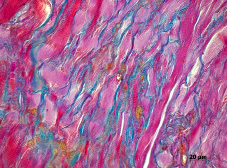
Способы регенерации трех видов мышечной ткани
6. Гистогенез и регенерация мышечной ткани
Гистогенез скелетной мышечной ткани . Источником развития элементов скелетной (соматической) поперечнополосатой мышечной ткани являются клетки миотомов мезодермы – миобласты. Одни из них дифференцируются на месте и участвуют в образовании так называемых аутохтонных мышц. Другие клетки мигрируют из миотомов в мезенхиму. Они уже детерминированы, хотя внешне не отличаются от других клеток мезенхимы. Их дифференцировка продолжается в местах закладки других мышц тела.
В ходе дифференцировки возникают две клеточные линии. Клетки одной из линий сливаются, образуя удлиненные симпласты – мышечные трубочки ( миотубы ). В них происходит дифференцировка специальных органелл – миофибрилл. В это время в миотубах отмечается хорошо развитая гранулярная эндоплазматическая сеть. Миофибриллы сначала располагаются под плазмолеммой, а затем заполняют большую часть миотубы . Ядра, напротив, из центральных отделов смещаются к периферии. Клеточные центры и микротрубочки при этом полностью исчезают. Гранулярная эндоплазматическая сеть редуцируется в значительной степени. Такие дефинитивные структуры называют миосимпластами .
Клетки другой линии остаются самостоятельными и дифференцируются в миосателлитоциты ( миосателлиты ). Эти клетки располагаются на поверхности миосимпластов .
Значит, из миотомов мезодермы в определенные участки мезенхимы выселяются малодифференцированные клетки — миобласты, часть из которых выстраивается в виде цепочки в стык друг к другу и в области контактов миобластов цитолеммы исчезает и образуется симпластическое образование — миотрубка , в которой ядра в виде цепочки располагаются в середине, а по периферии начинают дифференцироваться из миофиламентов миофибриллы. К миотрубке подрастают нервные волокна, образуя двигательные нервные окончания. Под влиянием эфферентной нервной импульсации начинается перестройка мышечной трубки в мышечное волокно: ядра перемещаются на периферию симпласта к плазмолемме, а миофибриллы занимают его центральную часть, из гладкой эндоплазматической сети развивается саркоплазматическая сеть, окружающая каждую миофибриллу на всем ее протяжении. Плазмолемма миосимпласта образует глубокие трубчатые впячивания — Т-канальцы. За счет деятельности зернистой эндоплазматической сети вначале миобластов, а затем и мышечных труб синтезируются и выделяются с помощью пластинчатого комплекса белки и полисахариды, из которых формируется базальная пластинка мышечного волокна.
Следует отметить, что при формировании миотрубки , а затем и дифференцировки мышечного волокна часть миобластов не входит в состав симпласта , а прилежит к нему, располагаясь под базальной пластинкой. Эти клетки носят название миосателлитов и играют важную роль в процессах физиологической и репаративной регенерации. Установлено, что закладка поперечно-полосатых скелетных мышечных волокон ( миогенез ) происходит только в эмбриональный период. В постнатальном периоде осуществляется их дальнейшая дифференцировка и гипертрофия, но количество мышечных волокон даже в условиях интенсивной тренировки не увеличивается.
Гистогенез сердечной мышечной ткани . Источники развития сердечной поперечнополосатой мышечной ткани – симметричные участки висцерального листка спланхнотома в шейной части зародыша – миоэпикардиальные пластинки. Из них дифференцируются также клетки мезотелия эпикарда. В ходе гистогенеза стволовые клетки сердечной мышечной ткани (в составе миоэпикардиальной пластинки) в процессе дифференцировки дают начало нескольким клеточным дифферонам : возникает 5 видов кардиомиоцитов – рабочие (сократительные), синусные ( ритмзадающие или пейсмекерные ), переходные, проводящие, а также секреторные.
Исходными клетками сердечной мышечной ткани являются кардиомиобласты – уплощенные клетки (крупное ядро, светлая цитоплазма с небольшим количество рибосом и митохондрий). Происходит развитие комплекса Гольджи , гранулярной ЭПС. Клетки обладают высокой способностью к делению. Кардиомиобласты дифференцируются в кардиомиоциты . В цитоплазме кардиомиоцитов увеличивается число полисом, канальцев гранулярной ЭПС, накапливаются гранулы гликогена, увеличивается объем актомиозинового комплекса. Кардиомиоциты путем контактов «конец в конец», «конец в бок» формируют клеточные комплексы – сердечные мышечные волокна.
Гистогенез гладкой мышечной ткани . Этот вид мышечной ткани расположен в стенках органов и имеет генез мезенхимного типа. Миоциты объединяются в пучки, между которыми располагаются тонкие прослойки соединительной ткани. В эти прослойки вплетаются ретикулярные и эластические волокна, окружающие миоциты . В прослойках проходят кровеносные сосуды и нервные волокна. Терминали последних оканчиваются не непосредственно на миоцитах , а между ними. Поэтому после поступления нервного импульса медиатор распространяется диффузно, возбуждая сразу многие клетки. Гладкая мышечная ткань мезенхимного происхождения представлена главным образом в стенках кровеносных сосудов и многих трубчатых внутренних органов, а также образует отдельные мелкие мышцы (цилиарные). Гладкая мышечная ткань в составе конкретных органов имеет неодинаковые функциональные свойства. Это обусловлено тем, что на поверхности органов имеются разные рецепторы к конкретным биологически активным веществам. Поэтому и на многие лекарственные препараты их реакция неодинакова. Возможно, разные функциональные свойства тканей связаны и с конкретной молекулярной организацией актиновых филаментов .
Как было сказано выше, гладкие мышцы развиваются из мезенхимы. Клетки мезенхимы начинают активно размножаться и образуют сгущения. Первым признаков начавшейся дифференциации служит возникновение в цитоплазме клеток протофибрилл . Малодифференцированные клетки располагаются рыхло, соединяются между собой отростками (как клетки мезенхимы). Миофиламенты не имеют правильной ориентации. Позднее гладкомышечные клетки становятся веретенообразными и плотно прилегают друг к другу. Количество протофибрилл в них увеличивается, и они располагаются только в направлении длинной оси клетки.
В активированных миоцитах увеличивается синтез сократительных белков, происходит укрупнение и гиперхроматоз ядра, гипертрофия ядрышка, увеличивается количество свободных рибосом и полисом, наблюдается активация ферментов. Клеточная регенерация осуществляется как за счет активации миоцитов малого объема (камбиальных элементов), так и за счет дифференцированных клеток (обладающих способностью к митозу).
При функциональной нагрузке (беременности) или при патологии наблюдается увеличение массы гладкомышечной ткани за счет гипертрофии (увеличения размеров) или за счет гиперплазии (увеличения количества) гладких миоцитов
Мышечная ткань эпидермального происхождения Миоэпителиальные клетки развиваются из эпидермального зачатка. Они встречаются в потовых, молочных, слюнных и слезных железах и имеют общих предшественников с их секреторными клетками. Миоэпителиальные клетки непосредственно прилежат к собственно эпителиальным и имеют общую с ними базальную мембрану. При регенерации те и другие клетки тоже восстанавливаются из общих малодифференцированных предшественников. Большинство миоэпителиальных клеток имеют звездчатую форму. Эти клетки нередко называют корзинчатыми : их отростки охватывают концевые отделы и мелкие протоки желез. В теле клетки располагаются ядро и органеллы общего значения, а в отростках – сократительный аппарат, организованный, как и в клетках мышечной ткани мезенхимного типа.
Мышечная ткань нейрального происхождения. Миоциты этой ткани развиваются из клеток нейрального зачатка в составе внутренней стенки глазного бокала. Тела этих клеток располагаются в эпителии задней поверхности радужки. Каждая из них имеет отросток, который направляется в толщу радужки и ложится параллельно ее поверхности. В отростке находится сократительный аппарат, организованный так же, как и во всех гладких миоцитах . В зависимости от направления отростков (перпендикулярно или параллельно краю зрачка) миоциты образуют две мышцы – суживающую и расширяющую зрачок.
Регенерация. В мышечной, как в других тканях, различают два вида регенерации — физиологическую и репаративную . Из всех видов мышечной ткани лучше всего регенерирует гладкая, так как ее клетки миоциты могут активно делиться митозом всю жизнь.
Физиологическая регенерация скелетной мышечной ткани проявляется в форме гипертрофии мышечных волокон, что выражается в увеличении их толщины и даже длины, увеличение числа органелл, главным образом миофибрилл, а также нарастании числа ядер, что, в конечном счете, проявляется увеличением функциональной способности мышечного волокна. Радиоизотопным методом установлено, что увеличение числа ядер в мышечных волокнах в условиях гипертрофии достигается за счет деления клеток миосателлитов и последующего вхождения в миосимпласт дочерних клеток.
Увеличение числа миофибрилл осуществляется посредством синтеза актиновых и миозиновых белков свободными рибосомами и последующей сборки этих белков в актиновые и миозиновые миофиламенты параллельно с соответствующими филаментами саркомеров . В результате этого вначале происходит утолщение миофибрилл, а затем их расщепление и образование дочерних миофибрилл. Кроме того возможно образование новых актиновых и миозиновых миофиламентов не параллельно, а встык предшествующим миофибриллам, чем достигается их удлинение. Саркоплазматическая сеть и Т-канальцы в гипертрофирующемся волокне образуются за счет разрастания предшествующих элементов.
При определенных видах мышечной тренировки может формироваться преимущественно красный тип мышечных волокон (у стайеров) или белый тип мышечных волокон (у спринтеров). Возрастная гипертрофия мышечных волокон интенсивно проявляется с началом двигательной активности организма (1-2 года), что обусловлено, прежде всего усилением нервной стимуляции. В старческом возрасте, а также в условиях малой мышечной нагрузки наступает атрофия специальных и общих органелл, истончение мышечных волокон и снижение их функциональной способности.
Репаративная регенерация развивается после повреждения мышечных волокон. При этом способ регенерации зависит от величины дефекта. При значительных повреждениях на протяжении мышечного волокна миосателлиты в области повреждения и в прилежащих участках растормаживаются, усиленно пролиферируют, а затем мигрируют в область дефекта мышечного волокна, где выстраиваются в цепочки, формируя миотрубку . Последующая дифференцировка миотрубки приводит к восполнению дефекта и восстановлению целостности мышечного волокна. В условиях небольшого дефекта мышечного волокна на его концах, за счет регенерации внутриклеточных органелл, образуются мышечные почки, которые растут навстречу друг другу, а затем сливаются, приводя к закрытию дефекта. Однако репаративная регенерация и восстановление целостности мышечных волокон могут осуществляться при определенных условиях: во-первых, при сохраненной двигательной иннервации мышечных волокон, во-вторых, если в область повреждения не попадают элементы соединительной ткани (фибробласты). Иначе на месте дефекта мышечного волокна развивается соединительно-тканный рубец.
Советским ученым А. Н. Студитским доказана возможность аутотрансплантации скелетной мышечной ткани и даже целых мышц при соблюдении определенных условий:
- механическое измельчение мышечной ткани трансплантата, с целью растормаживания клеток-сателлитов и последующей их пролиферации;
- помещение измельченной ткани в фасциальное ложе;
- подшивание двигательного нервного волокна к измельченному трансплантату;
- наличие сократительных движений мышц-антагонистов и синергистов.
Регенерация сердечной мышечной ткани. В сердечной мышечной ткани отсутствуют камбиальные клетки, а сами кардиомиоциты утрачивают способность делиться к моменту рождения ребенка или в первые месяцы жизни. Поэтому при регенерации ткани не образуются новые кардиомиоциты и волокна. Наблюдается гипертрофия (увеличение объема) сохранившихся клеток.
Источник
Способы регенерации трех видов мышечной ткани
Посттравматическое восстановление скелетных мышц является актуальной медико-биологической проблемой. Как правило, после глубоких мышечных повреждений полноценного восстановления ткани не происходит. На его месте формируется грубоволокнистый рубец, что приводит к нарушению функционирования органа. Существующие технологии коррекции данных дефектов – мышечная аутопластика, аллопластика, ксенопластика, клеточные технологии, генная терапия являются трудоемкими, травматичными и сопряжены с осложнениями [1]. Одним из перспективных направлений в регенеративной медицине являются тканевая инженерия с использованием биодеградируемых трансплантатов [3]. Биоматериалы Аллоплант в различной модификации зарекомендовали себя как эффективные стимуляторы регенерации соединительной ткани [6]. Целью исследования явилось определение морфологических аспектов регенерации скелетной мышечной ткани после механического повреждения с использованием одного из его видов – аллогенного губчатого биоматериала (АГБ).
Материалы и методы исследования
Для исследования использовали половозрелых крыс породы Вистар. Работу проводили с соблюдением «Правил проведения работ с использованием экспериментальных животных» (приказ Минвуза от 13 ноября 1984 г. № 724). В опытной серии (n=36) после разреза кожных покровов на задней поверхности голени производилось выделение икроножной мышцы и пяточного сухожилия, а также малоберцового нерва, который не повреждали. Затем на брюшко мышцы в средней трети наносили дефект длиной 3–4 мм. В толщу между проксимальной и дистальной культями укладывался АГБ соответствующих размеров и фиксировался нитевидным сухожильным трансплантатом. В контрольной серии (n=36) в области икроножной мышцы был нанесен дефект длиной 3-4 мм. После чего на кожу в обоих случаях накладывали швы Vicryl 6–0. Малоберцовый нерв не повреждали. АГБ был изготовлен в данном случае из сухожилий крысы и обработан методом лиофилизации, что позволяет добиться модификации структуры в губчатую форму с увеличением объема в 6 раз [7]. Нитевидный сухожильный трансплантат, также был аллогенного происхождения, изготовлен из сухожилия крысы и представлял собой нить, которая применялась для фиксации трансплантируемого АГБ к культям мышцы. Из опыта животные выводились путем инсуфляции летальной дозы паров раствора фторотана. Забор биопсийного материала проводили через 3, 7, 14, 30, 60 и 90 суток после эксперимента. Все трансплантаты были обработаны по оригинальной запатентованной технологии АллоплантÒ, разработанной в ФГБУ «Всероссийский центр глазной и пластической хирургии МЗ РФ» (Патент РФ на изобретение № 2189257, ТУ 9398-001-04537642-2011). Гистологические срезы тканей окрашивали гематоксилином и эозином, по Ван Гизону и по Маллори. Микроскопические исследования проводились с использованием светового микроскопа AxioImager Z1, оснащенного фотонасадкой ProgRes C3 и программой анализа изображений Axiovision (C. Zeiss, Германия). Для электронномикроскопического исследования кусочки тканей фиксировали в 2,5 %-м р-ре глютаральдегида, приготовленного на какодилатном буфере (рН 7,2–7,4) с дофиксацией в 1 %-ном р-ре OsO4 на том же буфере. Материал обезвоживали в спиртах возрастающей концентрации и заливали в эпон-812 по общепринятой методике. Предварительно готовили полутонкие срезы на ультратоме ЕМ UС 7 (Leica, Германия) и окрашивали их раствором толуидинового синего на 2,5 %-ном р-ре безводной соды. На данных срезах выбирали участки для электронномикроскопического исследования. Ультратонкие срезы контрастировали 2 %-ным водным р-ром уранилацетата, цитратом свинца по Рейнольдсу и изучали в трансмиссионном микроскопе JEM-1011 (Jeol, Япония) при ускоряющем напряжении 80 кв.
Результаты исследования и их обсуждение
В контрольной группе в начальные сроки в ране обнаруживались очаги острого воспаления и кровоизлияния. В период 7-14 суток отмечалось развитие пролиферативной стадии воспаления. Дефект замещался грануляционной тканью, представленной толстыми фуксинофильными пучками коллагеновых волокон, инфильтрированных соединительнотканными и иммуногенными клетками. Среди клеток соединительной ткани преобладали клетки фибробластического ряда: мезенхимные клетки, фибробласты с активной коллагенсинтетической деятельностью (коллагенобласты II типа). В меньшей степени выявлялись лимфоциты, макрофаги, преимущественно секреторного типа, и их производные – эпителиоидные клетки и гигантские клетки инородных тел. Отмечался скудный васкулярный рисунок. Резецированные мышечные волокна запечатывались коллагеновыми волокнами за счет наплыва сарколеммы. Через 21 сутки в месте дефекта выявлялись признаки трансформации грануляционной ткани в жировую за счет терминальной дифференцировки фибробластов в адипоциты. В цитоплазме фибробластов помимо характерных резко расширенных каналов гранулярного эндоплазматического ретикулюма выявлялись многочисленные разнокалиберные липидные капли (рис. 1).
Рис. 1. Фибробластическая клетка адипоцитарного направления с хорошо развитой сетью ГЭР. Через 21 сутки после нанесения дефекта в скелетной мышечной ткани. Электронограмма. Увеличение х6000
Спустя 30 суток в области дефекта обнаруживался регенерат, состоящий из мышечной, жировой и плотной волокнистой соединительной тканей (рис. 2).
Рис. 2. Жировое перерождение соединительной ткани через 30 суток после нанесения дефекта в скелетной мышечной ткани. Окраска по Маллори
В контрольной группе стадия острого воспаления переходила в фазу пролиферации с образованием гранулематозной ткани, где была наиболее усилена фибробластическая деятельность. Выраженная мезенхимная реакция и дифференциация в коллагенобласты II типа способствовала интенсивному синтезу коллагеновых волокон. Выявлялся их дефицит и дифференциация в неактивные гигантские формы с низкой секреторной активностью. Известно, что фенотипическая незрелость и фагоцитарная инертность макрофагов могла способствовать незавершенному фагоцитозу и привлечению лимфоидных клеток, что обуславливало фиброзирование дефекта в мышечной ткани [2]. Происходила редукция гемокапилляров. Ишемия тканей могла способствовать распаду мышечных волокон и массовой гибели клеток, что также провоцировало развитие фиброза [2]. Результатом заживления мышечного дефекта явилось образование рубца с последующим перерождением в жировую ткань.
В опытной группе через 3 суток после пересадки АГБ в паратравматической зоне обнаруживались дилятация и повышенная проницаемость кровеносных сосудов, нейтрофильная инфильтрация, отек межпучковых пространств, разрушения миоцитов, кровоизлияния. В зоне трансплантата выявлялся фуксинофильный тканевый экссудат, пронизанный фибриновыми нитями в виде тонковолокнистой сети. Признаки острого воспаления были обусловлены механическими воздействиями, возникшими вследствие оперативного вмешательства. Проницаемость кровеносных сосудов способствовала клеточной элиминации, набуханию и ферментативному воздействию на трансплантат. Через 7 суток воспалительная инфильтрация в реактивной зоне и в самом трансплантате менялась на макрофагально-фибробластическую. Выявлялись макрофаги фагоцитарного типа, а фибробласты с умеренно расширенными каналами гранулярного эндоплазматического ретикулюма классифицировались как коллагенобласты I типа – клетки с умеренным синтезом коллагена. Наряду с соединительнотканными клетками обнаруживались малодифференцированные клетки без определенной специализации, а также клетки миогенной дифференциации – миосателлитоциты II типа и миобласты. После лизиса и резорбции балок АГБ макрофагами происходило постепенное разрастание обильно васкуляризированной рыхлой неоформленной соединительной ткани. Спустя 14 суток происходило замещение АГБ от периферии до центра по всей площади. Наблюдались признаки формирования мышечно-соединительнотканного регенерата с преобладанием рыхлой соединительной ткани. Регенерат был представлен тонкими пучками коллагеновых волокон инфильтрированных макрофагами и фибробластами. Причем, макрофаги присутствовали в наибольшем количестве. Строму сопровождали гемокапилляры, свободные миоциты, образующие почки роста и тяжи новообразованных тонких мышечных волокон (рис. 3).
Рис. 3. Массивная инвазия макрофагов в центральной зоне через 14 суток после имплантации в скелетную мышцу крысы губчатого аллотрансплантата. Окраска гематоксилином и эозином
Через 30 суток в очаге трансплантации обнаруживался мышечно-соединительнотканный регенерат с преобладанием мышечной ткани. Пространственная ориентация растущих миосимпластов была параллельна балкам предсуществующего биоматериала. Через 60 – 90 суток регенерат был представлен пучками мышечных волокон окутанных эндо- и перимизием (рис. 4).
Рис. 4. Новообразованная мышечная ткань в зоне трансплантации губчатого аллотрансплантата спустя 90 суток. Параллельно ориентированные пучки мышечных волокон окутаны эндо- и перимизием. Окраска по Маллори
Биоматериалы Аллоплант изготавливаются из волокнистых соединительнотканных кадаверных тканей. После их имплантации при замещении у реципиента формируется собственная органотипическая рыхлая волокнистая соединительная ткань [5, 6], что подтверждает данное исследование. Между расширенными стромальными элементами свободно мигрировали эндотелиальные клетки гемокапилляров и малодифференцированные миогенные клетки. Продукты резорбции АГБ являются хемоаттрактантами макрофагов и способствуют их фенотипическому созреванию в клетки фагоцитарного типа [5], что наблюдалось в опытной группе. Активированные макрофаги, в свою очередь, влияют на фенотипизм фибробластов, которые ингибируют избыточный синтез коллагена. По данным исследователей, макрофаги также способствуют успешному приживлению миогенных клеток предшественников в раннем периоде заживления скелетной мускулатуры [8, 9, 10]. Происходила ранняя активация миосателлитоцитов и их дифференциация в зрелые миоциты. Новообразованные миосимплаты сопровождали коллагеновые волокна и свободно проникали между ними. За счет удлинения и гипертрофии мышечных волокон, они постепенно вытесняли новообразованную рыхлую соединительную ткань на периферию мышечного пучка. Так формировался эндомизий и перимизий. В данном случае, соединительная ткань выступает «в качестве источника индукционно-формативной тканевой регуляции», а мышечная ткань является регулируемой системой [4].
Таким образом, при использовании АГБ наблюдалось восстановление скелетной мышечной ткани на месте утраченной, в то время как в контрольной группе без применения биоматериала происходило формирование неполноценного соединительно-жировотканного регенерата.
Источник