Хлорид натрия: способы получения и химические свойства
Хлорид натрия NaCl — соль щелочного металла натрия и хлороводородной кислоты. Белое кристаллические вещество. Плавится и кипит без разложения. Умеренно растворяется в воде (гидролиза нет);
Относительная молекулярная масса Mr = 58,44; относительная плотность для ж. и тв. состояния d = 2,165; tпл = 800,8º C; tкип = 1465º C;
Способ получения
1. Хлорид натрия можно получить путем взаимодействия натрия и разбавленной хлороводородной кислоты, образуются хлорид натрия и газ водород:
2Na + 2HCl = 2NaCl + H2↑.
2. При комнатной температуре, в результате взаимодействия натрия и хлора, образуется хлорид натрия:
2Na + Cl2 = 2NaCl
3. Концентрированный раствор гидроксида натрия реагирует с концентрированным раствором хлорида аммония при кипении. При этом образуются хлорид натрия, газ аммиак и вода:
NaOH + NH4Cl = NaCl + NH3↑ + H2O
4. При взаимодействии с разбавленной и холодной хлороводородной кислотой пер окси д натрия образует хлорид натрия и пероксид водорода:
5. Разбавленная хлороводородная кислота реагирует с гидроксидом натрия . Взаимодействие хлороводородной кислоты с гидроксидом натрия приводит к образованию хлорида натрия и воды:
NaOH + HCl = NaCl + H2O
6. В результате взаимодействия сульфата натрия и хлорида бария образуется сульфат бария и хлорид натрия:
Качественная реакция
Качественная реакция на хлорид натрия — взаимодействие его с нитратом серебра, в результате реакции происходит образование белого творожного осадка:
1. При взаимодействии с нитратом серебра , хлорид натрия образует нитрат натрия и осадок хлорид серебра:
NaCl + AgNO3 = NaNO3 + AgCl↓
Химические свойства
1. Хлорид натрия вступает в реакцию со многими сложными веществами :
2.1. Хлорид натрия взаимодействует с кислотами :
2.1.1. Хлорид натрия в твердом состоянии при кипении реагирует с концентрированной серной кислотой с образованием сульфата натрия и газа хлороводорода:
а если температуру опустить до 50º С, то твердый хлорид натрия и концентрированная серная кислота образуют гидросульфат натрия и газ хлороводород:
2.2. Хлорид натрия способен вступать в реакцию обмена со многими солями :
2.2.1. Твердый хлорид натрия реагирует с концентрированной и горячей серной кислотой и твердым перманганатом калия . Взаимодействие хлорида натрия с перманганатом калия и серной кислотой приводит к образованию сульфата марганца, натрия, калия, газа хлора и воды:
2.2.2. Хлорид натрия взаимодействует с гидросульфатом натрия при температуре 450–800º C . При этом образуются сульфат натрия и хлороводородная кислота:
2.2.3. При взаимодействии холодного хлорида натрия с насыщенным нитритом серебра выделяются нитрат натрия и осадок хлорид серебра:
NaCl + AgNO2 = NaNO2 + AgCl↓
Источник
Распознавание соляной кислоты, хлоридов, бромидов, иодидов и иода. Лабораторная работа 20. Химия, 8 класс, Рудзитис и Фельдман
Привет! Давайте сейчас решим, пока есть время подумать!!
1. Для распознавания соляной кислоты, хлоридов, бромидов и иодидов в одну пробирку налейте 1—2 мл разбавленной соляной кислоты, во вторую — столько же водного раствора хлорида натрия, в третью — водного раствора бромида натрия, а в четвертую — иодида калия. Во все пробирки добавьте по нескольку капель раствора нитрата серебра(I) или нитрата свинца(II).
2. Для распознавания иода в пробирку налейте 2—3 мл воды, добавьте немного крахмала, перемешайте эту взвесь и влейте ее во вторую пробирку с 2—3 мл воды, нагретой до кипения. Полученный раствор крахмала налейте в две пробирки и охладите. В одну из них добавьте несколько капель иодида калия, а в другую — раствор иода в спирте.
Задания. 1. Напишите уравнения соответствующих реакций и подумайте, как можно отличить: а) соляную кислоту от других кислот; б) хлориды от других солей;
в) растворы хлоридов от соляной кислоты; г) бромиды, иодиды от хлоридов. Почему вместо раствора нитрата серебра(I) можно также использовать раствор нитрата свин- ца(II)? 2. Как можно доказать наличие свободного иода? Как обнаружить в продукте питания, например в белом хлебе, крахмал?
Мы с сыном сегодня только решали ее)
Задание 1.
1.
HCl + AgNO3 → AgCl + ΗΝO3
NaCl + AgNO3 → AgCl + HNO3
NaBr + AgNO3 → NaNO3 + AgBr
Kl + AgNO3 → KNO3 + AgI
или
2 HCl + Pb(NO3)2 → PbCl2 + 2 HNO3
2 NaCl + Pb(NO3)2 → PbCl2 + 2 NaNO3
2 NaBr + Pb(NO3)2 → 2 NaNO3 + PbBr2 ↓
2 KI + Pb(NO3)2 → 2 KNO3 + PbI2 ↓
Соляную кислоту обнаруживают реакцией с азотнокислым серебром:
HCl + AgNO3 → AgCl ↓ +HNO3,
при этом выделяется AgCl — белый творожистый
осадок.
б) Хлориды обнаруживают реакцией с концентрированным раствором перманганата калия в присутствии концентрированной серной кислоты. При этом происходит частичное или полное обесцвечивание раствора калия перманганата и выделение газообразного хлора. Выделяющийся хлор можно обнаружить по синему окрашиванию йодокрахмальной бумаги, характерному запаху хлора и др. В ионном виде уравнение будет выглядеть так:
10Сl — +2МnO4+16Н + → 2Мn+5Сl 2 ↑ +8Н2O.
в) Растворы хлоридов можно отличить от соляной кислоты с помощью индикаторов, которые изменяют свою окраску в зависимости от наличия гидрид-ионов.
г) Эти соли можно отличить по реакции с азотнокислым серебром, при этом образуются осадки разного цвета:
КСl + AgNO3 → АgСl(белый) + ΚΝO3
KBr + AgNO3 → AgBr (жeлτый) + KNO3
KI + AgNO3 → AgI (зeлeнoвaτый) + KNO3
Можно использовать раствор нитрата свинца (II), т.к. при взаимодействии данных веществ образуется характерный белый осадок.
2. Наличие свободного йода можно доказать с помощью крахмала, цвет которого становится синим. Так же можно обнаружить и крахмал в продуктах питания: можно добавить капельку раствора йода на продукт, если крахмал в нем имеется, то капля приобретет синий цвет.
Источник
Способы распознавания растворов хлоридов натрия
Решение качественных задач по определению веществ, находящихся в склянках без этикеток, предполагает проведение ряда операций, по результатам которых можно определить, какое вещество находится в той или иной склянке.
Первым этапом решения является мысленный эксперимент, представляющий собой план действий и их предполагаемые результаты. Для записи мысленного эксперимента используется специальная таблица-матрица, в ней обозначены формулы определяемых веществ по горизонтали и вертикали. В местах пересечения формул взаимодействующих веществ записываются предполагаемые результаты наблюдений: 

Решение задачи будет, следовательно, состоять из следующих этапов:
— предварительное обсуждение отдельных реакций и внешних характеристик веществ;
— запись формул и предполагаемых результатов попарных реакций в таблицу,
— проведение эксперимента в соответствии с таблицей (в случае экспериментальной задачи);
— анализ результатов реакций и соотнесение их с конкретными веществами;
— формулировка ответа задачи.
Необходимо подчеркнуть, что мысленный эксперимент и реальность не всегда полностью совпадают, так как реальные реакции осуществляются при определенных концентрации, температуре, освещении (например, при электрическом свете AgCl и AgBr идентичны). Мысленный эксперимент часто не учитывает многих мелочей. К примеру, Br2/aq прекрасно обесцвечивается растворами Na2CO3, На2SiO3, CH3COONa; образование осадка Ag3PO4 не идет в сильнокислой среде, так как сама кислота не дает этой реакции; глицерин образует комплекс с Сu (ОН) 2, но не образует с (CuOH)2SO4, если нет избытка щелочи, и т. д. Реальная ситуация не всегда согласуется с теоретическим прогнозом, и в этой главе таблицы-матрицы»идеала» и «реальности» иногда будут отличаться. А чтобы разбираться в том, что же происходит на самом деле, ищите всякую возможность работать руками экспериментально на уроке или факультативе (помните при этом о требованиях техники безопасности).
Пример 1. В пронумерованных склянках содержатся растворы следующих веществ: нитрата серебра, соляной кислоты, сульфата серебра, нитрата свинца, аммиака и гидроксида натрия. Не используя других реактивов, определите, в какой склянке раствор какого вещества находится.
Решение. Для решения задачи составим таблицу-матрицу, в которую будем заносить в соответствующие квадратики ниже пересекающей ее диагонали данные наблюдения результатов сливания веществ одних пробирок с другими.
Наблюдение результатов последовательного приливания содержимого одних пронумерованных пробирок ко всем другим:
1 + 2 — выпадает белый осадок; ;
1 + 3 — видимых изменений не наблюдается;
| Вещества | 1. AgNO3, | 2. НСl | 3. Pb(NO3)2, | 4. NH4OH | 5. NaOH |
| 1. AgNO3 | X | AgCl  белый белый | — | выпадающий осадок растворяется | Ag2O  бурый бурый |
| 2. НСl |  белый белый | X | PbCl2  белый, белый, | — | _ |
| 3. Pb(NO3)2 | — | белый PbCl2  | X | Pb(OH)2  помутнение) помутнение) | Pb(OH)2  белый белый |
| 4. NH4OH | — | — |  (помутнение) (помутнение) | — | |
| S. NaOH |  бурый бурый | — |  белый белый | — | X |
1 + 4 — в зависимости от порядка сливания растворов может выпасть осадок;
1 + 5 — выпадает осадок бурого цвета;
2+3— выпадает осадок белого цвета;
2+4— видимых изменений не наблюдается;
2+5 — видимых изменений не наблюдается;
3+4 — наблюдается помутнение;
3+5 — выпадает белый осадок;
4+5 — видимых изменений не наблюдается.
Запишем далее уравнения протекающих реакций в тех случаях, когда наблюдаются изменения в реакционной системе (выделение газа, осадка, изменение цвета) и занесем формулу наблюдаемого вещества и соответствующий квадратик таблицы-матрицы выше пересекающей ее диагонали:
| I. 1 + 2: | AgNO3 + НСl |  | AgCl  + HNO3; + HNO3; |
| II. 1 + 5: | 2AgNO3 + 2NaOH |  | Ag2O  + 2NaNO3 + H2O; + 2NaNO3 + H2O; |
бурый(2AgOH  Ag2O + H2O) Ag2O + H2O) | |||
| III. 2 + 3: | 2НСl + Рb(NO3)2 |  | РbСl2  + 2НNO3; + 2НNO3; |
| белый | |||
| IV. 3 + 4: | Pb(NO3)2 + 2NH4OH |  | Pb(OH)2  + 2NH4NO3; + 2NH4NO3; |
| помутнение | |||
| V. 3 + 5: | Pb(NO3)2 + 2NaOH |  | Pb(OH)2  + 2NaNO3 + 2NaNO3 |
| белый |
(при приливании нитрата свинца в избыток щелочи осадок может сразу раствориться).
Таким образом, на основании пяти опытов различаем вещества, находящиеся в пронумерованных пробирках.
Пример 2. В восьми пронумерованных пробирках (от 1 до 8) без надписей содержатся сухие вещества: нитрат серебра (1), хлорид алюминия (2), сульфид натрия (3), хлорид бария (4), нитрат калия (5), фосфат калия (6), а также растворы серной (7) и соляной (8) кислот. Как, не имея никаких дополнительных реактивов, кроме воды, различить эти вещества?
Решение. Прежде всего растворим твердые вещества в воде и отметим пробирки, где они оказались. Составим таблицу-матрицу (как в предыдущем примере), в которую будем заносить данные наблюдения результатов сливания веществ одних пробирок с другими ниже и выше пересекающей ее диагонали. В правой части таблицы введем дополнительную графу»общий результат наблюдения», которую заполним после окончания всех опытов и суммирования итогов наблюдений по горизонтали слева направо (см., например, с. 178).
| 1+2: | 3AgNO3 + A1C1, |  | 3AgCl  белый белый | + Al(NO3)3; |
| 1 + 3: | 2AgNO3 + Na2S |  | Ag2S  черный черный | + 2NaNO3; |
| 1 + 4: | 2AgNO3 + BaCl2 |  | 2AgCl  белый белый | + Ba(NO3)2; |
| 1 + 6: | 3AgN03 + K3PO4 |  | Ag3PO4  желтый желтый | + 3KNO3; |
| 1 + 7: | 2AgNO3 + H2SO4 |  | Ag,SO4  белый белый | + 2HNOS; |
| 1 + 8: | AgNO3 + HCl |  | AgCl  белый белый | + HNO3; |
| 2 + 3: | 2AlCl3 + 3Na2S + 6H2O |  | 2Al (OH)3, | + 3H2S  + 6NaCl; + 6NaCl; |
(Na2S + H2O  NaOH + NaHS, гидролиз); NaOH + NaHS, гидролиз); | ||||
| 2 + 6: | AlCl3 + K3PO4 |  | A1PO4  белый белый | + 3KCl; |
| 3 + 7: | Na2S + H2SO4 |  | Na2SO4 | + H2S |
| 3 + 8: | Na2S + 2HCl |  | -2NaCl | + H2S ; ; |
| 4 + 6: | 3BaCl2 + 2K3PO4 |  | Ba3(PO4)2  белый белый | + 6KC1; |
| 4 + 7 | BaCl2 + H2SO4 |  | BaSO4  белый белый | + 2HC1. |
Видимых изменений не происходит только с нитратом калия.
По тому, сколько раз выпадает осадок и выделяется газ, однозначно определяются все реагенты. Кроме того, ВаС12 и К3РО4 различают по цвету выпавшего осадка с AgNO3: AgCl — белый, a Ag3PO4 — желтый. В данной задаче решение может быть более простым — любой из растворов кислот позволяет сразу выделить сульфид натрия, им определяются нитрат серебра и хлорид алюминия. Нитратом серебра определяются среди оставшихся трех твердых веществ хлорид бария и фосфат калия, хлоридом бария различают соляную и серную кислоты.
Пример 3. В четырех пробирках без этикеток находятся бензол, хлоргексан, гексан и гексен. Используя минимальные количества и число реактивов, предложите метод определения каждого из указанных веществ.
Решение. Определяемые вещества между собой не реагируют, таблицу попарных реакций нет смысла составлять.
Существует несколько методов определения данных веществ, ниже приведен один из них.
Бромную воду обесцвечивает сразу только гексен:
Хлоргексан можно отличить от гексана, пропуская продукты их сгорания через раствор нитрата серебра (в случае хлоргексана выпадает белый осадок хлорида серебра, нерастворимый в азотной кислоте, в отличие от карбоната серебра):
2С6Н14+ 19O2= 12СO2+ 14Н2О;
С6Н13Сl + 9O2 = 6СO2 + 6Н2O + НС1;
HCl + AgNO3 = AgCl 
Бензол отличается от гексана по замерзанию в ледяной воде (у С6Н6 т. пл.= +5,5°С, а у С6Н14т. пл. = -95,3°С).
1. В два одинаковых химических стакана налиты равные объемы: в один воды, в другой — разбавленного раствора серной кислоты. Как, не имея под рукой никаких химических реактивов, различить эти жидкости (пробовать растворы на вкус нельзя)?
2. В четырех пробирках находятся порошки оксида меди(II), оксида железа (III), серебра, железа. Как распознать эти вещества, используя только один химический реактив? Распознавание по внешнему виду исключается.
3. В четырех пронумерованных пробирках находятся сухие оксид меди (II), сажа, хлорид натрия и хлорид бария. Как, пользуясь минимальным количеством реактивов, определить, в какой из пробирок находится какое вещество? Ответ обоснуйте и подтвердите уравнениями соответствующих химических реакций.
4. В шести пробирках без надписей находятся безводные соединения: оксид фосфора(V), хлорид натрия, сульфат меди, хлорид алюминия, сульфид алюминия, хлорид аммония. Как можно определить содержимое каждой пробирки, если имеется только набор пустых пробирок, вода и горелка? Предложите план анализа.
5. В четырех пробирках без надписей находятся водные растворы гидроксида натрия, соляной кислоты, поташа и сульфата алюминия. Предложите способ определения содержимого каждой пробирки, не применяя дополнительных реактивов.
6. В пронумерованных пробирках находятся растворы гидроксида натрия, серной кислоты, сульфата натрия и фенолфталеин. Как различить эти растворы, не пользуясь дополнительными реактивами?
7. В банках без этикеток находятся следующие индивидуальные вещества: порошки железа, цинка, карбоната кальция, карбоната калия, сульфата натрия, хлорида натрия, нитрата натрия, а также растворы гидроксида натрия и гидроксида бария. В Вашем распоряжении нет никаких других химических реактивов, в том числе и воды. Составьте план определения содержимого каждой банки.
8. В четырех пронумерованных банках без этикеток находятся твердые оксид фосфора (V) (1), оксид кальция (2), нитрат свинца (3), хлорид кальция (4). Определить, в какой из банок находится каждое из указанных соединений, если известно, что вещества (1) и (2) бурно реагируют с водой, а вещества (3) и (4) растворяются в воде, причем полученные растворы (1) и (3) могут реагировать со всеми остальными растворами с образованием осадков.
9. В пяти пробирках без этикеток находятся растворы гидроксида, сульфида, хлорида, йодида натрия и аммиака. Как определить эти вещества при помощи одного дополнительного реактива? Приведите уравнения химических реакций.
10. Как распознать растворы хлорида натрия, хлорида аммония, гидроксида бария, гидроксида натрия, находящиеся в сосудах без этикеток, используя лишь эти растворы?
11.. В восьми пронумерованных пробирках находятся водные растворы соляной кислоты, гидроксида натрия, сульфата натрия, карбоната натрия, хлорида аммония, нитрата свинца, хлорида бария, нитрата серебра. Используя индикаторную бумагу и проводя любые реакции между растворами в пробирках, установить, какое вещество содержится в каждой из них.
12. В двух пробирках имеются растворы гидроксида натрия и сульфата алюминия. Как их различить, по возможности, без использования дополнительных веществ, имея только одну пустую пробирку или даже без нее?
13. В пяти пронумерованных пробирках находятся растворы перманганата калия, сульфида натрия, бромная вода, толуол и бензол. Как, используя только названные реактивы, различить их? Используйте для обнаружения каждого из пяти веществ их характерные признаки (укажите их); дайте план проведения анализа. Напишите схемы необходимых реакций.
14. В шести склянках без наименований находятся глицерин, водный раствор глюкозы, масляный альдегид (бутаналь), гексен-1, водный раствор ацетата натрия и 1,2-дихлорэтан. Имея в качестве дополнительных химических реактивов только безводные гидроксид натрия и сульфат меди, определите, что находится в каждой склянке.
1. Для определения воды и серной кислоты можно использовать различие в физических свойствах: температурах кипения и замерзания, плотности, электропроводности, показателе преломления и т. п. Самое сильное различие будет в электропроводности.
2. Прильем к порошкам в пробирках соляную кислоту. Серебро не прореагирует. При растворении железа будет выделяться газ: Fe + 2HCl = FeCl2 + H2
Оксид железа (III) и оксид меди (II) растворяются без выделения газа, образуя желто-коричневый и сине-зеленый растворы: Fe2O3 + 6HCl = 2FeCl3 + 3H2O; CuO + 2HCl = CuCl2 + H2O.
3. CuO и С — черного цвета, NaCl и ВаВr2 — белые. Единственным реактивом может быть, например, разбавленная серная кислота H2SO4:
CuO + H2SO4 = CuSO4 + H2O (голубой раствор); BaCl2 + H2SO4 = BaSO4 
С сажей и NaCl разбавленная серная кислота не взаимодействует.
4. Небольшое количество каждого из веществ помещаем в воду:
CuSO4+5H2O = CuSO4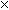 5H2O 5H2O | (образуется голубой раствор и кристаллы); |
Al2S3 + 6H2O = 2Al(OH)3  + 3H2S + 3H2S | (выпадает осадок и выделяется газ с неприятным запахом); |
AlCl3 + 6H2O = A1C13 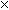 6H2O + Q AlCl3+ H2O 6H2O + Q AlCl3+ H2O  AlOHCl2+ HCl AlOHCl2+ HCl AlOHC12 + H20 = Al (OH) 2Cl + HCl А1(ОН)2С1 + Н2О = А1(ОН)2 + НСl | (протекает бурная реакция, образуются осадки основных солей и гидроксида алюминия); |
| P2O5 + H2O = 2HPO3 HPO3+H2O = H3PO4 | (бурная реакция с выделением большого количества тепла, образуется прозрачный раствор). |
Два вещества — хлорид натрия и хлорид аммония— растворяются, не реагируя с водой; их можно различить, нагревая сухие соли (хлорид аммония возгоняется без остатка): NH4Cl 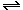


5. Составим таблицу попарных взаимодействий указанных реагентов
| Вещества | 1. NaOH | 2 НСl | 3. К2СО3 | 4. Аl2(SO4)3 | Общий результат наблюдения |
| 1, NaOH | — | — | Al(OH)3 | 1 осадок | |
| 2. НС1 | _ | CO2 | __ | 1 газ | |
| 3. К2СО3 | — | CO2 | Al(OH)3  CO2  | 1 осадок и 2 газа | |
| 4. Al2(S04)3 | А1(ОН)3 | — | А1(ОН)3 CO2  | 2 осадка и 1 газ | |
| NaOH + HCl = NaCl + H2O | |||||
| К2СO3 + 2HC1 = 2КС1 + Н2O + СO2 | |||||
3K2CO3 + Al2(SO4)3 + 3H2O = 2 Al(OH)3 

Al2(SO4)3 + 6NaOH = 2Al(OH)3  + 3Na2SO4 + 3Na2SO4 | (наличие осадка зависит от порядка сливания и избытка и щелочи) |
| Al(OH)3 + NaOH + 2H2O = Na[Al(OH)4(H2O)2] |
Исходя из представленной таблицы по числу выпадения осадка и выделения газа можно определить все вещества.
6. Попарно смешивают все растворы Пара растворов, дающая малиновую окраску, — NaOH и фенолфталеин Малиновый раствор прибавляют в две оставшиеся пробирки. Там, где окраска исчезает, — серная кислота, в другой — сульфат натрия. Остается различить NaOH и фенолфталеин (пробирки 1 и 2).
А. Из пробирки 1 прибавляют каплю раствора к большому количеству раствора 2.
Б. Из пробирки 2 — каплю раствора прибавляют к большому количеству раствора 1. В обоих случаях— малиновое окрашивание.
К растворам А и Б прибавляют по 2 капли раствора серной кислоты. Там, где окраска исчезает, содержалась капля NaOH. (Если окраска исчезает в растворе А, то NaOH — в пробирке 1).
7.
| Вещества | Fe | Zn | СаСО3 | К2СО3 | Na2SO4 | NaCl | NaNO3 |
| Ва(ОН)2 | осадок | осадок | раствор | раствор | |||
| NaOH | возможно выделение водорода | раствор | раствор | раствор | раствор | ||
| Осадка нет в случае двух солей у Ва(ОН)2 и в случае четырех солей У NaOH | темные порошки (раствсворяющийся в щелочах — Zn, нерастворяющийся в щелочах — Fe) | СаСО3 дает осадок с обеими щелочами | дают по одному осадку, различаются по окрашиванию пламени: К + — фиолетовое, Na+ — желтое | осадков не дают; различаются поведением при нагревании (NaNO3 плавится, а потом разлагается с выделением О2, затем NО2 | |||
8. Бурно реагируют с водой: Р2О5 и СаО с образованием соответственно H3PO4 и Са(ОН)2:
Р2O5 + 3Н2О = 2Н3РO4, СаО + Н2О = Са(ОН)2.
Вещества (3) и (4) -Pb(NO3)2 и СаСl2 — растворяются в воде. Растворы могут реагировать друг с другом следующим образом:
| Вещества | 1. Н3РО4 | 2. Са(ОН)2, | 3. Pb(NO3)2 | 4. CaCl2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1. Н3РО4 | CaHPO4  | PbHPO4 | CaHPO4 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 2. Са(ОН)2 | СаНРО4 | Pb(OH)2 | — | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 3. Pb(NO3)2 | РbНРО4 | Pb(OH)2 | РbСl2 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 4. СаС12 | CaHPO4 | PbCl2 |
| Вещества | 1. NaCl | 2. NH4C1 | 3. Ba(OH), | 4. NaOH | Общий результат наблюдения |
| 1. NaCl | ___ | _ | _ | взаимодействия не наблюдается | |
| 2. NH4Cl | _ | X | NH3 | NH3 | в двух случаях выделяется газ |
| 3. Ва(ОН)2 | — | NH3 | X | — | в одном случае выделяется газ |
| 4. NaOH | — | NH3 | — | X | в одном случае выделяется газ |
NaOH и Ва(ОН)2 можно различить по разному окрашиванию пламени (Na+ окрашивают в желтый цвет, а Ва 2 + — в зеленый).
11. Определяем кислотность растворов с помощью индикаторной бумаги:
1) кислая среда —НСl, NH4C1, Pb(NO3)2;
2) нейтральная среда — Na2SO4, ВаС12, AgNO3;
3) щелочная среда — Na2CO3, NaOH. Составляем таблицу:
| Вещества | AgNO3 | ВаС12 | HCl | NaOH | Na2SO4 | Na2CO3 | NH4C1 | Pb(NO3)2 |
| НС1 | AgCl | — | X | — | — | CO2 | _ | PbCl2 |
| NaOH | Ag2O | — | — | X | — | — | NH3 | Pb(OH)2 |
| Na2SO4 | может выпасть Ag2SO4  | BaSO4 | — | — | X | — | — | PbSO4 |
| Na2CO3 | Ag2O | BaCO3 | CO2 | — | — | X | NH3 | Pb(OH)2 |
| NH4C1 | AgCl | — | NH3 | — | NH3 | X | PbCl2 | |
| Pb(NO3)2 | — | PbCl2 | PbCl2 | Pb(OH)2 | PbSO4 | PbCO3 Pb(OH)2 Pb(OH)2 | PbCl2 | X |
| ВаС12 | AgCl | X | — | — | BaSO4 | BaCO3 | — | PbCl2 |
| AgNO3 | X | AgCl | AgCl | Ag2O | Ag2SO4  | Ag2O | AgCl | — |
12. В пустую пробирку наливают один из растворов и приливают каплю другого.
С л у ч а й п е р в ы й : образовался осадок и сразу растворился, или вовсе не образовался:
6NaOH + Al2(SO4)3 

Al(OH)3 + NaOH (избыток) + 2Н2О 
С л у ч а й в т о р о й : осадок образовался и не растворился. Тогда, наоборот, раствор (1) — Al2(SO4)3, а раствор (2)—NaOH.
13. По цвету определяют КМпО4 (розово-фиолетовый) и бромную воду (желтая или красно-бурая).
Раствор брома в воде определится сразу при взаимодействии с Na2S:
Na2S + Br2 

Раствор КМnО4 обесцвечивается Na2S и толуолом при кипячении:
2KMnO4 + 3Na2S + 4H2O 



Оставшееся вещество — бензол.
14. Прибавим последовательно сульфат меди и избыток гидроксида натрия ко всем веществам. С гексеном-1, ацетатом натрия, 1,2-дихлорэтаном реакция идти не будет, но в водном растворе ацетата натрия сульфат меди растворится. В пробирке с бу-таналем при нагревании выпадает красный осадок оксида меди(1). В пробирках с глицерином и глюкозой получится темно-синий раствор. При нагревании раствора глюкозы с добавленными реагентами выпадает оксид меди(1). Оставшиеся вещества, не смешивающиеся друг с другом, можно различить по плотности: гексен-1 имеет наименьшую плотность, а 1,2-дихлорэтан — наибольшую.


Сервер создается при поддержке Российского фонда фундаментальных исследований
Не разрешается копирование материалов и размещение на других Web-сайтах
Вебдизайн: Copyright (C) И. Миняйлова и В. Миняйлов
Copyright (C) Химический факультет МГУ
Написать письмо редактору
Источник




