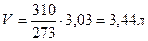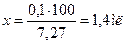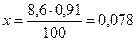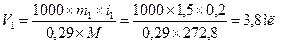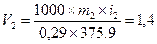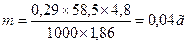Расчеты изотонических концентраций
ИЗОТОНИЧЕСКИЕ РАСТВОРЫ
ПЛАН ЛЕКЦИИ
ИЗОТОНИЧЕСКИЕ И ПЛАЗМОЗАМЕЩАЮЩИЕ РАСТВОРЫ
ЛЕКЦИЯ 27
1. Изотонические растворы.
2. Расчет изотонических концентраций.
3. Плазмозамещающие растворы.
4. Сложные солевые растворы
Растворы, у которых осмотическое давление равно осмотическому давлению плазмы крови, называются изотоническими. Кровяная плазма, лимфа, слезная и спинномозговая жидкости имеют постоянное осмотическое давление, которое поддерживается специальными осморегуляторами. Введение в кровяное русло больших количеств инъекционных растворов с другим значением осмотического давления может привести к сдвигу осмотического равновесия и вызвать тяжелые последствия. Это связано со следующими обстоятельствами. Как известно, клеточная оболочка полупроницаема. Она способна пропускать воду и не пропускать растворенные в ней вещества. Если ввести в кровь раствор с высоким осмотическим давлением (гипертонический раствор), возникнет разность осмотических давлений внутри эритроцитов и в окружающей их плазме. Жидкость из эритроцитов направится в плазму. Эритроциты сморщиваются. Такое явление называется плазмолизом. Если же ввести раствор с малым осмотическим давлением (гипотонический раствор), то жидкость пойдет внутрь клетки. Эритроцит разбухает, клеточная оболочка может лопнуть, а клетка — погибнуть. Это опасное явление называется гемолизом (лизисом). Чтобы избежать осмотических сдвигов, многие инфузионные растворы изотонируют — доводят их осмотическое давление до осмотического давления биологических жидкостей организма. В норме это 7,4 атм (или 0,74 МПа).
Для расчета изотонических концентраций применяют несколько методов:
1) на основании закона Вант-Гоффа. Согласно закону Вант-Гоффа, разбавленные растворы неэлектролитов ведут себя аналогично газам и поэтому подчиняются газовым законам. Исходя из этого, 1 моль любого недиссоциирующего вещества при t= 0° С и давлении Р=1 атм занимает объем V= 22,4 л. Чтобы создать давление 7,4 атм, необходимо растворить вещество в меньшем объеме:
V2 =
Учитывая, что осмотическое давление в растворе пропорционально температуре, вносят поправку на t.
t тела= 37°С = 310 К
t°раствора= 0°С = 273 К
Следовательно, чтобы получить изотонический раствор, 1 моль вещества необходимо растворить в 3,44 л воды. Тогда для приготовления 1 л раствора необходимо 0,29 М вещества:
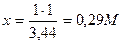
(Муравьев И.А. называет фактором изотонии электролитов)
Так, для приготовления 1 л изотонического раствора глюкозы необходимо:
М.м. глюкозы = 180
0,29 ∙ 180 = 52,2 г
Изотоническая концентрация глюкозы:
Аналогично проводят расчет изотонической концентрации гексаметилентетрамина:
2) Фактор изотонии можно вывести и из уравнения Менделеева-Клапейрона:
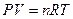
Произведение давления раствора на его объем прямо пропорционально числу грамм-молей и температуре. Число молей — это масса вещества, деленная на молекулярную массу. Подставим в уравнение Менделеева-Клапейрона:
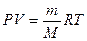
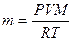
R — универсальная газовая постоянная = 0, 082 атмосферо-литров.
Т — абсолютная температура.
Приведенные расчеты верны, если речь идет о неэлектролитах. Если же растворяют в воде электролиты необходимо учитывать, что в растворе они диссоциируют на ионы.
Осмотическое давление будет тем больше , чем выше степень диссоциации. В уравнение для расчета количества вещества m = 0,29 М вводится изотонический коэффициент i. Он показывает, во сколько раз возрастает осмотическое давление раствора вследствие диссоциации и во столько раз меньше необходимо взять вещества для получения изотонического раствора
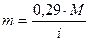
и во столько раз меньше необходимо взять вещества для получения изотонического раствора.
Коэффициент i рассчитывают по формуле

где a – степень электролитической диссоциации;
m– число частиц, образующихся из 1 молекулы при диссоциации.
Для разных групп электролитов коэффициент i может быть рассчитан следующим образом:
а) для бинарных электролитов с однозарядными ионами типа К + А —
(a= 0,86, m ∙ = 2), i = 1 + 0,86 (2-1) = 1,86
Относятся NaCl, KCl, NaNO3 , AgNO3 , пилокарпина гидрохлорид, эфедрина гидрохлорид.
б) для бинарных электролитов с двузарядными ионами типа K 2+ A 2- .
(a=0,5; m = 2), i = 1 + 0,5 (2-1) = 1,5
Относятся: ZnSO4 , MgSO4 , CuSO4 , FeSO4 , атропина сульфат.
в) для тринарных электролитов типа K + A 2- ; K 2+ A —
(a=0,75; m =3), i = 1+ 0,75 (3-1) = 2,5
г) для слабых электролитов i = 1,1.
Относятся: борная кислота, лимонная кислота.
В практической работе изотоничность растворов часто достигается с помощью других веществ, вводимых в лекарственную форму. Это бывает в тех случаях, когда основные вещества прописаны в количествах, не обеспечивающих изотоничность раствора. Чаще всего используют в качестве изотонирующих агентов NaCl, Na2SO4 или NaNO3 .
Rp.: Papaverini hydrochloridi 0,1
Natrii chloridi q. s.
ut f. solutio isotonica 10,0
Прописан 1 % раствор папаверина гидрохлорида. Вначале рассчитаем его изотоническую концентрацию:
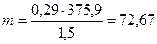
Чтобы получить 10 мл изотонического раствора попаверина гидрохлорида, необходимо было бы его взять 7,27 на 100 мл или 0,73 на 10 мл, а по прописи — только 0,1. Необходимо вводить дополнительное вещество — NaCl.
Определим теперь, какое количество раствора может быть изотонировано 0,1 г вещества:
На долю NaCl приходится 8,6 мл раствора. Его нужно взять:
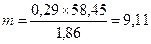
В работе для расчета изотонирующих веществ используют формулы.
1. Если изотоничность раствора достигается одним веществом

m — количество вещества, добавляемого для получения изотонического раствора (г);

V — объем прописанного раствора (мл);
M — молекулярная масса вещества.
2. Если изотоничность раствора вещества достигается с помощью другого (дополнительного) вещества
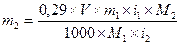
M1 — молекулярная масса основного вещества;
M2— молекулярная масса дополнительного вещества;
m1 — количество основного вещества, в г;
m2 — количество дополнительного вещества, в г;
V — объем прописанного раствора, в мл.
3. При более сложных прописях (с тремя и более компонентами) сначала находят, какой объем изотонического раствора могут дать вещества, количества которых известны. Затем по разности определяют, какой V приходится на долю дополнительного вещества. Потом определяют и его количество.
Rp.: Novocaini hydrochloridi 0,2
Papaverini hydrochloridi 0,1
Natrii chloridi q. s.
Aq. pro inject. 10 ml ut f. solutio isotonica
По закону Дальтона, осмотическое давление многокомпонентного раствора складывается из парциальных давлений отдельных компонентов:
На долю каждого компонента приходится изотонирование соответствующего объема раствора
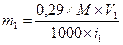
10 мл — 5,2 мл = 4,8 мл
Количество натрия хлорида:
3). Криоскопический метод (расчет на основе закона Рауля) Согласно следствию из закона Рауля, понижение температуры замерзания раствора прямо пропорционально его концентрации: Dt = K ∙ C,
где: Dt — депрессия (понижение) температуры замерзания раствора;
C — концентрация раствора;
K — криоскопическая константа.
Отсюда изотонические растворы любых солей замерзают при одной и той же температуре, т. е. имеют одинаковую температурную депрессию. Депрессия сыворотки крови 0,52°С. Если приготовленный раствор будет иметь такую же депрессию, он будет изотоничен сыворотке крови.
Для расчетов установлены температурные депрессии 1% растворов фармацевтических субстанций (приводятся в специальных таблицах). Например, ∆t 1 % раствора глюкозы 0,1. Отсюда легко рассчитать изотоническую концентрацию глюкозы:
х% – 0,52 х = 0,52/0,1 = 5,2 %
Общей для расчета является формула:
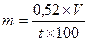
m — количество вещества в г, необходимое для изотонирования;
V — объем раствора;
t — температурная депрессия 1 % раствора.
При расчете многокомпонентных систем пользуются следующими формулами.
При двух компонентах в прописи:
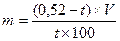
При трех и более компонентах:
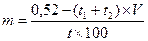
Rp.: Novocaini 0,2
Natrii chloridi q. s.
ut f. sol. isotonica 20,0
Депрессия температуры замерзания 1 % раствора новокаина Dt = 0,15, 2% раствора – 0,30.
Депрессия 1 % раствора глюкозы 0,1.
Депрессия 1 % раствора NaCl — 0,576 .
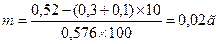
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Источник
РАСЧЕТ ИЗОТОНИЧЕСКИХ КОНЦЕНТРАЦИЙ РАСТВОРОВ С ИСПОЛЬЗОВАНИЕМ ИЗОТОНИЧЕСКИХ ЭКВИВАЛЕНТОВ



ПО НАТРИЯ ХЛОРИДУ
Преимущества метода (является фармакопейным):
Ø наиболее часто применим в аптечной практике.
| Изотонический эквивалент по натрия хлориду (Э) – количество натрия хлорида, которое создает в одинаковых условиях осмотическое давление, равное осмотическому давлению, созданному 1,0 лекарственного вещества |
| Наименование лека- рственных веществ | Эквивалент веществ по NaCl | Изотоническая концентрация, % |
| Натрия хлорид (NaCl) | — | 0,9 |
| Натрия нитрат (NaNО2) | 0,66 | 1,3 |
| Натрия сульфат (Na2SО4) | 0,23 | 3,9 |
| Глюкоза (безводная) (C6H12O6) | 0,18 | 5,2 |
| Кислота борная (H3BO3) | 0,53 | 1,7 |
2. МЕТОДЫ РАСЧЕТА ИЗОТОНИЧЕСКИХ КОНЦЕНТРАЦИЙ РАСТВОРОВ
РАСЧЕТ ИЗОТОНИЧЕСКИХ КОНЦЕНТРАЦИЙ РАСТВОРОВ ПО ЗАКОНУ РАУЛЯ (КРИОСКОПИЧЕСКИЙ МЕТОД)
| Давление пара над раствором пропорционально молярной доле растворенного вещества |
Закон Рауля

Ø понижение температуры замерзания (депрессия) пропорционально понижению давления пара и пропорционально концентрации растворённого вещества в растворе;
Ø изотонические растворы различных веществ замерзают при одной и той же температуре, т. е. имеют одинаковую температурную депрессию 0,52°С (депрессия сыворотки крови).
| Депрессия (понижение) температуры замерзания 1 % раствора лекарственного вещества (Δt) показывает, на сколько градусов понижается температура замерзания 1% раствора лекарственного вещества по сравнению с температурой замерзания растворителя |
Если приготовленный раствор какого-либо вещества будет иметь депрессию, равную 0,52°С, он будет изотоничен сыворотке крови.
| % |
| 0,52 С Δt |
| Х = |
1% – Δt (справочные данные)
| v |
| 100 |
| Δt |
| 0,52 º С · V |
| m = |
m — количество лекарст- венного вещества, необходимое для изотонирования, г;
V – объем, мл
2. МЕТОДЫ РАСЧЕТА ИЗОТОНИЧЕСКИХ КОНЦЕНТРАЦИЙ РАСТВОРОВ
Rp.: Sol. Glucosi 3% 100 ml isotonicae Sterilisa!
D. S. Для внутривенного введения.
Данный лекарственный препарат – инъекционный раствор для внутривенного введения, требующий стабилизации.
ППК (обратная сторона)
1) по Вант-Гоффу: m = 0,29 М; М = 180
m = 0,29 · 180 = 52
т.е. изотоническая концентрация раствора глюкозы – 5,2%
2) по закону Рауля: 1% – 0,104 ºС
3) по изотоническому эквиваленту по NaCl: Эглюкозы = 0,18 0,18 NaCl – 1,0 глюкозы
т.е. изотоническая концентрация глюкозы — 5 %
Натрия хлорида для доизотонирования
Ø 1,0 глюкозы – 0,18 NaCl 3,0 глюкозы
– х х = 0,54 0,9 – 0,54 = 0,36
Ø Объем, изотонируемый 3,0 глюкозы
Ø Непроизотонированный объем воды: 100 – 60 = 40 мл Натрия хлорида 0,9 – 100 мл
х – 40 мл х = 0,36
Ø Количество глюкозы, недостающее для изотоничности раствора: 5,0 — 3,0 = 2,0
2. МЕТОДЫ РАСЧЕТА ИЗОТОНИЧЕСКИХ
КОНЦЕНТРАЦИЙ РАСТВОРОВ
Количество натрия хлорида: 0,18 NaCl – 1,0 глюкозы
х – 2,0 глюкозы х = 0,36
Глюкозы безводной 3,0
Глюкозы (вл. 9%) а – масса глюкозы
Стабилизатора Вейбеля: 5 мл
(5 % от объема независимо от концентрации глюкозы)
Воды для инъекций до 100 мл
В асептических условиях в стерильную мерную колбу на 100 мл помещают 3,3 г глюкозы (влажность 9 %) и 0,36 г натрия хлорида, добавляют часть воды для инъекций и растворяют, добавляют
5 мл стабилизатора Вейбеля, перемешивают и доводят водой для инъекций до метки.
Проводят качественный и количественный анализ, фильтруют и укупоривают резиновой пробкой. Проводят контроль на механические примеси, закупоривают под обкатку металлическим колпачком и стерилизуют при 120°С 8 мин сразу после приготовления. После стерилизации проводят вторичный контроль качества. Оформляют к отпуску номером рецепта и этикетками «Для инъекций», «Стерильно».
Источник