- NSICU.RU neurosurgical intensive care unit сайт отделения реанимации НИИ им Н.Н. Бурденко
- Курсы повышения квалификации
- Внутричерепная гипертензия
- Асинхронии и графика ИВЛ
- Водно-электролитные нарушения в нейрореанимации
- Книга «Основы ИВЛ»
- Рекомендации по интенсивной терапии у пациентов с нейрохирургической патологией
- Статьи → Вентиляционные стратегии в нейрореанимации: ИВЛ в отделении реанимации НИИ нейрохирургии в 2010г (публикация на сайте)
- Введение
- Материалы и методы
- Методы протекции дыхательных путей
- Методика ухода за дыхательными путями
- Санация ротоглотки
- Методика проведения ИВЛ
- Методика увлажнения дыхательных путей
- Результаты и обсуждение
- Способы протекции верхних дыхательных путей
NSICU.RU neurosurgical intensive care unit
сайт отделения реанимации НИИ им Н.Н. Бурденко
Курсы повышения квалификации

Внутричерепная гипертензия

Асинхронии и графика ИВЛ

Водно-электролитные
нарушения
в нейрореанимации

Книга «Основы ИВЛ»

Рекомендации
по интенсивной терапии
у пациентов
с нейрохирургической патологией
Статьи → Вентиляционные стратегии в нейрореанимации: ИВЛ в отделении реанимации НИИ нейрохирургии в 2010г (публикация на сайте)
НИИ нейрохирургии им. акад. Н.Н. Бурденко РАМН, Москва
Введение
Первые отделения интенсивной терапии (ОИТ), где использовалась длительная ИВЛ для спасения жизни пациентов и лечения заболевания, были созданы в Европе в 1952 во время эпидемии полиомиелита. По существу первые ОИТ были отделениями нейроинтенсивной терапии для лечения пациентов с повреждением ЦНС. В настоящее время в мире по данным исследовательской группы профессора Pelosi среди пациентов ОИТ не менее 20% находится на ИВЛ по неврологическим показаниям [1]. Пациенты неврологических и нейрохирургических клиник, нуждающиеся в ИВЛ, имеют важное отличие от пациентов ОИТ общего профиля. Показанием для проведения ИВЛ в нейро-ОИТ является не заболевание легких рестриктивного или обструктивного типа, а нарушение работы дыхательного центра вследствие прямого или опосредованного повреждения ствола мозга или нарушение нервно-мышечной проводимости, приводящее к слабости дыхательной мускулатуры. Эта специфика показаний для ИВЛ обуславливает особенности выбора режимов ИВЛ и стратегии прекращения респираторной поддержки. В настоящей работе представлен годовой анализ использования продолжительной ИВЛ в лечении пациентов в отделении реанимации НИИ нейрохирургии им академика Н.Н. Бурденко РАМН за 2010 год.
Материалы и методы
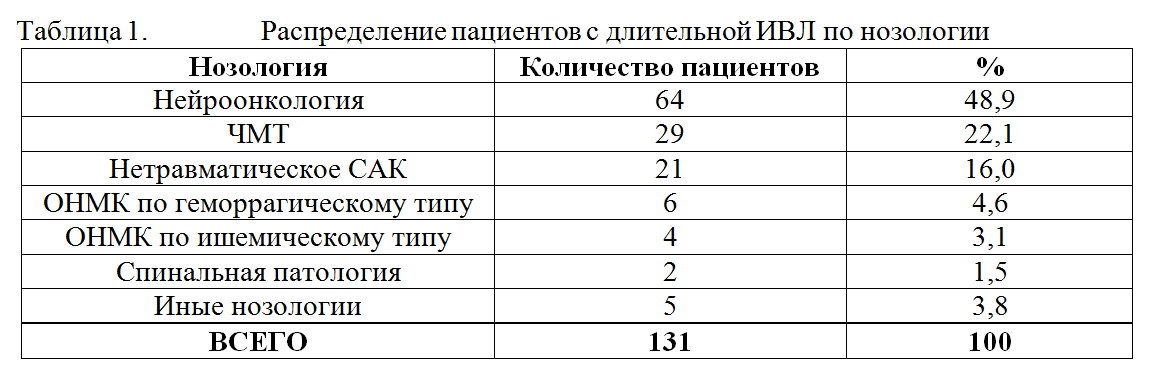
Исследование носило ретроспективный характер и было основано на анализе историй болезни пациентов, находившихся на лечении в отделении реанимации с января 2010 по декабрь 2010 г включительно. Критерием включения являлась продолжительность ИВЛ свыше 48 часов. Анализировалась длительность ИВЛ, показания к пролонгированию ИВЛ у разных категорий больных, сроки экстубации, сроки трахеостомии, частота развития вентилятор-ассоциированной пневмонии. Согласно критериям включения, для анализа была отобрана 131 история болезни. Среди включенных в исследование пациентов было 77 мужчин и 54 женщины в возрасте от 2 месяцев до 81 года (средний возраст составил 34,5±19,6 лет). Среди пациентов, потребовавших проведения пролонгированной ИВЛ, было 64 пациента с нейроонкологией, 29 пациентов с ЧМТ, 21 пациент с САК, 6 пациентов с геморрагическим инсультом, 4 пациента с ишемическим инсультом, 2 пациента со спинальной патологией и 5 пациентов с иными нозологиями. В таблице 1 представлено разделение пациентов, нуждавшихся в пролонгированной ИВЛ, по нозологии.
Методы протекции дыхательных путей
У 89 (67,9%) пациентов, получавших пролонгированную ИВЛ, была выполнена пункционная дилятационная трахеостомия. Показаниями для выполнения трахеостомии были: Ожидаемая длительная ИВЛ (>7 cуток); Грубые нарушения глотания [2]; Удаление опухоли трансоральным доступом. Всем взрослым пациентам пункционно-дилятационная трахеостомия (ПДТ) выполнялась по модификации, разработанной в Институте [3,4,5]. Во всех сложных случаях (короткая, толстая шея, положение без валика под плечами или иное нарушение анатомических ориентиров) на этапе пункции трахеи выполняется фиброскопический контроль.
Методика ухода за дыхательными путями
Уход за трахеостомой. Кожа вокруг трахеостомы обрабатывалась раствором «Октенисепт», затем на область вокруг стомы накладывалась мазь «Бетадин» на основе повидон-йода и стерильные салфетки. Перевязки выполнялись 2 раза в сутки, а в случае пропитывания салфеток отделяемым из стомы — чаще. Использовался условный критерий «вокруг трахеостомы всегда чистая, сухая салфетка». Санация носовых ходов выполнялась минимум 3-4 раза в сутки с использованием тонкого мягкого санационного катетера. После санации в носовые ходы впрыскивалась аэрозоль «Биопарокс». При обильном отделении слизи из носовых ходов, аспирация слизи производилась чаще, дополнительно использовались препараты на основе ксилометазолина («Нафтизин», «Галазолин»). В 9 случаях, при выявлении синуситов выполнялись лечебные пункции гайморовых пазух с отмыванием содержимого раствором «мирамистин» и последующим введением антибиотиков.
Санация ротоглотки
Полость рта и зубы обрабатывались с использованием раствора и аэрозоля «Гексорал» два раза в сутки или чаще. Для механического удаления густой слизи и налётов использовались палочки с ватными тампонами на конце. Часть трахеостомированных пациентов на ИВЛ получала пероральное кормление. В этом случае рот обрабатывали после каждого кормления, начиная с полоскания рта чистой водой. Для ротоглотки использовались гибкие мягкие санационные катетеры и твердые пластиковые изогнутой формы. Санация трахеи выполнялась с использованием гибких одноразовых стерильных катетеров. После однократного использования катетер выбрасывался. При наличии избыточного количества мокроты гнойного характера при санации использовался 0,1% раствор диоксидина, ex-temporo приготовленный на физиологическом растворе. При санационных фибробронхоскопиях использовался такой же раствор. У всех трахеостомированных пациентов были использованы трахеостомические трубки с каналом для санации надманжеточного пространства и особо мягкой герметизирующей манжетой – трубки фирмы «Portex» серии «Blue line Ultra Soft Seal». Использование таких трубок позволяло эффективно удалять из трахеи секрет, скапливающийся выше герметизирующей манжеты, и промывать верхние отделы трахеи и гортань.
Методика проведения ИВЛ
Искусственная вентиляция легких проводилась с использованием аппаратов Puritan Bennet 7200, Hamilton G5, Hamilton Raphael, Puritan Bennet 840. В качестве стартовых режимов ИВЛ мы использовали режимы SIMV, управляемые по объему или по давлению (272 пациента), режим ASV (33 пациента) и режим DuoPAP (10 пациентов).
В качестве стартового режима SIMV использовался в 272 случаях. Дыхательный объем составлял 8-10мл/кг. Исходная частота дыханий составляла 10-12 в мин. Поддержка давлением составляла 12-16 мбар. При появлении самостоятельных дыхательных попыток частота дыхания аппаратных вдохов уменьшалась, а уровень поддержки давлением подбирался с целью обеспечения нормовентиляции (минутный объем 100 мл/кг/мин, РаCO2 35-40 мм рт.ст.). При развитии бради- или тахипноэ наращивалась частота принудительных вдохов. Отлучение пациентов от респиратора проводилось либо путем постепенного уменьшения числа принудительных вдохов в режиме SIMV, либо путем перевода в режим Pressure Support с постепенным снижением уровня поддержки давлением, либо путем перевода в режим ASV.
Режим ASV использовался в качестве стартового у 33 пациентов. Исходный процент замещения минутного объема составлял 100% и в дальнейшем корригировался под контролем PaCO2. В большинстве случаев режим ASV хорошо переносился пациентами, и вентиляция в этом режиме осуществлялась в течение всего периода респираторной поддержки вплоть до отключения от респиратора. В ряде случаев, ввиду развития выраженной гипервентиляции при осуществлении ИВЛ в режиме ASV, приходилось переходить на другие режимы.
Режим DuoPAP использовался у 10 пациентов, у которых течение основного заболевания осложнялось развитием острого повреждения легких или острого респираторного дистресс синдрома. В этих случаях во избежание баро- и ателектотравмы легких с использованием построения квазистатической петли давление-объем (инструмент PV-tool на аппаратах Hamilton G5) определялись нижняя и верхняя точка перегиба. В дальнейшем ИВЛ осуществлялась в режиме DuoPAP с выставлением нижнего давления на уровне на 2 мбар выше нижней точки перегиба, а верхнего уровня давления на уровне на 2 мбар ниже верхней точки перегиба (рисунок 3).
Методика увлажнения дыхательных путей
У всех пациентов, находившихся на ИВЛ более суток, для увлажнения дыхательной смеси использовались увлажнители – обогреватели Fisher&Pyker, где в дополнение к емкости испарителя в шлангах проложен нагревающий провод. Благодаря системе автоматического поддержания температуры, получающей информацию из трех точек дыхательного контура, удаётся добиться оптимального увлажнения и согревания дыхательной смеси и избежать выпадения конденсата в дыхательном контуре. Для оценки качества увлажнения использовалась шкала оценки вязкости бронхиального секрета [9]. Жидкий – после аспирации мокроты санационный катетер чист. Умеренно вязкий – после аспирации мокроты санационный катетер сразу очищается при промывании водой. Вязкий – после аспирации мокроты санационный катетер трудно отмыть от мокроты. Во всех наблюдениях консистенция мокроты у пациентов на ИВЛ была жидкой. При анализе данных использовались методы описательной статистики. Данные представлены, как среднее ± стандартное отклонение.
Результаты и обсуждение
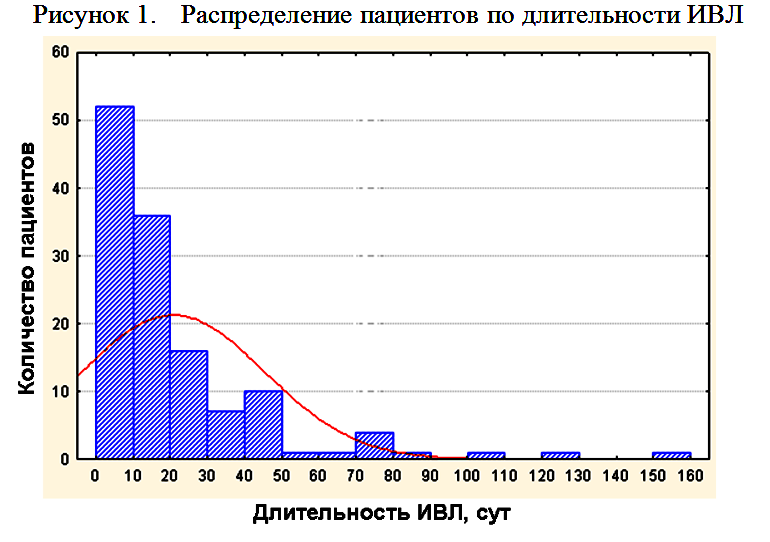
Средняя длительность ИВЛ составила 20,8±24,5 суток. На рисунке 1 и в таблице 2 представлено распределение пациентов по длительности ИВЛ.
Причинами проведения пролонгированной ИВЛ служило угнетение сознания в 81 (61,8%) случаев, необходимость седации в 21 (16,8%) случаев (из них в 7 (5,3%) случаях в связи с судорогами, в 15(11,5%) случаях в связи с психо-моторным возбуждением), угнетение респираторного драйва в 17 (13%) случаев, паренхиматозная дыхательная недостаточность в 11 (8,4%) случаев (рисунок 2).
Источник
Способы протекции верхних дыхательных путей
Механическая вентиляция легких является одним из наиболее распространенных методов лечения пациентов в отделениях интенсивной терапии и реанимации. Этот метод способен обеспечить пациенту как замещение функции внешнего дыхания при полной его остановке, так и поддержку спонтанной вентиляции пациента, если эта функция у него сохранена.
За время своего развития искусственная вентиляция легких претерпела множество изменений и прошла путь от простой объемной поддержки дыхания до сложных высокоинтеллектуальных режимов,который способны самостоятельно определить степень необходимой респираторной поддержки и обеспечить ее пациенту.
По мере развития механической вентиляции легких менялось и отношение специалистов к этому методу. Если вначале представление об искусственной вентиляции базировалось на том, что она безусловно полезна,то в дальнейшем,по мере накопления клинического опыта, появлялось все больше данных о негативном влиянии ИВЛ на функцию легких, а также о разнообразных осложнениях, сопровождающих данный вид лечения. Именно поэтому в настоящее время сформировалось представление о так называемой протективной искусственной вентиляции легких, то есть методике, обеспечивающей защиту пациента в процессе проведения ему респираторной терапии.
Говоря собственно о протекции, следует отметить, что речь идет прежде всего о защите здоровой или относительно здоровой части легких, то есть той их части, которая либо не вовлечена в патологический процесс, либо вовлечена в него в незначительной степени. Эта защита подразумевает предохранение здоровой или относительно здоровой части легких от повреждающего действия самой механической вентиляции. Цель протективной ИВЛ: минимизация риска вентиляционных повреждений легких. При правильном проведении протективная ИВЛ увеличивает выживаемость пациентов, находящихся на механической вентиляции.
Если говорить о патофизиологии вызванных вентиляцией повреждений легких, то речь идет о механической травме, биотравме и шунтировании кровотока вследствии этого. Общеизвестно, что механическая вентиляция путем поступления извне дыхательной смеси в легкие пациента нефизиологична, так как при этом возрастает давление в дыхательных путях и создаются условия для развития баротравмы и волюмотравмы. Патологически измененная часть легких обычно имеет более низкую растяжимость, что приводит к перерастяжению более здоровых участков в процессе проведения вентиляции. Также в процессе проведения ИВЛ нередко создаются условия для формирования ателектазов. Все это приводит к так называемой биотравме. Механическая травма легких совместно с биотравмой и шунтированием кровотока приводит к возрастанию гипоксемии, что в свою очередь ведет к нарастанию синдрома полиорганной недостаточности.
Существует несколько способов снижения риска вызванных вентиляций повреждений легких. Во-первых, это ограничение дыхательного объема до необходимых цифр, а также ограничение давления на вдохе до безопасных величин. Во-вторых, это использование положительного давления в конце выдоха (PEEP), а также при необходимости рекрутмент-маневра. В-третьих, это обеспечение вентиляции и перфузии различных участков легких, то есть использование прон-позиции.
Основные принципы протективной ИВЛ заключаются в следующем. Используют ограничение дыхательного объема до 5–7 мл/кг идеальной массы тела. Используют ограничение давления на вдохе: Pplat менее 30 см вод. ст., ∆P (Pplat — PEEP) менее 15 см вод. ст. Кроме этого, используют предупреждение ателектотравмы — положительное давление в конце выдоха (PEEP). Кроме того, значение имеют достаточное время вдоха и выдоха, достаточная оксигенация и пермиссивная гиперкапния (только в том случае, если отсутствуют противопоказания). Избегают гипероксии — концентрация кислорода на вдохе должна по возможности составлять не более 60%. Как известно, чрезмерно высокая концентрация кислорода на вдохе оказывает негативный эффект.
Для лечения острого респираторного дистресс-синдрома была разработана концепция ультрапротективной ИВЛ: дыхательный объем 3–3,5 мл/кг, качественная седация пациента, экстракорпоральное удаление углекислого газа, регуляция PEEP и FiO2 для достижения необходимой оксигенации, а также ЭКМО при рефрактерной к остальным методам гипоксемии.
В настоящее время разработаны и продолжают разрабатываться различные режимы для протективной вентиляции легких. Кроме того, большое значение имеет качественный мониторинг дыхания, гемодинамики и других параметров пациента для своевременного реагирования и быстрой оценки ситуации.
Источник