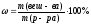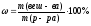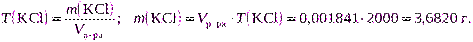СПОСОБЫ ПРИГОТОВЛЕНИЯ РАСТВОРОВ
Известны четыре способа приготовления растворов: по точной навеске, по приблизительной навеске, разбавлением и из фиксанала. Способ приготовления раствора зависит от свойств растворяемых веществ. Навеску вещества, как правило, не используют, если вещество является жидким. Разбавлением можно готовить растворы всех веществ, если в наличии есть более концентрированные растворы. Четвертый способ используют только в том случае, если фиксаналы этих веществ выпускаются промышленностью. Рассмотрим основные этапы приготовления растворов различными способами.
По точной навескеготовят только растворы стандартных веществ (см. критерии стандартности на с. 8). Для приготовления растворов этим способом должны быть заданы концентрация раствора и его объем. Основные этапы приготовления растворов следующие:
— рассчитывают необходимую навеску для взвешивания с точностью до 0,0001 г с использованием формул (4.2)-(4.13) (см. с. 21-24);
— взвешивают точную навеску на аналитических весах;
— взвешенную навеску растворяют, количественно переносят в мерную колбу вместимостью, равной Vр-ра, доводят до метки дистиллированной водой и перемешивают;
— если взятая навеска (mпракт) отличается от теоретически рассчитанной, то концентрацию раствора пересчитывают, используя указанные выше формулы, например:


Приготовленные таким образом растворы называют первичными стандартами.
Запомните: если объем приготавливаемого раствора больше 2 дм 3 , то расчеты массы навески ведут с точностью не более чем до 0,01 г, независимо от стандартности вещества, и берут ее на технических весах, так как максимальная вместимость мерных колб, выпускаемых промышленностью, равна 2 дм 3 .
По приблизительной навеске готовят растворы нестандартных веществ. Если вещество, которое используют для анализа, содержит примеси (более 1 %), вещество квалифицируют «ч.» или «техн.» (см. с. 8) и его массу рассчитывают с учетом имеющихся примесей. Этапы работы такие же, как и при приготовлении растворов по точной навеске, но навеску рассчитывают с точностью не более чем до 0,01 г и берут ее на технических весах. Точную концентрацию такого раствора устанавливают титрованием (часто растворами первичных стандартов) и рассчитывают ее по закону эквивалентов:

Приготовленные таким образом растворы с точно установленной концентрацией называются вторичными стандартами, или титрованными.
Из фиксанала (норма-дозы, стандарт-титра) готовят растворы точной концентрации. Фиксанал — стеклянная или полимерная ампула, в которой содержится точно известное количество вещества в сухом виде или в виде раствора. Содержимое фиксанала количественно переносят в мерную колбу, после растворения вещества доводят уровень раствора до метки и перемешивают. Концентрация раствора должна быть задана, а вместимость мерной колбы рассчитывают, используя формулу:


Разбавлением концентрированных растворовготовят растворы многих веществ. В этом случае должны быть заданы объем разбавленного раствора, его концентрация и концентрация концентрированного раствора. Рассчитывают необходимый для разбавления объем концентрированного раствора, затем измеряют рассчитанный объем, переносят в мерную колбу или в мерный стакан, доводят уровень жидкости до метки дистиллированной водой и перемешивают.
Запомните: при разбавлении водой масса (или количество) растворенного вещества одинаковы в концентрированном и разбавленном растворах.
Если исходный раствор имел точную концентрацию и при его разбавлении использовали точную мерную посуду, то получают раствор точной концентрации. В противном случае получают раствор приблизительной концентрации, все расчеты концентраций ведут с точностью не более чем до 0,01 и точную концентрацию устанавливают титрованием. Эти правила справедливы и при смешивании растворов.
ЧТО И КАК ПИСАЛИ О МОДЕ В ЖУРНАЛАХ НАЧАЛА XX ВЕКА Первый номер журнала «Аполлон» за 1909 г. начинался, по сути, с программного заявления редакции журнала.
Живите по правилу: МАЛО ЛИ ЧТО НА СВЕТЕ СУЩЕСТВУЕТ? Я неслучайно подчеркиваю, что место в голове ограничено, а информации вокруг много, и что ваше право.
ЧТО ПРОИСХОДИТ, КОГДА МЫ ССОРИМСЯ Не понимая различий, существующих между мужчинами и женщинами, очень легко довести дело до ссоры.
Что способствует осуществлению желаний? Стопроцентная, непоколебимая уверенность в своем.
Не нашли то, что искали? Воспользуйтесь поиском гугл на сайте:
Источник
1.4.Способы приготовления растворов. Способы приготовления стандартных растворов.
Растворы с известной концентрацией, которые служат для определения концентрации других растворов, называются стандартными или рабочими. Это некоторые растворы кислот, щелочей, солей.
Метод точной навески. Предполагает работу с растворами, которые не меняют свою молекулярную массу и объем при взаимодействии с воздухом. К таким веществам относятся щавелевая кислота, сода, бура (Na2B4O7·10H2O), бихромат калия и ряд других веществ. На аналитических (погрешность таких весов составляет 0,0002г) весах точно взвешивают вещество и переносят в мерную колбу для растворения, доводят до метки растворителем (водой) и тщательно перемешивают.
Растворы точной навески можно приготовить лишь для немногих веществ. Эти вещества должны отвечать следующим требованиям:
— устойчивость вещества на воздухе и в растворе.
Такие соединения называются установочными. К ним относятся: щавелевая кислота (Н2С2О4 · 2Н2О), тетраборат натрия (бура) (Na2B4O7 · 12H2O), дихромат калия (K2Cr2O7). Для всех других веществ растворы готовят из неточной навески или разбавлением.
Фиксанальный метод. Предполагает приготовление растворов из фиксаналов. Фиксанал — ампула с сухим веществом или раствором с точно известной концентрацией. Фиксанал разбивают и переносят в колбу для растворения. Этот метод считается наиболее точным.
Метод приблизительной навески. Предполагает работу с растворами, которые меняют свою массу на воздухе, например, перманганат калия. Работать с такими растворами нельзя, поэтому перед применением их в качестве стандартных, необходимо оттитровать другим раствором с точно известной концентрацией.
Метод разбавления. Из раствора с точно известной концентрацией готовят разбавлением раствор другой концентрации. Концентрация полученного раствора зависит от концентрации исходного.
1.5.Решение задач на приготовление растворов с массовой долей (%) концентрации.
Задача 1. Как приготовить 500 г раствора С6Н12О6 с массовой долей равной 10% ?
m (р-ра С6Н12О6) = 500 г
__________________ формуле: m (в-ва) =
Найти: m (С6Н12О6) = ? m (С6Н12О6) =
2. Определяем массу воды согласно формуле:
m (р-ра) = m (р-ля) + m (вещ-ва), m (Н2О) = m (р-ра) – m (в-ва),
m (H2O) = 500 – 50 = 450 г.
Согласно формуле: 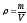

Ответ: чтобы приготовить 500 г раствора глюкозы с массовой долей 10%, необходимо отвесить на весах 50 г глюкозы, отмерить любой мерной склянкой 450 мл воды, поместить этот раствор в любую подходящую посуду и перемешать.
Задача 2. Как приготовить 800 мл раствора NaCl с массовой долей равной 12% и плотностью равной 1,1 г/мл?
V (р-ра) = 800 мл
ρ = 1,1 г/мл 1. Определяем массу р-ра NaCl согласно
__________________ формуле: m (р-ра)=800 мл · 1,1г/мл = 880 г
2. Определяем массу NaCl согласно формуле: m (в-ва) =
m (NaCl) =
3. Определяем массу воды согласно формуле:
m (Н2О) = m (р-ра) – m (в-ва), ), m (Н2О) = 880 – 105,6 = 774,4 г или 774,4 мл, т.к. плотность воды равна 1 г/мл.
Ответ: для приготовлшения 800 мл раствора хлорида натрия с массовой долей равной 12 %, необходимо отвесить на весах 105,6 г NaCl, отмерить любой мерной склянкой 774,4 мл воды, поместить все это в любую подходящую посуду и перемешать.
Задача 3 Приготовить 100 г ра-ра MgSO4 c ω = 2 % из р-ра MgSO4 c ω = 10 % ?
ω1( MgSO4) = 10 %
ρ = 1,1 г/мл 1. Определяем массу чистого MgSO4
__________________ содержащегося в 100 г 2 % р-ра MgSO4
Найти: m 1 ( MgSO4) = ? m (в-ва) = 
m (H2O) = ? m (MgSO4) =
2. Определяем массу р-ра MgSO4 (исходного) с ω = 10 % содержащего 2 г чистого MgSO4 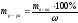
3. Определяем объём исходного (первого) р-ра MgSO4 с ω = 10 %
Vр-ра = 
4. Определяем массу Н2О, которая необходима для разбавления исходного раствора MgSO4.
m (H2O) = 100 – 20 = 80 г или для чистой воды 80 мл.
Ответ: для приготовления 100 г раствора MgSO4 с массовой долей равной
2 % из раствора MgSO4 с массовой долей 10 % и ρ = 1,1 г/мл, необходимо отмерить из бюретки 18,2 мл 10 % р-ра MgSO4, поместить их в колбу, добавить туда цилиндром 80 мл воды и перемешать.
Тут вы можете оставить комментарий к выбранному абзацу или сообщить об ошибке.
Источник
Способы приготовления растворов
Существует несколько способов приготовления растворов. По способу приготовления различают первичные и вторичные стандартные растворы.
1.
По точной навескеготовят первичные стандартные растворы, растворы стандартных установочных веществ, которые должны удовлетворять следующим требованиям:
а) состав их должен строго соответствовать химической формуле;
б) вещества должны быть устойчивыми при хранении в растворе и в сухом виде (не окисляться, не поглощать диоксид углерода, воду, не терять кристаллизационную воду);
в) величина молярной массы эквивалента должна быть по возможности наибольшей для уменьшения погрешности взвешивания и титрования.
При приготовлении растворов по точной навеске задаются концентрацией раствора и его объемом. Основные этапы работы:
- рассчитывают необходимую навеску для взвешивания с точностью до 0,0001 г по одной из формул:
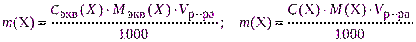
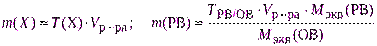
где Vр-ра – объем раствора, см 3 ;
- взвешивают точную навеску на аналитических весах;
- взвешенную навеску количественно переносят в мерную колбу вместимостью, равной Vр-ра, растворяют вещество, доводят до метки дистиллированной водой и перемешивают;
- если взятая навеска отличается от теоретически рассчитанной, то концентрацию раствора пересчитывают, используя указанные выше формулы, например:
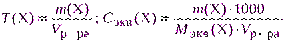
где Vр-ра – объем раствора, см 3 ; m(Х) – практическая навеска, г.
2.
По приблизительной навескеготовят растворы нестандартных веществ или растворы приблизительной концентрации. Этапы работы такие же, как и при приготовлении растворов по точной навеске, но навеску рассчитывают с точностью не более, чем до 0,01 г и берут ее на технических весах. Точную концентрацию такого раствора устанавливают титрованием (часто растворами первичных стандартов) и рассчитывают по закону эквивалентов:
Сэкв 1·V1 = Cэкв 2·V2 (2.16)
Приготовленные таким образом растворы с точно установленной концентрацией называются вторичными стандартами или титрованными.
3.
Из фиксанала (норма-дозы, стандарт-титра)готовят первичные стандартные растворы точной концентрации. Фиксанал – стеклянная ампула, в которой содержится точно известное количество nэкв вещества в кристаллическом виде или в виде раствора. Содержимое фиксанала количественно переносят в мерную колбу, доводят уровень раствора до метки, раствор перемешивают. Концентрация раствора должна быть задана, а вместимость мерной колбы рассчитывают, используя формулу (2.6).
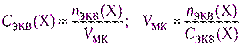
4.
Разбавлением концентрированных растворовготовят растворы многих веществ. В этом случае должны быть заданы объем разбавленного раствора, его концентрация и концентрация концентрированного раствора. Рассчитывают необходимый для разбавления объем концентрированного раствора, затем измеряют рассчитанный объем, переносят в мерную колбу или в мерный стакан, доводят уровень жидкости до метки дистиллированной водой и перемешивают. Если исходный раствор имел точную концентрацию и при его разбавлении использовали точную мерную посуду, то получают раствор точной концентрации. В противном случае получают раствор приблизительной концентрации, все расчеты ведут с точностью не более чем до 0,01, точную концентрацию устанавливают титрованием и рассчитывают по формуле (2.16).
Пример.Сколько грамм хлорида калия KCl потребуется для приготовления 2 дм 3 раствора:
а) с массовой долей, равной 30% и плотностью 1,110 г/см 3 ;
б) с титром, равным 0,001841 г/см 3 ;
в) с молярной концентрацией эквивалента, равной 0,2000 моль/дм 3 .
Решение.
| Дано: ω(KCl) = 30% | а) Массу хлорида калия рассчитаем, используя формулу (2.11): |
| Vр-ра= 2 дм 3 = 2000 см 3 ρ р-ра = 1,110 г/см 3 | 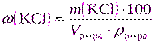 |
| Сэкв(KCl) = 0,2000 моль/дм 3 T(KCl) = 0,001841 г/см 3 |  |
| m(KCl) = ? |
б) Для расчета используем формулу (2.12):
в) Для расчета можно использовать формулу (2.7):
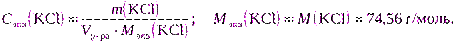
m(KCl) = Cэкв(KCl) · Vр-ра · Mэкв(KCl) = 0,2000·2·74,56 = 29,8240 г.
Нам важно ваше мнение! Был ли полезен опубликованный материал? Да | Нет
Источник