- Способы повышения растворимости веществ
- Как можно повлиять на растворимость веществ в воде
- Химическое равновесие
- Следующие параметры могут влиять на растворимость вещества в воде:
- Полярность
- Температура
- Давление
- Значение pH
- Соленость и наличие других веществ
- ОСНОВНЫЕ МЕТОДЫ ПОВЫШЕНИЯ РАСТВОРИМОСТИ ГИДРОФОБНЫХ И ТРУДНОРАСТВОРИМЫХ ВЕЩЕСТВ
- Полный текст:
- Аннотация
- Ключевые слова
- Об авторах
- Список литературы
- Для цитирования:
- For citation:
Способы повышения растворимости веществ
Управление солюбилизационными характеристиками лекарственных веществ является одним из основных направлений в разработках современных систем доставки лекарств (Drug Delivery Systems) [22]. В этом направлении наиболее востребованы методы повышения растворимости и скорости растворения активных фармацевтических субстанций – лекарственных веществ (ЛВ). Растворимость играет существенную роль в действии лекарств, прежде всего предназначенных для перорального приема, так как максимальная скорость пассивного транспорта препарата через биологические мембраны – основной путь для поглощения ЛВ – зависит от проницаемости мембраны и концентрации раствора/растворимости. Учитывая, что
40 % выпускающихся лекарственных субстанций классифицируются как практически нерастворимые, а
85 % самых продаваемых препаратов в США и Европе принимаются перорально, актуальность исследований в данном направлении становится очевидной.
В настоящее время FDA принята система биофармацевтической классификации лекарств [24, 26] для прогнозирования биодоступности при пероральном приеме. Эта система основана на использовании соотношений параметров растворимости и проницаемости стенок желудочно-кишечного тракта (ЖКТ). Растворимость классифицирована на основании стандартов Фармакопеи США (USP) [23]. Так, лекарственное вещество считается хорошо растворимым, когда максимальная разрешенная его доза растворяется в 90 процентов его дозы проникает в кровоток при пероральном введении. Ниже приводятся основные классы ЛВ по критериям «проницаемость стенок ЖКТ – растворимость».
Класс I – высокая проницаемость, высокая растворимость. Эти соединения хорошо всасываются и скорость абсорбции, как правило, выше, чем выведение.
Класс II – высокая проницаемость, низкая растворимость. Пример: большинство нестероидных противовоспалительных средств. Биодоступность таких продуктов ограничена скоростью их растворения (кинетический барьер) и растворимостью (термодинамический барьер). К этому классу относится
> 30 % выпускающихся и разрабатываемых лекарств.
Класс III – низкая проницаемость, высокая растворимость. Пример: большинство антибиотиков бета-лактамного типа. Низкая скорость абсорбции ограничивает проникновение в кровоток, но препараты растворяются очень быстро.
Класс IV – низкая проницаемость, низкая растворимость. Пример: антигельминтики – альбендазол, карбендацим, фенбендазол; растительные флавоноиды – рутин, кверцетин, дигидрокверцетин. Эти соединения имеют низкую биодоступность. Обычно они плохо поглощаются слизистой оболочкой кишечника. К этому классу относится
10 % выпускающихся и разрабатываемых лекарств.
Таким образом, ЛВ, относящиеся к II и IV классам, нуждаются в технологиях повышения их водорастворимости. К этим классам относятся до 50 % разрабатываемых и выпускающихся фармацевтической промышленностью ЛВ.
Для повышения растворимости лекарств используют различные физико-химические подходы: уменьшение размеров частиц, модификация кристаллической структуры, получение твердых дисперсий ЛВ с наполнителями и т.д. [20, 18]. Так, при измельчении субстанций антигельминтных препаратов «карбендацим» (бензимидазолил-2-метил карбамат) и «альбендазол» (5-тиопропилбензимидазолил-2-метилкарбамат) в планетарно-центробежном активаторе АГО–2 в «жестких» условиях активации (40 – 60g) было показано не только уменьшение размера частиц, но также стабильность химической структуры, а именно, при сравнении ИК-спектров исходных и измельченных субстанций не было обнаружено изменений в расположении полос поглощения основных функциональных групп (NH, C = N, C = O, OCH3). В спектрах измельченных субстанций наблюдалось увеличение интенсивности этих сигналов, что позволило предполагать лишь о разрушении межмолекулярных водородных связей [11]. Изучение растворения исходного и измельченного образцов карбендацима в среде «желудочного сока» показало, что скорость растворения измельченной субстанции выше, нежели неизмельченной субстанции.
Однако, по нашему мнению, наиболее значимые результаты достигаются за счет перевода ЛВ в их водорастворимые соли (если ЛВ имеет выраженные кислотно-основные свойства), а также за счет включения молекул ЛВ в супрамолекулярные водорастворимые образования (межмолекулярные комплексы, мицеллы) со специально подобранными «вспомогательными» веществами.
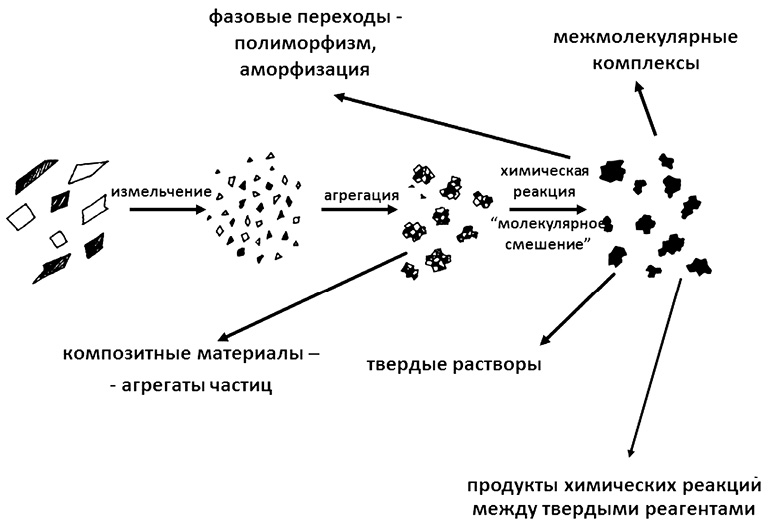
Механохимия является разделом химии твердого тела, в котором изучаются физико-химические превращения твердых веществ и их смесей в условиях интенсивных ударно-истирающих воздействий, обычно реализующихся в специальных мельницах. На рис. 1 показаны возможные пути трансформаций в смесях твердых веществ при их механохимической обработке [3].
Суть нашей технологии заключается в получении твердых дисперсий лекарственных веществ со вспомогательными веществами различной химической природы. Увеличение растворимости ЛВ и повышение эффективности фармакологического действия в зависимости от их физико-химических свойств достигается:
– образованием твердых дисперсий, в которых ЛВ диспергировано в молекулярной форме или находится в аморфном состоянии;
– образованием водорастворимых солей;
– образованием водорастворимых комплексов включения с полисахаридами по типу «гость-хозяин», а также мицелл.
Далее мы рассмотрим вышеуказанные случаи.
Рис. 1. Схема механохимических превращений в смесях твердых веществ (ЛВ + вспомогательные вещества) при их механической обработке ударно-истирающими воздействиями
Получение и свойства твердых дисперсий, в которых ЛВ находится в аморфизованном состоянии или диспергирована в молекулярной форме
Высвобождение в раствор фармакологически активного вещества из твердых лекарственных форм (порошков, таблеток и т.д.) во многом определяется скоростью растворения его кристаллической фазы. Однако многие фармакологические активные вещества крайне медленно растворяются в воде во многом за счет плохой смачиваемости и «прочности» кристаллической решетки. Очевидно, что получение твердых растворов – молекулярных дисперсий – таких веществ в хорошо растворимом наполнителе либо разупорядочение их кристаллических фаз будет способствовать ускорению процесса растворения. Именно этот принцип был применен нами к модификации антигельминтика карбендацима и ряда транквилизаторов бензодиазепинов – диазепама, оксазепама и медазепама, лекарственные субстанции которых практически нерастворимы в воде.
Для модификации солюбилизационных характеристик бензодиазепинов нами механохимическим способом были получены их твердые дисперсии с лактозой и микрокристаллической целлюлозой в весовых соотношениях 1:5, 1:10 и 1:15. В дифрактограммах механически активированных образцов наблюдалось резкое падение интенсивности рефлексов (без их заметного уширения) кристаллических фаз ЛВ вплоть до их полного исчезновения. Рефлексы веществ – наполнителей (лактозы и отчасти целлюлозы) претерпевали уширение, что свидетельствовало о накоплении дефектов и уменьшении кристалличности. К сожалению, методы термического анализа оказались неэффективны из-за относительно низких температур разложения веществ-наполнителей.
Проведенные исследования растворимости образцов продемонстрировали во всех случаях увеличение скорости растворения ЛВ в механохимически полученных образцах по сравнению со смесями, не подвергавшимися механохимической обработке и тем более измельченными исходными субстанциями [5]. Проведенные испытания биологической доступности образцов модифицированных препаратов оксазепама на лабораторных животных – кроликах – показали увеличение действующей концентрации оксазепама в крови и сокращение времени достижения ее максимального значения. Биодоступность оксазепама по сравнению с неактивированной смесью увеличивается в 1,56 ± 0,25 раза. Таким образом повышается эффективность действия лекарственного средства.
Получение и свойства твердых дисперсий, образующих водорастворимые соли ЛВ
Многие малорастворимые ЛВ обладают кислотными или основными свойствами и способны к ионизации в водных растворах и образованию соответствующих солей. Как правило, ионизированная форма является более гидрофильной и имеет более высокую водорастворимость. Многие ЛВ с целью повышения их растворимости выпускаются в виде их солей [9, 12]. Так, лекарственные вещества, имеющие основной характер, – в виде гидрохлоридов, а органические кислоты – в виде солей металлов или органических оснований. Соли получают реакцией жидкофазной нейтрализации с последующим выделением (сушкой). При этом требуются большие объемы растворителей, громоздкое оборудование, значительные производственные площади. Кроме того, в процессе сушки возможно разложение целевого продукта.
Рассмотрим возможности этого подхода на примере ацетилсалициловой кислоты (аспирина). Малая растворимость в воде ( Примечания:
Cmax – максимальная концентрация в крови;
Tmax – время достижения максимальной концентрации в крови;
AUC – площадь под фармакокинетической кривой, в относительных единицах;
* – навески препаратов взяты в эквивалентных по действующему веществу концентрациях.
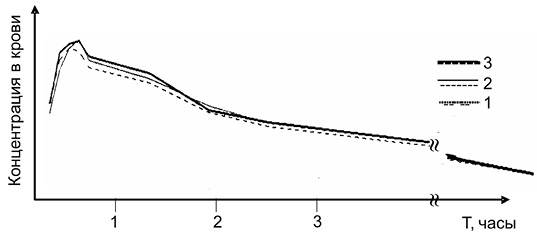
Рис. 3. Фармакокинетика препаратов «АСК – Na2CO3» и «Аспирин + С» при разных способах приема препаратов. Прием раствора таблеток «Аспирин + С» (1), раствора таблеток нашего препарата (2) и таблеток нашего препарата без предварительного растворения (3) в эквивалентных по АСК дозах
В соответствии с действующими правилами нами были разработаны фармакопейные статьи на таблетки и субстанцию, проведены фармакологические испытания [1, 2] и препарат зарегистрирован для применения в РФ.
Композиция состава АСК/CaCO3 = 78/22 вес. % также представляет значительный интерес. Она обладает высокой химической стабильностью при хранении и меньшей гигроскопичностью, но замедленной скоростью растворения. Методом прямого прессования из нее были получены таблетки с двумя дозировками АСК – 0,1 г (вес таблетки 0,128 г) и 0,5 г (вес таблетки 0,64 г). По своим характеристикам – химическая чистота, время растворения, кислотонейтрализующая емкость (для таблеток по 0,5 г) – эти таблетки соответствуют требованиям USP к так называемым «буферированным» таблеткам ацетилсалициловой кислоты. Разработанный нами препарат, получивший название «Антиагрегин», показал при сравнительных опытах с применяемыми в медицинской практике импортными препаратами практически равнозначную эффективность и безопасность для лечения и профилактики сердечно-сосудистых заболеваний (табл. 2).
Сравнительные характеристики разработанных в ИХТТМ СО РАН растворимых таблеток и их импортных аналогов
Источник
Как можно повлиять на растворимость веществ в воде
Растворы представляют собой однородные смеси. Однако есть растворы с другими жидкими, газообразными или даже твердыми веществами.
Максимальное количество вещества, которое может быть растворено в определенном количестве растворителя, образуя стабильную систему, называется растворимостью. В обычных условиях это всегда вопрос температуры и, возможно, давления. Любое количество вещества по отношению к количеству растворителя называется концентрацией.
Химическое равновесие
В обратимых реакциях, которые состоят не только из прямой, но и из обратной реакции, существует характерное соотношение исходных материалов и продуктов при постоянной температуре. В результате устанавливается равновесие, при котором скорость прямой и обратной реакции одинакова.
Растворение вещества в воде возможно до тех пор, пока концентрация вещества не достигнет предела растворимости. В этот момент образуется фаза нерастворенного материала. В случае твердых тел это почва.
Раствор может быть перенасыщен на короткое время, но избыток растворенного вещества быстро выпадет в осадок. Устанавливается динамическое равновесие, при котором вещество растворяется с той же скоростью, что и выходит из раствора, в результате раствор становится насыщенным.
Если температура и давление специально не указаны для растворимости, обычно применяются стандартные условия: температура 20-22 C, давление — 1 бар.
Следующие параметры могут влиять на растворимость вещества в воде:
Полярность
Вещества, состоящие из ионов или молекул, содержащих заряды, называются полярными. Молекулы без этих зарядов называются неполярными. Молекула воды полярна, потому что две ее молекулы водорода имеют положительный частичный заряд, а молекула кислорода имеет отрицательный заряд. Поскольку подобное растворяется в подобном, полярные вещества, такие как соли, более растворимы в воде, чем неполярные вещества, например, масло.
Температура
Температура прямо влияет на растворимость веществ. Когда вещество растворяется в воде, энергия либо выделяется, либо поглощается (в виде тепла). Первые процессы растворения называются экзотермическими, а вторые — эндотермическими. Если процесс эндотермический, растворимость вещества увеличивается с повышением температуры. Это верно для большинства твердых тел. В экзотермических процессах растворимость уменьшается с повышением температуры, что обычно свойственно газам.
Давление
Давление практически не влияет на растворимость твердых веществ в воде. С другой стороны, объем газов сильно зависит от давления. Поэтому их растворимость в воде напрямую зависит от давления. При этом действует следующее правило: чем выше давление, тем больше газа переходит в раствор.
Значение pH
Когда некоторые вещества растворяются, из молекул воды образуются ионы. Примером этого является хлор, который вызывает образование ионов H+ в воде. В зависимости от pH растворителя он может содержать больше ионов H+ или больше ионов OH-.
Чистая вода — нейтральный растворитель.
Соленость и наличие других веществ
На растворимость веществ также влияет то, содержатся ли в воде другие вещества. Однако не только концентрация одной соли может влиять на растворимость другой соли в воде, но, например, содержание солей может изменять растворимость газов. Кислород менее растворим в соленой воде, чем в пресной.
Источник
ОСНОВНЫЕ МЕТОДЫ ПОВЫШЕНИЯ РАСТВОРИМОСТИ ГИДРОФОБНЫХ И ТРУДНОРАСТВОРИМЫХ ВЕЩЕСТВ
Полный текст:
Аннотация
Ключевые слова
Об авторах
Список литературы
1. Государственная фармакопея Российской Федерации. XIII изд. Т. II — М.: ФЭМБ, 2015.
2. Н.А. Оборотова, Е.В. Санарова. Роль новых фармацевтических технологий в повышении избирательности действия противоопухолевых препаратов // Российский химический журнал. 2012. № 3-4. С. 33-40.
3. K. Kawakami, N. Oda, K. Miyoshi et al. Solubilization behavior of a poorly soluble drug under combined use of surfactants and cosolvents // European journal of pharmaceutical sciences. 2006. № 28. P. 7-14.
4. И.Д. Гулякин, Н.А. Оборотова, В.М. Печенников. Солюбилизация гидрофобных противоопухолевых препаратов // Химико-фармацевтический журнал. 2014. № 3. С. 43-48.
5. Г.А. Чернышева, В.И. Смольякова, М.Б. Плотников и др. Фармакокинетика высокомолекулярного полиэтиленоксида // Химико-фармацевтический журнал. 2006. Т. 40. № 9. С. 7-8.
6. J. Vancoillie. Continuous melt granulation: Effect of different binders upon granule and tablet properties // Faculty Of Pharmaceutical Sciences — Ghent University. 2014. 56 p.
7. S. Talegaonkar, A. Azeem, F.J. Ahmad et al. Microemulsions: a novel approach to enhanced drug delivery // Recent Patents on Drug Delivery & Formulation. 2008. Т. 2. № 3. С. 238-257.
8. А.П. Ластовой, А.А. Игнатова, А.В. Феофанов и др. Исследование свойств нового фотосенсибилизатора β,β,β’,β’-тетраметилтрибензотетраазохлорина // Химико-фармацевтический журнал. 2014. № 2. С. 7-12.
9. European Pharmacopoeia. 7rd ed. — Strasbourg: Council of Europe, 2010. 3310 p.
10. G. Morral-Ruíz, P. Melgar-Lesmes, M.L. García et al. Polyurethane and polyurea nanoparticles based on polyoxyethylene castor oil derivative surfactant suitable for endovascular applications // International journal of pharmaceutics. 2014. V. 461(1). P. 1-13.
11. В.И. Иванова-Радкевич, Л.В. Умнова, С.В. Барканова и др. Фотодинамическая активность производного тетраазахлорина // Российский биотерапевтический журнал. 2008. Т. 7. № 3. С. 39-41.
12. Патент US 9302003 B2. Compositions comprising a radiosensitizer and an anticancer agent and methods of uses thereof / L. Sanche, G. Charest; № 13/259,213; заявл. 26.04.10; опубл. 5.04.16.
13. P. Benito-Gallo, P. Gershkovich, M. Marlow et al. Smart Lipid-Based Drug Delivery Systems // Smart Pharmaceutical Nanocarriers. 2016. P. 309-371.
14. Е.В. Санарова, А.В. Ланцова, Н.А. Оборотова. Применение диметилсульфоксида в фармации и медицине (обзор) // Биофармацевтический журнал. 2015. № 3. С. 3-9.
15. Vaccine Therapy With or Without Imiquimod in Treating Patients Who Have Undergone Surgery for Stage II, Stage III, or Stage IV Melanoma. URL: http://clinicaltrials.gov/ct2/show/NCT00118313?term=DMSO&rank=15 (дата обращения 25.10.13).
16. Chemo-immunotherapy (Gemcitabine, Interferonalpha 2b and p53 SLP) in Patients With Platinum-resistant Ovarian Cancer (CHIP). URL: http://clinicaltrials.gov/ct2/show/NCT01639885?term=DMSO&rank=25 (дата обращения 25.10.13).
17. Safety and Effectiveness of a Vaccine for Prostate Cancer That Uses Each Patients’ Own Immune Cells. URL: http://clinicaltrials.gov/ct2/show/NCT00289341?term=DMSO&rank=27 (дата обращения 25.10.13).
18. Safety of Active Immunotherapy in Subjects With Ovarian Cancer. URL: http://clinicaltrials.gov/ct2/show/NCT01456065?term=DMSO&rank=21 (дата обращения 25.10.13).
19. A Study of the BRAF Inhibitor Dabrafenib in Combination With the MEK Inhibitor Trametinib in the Adjuvant Treatment of High-risk BRAF V600 Mutation-positive Melanoma After Surgical Resection. (COMBI-AD). URL: http://clinicaltrials.gov/ct2/show/NCT01682083?term=DMSO&rank=26 (дата обращения 25.10.13).
20. A Study to Determine the Relative Bioavailability of the MEK Inhibitor, Trametinib, in Subjects With Solid Tumor Malignancies. URL: http://clinicaltrials.gov/ct2/show/NCT01725100?term=DMSO&rank=5 (дата обращения 25.10.13).
21. А.В. Ланцова, Е.В. Санарова, Н.А. Оборотова и др. Разработка технологии получения инъекционной лекарственной формы на основе отечественной субстанции производной индолокарбазола ЛХС-1208 // Российский биотерапевтический журнал. 2014. № 3. С. 25-32.
22. И.И. Краснюк (мл.), Л.В. Овсянникова, О.И. Никулина и др. Изучение растворимости кислотной формы диклофенака из твердых дисперсий // Химико-фармацевтический журнал. 2014. № 11. С. 23-27.
23. И.И. Краснюк (мл.), О.И. Степанова, А.В. Беляцкая, И.И. Краснюк. Перспективы получения лекарственных форм на основе твёрдых дисперсий фурацилина // Разработка и регистрация лекарственных средств. 2015. № 2(11). С. 72-78.
24. А.А. Теслев. К вопросу применения твердых дисперсных систем для улучшения биофармацевтических характеристик лекарственных средств // Фармацевтические технологии и упаковка. 2014. № 2. С. 18-21.
25. M.E. Brewster. Cyclodextrins as pharmaceutical solubilizers // Advanced Drug Delivery Reviews. 2007. V. 59. P. 645-666.
26. Wen Chen, Li-Juan Yang, Shui-Xian Ma et al. Crassicauline α/β-cyclodextrin host-guest system: Preparation, characterization, inclusion mode, solubilization and stability // Carbohydrate Polymers. 2011. V. 84. P. 1321-1328.
27. A. Vyas, S. Saraf, S. Saraf. Cyclodextrin based novel drug delivery systems // J Incl Phenom Macrocycl Chem. 2008. V. 62. P. 23-42.
28. J. Alsenz, M. Kansy. High throughput solubility measurement in drug discovery and development // Advanced Drug Delivery Reviews. 2007. V. 59. P. 546-567.
29. Л.Л. Николаева, А.В. Ланцова, Е.В. Санарова и др. Парентеральная лекарственная форма нового соединения из класса алкилнитрозомочевины // Российский биотерапевтический журнал. 2015. № 1. С. 113.
30. М.В. Дмитриева, Н.А. Оборотова, Е.В. Санарова и др. Наноструктурированные системы доставки противоопухолевых препаратов // Российский биотерапевтический журнал. 2012. № 4. С. 21-27.
31. Н.Б. Демина, С.А. Скатков, А.И. Тенцова. Нанотехнологические аспекты современной лекарственной формы // Фармация. 2012. № 4. C. 37-41.
32. Н.Б. Демина, С.А. Скатков, А.И. Тенцова. Перспективные стратегии развития технологии наноносителей // Фармация. 2012. № 7. C. 53-55.
33. A.D. Carvalho Junior, F.P. Vieira, V.J. De Melo et al. Preparation and cytotoxicity of cisplatin-containing liposomes // Brazilian Journal of Medical and Biological Research. 2007. V. 40. P. 1149-1157.
34. J. Huober, W. Fett, A. Nusch et al. A multicentric observational trial of pegylated liposomal doxorubicin for metastatic breast cancer // BMC Cancer. 2010. V. 7(10). С. 2.
35. E. Blanco, C.W. Kessinger, B.D. Sumer, J. Gao. Multifunctional micellar nanomedicine for cancer therapy // Experimental Biology and Medicine (Maywood). 2009. V. 234(2). P. 123-131.
36. Kang Moo Huh, Hyun Su Min, Sang Cheon Lee et al. A new hydrotropic block copolymer micelle system for aqueous solubilization of paclitaxel // Journal of Controlled Release. 2008. V. 126. P. 122-129.
37. Ling Bing Li, Guangxi Zhai, Yan Gao. Preparation and characterization of Pluronic/TPGS mixed micelles for solubilization of camptothecin // Colloids and Surfaces B: Biointerfaces. 2008. V. 64. P. 194-199.
38. L. Ostacolo, M. Marra, F. Ungaro et al. In vitro anticancer activity of docetaxel-loaded micelles based on poly(ethylene oxide)-poly(epsilon-caprolactone) block copolymers: Do nanocarrier properties have a role? // Journal of Controlled Release. 2010. V. 148. P. 255-263.
39. D.J. Bharali, M. Khalil, M. Gurbuz et al. Nanoparticles and cancer therapy: A concise review with emphasis on dendrimers // International Journal of Nanomedicine. 2009. V. 4. P. 1-7.
40. Е.В. Санарова, З.С. Смирнова, А.П. Полозкова и др. Биофармацевтические исследования новой липосомальной лекарственной формы тиосенса // Биофармацевтический журнал. 2011. № 6. С. 33-36.
41. T.T.H. Yen, I.G. Meerovich, G.A. Meerovich et al. Comparative studies in vivo of free and liposomal forms of photosensitizer on a base of hydrophilic derivative of chlorine e6 // Journal Drug Del. Sci. Tech. 2012. V. 4. P. 291-294.
42. О.Ю. Аршинова, А.П. Полозкова, О.Л. Орлова и др. Получение и биофармацевтическое исследование лиофилизированной лекарственной формы Фотодитазина // Биофармацевтический журнал. 2013. № 1. С. 27-29.
43. М.В. Дмитриева, Н.А. Оборотова, О.Л. Орлова и др. Липосомальная лекарственная форма борхлорина // Российский биотерапевтический журнал. 2014. № 1. С. 31-36.
44. A. Lantsova, E. Kotova, K. Sanarova et al. Biopharmaceutical study of nanostructured formulation of the anticancer drug derivative of nitrosoalkylurea lysomustine // Journal of Drug Delivery Science and Technology. 2012. V. 6. P. 469-472.
45. Н.В. Грищенко, М.А. Барышникова, А.П. Полозкова и др. Липосомальные противоопухолевые препараты не используют СБ95-зависимый сигнальный путь апоптоза // Российский биотерапевтический журнал. 2014. № 1. С. 37-41.
46. С.Г. Козеев, М.А. Барышникова, Д.А. Афанасьева и др. Сравнение цитотоксического действия двух лекарственных форм аранозы // Российский биотерапевтический журнал. 2012. № 2. С. 24.
Для цитирования:
Гулякин И.Д., Николаева Л.Л., Оборотова Н.А., Дмитриева М.В., Ланцова А.В., Санарова Е.В., Орлова О.Л., Полозкова А.П., Лаврухин Н.И., Бунятян Н.Д. ОСНОВНЫЕ МЕТОДЫ ПОВЫШЕНИЯ РАСТВОРИМОСТИ ГИДРОФОБНЫХ И ТРУДНОРАСТВОРИМЫХ ВЕЩЕСТВ. Разработка и регистрация лекарственных средств. 2016;(2):52-59.
For citation:
Gulyakin I.D., Nikolaeva L.L., Oborotova N.A., Dmitrieva M.V., Lantsova A.V., Sanarova E.V., Orlova O.L., Polozkova A.P., Lavrukhin H.I., Bunyatyan N.D. COMMON METHODS INCREASING THE SOLUBILITY OF POORLY SOLUBLE HYDROPHOBIC SUBSTANCES. Drug development & registration. 2016;(2):52-59. (In Russ.)

Контент доступен под лицензией Creative Commons Attribution 4.0 License.
Источник