- Сульфид железа (III)
- Содержание
- Получение
- Физические свойства
- Сульфид железа (II), характеристика, свойства и получение, химические реакции
- Сульфид железа (II), характеристика, свойства и получение, химические реакции.
- Краткая характеристика сульфида железа (II):
- Физические свойства сульфида железа (II):
- Получение сульфида железа (II):
- Химические свойства сульфида железа (II). Химические реакции сульфида железа (II):
- Применение и использование сульфида железа (II):
- Мировая экономика
- Справочники
- Востребованные технологии
- Поиск технологий
- О чём данный сайт?
- О Второй индустриализации
- Сульфид железа (II)
- Содержание
- Описание и структура
- Получение
- Химические свойства
- Применение
Сульфид железа (III)
| Сульфид железа (III) | |
|---|---|
| Систематическое наименование | Сульфид железа (III) |
| Традиционные названия | Сернистое железо |
| Хим. формула | Fe2S3 |
| Состояние | жёлто-зелёные кристаллы |
| Молярная масса | 207,89 г/моль |
| Плотность | 4,3 г/см³ |
| Растворимость | |
| • в воде | слабо растворяется |
| Рег. номер CAS | 12063-27-3 |
| PubChem | 160957 |
| SMILES | |
| ChEBI | 75899 |
| ChemSpider | 141408 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Сульфид железа (III) — неорганическое соединение, соль железа и сероводородной кислоты с формулой Fe2S3, жёлто-зелёные кристаллы, не растворяется в воде.
Содержание
Получение
- Обменная реакция между сульфидом аммония и соли трёхвалентного железа:
2Fe(NO3)3 + 3(NH4)2S → Fe2S3↓ + 6NH4NO3
- Действие сероводорода на суспензию гидроксида железа (III) в отсутствии воздуха:
2Fe(OH)3 + 3H2S → Fe2S3↓ + 6H2O
- Пропускание горячего сероводорода через оксид железа (III):
Fe2O3 + H2S → C Fe2S3 + H2O
Физические свойства
Сульфид железа (III) образует жёлто-зелёные кристаллы кубической сингонии, пространственная группа F d3m, параметры ячейки a = 0,99342 нм, Z = 12.
Весьма слабо растворяется в воде.
Кристаллы образуются при длительной выдержке аморфной суспензии под давлением сероводорода в 10 ат.
Источник
Сульфид железа (II), характеристика, свойства и получение, химические реакции
Сульфид железа (II), характеристика, свойства и получение, химические реакции.
Сульфид железа (II) – неорганическое вещество, имеет химическую формулу FeS.
Краткая характеристика сульфида железа (II):
Сульфид железа (II) – неорганическое вещество коричнево-черного цвета с металлическим блеском, соединение железа и серы, соль железа и сероводородной кислоты.
Сульфид железа (II) представляет собой коричнево-черные кристаллы.
Химическая формула сульфида железа (II) FeS.
Не растворяется в воде . Не притягивается магнитом. Тугоплавок.
Разлагается при нагревании в вакууме.
Во влажном состоянии чувствителен к кислороду воздуха, т.к. вступает с кислородом в реакцию, образуя сульфит железа (II).
Физические свойства сульфида железа (II):
| Наименование параметра: | Значение: |
| Химическая формула | FeS |
| Синонимы и названия иностранном языке | iron (II) sulfide (англ.) |
| Тип вещества | неорганическое |
| Внешний вид | коричнево-черные гексагональные кристаллы |
| Цвет | коричнево-черный |
| Вкус | —* |
| Запах | без запаха |
| Агрегатное состояние (при 20 °C и атмосферном давлении 1 атм.) | твердое вещество |
| Плотность (состояние вещества – твердое вещество, при 20 °C), кг/м 3 | 4840 |
| Плотность (состояние вещества – твердое вещество, при 20 °C), г/см 3 | 4,84 |
| Температура кипения, °C | — |
| Температура плавления, °C | 1194 |
| Молярная масса, г/моль | 87,91 |
Получение сульфида железа (II):
Сульфид железа (II) получается в результате следующих химических реакций:
- 1. взаимодействия железа и серы:
Fe + S → FeS (t = 600-950 о С).
Реакция протекает путем сплавления алюминия с углеродом в дуговой печи.
- 2. взаимодействия оксида железа и сероводорода:
FeO + H2S → FeS + H2O (t = 500 о С).
- 3. взаимодействия хлорида железа и сульфида натрия:
- 4. взаимодействия сульфата железа и сульфида натрия:
Химические свойства сульфида железа (II). Химические реакции сульфида железа (II):
Химические свойства сульфида железа (II) аналогичны свойствам сульфидов других металлов . Поэтому для него характерны следующие химические реакции:
1. реакция сульфида железа (II) и кремния:
Si + FeS → SiS + Fe (t = 1200 о С).
В результате реакции образуются сульфид кремния и железо.
2. реакция сульфида железа (II) и кислорода:
В результате реакции образуются сульфат железа (II). Реакция протекает медленно. В ходе реакции используется влажный сульфид железа. Также образуются примеси: сера S, полигидрат оксида железа (III) Fe2O3 • nH2O.
3. реакция сульфида железа (II), кислорода и воды:
В результате реакции образуются гидроксид железа и сероводород.
4. реакция сульфида железа (II), оксида кальция и углерода:
FeS + CaO + C → Fe + CO + CaS (t о ).
В результате реакции образуются железо , оксид углерода и сульфид кальция.
5. реакция сульфида железа (II) и сульфида меди:
В результате реакции образуются дитиоферрата (II) меди (II) (халькопирит).
6. реакции сульфида железа (II) с кислотами:
Сульфид железа (II) реагирует с сильными минеральными кислотами.
7. реакция термического разложения сульфида железа (II):
FeS → Fe + S (t = 700 о С).
В результате реакции термического разложения сульфида железа (II) образуются железо и сера . Реакция протекает в вакууме .
Применение и использование сульфида железа (II):
Сульфид железа (II) используется лишь в нескольких отраслях:
– в качестве исходного продукта для получения сероводорода в лабораторных условиях,
– в качестве сырья в производстве чугуна, как твердый источник сероводорода.
Примечание: © Фото https://www.pexels.com, https://pixabay.com

Мировая экономика
Справочники
Востребованные технологии
- Концепция инновационного развития общественного производства – осуществления Второй индустриализации России на период 2017-2022 гг. (106 545)
- Экономика Второй индустриализации России (102 552)
- Программа искусственного интеллекта ЭЛИС (27 771)
- Метан, получение, свойства, химические реакции (24 221)
- Этилен (этен), получение, свойства, химические реакции (24 027)
- Природный газ, свойства, химический состав, добыча и применение (21 590)
- Крахмал, свойства, получение и применение (20 907)
- Пропилен (пропен), получение, свойства, химические реакции (20 045)
- Целлюлоза, свойства, получение и применение (19 755)
- Прямоугольный треугольник, свойства, признаки и формулы (19 011)
Поиск технологий
О чём данный сайт?
Настоящий сайт посвящен авторским научным разработкам в области экономики и научной идее осуществления Второй индустриализации России.
Он включает в себя:
– экономику Второй индустриализации России,
– теорию, методологию и инструментарий инновационного развития – осуществления Второй индустриализации России,
– организационный механизм осуществления Второй индустриализации России,
– справочник прорывных технологий.
Мы не продаем товары, технологии и пр. производителей и изобретателей! Необходимо обращаться к ним напрямую!
Мы проводим переговоры с производителями и изобретателями отечественных прорывных технологий и даем рекомендации по их использованию.
О Второй индустриализации
Осуществление Второй индустриализации России базируется на качественно новой научной основе (теории, методологии и инструментарии), разработанной авторами сайта.
Конечным результатом Второй индустриализации России является повышение благосостояния каждого члена общества: рядового человека, предприятия и государства.
Вторая индустриализация России есть совокупность научно-технических и иных инновационных идей, проектов и разработок, имеющих возможность быть широко реализованными в практике хозяйственной деятельности в короткие сроки (3-5 лет), которые обеспечат качественно новое прогрессивное развитие общества в предстоящие 50-75 лет.
Та из стран, которая первой осуществит этот комплексный прорыв – Россия, станет лидером в мировом сообществе и останется недосягаемой для других стран на века.
Источник
Сульфид железа (II)
| Сульфид железа (II) | |
|---|---|
 | |
| Систематическое наименование | Сульфид железа (II) |
| Хим. формула | FeS |
| Состояние | твёрдое |
| Молярная масса | 87,910 г/моль |
| Плотность | 4,84 г/см³ |
| Температура | |
| • плавления | 1194 °C |
| Рег. номер CAS | 1317-37-9 |
| PubChem | 14828 |
| Рег. номер EINECS | 215-268-6 |
| SMILES | |
| ChemSpider | 8466211 |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Сульфид железа (II) — сложное неорганическое вещество с химической формулой FeS класса неорганических сульфидов .
Содержание
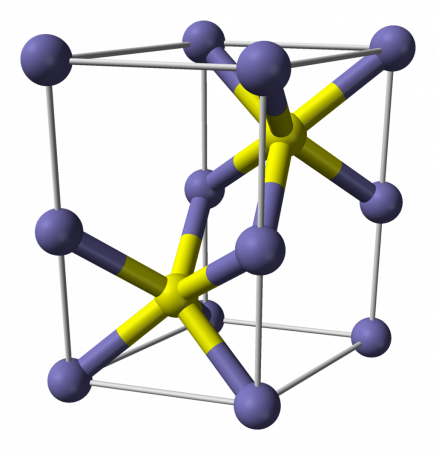
Описание и структура
Сульфид железа (II) — бескислородная соль. Кристаллы чёрного цвета с металлическим блеском и гексагональной кристаллической решёткой, тугоплавкий, разлагается при нагревании в вакууме. Во влажном состоянии чувствителен к кислороду воздуха. Нерастворим в воде. Не выпадает в осадок при насыщении растворов солей железа (II) сероводородом. Разлагается кислотами. Применяется как сырье в производстве чугуна, твердый источник сероводорода. Не притягивается магнитом.
Получение
1. Взаимодействие железа с серой:
Реакция начинается при нагревании смеси железа с серой в пламени горелки, далее может протекать и без подогрева, с выделением теплоты.
2. Взаимодействие оксида железа (III) с водородом и сероводородом:
Химические свойства
1. Взаимодействие с концентрированной HCl:
2. Взаимодействие с концентрированной HNO3:
Применение
Сульфид железа (II) служит обычным исходным продуктом при получении сероводорода в лабораторных условиях. Гидросульфид железа [Fe(SH)2] и/или отвечающая ему основная соль [Fe(SH)OH] является важнейшей составной частью некоторых лечебных грязей.
Источник
















