- Способы получения оксидов хлора
- Оксиды хлора
- Оглавление
- Обзор
- характеристики
- Диоксид хлора
- Дихлороксид
- Окись хлора
- Диоксид дихлора
- Хлоропероксид
- Дихлортриоксид
- Дихлортетраоксид
- Триоксид хлора
- Тетраоксид хлора
- Дихлоргексид
- Дихлоргептоксид
- Как получить оксиды хлора
- Содержание статьи
- Получение Cl2O
- Получение ClO2
- Получение Cl2O6
- Получение Cl2O7
- Физические свойства оксидов
Способы получения оксидов хлора
Большинство оксидов галогенов неустойчивы и получаются косвенным путем, так как галогены с кислородом не взаимодействуют.Известны следующие оксиды галогенов (табл.6).
Таблица 6. Оксиды галогенов.
Оксиды галогенов (I). Молекулы оксидов Х2О (Х = F, Cl, Br) имеют угловое строение:
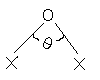 | X = F; | = 103.2 0 ; | 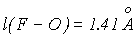 ; ; |
| X = Cl; | =110.9 0 ; | 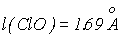 |
F2O (иногда его называют дифторидом кислорода) — бесцветный газ (т.пл. -224 0 С, т.кип. -145 0 С), который может быть получен при пропускании фтора через 2%-ный водный раствор NaOH:
При увеличении концентрации NaOН выход F2O уменьшается из-за протекания побочной реакции:
то есть вместо F2O наблюдается выделение кислорода.
Оксид хлора (I) Cl2O — желто-коричневый газ (т.пл. -116 0 С, т.кип. 4 0 С).
Его получают, пропуская ток хлора через трубку со свежеосажденным и затем высушенным оксидом ртути (II):
2HgO + 2Cl2 Hg2OСl2 + Cl2O .
Образующийся Cl2O конденсируют при температуре -60 о С. Соединение крайне неустойчиво, при повышенной температуре разлагается со взрывом.
Cl2O хорошо растворим в воде (при 0 о С 1 об.H2O растворяет 200 об. Cl2O), его водный раствор проявляет свойства слабой кислоты:
Оксид брома (I) Br2O напоминает по свойствам и методу синтеза Cl2O.
Диоксиды ClO2 и BrO2. Диоксид хлора ClO2 при стандартных условиях — желтый газ (т.пл.-60 0 С, т.кип. 10 0 С). Это единственный из оксидов галогенов, который используется в промышленности, например, как отбеливающее вещество. В технике его получают пропусканием SO2 в подкисленный раствор хлората натрия:
В лабораторных условиях ClO2 синтезируют из хлората KClO3 и влажной щавелевой кислоты в присутствии концентрированной серной кислоты:
Образующийся ClO2 разбавлен CO2 , что снижает вероятность взрыва. Если же использовать концентрированную H2SO4 и KClO3, то реакция становится взрывоопасной:
Работать с ClO2 нужно крайне осторожно: он взрывается от внезапного механического воздействия, введения в систему восстановителя (резиновая пробка), при нагревании до 100 о С.
Молекулы ClO2 и BrO2 имеют угловое строение: 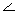
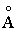
BrO2 (т.пл. -40 0 С) — неустойчивый оксид и выше -40 0 С разлагается:
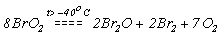
I2O4 — желтое кристаллическое вещество, построенное из ионов IO + и IO — 3 . При нагревании выше 100 0 С разлагается на I2 и O2.
Оксид хлора (VI) Cl2O6— красная маслообразная жидкость (т.пл. 3.5 0 С, т.кип. 203 0 С), взрывоопасная, легко разлагается на ClO2 и O2. В твердой фазе построен из ионов 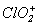
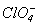
Образуется при окислениии ClO2 озоном:
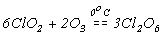
Оксид иода (V) I2O5 — белое твердое вещество (т.пл. 300 0 С), единственный термодинамически устойчивый из оксидов галогенов. Твердый оксид I2O5 состоит из молекул O2IOIO2,, связанных между собой слабым межмолекулярным взаимодействием. Получают I2O5 дегидратацией HIO3 при 200-250 0 С в потоке сухого воздуха. I2O5 используется как окислитель в количественном анализе для определения СО:
5СО + I2O5 I2 + 5CO2.
Выделяющийся в эквивалентном количестве иод определяют титрованием тиосульфатом.
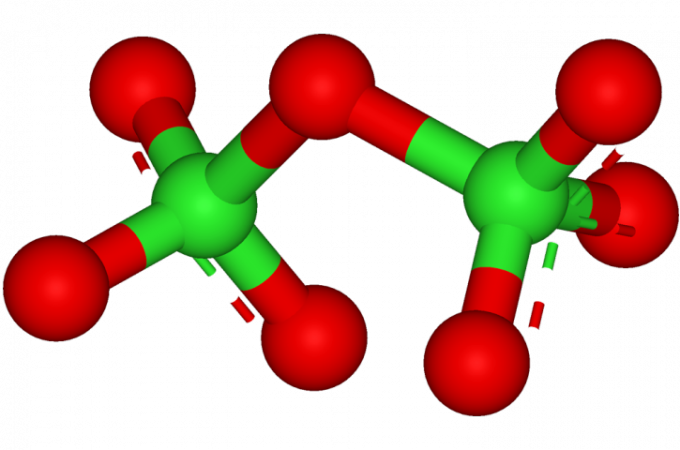
Оксид хлора (VII) Cl2O7 — маслянистая бесцветная жидкость (т.пл.-93 0 С, т.кип. 80 0 С), легко взрывается. Молекула Cl2O7 построена из двух тетраэдров ClO4, имеющих общую вершину. Cl2O7 — ангидрид хлорной кислоты HClO4. Его получают дегидратацией концентрированной хлорной кислоты с помощью P2O5 с последующей осторожной перегонкой в вакууме:
6HClO4 + P2O5 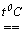
Источник
Оксиды хлора
Оксиды хлора — это химические соединения между галогеном, хлором и кислородом . В зависимости от степени окисления хлор образует ряд оксидов, которые обычно и особенно легко разлагаются при нагревании. В присутствии окисляемых веществ оксиды хлора имеют тенденцию к взрыву , все они являются нестабильными соединениями и, следовательно, очень химически активными и сильными окислителями.
Оглавление
Обзор
| Число окисления | |||||||
| Я. | II | III | IV | V | VI | VII | |
| ClO x | ClO | ClO 2 | ClO 3 | ||||
| Cl 2 O y | Cl 2 O | Cl 2 O 2 | Cl 2 O 3 | Cl 2 O 4 | Cl 2 O 5 * | Cl 2 O 6 | Cl 2 O 7 |
* Дихлорпентаоксид (Cl 2 O 5 ) пока неизвестен.
характеристики
Диоксид хлора
Технически важен только диоксид хлора (ClO 2 ). При стандартной температуре это желто-красноватый газ с молярной массой 67,46 г / моль. При нагревании он взрывоопасно разлагается на Cl 2 и O 2 .
Дихлороксид
Дихлороксид ( дихлормоноксид , Cl 2 O) представляет собой желто-коричневый газ с молярной массой 86,91 г / моль. При стандартной температуре он имеет плотность 3,89 г / л. Монооксид дихлор замерзает при −116 ° C, кипит при 4 ° C и взрывоопасен . Dichloroxide является ангидридом из хлорноватистой кислоты .
Cl 2 O можно получить, пропустив хлор над свежим оксидом ртути (II) :
2 С. л 2 + 2 ЧАС грамм О → С. л 2 О + ЧАС грамм О ⋅ ЧАС грамм С. л 2 <\ Displaystyle \ mathrm <2 \ cl_ <2>+2 \ HgO \ rightarrow \ Cl_ <2>O + HgO \ cdot HgCl_ <2>>>
Окись хлора
Окись хлора (ClO), радикал, играет важную роль в создании озоновой дыры в стратосфере, когда присутствует хлор. Он образуется, например, при фотолизе или микроволновом разряде смесей хлор / кислород. Альтернативно, он может возникать в результате реакции элементарного хлора с озоном или дихлормоноксидом.
С. л + О 3 → С. л О + О 2 <\ Displaystyle \ mathrm
Диоксид дихлора
Дихлордиоксид (Cl 2 O 2 , пероксид дихлора, иногда называемый пероксидом хлора) получают димеризацией двух радикалов монооксида хлора в соответствии с:
2 С. л О → С. л 2 О 2 + 73 k J <\ displaystyle \ mathrm <2 \ clo rightarrow cl_ <2>O_ <2>+73 \, кДж>>
Термически он распадается на хлор и кислород, фотохимически — на атомы хлора, среди прочего. Они также катализируют распад озона в атмосфере.
Хлоропероксид
Хлорпероксид (ClOO) — это короткоживущий изомер диоксида хлора. Он может быть образован путем перегруппировки из диоксида хлора после того, как он был разделен светом, или из радикала хлора и кислорода, и имеет срок службы всего 0,3-0,4 наносекунды .
Дихлордиоксид также иногда называют хлорпероксидом, но из-за короткого срока службы ClOO вряд ли возникнет какой-либо риск путаницы.
Дихлортриоксид
Дихлортриоксид (Cl 2 O 3 ) представляет собой метастабильное твердое вещество темно-коричневого цвета при -78 ° C, которое медленно разлагается при -45 ° и взрывоопасно при температуре около 0 ° C с образованием Cl 2 и O 2 . Дихлортриоксид можно рассматривать как хлорат хлора (Cl — OClO 2 ). Дихлортриоксид имеет молярную массу 118,91 г / моль. Он может образоваться из диоксида хлора в результате низкотемпературного фотолиза:
С. л О + С. л О 2 ⇄ С. л 2 О 3 + 46 k J <\ displaystyle \ mathrm
Дихлортетраоксид
Дихлортетраоксид (Cl 2 O 4 ) можно рассматривать как хлорперхлорат (Cl — OClO 3 , оксид хлора (I, VII)). Он может быть представлен фотохимически из диоксида хлора и хлорированием перхлоратов хлорфторсульфонатом.
Триоксид хлора
Триоксид хлора (ClO 3 ) имеет пирамидальную структуру. Под воздействием радиации он отщепляет атомы кислорода.
Тетраоксид хлора
Тетраоксид хлора (ClO 4 ) представляет собой радикал. Он существует только как промежуточный продукт реакции и также образуется во время термолиза Cl 2 O 6 .
Дихлоргексид
Дихлоргексаоксид (Cl 2 O 6 ) представляет собой маслянистую жидкость черно-красного цвета с плотностью 2,02 г / мл и молярной массой 166,91 г / моль. Он замерзает при 3,5 ° C и закипает при 203 ° C. Это сильный окислитель, который при взрыве вступает в реакцию со многими восстановителями. В виде газа и жидкости он присутствует в виде перхлората ковалентного хлора (оксид хлора (V, VII), смешанный ангидрид из хлорной и хлорной кислоты), в виде твердого вещества с изолированными ионами ClO 2 + и ClO 4 — .
Он может быть представлен окислением диоксида хлора разбавленным кислородом озоном:
2 С. л О 2 + 2 О 3 → С. л 2 О 6-е + 2 О 2 <\ Displaystyle \ mathrm <2 \ clo_ <2>+2 \ O_ <3>\ rightarrow \ Cl_ <2>O_ <6>+2 \ O_ <2>>>
Реакция с водой производит хлорную кислоту и хлорную кислоту , с помощью озона медленно dichloroheptaoxide:
С. л 2 О 6-е + ЧАС 2 О ⇄ ЧАС С. л О 3 + ЧАС С. л О 4-й <\ displaystyle \ mathrm
Дихлоргептоксид
Дихлоргептаоксид (Cl 2 O 7 ) представляет собой бесцветное масло с плотностью 1,86 г / мл. Он замерзает при -92 ° C, кипит при 82 ° C и имеет молярную массу 182,91 г / моль. У молекулы нет зеркальной плоскости, две группы ClO 3 повернуты друг относительно друга на 15 градусов. Дихлоргептаоксид взрывоопасен, но по-прежнему остается наиболее стойким оксидом хлора.
Дихлоргептаоксид — ангидрид хлорной кислоты ; соответственно, его можно приготовить путем дегидратации хлорной кислоты пятиокисью фосфора с последующей вакуумной перегонкой:
4-й ЧАС С. л О 4-й + П. 4-й О 10 → 2 С. л 2 О 7-е + 4-й ЧАС П. О 3 <\ Displaystyle \ mathrm <4 \ hclo_ <4>+ P_ <4>O_ <10>\ rightarrow \ 2 \ Cl_ <2>O_ <7>+ \ 4 \ HPO_ <3>>>
Источник
Как получить оксиды хлора
Содержание статьи
Хлор образует с кислородом целый ряд оксидов, общее число которых составляет целых пять видов. Все их можно описать общей формулой ClxOy. В них валентность хлора меняется от 1 до 7.
Валентность разных оксидов хлора различна: Cl2O — 1, Cl2O3 — 3, ClO2 — 4, Cl2O6 — 6, Cl2O7 — 7.
Оксид хлора(I) применяют для производства гипохлоритов, которые являются сильными отбеливающими и обеззараживающими агентами.
Оксид хлора(II) активно применяют для отбеливания муки, целлюлозы, бумаги и других вещей, а также для стерилизации и дезинфекции.
Оксид хлора(VI) и оксид хлора(VII) применяют для синтеза органических соединений.
Получение Cl2O
Данный оксид на крупнотоннажных производствах получают двумя способами.
1. По методу Пелуза. Проводят реакцию между газообразным хлором и оксидом ртути. В зависимости от условий может образоваться иное соединение ртути, однако целевой продукт остается. После этого газообразный оксид хлора сжижают при температуре -60 градусов Цельсия.
Уравнения реакции, описывающие метод Пелуза:
2HgO + Cl2 = Hg2OCl2 + Cl2O
HgO + 2Cl2 = HgCl2 + Cl2O
2. Взаимодействие хлора с водным раствором карбоната натрия по реакции:
2Cl2 + 2Na2CO3 + H2O = 2NaHCO3 + Cl2O + 2NaCl
Карбонат натрия может быть заменен другими карбонатами щелочных или щелочноземельных металлов.
Получение ClO2
Единственный промышленный метод получения диоксида хлора основан на взаимодействии хлората натрия и диоксида серы в кислой среде. Результатом такого взаимодействия становится реакция:
2NaClO3 + SO2 + H2SO4 = 2NaHSO4 + ClO2
Получение Cl2O6
В промышленности Cl2O6 получают взаимодействием диоксида хлора с озоном:
2ClO2 + 2O3 = 2O2 + Cl2O6
Получение Cl2O7
1. Осторожное нагревание хлорной кислоты с фосфорным ангидридом приводит к отделению маслянистой жидкости, которая является оксидом хлора (VII). Весь процесс описывается реакцией:
2HClO4 + P4O10 = H2P4O11 + Cl2O7
2. Второй способ получения данного оксида связан с электричеством. Если проводить электролиз раствора хлорной кислоты, то в анодном пространстве можно обнаружить Cl2O7.
3. Нагревание в вакууме перхлоратов переходных металлов приводит к образованию оксида хлора (VII). Наиболее часто нагревают перхлорат ниобия либо молибдена.
Физические свойства оксидов
Cl2O: при стандартных условиях буровато-желтый газ с запахом хлора, а при температуре ниже +2 градусов Цельсия золотисто-красная жидкость. Взрывоопасен в больших концентрациях.
ClO2: при стандартных условиях – газ с характерным запахом красно-желтого цвета, при температуре ниже +10 градусов Цельсия – красно-коричневая жидкость. Взрывается на свету, в присутствии восстановителей и при нагревании.
Cl2O6: неустойчивый газ, который начинает разлагаться при температуре от 0 до +10 градусов Цельсия с образованием диоксида хлора, при 20 градусах Цельсия образуется хлор. Ввиду образования диоксида хлора – взрывоопасен.
Cl2O7: бесцветная маслянистая жидкость, которая при нагревании выше 120 градусов Цельсия взрывается. Может детонировать от удара.
Источник