- Способы получения оксида ртути
- Свойства оксида ртути и реакция ее разложения
- Свойства оксида ртути
- Получение оксида ртути (на примере опыта)
- Реакция разложения оксида ртути
- Оксид ртути II
- Содержание
- История
- Получение
- Свойства
- Токсикология
- Красная ртуть и HgO
- Структура оксида ртути (Hg2O), свойства, применение
- Химическая структура
- свойства
- приложений
- риски
Способы получения оксида ртути
Для ртути (II) известны оксид HgO, галогениды HgГ2 (где Г – галоген) и соли.
Оксид ртути (II) HgO существует в двух формах – красной и желтой, обе формы имеют одинаковую структуру, кристаллизуются в ромбической сингонии, цвет зависит от размера кристаллов: при размерах до 4 мкм цвет оксида желтый, выше 8 мкм – красный. Красная форма образуется при осторожном нагревании нитрата ртути (II) при 350 °С:
Желтая – при добавлении щелочей к раствору соли Hg (II) 
Оксид ртути (II) обладает только основными свойствами, растворяется в кислотах:
Гидроксид ртути (II) Hg(OH)2 не выделен, он разлагается в момент образования на оксид и воду.
Хлорид ртути (II) HgCl2 – сулема – образуется при нагревании смеси сульфата ртути (II) с хлоридом натрия:
Сулема – бесцветное кристаллическое вещество, плотность 5,44 г/см 3 , температура плавления 277°С, плохорастворима в воде.
Одно из широко используемых соединений ртути (II) – фульмиат ртути (II) Hg(CNO)2, соль гремучей кислоты, его называют гремучей ртутью. Это первое взрывчатое вещество, при ударе мгновенно разлагается:
Источник
Свойства оксида ртути и реакция ее разложения
Получение оксида ртути на примере опыта
Оксид ртути — это бинарное соединение кислорода и ртути, формула вещества — HgO. При нормальных условиях это твердое непрочное вещество, в зависимости от дисперсности бывает красного или желтого цвета — основной и важнейший оксид ртути. В природе оксид ртути практически не встречается, исключение — редкий минерал монтроидит. В 1774 году ученый Джозеф Пристли с помощью оксида ртути открыл кислород (реакция разложения оксида ртути).
Свойства оксида ртути
HgO желтого цвета — более химически активное вещество, разлагающееся при температуре 332 градусов Цельсия, краснеющее при нагревании. Красный оксид ртути распадается при 500 °С, а при нагревании меняет свой цвет на черный (эта реакция обратимая). Оксид ртути(II) малорастворим в воде и проявляет слабые основные свойства. Растворяется в концентрированных растворах щелочей, образуя при этом гидроксокомплексы. HgO желтого цвета взаимодействует с NH₃, образуя основания Миллона:
2HgO + NH₃ → [Hg₂N]OH · H₂O + Q
Это вещество вступает в реакцию с кислотами, образуя соответствующие соли. Применяется для получения ртути, а также используется при изготовлении некоторых видов гальванических элементов. Оксид ртути очень токсичен.
Получение оксида ртути (на примере опыта)
Оксид ртути (II) — полезный реактив, из которого в лабораторных условиях можно получить разнообразные соли ртути, к примеру хлорид или ацетат ртути(II). Ацетат ртути(II) используется в органическом синтезе (например, для получения изопропилата алюминия), а с помощью HgCl₂ можно получить активированную амальгаму магния.
Для проведения опыта потребуется оборудование:
- колба со шлифом;
- пробирка;
- обратный холодильник;
- пористый стеклянный фильтр;
- коническая колба.
Используемые реактивы:
- азотная кислота (65%-ная);
- ртуть;
- едкий натр;
- хлорид натрия или соляная кислота.
Техника безопасности во время проведения опыта
Оксиды азота (II) и (IV) ядовиты и канцерогенны, работать с ним необходимо очень осторожно. Соли ртути токсичны для людей и опасны для окружающей среды. Ядовитый нитрат ртути легко всасывается через кожу. Работать необходимо под тягой и с обратным холодильником, так как отходящие газы часто содержат пары ртути, опасные сами по себе.
Синтез следует проводить с крайней осторожностью. Смертельная доза нитрата ртути — от 0,2 до 0,4 гр.
Процесс синтеза оксида ртути
В пробирке взвешивают 30 г (0,15 моль) ртути. В колбу на 250 мл с обратным холодильником наливают 60 мл (0,9 моль) HNO₃. Пипеткой небольшими порциями ртуть добавляют в кислоту — тут же происходит реакция. Затем снова надевают обратный холодильник. Раствор нагревается и «закипает» от сильного выделения диоксида азота. По мере завершения реакции выделение бурого газа прекращается и раствор в колбе становится бесцветным. Уравнение реакции:
Hg + 4HNO₃ => Hg(NO₃)₂ + 2NO₂ + 2H₂O
Чтобы предотвратить образование нитрата ртути(I), азотную кислоту берут в избытке. Жидкость остывает, и к ней добавляют HCl или NaCl — это проба на наличие ртути(I) Hg₂²⁺. При выпадении осадка Hg₂Cl₂ в растворе присутствует ртуть (I). К раствору необходимо добавить немного азотной кислоты, затем нагреть. При отрицательной пробе на наличие ртути(I) раствор медленно выливают в 250 мл 4М раствора гидроксида натрия. При этом образуется оранжевый осадок оксида ртути(II) HgO, который нужно отфильтровать. Уравнение реакции:
Hg(NO₃)₂ + 2NaOH => HgO + 2NaNO₃ + H₂O
Продукт промывают водой на фильтре и высушивают до постоянной массы в эксикаторе над силикагелем. Выход оксида ртути (II) составляет 32,467 г.
При проведении опытов с оксидом ртути следует строго соблюдать правила техники безопасности. Здесь вы найдете безопасные опыты, которые можно проводить дома.
Обезвреживание отходов ртути
Весь фильтрат и промывные воды собирают в большой стакан, при необходимости реакцию раствора доводят до щелочной и добавляют избыток сульфида натрия. При этом образуется черный сульфид ртути HgS, который можно слить в канализацию.
Запрещено выливать в раковину растворимые соли ртути. Полученный оксид ртути хранится в плотно закрытых банках.
Реакция разложения оксида ртути
Получение кислорода в лабораторных условиях основано на разложении непрочных кислородсодержащих соединений, в частности бертолетовой соли, марганцовокислого калия, перекиси натрия и окиси ртути. При нагревании эти вещества разлагаются с выделением кислорода. Реакцию разложения оксида ртути можно продемонстрировать в опыте.
Чтобы провести такой эксперимент, необходимо взять пробирку из тугоплавкого стекла с согнутым нижним концом (длина 17 см, диаметр 1,5 см, длиной 3 см). В нижний конец насыпают 3—5 г красной окиси ртути. В укрепленную в штативе пробирку в наклонном положении вставляют резиновую пробку с отводной трубкой. По ней выделяющийся при нагревании кислород отводится в кристаллизатор с водой.
При нагревании красной окиси ртути до 500 °С из отводной трубки будет выделяться кислород, а внутренние стенки пробирки покроются капельками. Кислород плохо растворяется в воде, поэтому его собирают, вытесняя воду после полного удаления воздуха из прибора.
После завершения опыта необходимо вынуть отводную трубку из кристаллизатора с водой, погасить горелку и открыть пробку только после полного остывания пробирки (пары ртути очень ядовиты). Вместо пробирки можно использовать реторту с приемником для ртути. Из 10 г красной окиси ртути получают 500 мл кислорода. Уравнение реакции разложения оксида ртути:
2HgO = 2Hg + O₂ — 2×25 ккал.
Внимание! В эксперименте использованы токсичные и опасные для здоровья вещества. Не пытайтесь повторить этот опыт самостоятельно.
Источник
Оксид ртути II
| Оксид ртути II | |
|---|---|
 | |
| Систематическое наименование | Оксид ртути II |
| Хим. формула | HgO |
| Состояние | твёрдые кристаллы оранжевого/красного цвета |
| Молярная масса | 216.59 г/моль г/моль |
| Плотность | около 10 г/см³ |
| Температура | |
| • разложения | 500 °C |
| Энтальпия | |
| • образования | 90,458 кДж/моль |
| Растворимость | |
| • в воде | нерастворим |
| Рег. номер CAS | [21908-53-2] |
| PubChem | 30856 |
| Рег. номер EINECS | 244-654-7 |
| SMILES | |
| RTECS | OW8750000 |
| ChEBI | 81882 |
| Номер ООН | 1641 |
| Предельная концентрация | 0.0003 мг/м3 (в пересчёте на Hg) |
| ЛД50 | 18 мг/кг |
| Пиктограммы ECB |  |
| Приведены данные для стандартных условий (25 °C, 100 кПа), если не указано иное. | |
Оксид ртути II — бинарное соединение ртути и кислорода с формулой HgO. Это твёрдое непрочное при нормальных условиях вещество в зависимости от дисперсности красного или оранжевого (жёлтого) цвета является основным и важнейшим оксидом ртути и практически не встречается в природе, за исключением редкого минерала монтроидита. Очень ядовит.
Содержание
История
В 1774 году с помощью оксида ртути II Джозеф Пристли открыл новый химический элемент — кислород.
Получение
Красный оксид ртути получают нагреванием ртути до 300 °C или пиролизом нитрата ртути.
2 Hg + O2 → 2 HgO
Жёлтый оксид получают осаждением солей ртути II щелочами, например:
HgS + 2 NaOH → HgO ↓ + Na2S + H2O
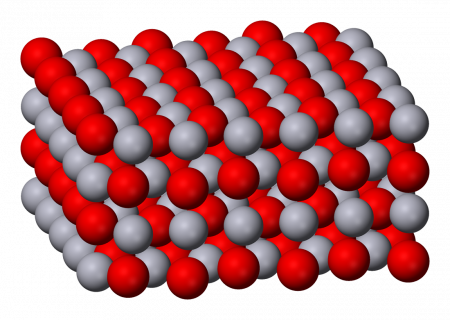
Разница в цвете объясняется размером частиц, обе формы имеют одинаковую структуру — цепь линейных звеньев состава O-Hg-O соединённых под углом 108°. Размеры частиц жёлтого оксида ртути составляют до 4 мкм, красной — более 8 мкм.
Свойства
Жёлтый HgO является более химически активным, разлагается при температуре 332 o C, при нагревании краснеет. Красный HgO распадается при 500, а при нагревании обратимо меняет свой цвет на чёрный.
Оксид ртути II в воде малорастворим, его насыщенный водный раствор имеет концентрацию 2,6⋅10 -4 моль/л для жёлтой формы и 2,4⋅10 -4 моль/л для красной. Проявляет слабые основные свойства.
Растворяется в концентрированных растворах щелочей, при этом образуются гидроксокомплексы. Жёлтый HgO взаимодействует с NH3 с образованием основания Миллона:
Это вещество реагирует с кислотами, образуя соответствующие соли [Hg2N]X•H2O (X = NO3 — , ClO3 — , Cl3 — , Br3 — , I3 — ).
Применяется для получения ртути, а также в некоторых видах гальванических элементов.
Обладает сильным токсическим действием.
Токсикология
Как и все соединения ртути, оксид ртути II высокотоксичен. Случайное проглатывание этого вещества приводит к смертельному исходу. Смертельная доза (ЛД50) — 18 мг/кг.
Красная ртуть и HgO
В 90-е годы оксид ртути нередко выдавался за несуществующую красную ртуть, так как он действительно красного, скорее ярко-рыжего цвета и содержит ртуть. Во времена «краснортутной лихорадки» фиксировалось немало случаев хищения и продажи этого вещества под видом «красной ртути».
Источник
Структура оксида ртути (Hg2O), свойства, применение
оксид ртути (I), чья химическая формула представлена как Hg2Или это соединение в твердой фазе, считающееся токсичным и нестабильным с химической точки зрения, превращающееся в ртуть в ее элементарной форме и оксид ртути (II).
Есть только два химических вещества, которые могут образовывать ртуть в сочетании с кислородом, потому что этот металл имеет две уникальные степени окисления (Hg). + и рт 2+ ): оксид ртути (I) и оксид ртути (II). Оксид ртути (II) находится в состоянии твердой агрегации, получая в двух относительно стабильных кристаллических формах.
Это соединение также известно просто как оксид ртути, поэтому только этот вид будет рассматриваться в дальнейшем. Очень распространенная реакция, которая происходит с этим веществом, заключается в том, что при нагревании происходит разложение с образованием ртути и газообразного кислорода в эндотермическом процессе..
- 1 Химическая структура
- 2 свойства
- 3 использования
- 4 риска
- 5 ссылок
Химическая структура
В условиях атмосферного давления этот вид встречается в двух уникальных кристаллических формах: одна называется киноварь, а другая — монтродита, которая встречается очень редко. Обе формы становятся тетрагональными при давлении выше 10 ГПа.
Структура киновари основана на примитивных гексагональных клетках (hP6) с тригональной симметрией, спиральная ось которых ориентирована влево (P3)221); вместо этого структура монодита орторомбическая, основанная на примитивной сетке, которая формирует плоскости скольжения, перпендикулярные трем осям (Pnma).
Напротив, две формы оксида ртути могут быть визуально различимы, потому что одна красная, а другая желтая. Это различие в цвете происходит благодаря размерам частицы, потому что две формы имеют одинаковую структуру.
Чтобы получить красную форму оксида ртути, можно прибегнуть к нагреву металлической ртути в присутствии кислорода при температуре около 350 ° C или к процессу пиролиза нитрата ртути (II) (Hg (NO.).3)2).
Таким же образом, для получения желтой формы этого оксида можно прибегнуть к осаждению иона Hg 2+ в водной форме с основанием.
свойства
— Он имеет температуру плавления приблизительно 500 ° С (эквивалентную 773 К), выше которой он подвергается разложению, и молярную массу или молекулярную массу 216,59 г / моль..
— Он находится в состоянии сплошной агрегации разных цветов: оранжевого, красного или желтого в зависимости от степени рассеивания..
— Это оксид неорганической природы, доля которого в кислороде составляет 1: 1, что делает его бинарным видом.
— Он считается нерастворимым в аммиаке, ацетоне, эфире и спирте, а также в других растворителях органической природы..
— Его растворимость в воде очень низкая, составляет примерно 0,0053 г / 100 мл при стандартной температуре (25 ° C) и увеличивается с ростом температуры.
— Это считается растворимым в большинстве кислот; однако желтая форма проявляет большую реакционную способность и большую растворяющую способность.
— Когда оксид ртути подвергается воздействию воздуха, он подвергается разложению, а его красная форма подвергается воздействию источников света..
— При нагревании до температуры, при которой он разлагается, он выделяет ртутные газы с высокой токсичностью.
— Только при нагревании до 300-350 ° C можно сочетать ртуть с кислородом с экономической эффективностью.
приложений
Он используется в качестве прекурсора при получении элементарной ртути, поскольку он довольно легко подвергается процессам разложения; в свою очередь, когда он разлагается, он производит кислород в газообразной форме.
Подобным образом, этот оксид неорганической природы используется в качестве титранта или титрантного агента стандартного типа для анионных частиц, поскольку образуется соединение, которое имеет большую стабильность, чем его исходная форма..
В этом смысле оксид ртути растворяется, когда он обнаруживается в концентрированных растворах основных веществ, образуя соединения, называемые гидроксокомплеями..
Эти соединения представляют собой комплексы со структурой Мх(ОН)и, где М представляет собой атом металла, а индексы x и y представляют количество раз, когда этот вид обнаружен в молекуле. Они очень полезны в химических исследованиях.
Кроме того, оксид ртути (II) можно использовать в лабораториях для производства различных солей металлов; например, ацетат ртути (II), который используется в процессах органического синтеза.
Это соединение также используется при смешивании с графитом в качестве материала для катодного электрода при производстве ртутных батарей и элементов электрического типа из оксида ртути и цинка..
риски
— Это вещество, которое проявляет основные характеристики в очень слабой форме, является очень полезным реагентом для различных применений, таких как упомянутые ранее, но в то же время оно представляет значительный риск для человека при воздействии этого.
— Оксид ртути обладает высокой токсичностью и способен всасываться через дыхательные пути, поскольку он выделяет раздражающие газы, когда он находится в форме аэрозоля, а также чрезвычайно токсичен, если он попадает в организм или поглощается кожей при непосредственном контакте с этим.
— Это соединение вызывает раздражение глаз и может привести к повреждению почек, что впоследствии приводит к проблемам с почечной недостаточностью..
— Когда это химическое вещество так или иначе потребляется водными видами, оно накапливается в них и воздействует на организм людей, которые регулярно их потребляют..
— Нагревание оксида ртути приводит к образованию паров ртути, которые обладают высокой токсичностью в дополнение к газообразному кислороду, что увеличивает риск воспламеняемости; то есть, чтобы произвести огни и улучшить сгорание в этих.
— Этот неорганический оксид обладает сильным окислительным поведением, при котором он вызывает бурные реакции при контакте с восстановителями и некоторыми химическими веществами, такими как хлорид серы (Cl2S2), перекись водорода (H2О2), хлор и магний (только при нагревании).
Источник









