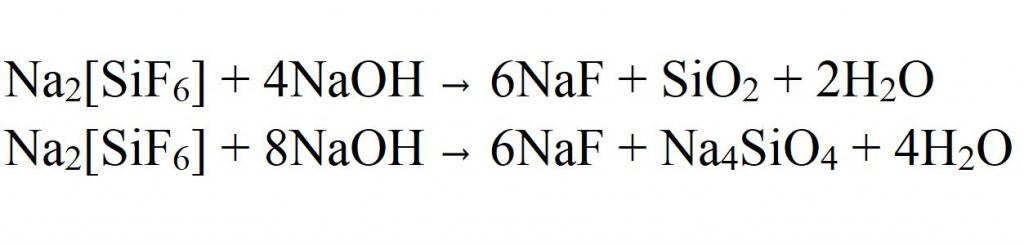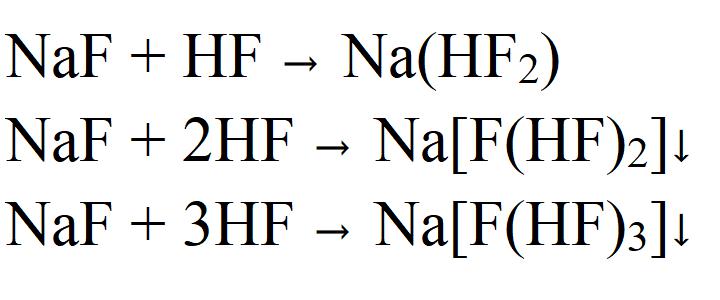- Фторид натрия: способы получения и химические свойства
- Способ получения
- Качественная реакция
- Химические свойства
- Фторид натрия: формула, свойства, польза и вред
- Распространение в природе
- Получение в промышленности
- Получение в лаборатории
- Физические свойства
- Химические свойства
- Токсичность
- Применение
- Позитивное влияние фтора на организм
- Проблемы при избытке фтора в организме
- Фторирование воды
- Применение в фармакологии
- Способ получения фторида натрия
Фторид натрия: способы получения и химические свойства
Фторид натрия — соль щелочного металла натрия и плавиковой кислоты. Белое вещество, плавится без разложения. Умеренно растворяется в воде (гидролиз по аниону), растворимость мало зависит от температуры.
Относительная молекулярная масса Mr = 41,99; относительная плотность тв. и ж. вещества d = 2,558; tпл = 997º C;
Способ получения
1. Фторид натрия можно получить путем взаимодействия при комнатой температуре натрия и фтора:
2Na + F2 = 2NaF
2. В результате взаимодействия разбавленной плавиковой кислоты и гидроксида натрия, образуется фторид натрия и вода:
NaOH + HF = NaF + H2O
Качественная реакция
Качественная реакция на фторид натрия — взаимодействие его с хлоридом кальция, в результате реакции происходит выпадение белого осадка:
1. При взаимодействии с хлоридом кальция , фторид натрия образует фторид кальция и хлорид натрия:
2NaF + CaCl2 → 2NaCl + CaF2↓
Химические свойства
1. Фторид натрия вступает в реакцию со сложными веществами :
1.1. Фторид натрия вступает во взаимодействие с концентрированными кислотами .
При кипении в результате взаимодействия с концентрированной серной кислотой фторид натрия образует сульфат натрия и газ фтороводород:
1.2. В реакции с насыщенным гидроксидом лития фторид натрия образует гидроксид натрия и фторид лития:
Источник
Фторид натрия: формула, свойства, польза и вред
Фторид натрия — это неорганическое соединение, соль плавиковой кислоты и натрия. Представляет собой белое кристаллическое вещество без запаха. Химическая формула фторида натрия — NaF. Химическая связь — ионная.
Распространение в природе
В природе это вещество существует в основном в виде минерала виллиомита. Этот минерал и представляет фторид натрия в чистом виде. Он может иметь очень красивую расцветку от карминово-красной, розовой до бесцветной. Является довольно хрупким и относительно нетвердым. Блеск этого минерала напоминает блеск стекла. Его месторождения находятся в Северной Америке, Африке и на Кольском полуострове, но в целом он встречается довольно редко.
Получение в промышленности
Фторид натрия — довольно полезное соединение, поэтому синтезируется он в промышленных масштабах. Мировое производство составляет более 10000 тонн в год. В большинстве случаев сырьем являются гексафторсиликаты, которые также получают искусственно. На производстве их подвергают щелочному гидролизу, в результате которого в реакционной смеси выделяется фторид натрия. Но его еще необходимо отделить от примесей оксида кремния и силиката натрия. Делают это зачастую обыкновенной фильтрацией.
Но гексафторсиликаты даже при термическом разложении или при взаимодействии с карбонатом натрия могут давать фторид натрия. Это также может быть использовано при промышленном синтезе.
Также в промышленности существует способ получения фторида натрия из кальцинированной соды (карбоната натрия) и плавиковой кислоты. В результате их взаимодействия с помощью фильтрации удается получать технически чистый продукт:
Получение в лаборатории
В лаборатории возможны и другие способы получения этого соединения. Самый простой — это реакция нейтрализации гидроксида натрия плавиковой кислотой. Другой вариант: взаимодействие гидроксида натрия с фторидом аммония. Гидроксид натрия может давать фторид и при взаимодействии с простым фтором.
В теории фторид натрия можно получать и из простых веществ: натрия и фтора. Эта реакция протекает очень бурно, хотя на практике ее проводят очень редко.
Еще один способ получения — это термическое разложение дифторгидрата и некоторых комплексных солей. В этом случае получается продукт очень высокой чистоты.
При окислении простого фтора броматом натрия или другими окислителями, содержащими натрий, в качестве продукта может получаться фторид натрия.
Взаимодействием трифторида бора с гидридом натрия, также можно получить эту соль.
Физические свойства
Фторид натрия — это твердое кристаллическое вещество белого цвета. Температура плавления — 992°C, кипения — 1700°C. Не горюч. Так как химическая связь у фторида натрия — ионная, он хорошо растворим в воде, а еще лучше — во фтороводороде. Почти не растворим в органических растворителях. Не гигроскопичен и не образует кристаллогидратов.
Химические свойства
В водных растворах фторид натрия диссоциирует и образует комплексное соединение.
При взаимодействии с плавиковой кислотой образуется дифторгидрат. Но при избытке фтороводорода могут образовываться иные комплесксные соединения, которые называются гидрофториды натрия. Их состав может быть разным в зависимости от соотношения реагентов.
Как видно из химической формулы, фторид натрия — это типичная соль, поэтому он вступает в реакции обмена с другими солями, если в результате реакции образуется осадок или газ. При взаимодействии с кислотами выделяется газообразный фтороводород. А с гидроксидом лития образуется осадок фторида лития.
Фторид натрия может образовывать и другие комплексные соли, в зависимости от реагентов и условий реакции.
Токсичность
Фторид натрия — опасное вещество. Он имеет третий уровень опасности из четырех по стандарту NFPA 704. Смертельная доза для человека составляет 5-10 грамм. Это довольно много, но даже меньшие дозы фторида натрия вредят сердечно-сосудистой системе. Отравление может происходить как при вдыхании отравленного воздуха, так и при попадании этого неорганического соединения в пищу. В последнем случае может происходить раздражение желудка, вплоть до язвы.
Применение
Фторид натрия обладает хорошими антисептическими свойствами, поэтому его иногда добавляют в моющие средства. По той же причине он используется для обработки древесины. Раствор этой соли помогает бороться с плесенью, грибком и насекомыми. Чаще всего используют трехпроцентный раствор. Он хорошо проникает в древесину и защищает ее от гниения. Но у этого средства есть недостаток, из-за которого фторид натрия редко используют, — он легко вымывается из древесины во время дождей, так как эта соль хорошо растворима в воде.
Он также используется при синтезе некоторых химических соединений, в частности фреонов и инсектицидов. Ионы фтора останавливают гликолиз (окисление глюкозы), поэтому фторид натрия применяют для биохимических исследований.
Часто его используют и в металлургической промышленности для очистки поверхностей металлов, а также при их плавке и пайке. Вещество иногда добавляют и в цемент, делая бетон стойким к воздействию кислот, и в смазки для повышения термостойких качеств.
Самое спорное его применение — это добавление в зубные пасты. Для зубов фторид натрия — это источник фтора, который необходим для придания костям и зубам прочности, также служит для профилактики кариеса. Но при высоком потреблении этого элемента могут возникать негативные последствия. Поэтому до сих пор ведутся споры о применении фторидов в качестве добавок для зубной пасты.
Позитивное влияние фтора на организм
Фтор является довольно важным микроэлементом в организме человека, без которого невозможна нормальная его жизнедеятельность. В сутки необходимо потреблять 0,03 мг фтора на килограмм массы тела для взрослого человека. Ребенку же необходимо в 5 раз больше.
Функции фтора в организме очень разнообразны. Он способствует правильному росту и формированию костей, волос и ногтей, так как стабилизирует кальций в процессе минерализации. Особенно это важно во время роста и развития детей, а также при переломах. Этот элемент необходим для поддержания иммунитета. Железо лучше усваивается организмом, если в этом процессе участвует фтор.
При недостатке этого элемента ослабляется зубная эмаль, возрастает риск кариеса. У детей в этом случае могут появляться дефекты при развитии скелета. У взрослых появляется риск развития остеопороза. Это заболевание характеризуется пониженной плотностью костей, из-за чего возрастает их хрупоксть.
Проблемы при избытке фтора в организме
При повышенном содержании фтора в организме может возникнуть флюороз. Это заболевание характеризуется рядом необратимых последствий. В начальных периодах развития болезни страдает зубная эмаль. На ней появляются пятна разной формы и цвета. Пятна легко диагностируются стоматологом, и при своевременном лечении от них можно без труда избавится. Для отбеливания часто используют растворы неорганических кислот, раствор перекиси водорода или растворы других перекисей. После отбеливания эмали проводят реминерализацию раствором глюконата кальция. При лечении более тяжелых форм флюороза рекомендуется приминать глюконат кальция внутрь до окончания терапии. Если при флюорозе возникла эрозия зубной эмали, то применяют композитные материалы и восстанавливают форму зуба, примерно так же, как при пломбировании.
В качестве профилактики данного заболевания можно снизить поступление фтора в организм, если его концентрация в питьевой воде велика. Для этого обычно заменяют источник воды либо же просто проводят фильтрацию. Также можно убрать из рациона продукты, в которых содержится много фтора: морскую рыбу, животное масло, шпинат. Может помочь введение в пищу витаминов С и D, а также глюконата кальция.
Если избыток фтора наблюдается на протяжении длительного периода (10-20 лет), начинают страдать кости. Возникает остеосклероз, при котором, в отличие от остеопороза, плотность костей становится выше нормы, что приводит к снижению их упругости. Это также может стать причиной частых переломов. Но переживать не стоит. Настолько сильный переизбыток фтора в организме может возникнуть только у людей, работающих на производстве фторидов без соблюдения техники безопасности.
Фторирование воды
Как уже было сказано выше, фтор может использоваться для профилактики кариеса. По этой причине в середине прошлого века в некоторых странах начали применять фторирование водопроводной воды. Его суть напоминает хлорирование. В воду добавляют небольшое количество фторида натрия или иного компонента, содержащего фтор, для придания ей определенных свойств. Сегодня в США фторируется 2/3 всей воды.
Чтобы человек получал необходимое количество фтора, по данным Всемирной организации здравоохранения, питьевая вода должна содержать 0,5-1,0 мг фтора в литре. Но обыкновенная вода не всегда содержит такое количество, поэтому приходится увеличивать его искусственно.
Фторирование воды никак не влияет на ее вкус или запах. Благодаря этому процессу очень сильно снижается риск заболевания кариесом, особенно среди детей. Это происходит из-за того, что фтор уничтожает бактерии, которые могут растворять эмаль зубов и вызывать кариес.
Конечно, повышенное содержание фтора может привести к флюорозу, но, согласно авторитетным исследованиям, фторирование воды не может являться причиной развития данной патологии. Других побочных действий у такой воды также не наблюдается. Хотя в последнее время стали появляться некоторые низкокачественные исследования, говорящие об обратном. Набирал популярность и миф, что фторирование воды служит способом для утилизации фторидов, которые являются отходом алюминиевых предприятий. Но эта версия не нашла подтверждения.
Употребление фторированной воды не рекомендуется лишь при некоторых заболеваниях: диабете, гормональных нарушениях, артрите, болезнях щитовидной железы, почек и сердца.
В любом случае воду несложно избавить от присутствия фтора. Фильтры, работающие по принципу обратного осмоса, удаляют почти весь фтор, а дистилляция очищает воду от него полностью. Бытовые фильтры также могут частично или полностью задерживать фтор в себе. Пропуская воду через глинозем, костную муку или костный уголь можно также убрать фтор из воды. Некоторые фториды (например, фторид кальция) нерастворимы в воде, поэтому можно использовать метод осаждения, чтобы перевести весь фтор в осадок. Для этого зачастую используют известь.
Применение в фармакологии
Фторид натрия является действующим веществом некоторых лекарственных препаратов. Как правило, прием таких таблеток осуществляется по назначению врача, иногда терапия требует специального наблюдения и сопровождается регулярными исследованиями динамики протекания. Торговые названия препаратов фтора: «Натрия фторид», «Натриум флуоратум» и «Оссин». Их прописывают при недостатке фтора в организме, в частности при остеопорозе.
Препарат в виде драже и таблеток принимают внутрь. Почти весь фтор усваивается организмом, вне зависимости от приема пищи. Обычно такую терапию сочетают с приемом кальция и магния по 1-1,5 г в сутки. Это помогает костям более стабильно минерализоваться.
Но препарат опасно принимать свыше нормы. В таком случае может возникнуть избыток фтора, приводящий к флюорозу. При приеме лекарственных средств, содержащих фторид натрия, необходимо наблюдаться у стоматолога, чтобы предупредить развитие флюороза.
Источник
Способ получения фторида натрия
Владельцы патента RU 2513200:
Изобретение может быть использовано в неорганической химии. Фторид натрия может быть получен из побочного продукта производства экстракционной фосфорной кислоты — кремнефтористоводородной кислоты, содержащей диоксид кремния. Способ получения фторида натрия включает взаимодействие кремнефтористоводородной кислоты с гидроксидом натрия в водной среде при температуре 80-90°С, перемешивание с получением суспензии, отделение осадка фторида натрия и его промывку. Промывку проводят 6-10% раствором карбоната или гидроксида натрия при температуре 20-50°С. Количество гидроксида натрия, требуемое для разложения кремнефтористоводородной кислоты и перевода диоксида кремния в силикат натрия, рассчитывают по формуле mNaOH=2,22·mH2SiF6+1,33·mSiO2, где mH2SiF6 — масса кремнефтористоводородной кислоты в пересчете на 100% H2SiF6, mSiO2 — масса диоксида кремния в исходной кислоте. Изобретение позволяет улучшить фильтрационные свойства осадка фторида натрия, снизить потери фторида натрия на стадии промывки. 2 табл., 2 пр.
Изобретение относится к технологии извлечения фтора в виде фторида натрия из кремнефтористоводородной кислоты (КФВК), который может быть использован в качестве сырья для получения криолита, фтористого алюминия, для фторирования воды.
Известен способ получения фторида натрия путем нейтрализации технической плавиковой кислоты содовым раствором при температуре 90-95°С в течение часа. Осадок фторида натрия отфильтровывают, промывают от маточного раствора и высушивают [М.Е.Позин. Технология минеральных солей II ч. — Л.: Изд. «Химия», 1974, с.1128-1129].
Недостатками известного способа являются применение плавиковой кислоты — дорогого и дефицитного реагента в качестве сырья, и низкое качество фторида натрия из-за значительного содержания диоксида кремния.
Известен способ получения фтористого натрия [а.с. СССР №767019, кл. С01В 9/08, опубл. 30.09.80] путем взаимодействия раствора гидроксида натрия с плавиковой кислотой концентрацией 60-95 масс.%, при температуре 30-95°С и рН 4-6,5, выделения фтористого натрия при температуре плюс 20°С — минус 16°С предельным спиртом, взятым в весовом соотношении спирт:вода, равным 0,1-4:1. Далее осадок фтористого натрия сушат с получением целевого продукта. Способ позволяет увеличить выход продукта и повысить содержание основного вещества.
Недостатками способа являются использование плавиковой кислоты — дорогого и дефицитного сырья, а также сложность технологического процесса, связанная с применением пропилового, этилового, изопропилового спиртов — пожаро- и взрывоопасных веществ.
Известен способ получения фторида натрия [патент РФ №2219124, кл. С01В 9/08, C01D 3/02, опубл. 20.12.2003] путем взаимодействия 10-20%-ного раствора гидроксида натрия с фторидом водорода при температуре 60-90°С до достижения стехиометрического соотношения реагентов, определяемого по скачкообразному изменению потенциала вольфрамового электрода в паре с хлоридсеребряным электродом от 600-700 мВ до 540-615 мВ. Способ позволяет уменьшить потери фторида водорода, повысить выход продукта, снизить энергозатраты при проведении процесса.
Недостатками способа являются использование фторида водорода -дорогого и дефицитного сырья, сложность определения стехиометрического соотношения реагентов.
Известен способ получения фторида натрия из кремнефтористоводородной кислоты [патент США №4213951, кл. C01D 3/02, опубл. 22.07.1980] путем ее обработки при температуре 20-80°С с достаточным количеством гидроксида натрия для получения водно-щелочной суспензии с рН 11-14, содержащей осажденный фторид натрия и раствор метасиликата натрия, после отделения и обработки которого кремнефтористыми соединениями образуется осадок аморфной двуокиси кремния и насыщенный маточный раствор фторида натрия.
Недостатками способа являются повышенная влажность целевого продукта, высокое содержание примеси диоксида кремния, что приводит к получению соли NaF недостаточно высокого качества и дополнительным затратам на ее очистку и сушку. Способ также характеризуется большим объемом сточных вод, обусловленным использованием насыщенного раствора фторида натрия и низкой растворимостью последнего.
Наиболее близким к предлагаемому по технической сущности и по достигаемому результату является известный способ получения фторида натрия из кремнефтористых солей [патент РФ №2175639, кл. C01D 3/02, опубл. 10.11.2001], включающий ее взаимодействие с гидроксидом натрия в водной среде при температуре 80-90°С и перемешивании с получением суспензии, отделение осадка фторида натрия фильтрацией, промывку осадка, при этом рН суспензии поддерживают в пределах 10,0-10,9, а осадок фторида натрия промывают насыщенным раствором фторида натрия. В качестве кремнефтористых соединений использовали кремнефторид натрия, кремнефтористоводородную кислоту и тетрафторид кремния. Расчет расхода гидроксида натрия NaOH для разложения КФВК производили в соответствии с уравнением реакции:
H 2 S i F 6 + 8 N a O H = 6 N a F + N a 2 S i O 3 + 5 H 2 O ( 1 )
Коэффициент фильтрации осадка характеризуется на уровне от 2,1·10 -5 до 6,2·10 -3 см/с, или скорость фильтрации составила 0,1-1,0 м 3 /м 2 ·ч.
Недостатком способа является недостаточно высокий выход продукта, связанный с использованием части полученного продукта для приготовления насыщенного раствора фторида натрия NaF для промывки осадка. Недостатком способа является также низкая фильтруемость полученного осадка фторида натрия, в частности при использовании в качестве исходного реагента технической КФВК, содержащей диоксид кремния. Последнее связано с неполным переводом диоксида кремния в растворимый силикат натрия.
Цель изобретения — снизить потери фторида натрия на стадии промывки и улучшение фильтрационных свойств осадка фторида натрия при использовании кремнефтористоводородной кислоты, содержащей примесь диоксида кремния.
Поставленная цель достигается в предлагаемом способе получения фторида натрия из композиции кремнефтористого соединения, включающей ее взаимодействие с гидроксидом натрия в водной среде при температуре 80-90°С и перемешивание с получением суспензии, отделение осадка фторида натрия и его промывку, отличающемся тем, что в качестве композиции кремнефтористого соединения берут побочный продукт производства экстракционной фосфорной кислоты — кремнефтористоводородную кислоту, содержащую диоксид кремния. Количество гидроксида натрия, требуемое для разложения кремнефтористоводородной кислоты и перевода диоксида кремния в силикат натрия, рассчитывают последующей формуле:
m N a O H = 2,22 ⋅ m H 2 S i F 6 + 1,33 ⋅ m S i O 2
где mH2SiF6 — масса кремнефтористоводородной кислоты в пересчете на 100% H2SiF6, mSiO2 — масса диоксида кремния в исходной кислоте, а осадок фторида натрия промывают 6-10% раствором карбоната или гидроксида натрия при температуре 20-50°С.
Сущность изобретения состоит в следующем. Техническая КФВК, получаемая в качестве побочного продукта в производстве экстракционной фосфорной кислоты, всегда содержит значительное количество диоксида кремния [И.Г.Рысс. Химия фтора и его неорганических соединений. Гос. научно-техн. издательство химической литературы. 1956, с.352-353]. Техническая КФВК, как правило, содержит 12-20% H2SiF6 и 0,8-1,8% диоксида кремния SiO2. При ее использовании для получения фторида натрия для полноты перевода диоксида кремния в растворимое соединение — силикат натрия — необходимо дополнительное количество гидроксида натрия для протекания химической реакции натрия по уравнению:
S i O 2 + 2 N a O H = N a 2 S i O 3 + H 2 O ( 2 )
Для разложения КФВК согласно уравнению (1) требуется следующее количество гидроксида натрия mNaOH:
где mH2SiF6 — масса кремнефтористоводородной кислоты (г) в пересчете на 100% H2SiF6; 40,00 и 144,09 — молекулярные массы NaOH и H2SiF6 соответственно Для перевода диоксида кремния в силикат натрия по уравнению (2) требуется дополнительное количество гидроксида натрия, равное
где 60,08 — молекулярная масса диоксида кремния, mSiO2 — масса диоксида кремния (г) в исходной КФВК.
Таким образом, общее количество гидроксида натрия для разложения КФВК, содержащей диоксид кремния, рассчитывается по следующей формуле:
При введении гидроксида натрия, достаточного для разложения КФВК, и перевода диоксида кремния в силикат натрия достигается образование легкофильтруемого осадка. Скорость фильтрации суспензии фторида натрия составляет 2,2-2,5 м 3 /м 2 ·ч, по осадку — до 300-350 кг/м 2 ·ч.
Увеличение выхода фторида натрия обеспечивается посредством промывки осадка фторида натрия 6-10%-ным раствором гидроксида натрия или карбоната натрия. Растворы гидроксида и карбоната натрия и их указанные пределы концентраций выбраны по следующим основаниям. Данные растворы имеют щелочную среду и эффективны для отмывки осадка фторида натрия от примеси силиката натрия. В щелочной среде не происходит реакции гидролиза силиката натрия с выделением диоксида кремния в осадок, чем достигается эффективность промывки осадка целевого продукта — фторида натрия. Концентрационные и температурные параметры процесса промывки осадка определены по результатам проведенных исследований по изучению растворимости фторида натрия в фильтрате после промывки. Полученные результаты представлены в таблицах 1 и 2.
На основании полученных данных для промывки осадка фторида натрия выбраны растворы гидроксида натрия и карбоната натрия концентрации 6-10% при температуре 20-50°С. В растворе гидроксида натрия концентрации 6-10% растворимость фторида в пересчете на фтор составляет 0,45-0,29% и незначительно зависит от температуры. При снижении концентрации раствора гидроксида натрия ниже 5% растворимость фторида натрия повышается до 0,82-0,84% F. Таким образом, использование раствора гидроксида натрия концентрацией ниже 5% приводит к увеличению потерь фторида натрия с промывными растворами. Растворимость фторида натрия в растворе карбоната натрия зависит от концентрации и температуры. В растворе концентрации 6-10% при температуре 50°С растворимость фторида составляет 0,45-0,29% F, при снижении концентрации ниже 6% растворимость повышается до 0,84% F и более. Снижение температуры растворов гидроксида натрия ниже 20°С не целесообразно, так как при этом снижается скорость промывки осадка, а также требуется охлаждение исходных растворов. Повышение температуры растворов гидроксида и карбоната натрия выше 50°С также нежелательно из-за повышения потерь фторида натрия. Повышение концентрации растворов выше 10% нецелесообразно из-за повышенного расхода реагентов.
Содержание фторида натрия (в пересчете на фтор, % масс.) в промывном растворе при промывке осадка раствором гидроксида натрия показано в таблице 1:
| Таблица 1 | |||||||
| Температура раствора NaOH,°С | Концентрация раствора гидроксида натрия, % масс. | ||||||
| 1 | 3 | 5 | 6 | 8 | 10 | 12 | |
| 15 | 1,40 | 1,10 | 0,80 | 0,44 | 0,35 | 0,29 | 0,29 |
| 20 | 1,40 | 1,10 | 0,82 | 0,45 | 0,34 | 0,30 | 0,29 |
| 40 | 1,40 | 1,15 | 0,83 | 0,45 | 0,34 | 0,30 | 0,28 |
| 50 | 1,50 | 1,15 | 0,84 | 0,45 | 0,35 | 0,30 | 0,29 |
| 60 | 1,60 | 1,30 | 0,90 | 0,55 | 0,43 | 0,40 | 0,34 |
Содержание фторида натрия (в пересчете на фтор, % масс.) в промывном растворе при промывке осадка раствором карбоната натрия показано в таблице 2:
| Таблица 2 | |||||||
| Температура раствора Na2CO3,°С | Концентрация раствора карбоната натрия, % масс. | ||||||
| 1 | 3 | 5 | 6 | 8 | 10 | 12 | |
| 15 | 0,86 | 0,60 | 0,29 | 0,25 | 0,23 | 0,20 | 0,20 |
| 20 | 0,96 | 0,59 | 0,30 | 0,26 | 0,24 | 0,26 | 0,25 |
| 40 | 1,05 | 0,75 | 0,50 | 0,48 | 0,45 | 0,41 | 0,40 |
| 50 | 1,18 | 0,94 | 0,74 | 0,70 | 0,68 | 0,57 | 0,50 |
| 60 | 1,29 | 1,12 | 0,90 | 0,85 | 0,80 | 0,69 | 0,65 |
Пример 1. Опыты по разложению КФВК проводили во фторопластовом реакторе, снабженном механической мешалкой. Для разложения взяли 150 г технической КФВК, полученной в производстве экстракционной фосфорной кислоты. Исходная КФВК содержит 18% H2SiF6 и 0,9% диоксида кремния. 150 г КФВК содержит 27,0 г H2SiF6 и 1,35 г диоксида кремния. Для разложения H2SiF6 и перевода диоксида кремния в растворимое состояние брали гидроксид натрия в количестве, рассчитанном по формуле mNaOH=2,22·mH2SiF6+1,33·mSiO2=2,22·27,0+1,33·1,35=61,74 г (в пересчете на 100% NaOH). В реактор загрузили предварительно нагретый до 75°С 46%-ный раствор гидроксида натрия в количестве 134,2 г. Раствор гидроксида натрия содержит 134,2·46/100=61,74 г 100% NaOH. Далее в реактор при перемешивании добавляли КФВК. Взаимодействие щелочи и кислоты сопровождается выделением тепла, за счет саморазогрева температуру реакционной смеси поддерживали в пределах 80-90°С. Реакционную смесь перемешивали в течение 20-30 минут. Показатель рН суспензии 12. Осадок фторида натрия отделяли от реакционной смеси фильтрацией при разрежении 0,4 атм. Скорость фильтрации составила 2,1 м 3 /м 2 ·ч по суспензии и 324 кг/м 2 ·ч по сухому веществу. Получили 237,7 г фильтрата, представляющего раствор силиката натрия. Осадок фторида натрия промывали 82 г 8%-ным раствором карбоната натрия при температуре 40°С. Получили 45,5 г осадка фторида натрия с влажностью 10%. Осадок фторида натрия сушили и получили 41,4 г целевого продукта. Содержание основного вещества в продукте 98%.
Пример 2. Для разложения взяли 200 г технической КФВК, полученной в производстве экстракционной фосфорной кислоты. Исходная КФВК содержит 17% H2SiF6 и 1,2% диоксида кремния или 34,0 г H2SiF6 и 2,4 г диоксида кремния. Для разложения H2SiF6 и перевода диоксида кремния в растворимое состояние брали гидроксид натрия в количестве, рассчитанном по формуле mNaOH=2,22·mH2SiF6+1,33·mSiO2=2,22·34,0+1,33·2,4=78,7 г (в пересчете на 100% NaOH). В реактор загрузили предварительно нагретый до 75°С 45%-ный раствор гидроксида натрия в количестве 174,8 г. Раствор гидроксида натрия содержит 174,8·45/100=78,7 г 100% NaOH. Далее в реактор при перемешивании добавляли КФВК. Взаимодействие щелочи и кислоты сопровождается выделением тепла, за счет саморазогрева температуру реакционной смеси поддерживали в пределах 80-90°С. Реакционную смесь перемешивали в течение 30 минут. Показатель рН суспензии 12. Осадок фторида натрия отделяли от реакционной смеси фильтрацией при разрежении 0,4 атм. Скорость фильтрации составила 2,2 м 3 /м 2 ·ч по суспензии и 335 кг/ м 2 ·ч по сухому веществу. Получили 317,8 г фильтрата, представляющего раствор силиката натрия. Осадок фторида натрия промывали 104 г 8%-ным раствором гидроксида натрия при температуре 40°С. Получили 57,0 г осадка фторида натрия с влажностью 10%. Осадок фторида натрия сушили и получили 51,8 г целевого продукта. Содержание основного вещества в продукте 98%.
Предлагаемый способ позволяет получить легкофильтрующиеся кристаллы фторида натрия из технической кремнефтористоводородной кислоты, содержащей диоксид кремния, снизить потери фторида натрия на стадии промывки осадка. Целевой продукт отвечает требованиям ТУ 113-08-586-86 (Натрий фтористый технический) марки А высший сорт.
Способ получения фторида натрия из композиции кремнефтористого соединения, включающий ее взаимодействие с гидроксидом натрия в водной среде при температуре 80-90°С и перемешивание с получением суспензии, отделение осадка фторида натрия и его промывку, отличающийся тем, что в качестве композиции кремнефтористого соединения берут побочный продукт производства экстракционной фосфорной кислоты — кремнефтористоводородную кислоту, содержащую диоксид кремния, количество гидроксида натрия, требуемое для разложения кремнефтористоводородной кислоты и перевода диоксида кремния в силикат натрия, рассчитывают по следующей формуле:
mNaOH=2,22·mH2SiF6+1,33·mSiO2,
где mH2SiF6 — масса кремнефтористоводородной кислоты в пересчете на 100% H2SiF6, mSiO2 — масса диоксида кремния в исходной кислоте; а осадок фторида натрия промывают 6-10% раствором карбоната или гидроксида натрия при температуре 20-50°С.
Источник