- Получение металлов высокой чистоты.
- Получение металлов высокой чистоты
- Методы получения металлов высокой чистоты.
- Понятие о металлургии: общие способы получения металлов
- 1. Нахождение металлов в природе
- 2. Получение активных металлов
- 3. Получение малоактивных и неактивных металлов
- 3.1. Обжиг сульфидов
- 3.2. Восстановление металлов углем
- 3.3. Восстановление металлов угарным газом
- 3.4. Восстановление металлов более активными металлами
- 3.5. Восстановление металлов из оксидов водородом
- 4. Производство чугуна
- Добавить комментарий Отменить ответ
Получение металлов высокой чистоты.
В ряде отраслей техники требуется получение металлов высокой степени чистоты. Например, для ядерных реакторов нужен химически чистый цирконий без примеси гафния. Для электронной промышленности необходим германий, в котором не должно быть более одного атома фосфора, мышьяка или сурьмы на миллион атомов германия. Исследование металлов в чистом состоянии показало, что некогда существовавшие представления об их свойствах являются ошибочными. Так, например, чистые титан, хром оказались настолько пластичными, что их можно ковать, прокатывать в тонкие листы и пр. Алюминий высокой чистоты мягок, как свинец, а его электропроводимость значительно выше.
Чистые металлы можно получить электролизом, но степень их чистоты недостаточно высокая, поэтому для получения металлов ОСЧ – особой чистоты, используют специальные методы:
— переплавка в вакууме (получают ОСЧ литий, щелочно-земельные металлы, хром, марганец, бериллий);
— разложение летучих соединений на раскаленной поверхности (получают ОСЧ титан, цирконий, хром, тантал, ниобий, кремний и др.);
— использование так называемой «зонной плавки» (получают германий, кремний, олово, алюминий, висмут и галлий).
Зонная плавка основана на различной растворимости примесей в твердой и жидкой фазах очищаемого металла. Лодочку или тигель специальной формы со слитком металла передвигают с очень медленной скоростью (несколько мм в час) через печь При этом происходит расплавление небольшого участка (зоны) металла. По мере продвижения тигля зона жидкого металла перемещается от одного конца слитка к другому. Примеси, содержащиеся в металле, собираются в зоне плавления, перемещаются вместе с ней и после окончания плавки оказываются в конце слитка. Многократное повторение операции дает возможность получить металл высокой степени чистоты.
Дополнения к теме «Физико-хмический анализ»
Многочисленные работы Ник. Семен. Курнакова по выяснению природы металлических сплавов внесли ясность в понимание процессов, происходящих при затвердевании сплавов. В частности, при изучении сплавов были открыты химические соединения, состав которых может меняться в широких пределах. Эти соединения, состав которых может меняться в широких пределах, Курнаков назвал бертоллидами, по имени французского химика Бертолле, допустившего их существование. Тогда как соединения постоянного состава (подчиняющиеся закону постоянства состава), были названы дальтониды. Стехиометрическое соотношение компонентов, образующих химическое соединение постоянного состава соблюдается только в парообразном состоянии, в молекулярных кристаллах и жидкостях. Исходя из вышесказанного, можно дать более развернутое определение, что такое химическое соединение. Химическое соединение – это вещество постоянного или переменного состава, образованное из атомов одного или нескольких химических элементов, с качественно своеобразным химическим и кристаллохимическим строением.
При сплавлении металлов может образоваться твердый раствор или химическое соединение переменного состава. В отличие от твердых растворов (общее между растворами и хим. соединениями – однородность и наличие теплового эффекта при образовании), соединение переменного состава характеризуется только ему присущим кристаллохимическим строением, отличающимся от строения исходных компонентов.
Источник
Получение металлов высокой чистоты
В связи с развитием новых отраслей техники требуются металлы очень высокой чистоты. Например, в металле германии, используемом в качестве полупроводника, допустимо содержание на десять миллионов атомов германия только одного атома фосфора, мышьяка или сурьмы. В жаропрочных сплавах, применяемых в ракетостроении, совершенно недопустима даже ничтожная примесь свинца или серы.
Один из лучших конструкционных материалов для атомных реакторов – цирконий становится совершенно непригодным, если в нем содержится даже незначительная примесь гафния, кадмия или бора, поэтому содержание этих элементов в материалах атомной энергетики не должно превышать 10 -6 . Электрическая проводимость меди снижается на 14 % при наличии примеси мышьяка лишь 0,03 %. Особенно большое значение имеет чистота металлов в электронной и вычислительной технике, а так же ядерной энергетике. Для металлических материалов термоядерных реакторов и полупроводниковых приборов содержание примесей не должно превышать 10 -10 %. Существует несколько методов очистки металлов.
1. Перегонка в вакууме. Этот метод основан на различии летучести металла и имеющихся в нем примесей.
2. Термическое разложение летучих соединений металлов. В основе данного способа лежат химические реакции, в которых металл с тем или иным реагентом образует газообразные продукты, разлагающиеся затем с выделением высокочистого металла. Рассмотрим принцип данного способа на примере карбонильного и йодидного методов.
А) Карбонильный метод. Этот метод применяется для получения высокочистых никеля и железа. Подлежащий очистке технический металл нагревают при данном методе в присутствии оксида углерода (II): Ni + 4CO = Ni(CO)4 , Fe + 5CO = Fe(CO)5
Полученные летучие карбонилы Ni(CO)4 (температура кипения 43 °С) или Fe(CO)5 (температура кипения 105 °С) перегоняют для очистки от примесей. Затем карбонилы разлагают при температуре выше 180 °С, в результате образуются чистые металлы и газообразный оксид углерода (II): Ni(CO)4 = Ni + 4CO, Fe(CO)5 = Fe + 5CO
Б) Йодидный метод. При данном методе очищаемый металл, например титан, нагревают вместе с йодом до температуры 900 °С: Ti + 2I2 = ТI4
Образующийся летучий тетрайодид титана поступает в реактор, в котором находится проволока из чистого титана, нагреваемая электрическим током до 1400 °С. При этой температуре тетрайодид титана термически диссоциирует: Til4 = Ti + 2I2
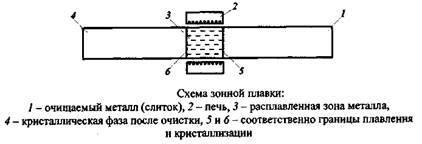
3. Зонная плавка. Замечательным методом очистки является так называемая зонная плавка. Зонная плавка заключается в медленном протягивании слитка очищаемого металла через кольцевую печь. Зонной плавке подвергаются металлы, прошедшие предварительную очистку до концентрации примесей приблизительно 1 %. Метод основан на различном содержании примесей в твердом и расплавленном металле. Процесс проводят путем медленного перемещения вдоль твердого удлиненного образца (слитка) узкой расплавленной зоны, создаваемой специальным нагревателем (кольцевая печь).
Участок (зона) слитка металла, который в данный момент находится в печи, переходит в расплавленное состояние.
Возникает две подвижные межфазные границы: на одной (вхождение металла в печь) происходит плавление, на другой (выход металла из печи) происходит кристаллизация.
В зависимости от растворимости примесей одни концентрируются в расплавленной зоне и перемещаются вместе с ней к концу слитка, примеси других металлов концентрируются в образующихся кристаллах и остаются за движущейся зоной, при неоднократном повторении процесса они перемещаются к началу слитка. Вследствие этого состав образующихся кристаллов отличается от состава расплава.
Для достижения высокой степени очистки обычно производят несколько проходов расплавленной зоны вдоль слитка металла. В результате средняя часть слитка получается наиболее чистой, ее вырезают и используют.
Метод зонной плавки позволяет получить особо чистые металлы с содержанием примесей 10 -7 -10 -9 %. Данный метод применяется для получения сверхчистых германия, висмута, теллура и др.
Основное достоинство данного метода — высокая эффективность. Недостатки метода — низкая производительность, высокая стоимость, большая продолжительность процесса.
4. электрохимический метод очистки металлов (рафинирование металлов).
Источник
Методы получения металлов высокой чистоты.



Методы получения металлов высокой чистоты
Металлы высокой степени чистоты необходимы для получения сплавов при конструировании ядерных реакторов, в ракетостроении, в материалах для электронной техники.
1) Перегонка в вакууме основана на различии летучестей очищаемого металла и имеющихся в нем примесей.
Металл загружают в специальный сосуд, соединенный с вакуумным насосом. Нагревают нижнюю часть, на холодных частях осаждаются более летучие соединения, (либо примеси, либо металл – в зависимости от летучести ). Непрерывно откачивается воздух для устранения окисления металла и торможения испарения.
2) Зонная плавка используется для получения особо чистого германия для полупроводниковой техники (1952 г. Пфанн, Германия). Метод используется для очистки металлов и других веществ.
Очищаемый образец в лодочке медленно протягивают через кольцевую печь. Тот участок (зона), который в данный момент находится в печи, плавится. Поскольку растворимость примеси в жидкой фазе выше, примесь собирается в расплавленной зоне и вместе с ней перемещается к концу образца. Проход зоны повторяют несколько раз. Конец слитка, содержащий примеси, отрезают.
Полученный Ge из природных соединений подвергают зонной плавке.
3) Термическое разложение летучих соединений металла:
а) карбонильный процесс – для получения высокочистых никеля и железа.
Подлежащий очистке никель нагревают при 20 МПа в атмосфере СО:
Примеси в реакцию не вступают. Температура кипения Ni(CO)4 равна 42 °С. Тетракарбонил никеля отгоняют, а затем нагревают до более высокой температуры. Он разрушается с выделением высокочистого металла. Аналогично очищают железо последовательным применением синтеза и последующего разложения Fe(CO)5, температура кипения которого tкип. = 105°С
б) иодидный способ используется для получения высокочистых титана, циркония и др.
Порошок металла нагревают в герметичном аппарате до 100 – 200 °С с небольшим количеством иода. В аппарате натянуты титановые нити, нагреваемые электрическим током до 1300 – 1500 °С. Титан, но не примеси — образует с иодом летучий иодид, который разлагается на раскаленных нитях. Выделяющийся чистый титан осаждается на них, а иод образует с исходным металлом новые порции иодида. Процесс идет непрерывно до переноса всего металла на титановые нити
Источник
Понятие о металлургии: общие способы получения металлов
Понятие о металлургии: общие способы получения металлов
Металлургия — это наука о промышленных способах получения металлов. Различают черную и цветную металлургию.
Черная металлургия — это производство железа и его сплавов (сталь, чугун и др.).
Цветная металлургия — производство остальных металлов и их сплавов.
Широкое применение находят сплавы металлов. Наиболее распространенные сплавы железа — чугун и сталь.
Чугун — это сплав железа, в котором содержится 2-4 масс. % углерода, а также кремний, марганец и небольшие количества серы и фосфора.
Сталь — это сплав железа, в котором содержится 0,3-2 масс. % углерода и небольшие примеси других элементов.
Легированные стали — это сплавы железа с хромом, никелем, марганцем, кобальтом, ванадием, титаном и другими металлами. Добавление металлов придает стали дополнительные свойства. Так, добавление хрома придает сплаву прочность, а добавление никеля придает стали пластичность.
Основные стадии металлургических процессов:
- Обогащение природной руды (очистка, удаление примесей)
- Получение металла или его сплава.
- Механическая обработка металла
1. Нахождение металлов в природе
Большинство металлов встречаются в природе в виде соединений. Наиболее распространенный металл в земной коре — алюминий. Затем железо, кальций, натрий и другие металлы.
| Нахождение металлов в природе | ||
| Активные металлы — в виде солей | Металлов средней активности — в виде оксидов и сульфидов | Малоактивные металлы -в виде простых веществ |
Хлорид натрия NaCl 2. Получение активных металловАктивные металлы (щелочные и щелочноземельные) классическими «химическими» методами получить из соединений нельзя. Такие металлы в виде ионов — очень слабые окислители, а в простом виде — очень сильные восстановители, поэтому их очень сложно восстановить из катионов в простые вещества. Чем активнее металл, тем сложнее его получить в чистом виде — ведь он стремится прореагировать с другими веществами. Получить такие металлы можно, как правило, электролизом расплавов солей, либо вытеснением из солей другими металлами в жестких условиях. Натрий в промышленности получают электролизом расплава хлорида натрия с добавками хлорида кальция: 2NaCl = 2Na + Cl2 Калий получают пропусканием паров натрия через расплав хлорида калия при 800°С: KCl + Na = K↑ + NaCl Литий можно получить электролизом расплава хлорида лития в смеси с KCl или BaCl2 (эти соли служат для понижения температуры плавления смеси): 2LiCl = 2Li + Cl2 Цезий можно получить нагреванием смеси хлорида цезия и специально подготовленного кальция: Са + 2CsCl = 2Cs + CaCl2 Магний получают электролизом расплавленного карналлита или хлорида магния с добавками хлорида натрия при 720–750°С: Кальций получают электролизом расплавленного хлорида кальция с добавками фторида кальция: Барий получают из оксида восстановлением алюминием в вакууме при 1200 °C: 4BaO+ 2Al = 3Ba + Ba(AlO2)2 Алюминий получают электролизом раствора оксида алюминия Al2O3 в криолите Na3AlF6: 3. Получение малоактивных и неактивных металловМеталлы малоактивные и неактивные восстанавливают из оксидов углем, оксидом углерода (II) СО или более активным металлом. Сульфиды металлов сначала обжигают. 3.1. Обжиг сульфидовПри обжиге сульфидов металлов образуются оксиды: 2ZnS + 3O2 → 2ZnO + 2SO2 Металлы получают дальнейшим восстановлением оксидов. 3.2. Восстановление металлов углемЧистые металлы можно получить восстановлением из оксидов углем. При этом до металлов восстанавливаются только оксиды металлов, расположенных в ряду электрохимической активности после алюминия. Например , железо получают восстановлением из оксида углем: 2Fe2O3 + 6C → 2Fe + 6CO ZnO + C → Zn + CO Оксиды металлов, расположенных в ряду электрохимической активности до алюминия, реагируют с углем с образованием карбидов металлов: CaO + 3C → CaC2 + CO 3.3. Восстановление металлов угарным газомОксид углерода (II) реагирует с оксидами металлов, расположенных в ряду электрохимической активности после алюминия. Например , железо можно получить восстановлением из оксида с помощью угарного газа: 3.4. Восстановление металлов более активными металламиБолее активные металлы вытесняют из оксидов менее активные. Активность металлов можно примерно оценить по электрохимическому ряду металлов: Восстановление металлов из оксидов другими металлами — распространенный способ получения металлов. Часто для восстановления металлов применяют алюминий и магний. А вот щелочные металлы для этого не очень подходят – они слишком химически активны, что создает сложности при работе с ними. Алюмотермия – это восстановление металлов из оксидов алюминием. Например : алюминий восстанавливает оксид меди (II) из оксида: 3CuO + 2Al = Al2O3 + 3Cu Магниетермия – это восстановление металлов из оксидов магнием. CuO + Mg = Cu + MgO Железо можно вытеснить из оксида с помощью алюминия: При алюмотермии образуется очень чистый, свободный от примесей углерода металл. Активные металлы вытесняют менее активные из растворов их солей. Например , при добавлении меди (Cu) в раствор соли менее активного металла – серебра (AgNO3) произойдет химическая реакция: 2AgNO3 + Cu = Cu(NO3)2 + 2Ag Медь покроется белыми кристаллами серебра. При добавлении железа (Fe) в раствор соли меди (CuSO4) на железном гвозде появился розовый налет металлической меди: CuSO4 + Fe = FeSO4 + Cu При добавлении цинка в раствор нитрата свинца (II) на цинке образуется слой металлического свинца: 3.5. Восстановление металлов из оксидов водородомВодород восстанавливает из оксидов только металлы, расположенные в ряду активности правее алюминия. Как правило, взаимодействие оксидов металлов с водородом протекает в жестких условиях – под давлением или при нагревании. CuO + H2 = Cu + H2O 4. Производство чугунаЧугун получают из железной руды в доменных печах. Печь последовательно загружают сверху шихтой, флюсами, коксом, затем снова рудой, коксом и т.д. 1- загрузочное устройство, 2 — колошник, 3 — шахта, 4 — распар, 5 — горн, 6 — регенератор Доменная печь имеет форму двух усеченных конусов, соединенных основаниями. Верхняя часть доменной печи — колошник, средняя — шахта, а нижняя часть — распар. В нижней части печи находится горн. Внизу горна скапливается чугун и шлак и отверстия, через которые чугун и шлак покидают горн: чугун через нижнее, а шлак через верхнее. Наверху печи расположено автоматическое загрузочное устройство. Оно состоит из двух воронок, соединенных друг с другом. Руда и кокс сначала поступают в верхнюю воронку, а затем в нижнюю. Из нижней воронки руда и кокс поступают в печь. во время загрузки руды и кокса печь остается закрытой, поэтому газы не попадают в атмосферу, а попадают в регенераторы. В регенераторах печной газ сгорает. Шихта — это железная руда, смешанная с флюсами. Снизу в печь вдувают нагретый воздух, обогащенный кислородом, кокс сгорает: Образующийся углекислый газ поднимается вверх и окисляет кокс до оксида углерода (II): CO2 + С = 2CO Оксид углерода (II) (угарный газ) — это основной восстановитель железа из оксидов в данных процессах. Последовательность восстановления железа из оксида железа (III): Последовательность восстановления оксида железа (III): FeO + CO → Fe + CO2 Суммарное уравнение протекающих процессов: При этом протекает также частичное восстановление примесей оксидов других элементов (кремния, марганца и др.). Эти вещества растворяются в жидком железе. Чтобы удалить из железной руды тугоплавкие примеси (оксид кремния (IV) и др.). Для их удаления используют флюсы и плавни (как правило, известняк CaCO3 или доломит CaCO3·MgCO3). Флюсы разлагаются при нагревании: и образуют с тугоплавкими примесями легкоплавкие вещества (шлаки), которые легко можно удалить из реакционной смеси: CaO + SiO2 → CaSiO3 Добавить комментарий Отменить ответЭтот сайт использует Akismet для борьбы со спамом. Узнайте, как обрабатываются ваши данные комментариев. Источник | ||









