ООО «РосСнаб»
НАША РАБОТА — ЭТО УСПЕХ НАШИХ ПАРТНЕРОВ
Главное меню
Ионообменные смолы
Ионообменные смолы — синтетические высокомолекулярные (полимерные) органические иониты — высокомолекулярные синтетические соединения с трехмерной гелевой и макропористой структурой, которые содержат функциональные группы кислотного характера, способные к реакциям ионного обмена. Ионообменная смола представляет собой скопление достаточно мелких шариков, именуемых для простоты «смолой». Внешне такая смола может напоминать рыбью икру. Однако, эта «икра» обладает уникальными свойствами. Шарики смолы способны улавливать из воды ионы различных веществ и «впитывать» их в себя, отдавая взамен «запасенные» ранее ионы. Таким образом осуществляется ионный обмен — отсюда и обобщающее название этих смол — «ионообменные» или более по научному «иониты».
Свойства
Ионообменные смолы представляют собой твёрдые полимеры, нерастворимые, ограниченно набухающие в растворах электролитов и органических растворителях. Они способны к ионному обмену в водных и водноорганических растворах.
Макропористые смолы гетерогенны; их частицы имеют губчатую структуру, т. е. пронизаны системой сквозных пор, средний диаметр которых намного превышает размеры молекул растворителя и обменивающихся ионов. Раствор электролита свободно проникает по порам внутрь частиц таких ионообменных смол, что значительно облегчает ионный обмен, особенно в неводных средах.
Ионообменные смолы можно рассматривать как нерастворимые полиэлектролиты. Поливалентный (многозарядный) ион, образующий структурный каркас ионообменной смолы, практически неподвижен из-за огромной молекулярной массы. Этот ион-каркас, или ион-сетка, связывает малые подвижные ионы противоположного знака (противоионы), которые способны к эквивалентному обмену на ионы окружающего раствора. Средний размер частиц таких ионообменных смол составляет 0,2—2,0 мм, насыпная масса 0,5—0,9 т/м 3 .
Некоторые типы ионитов обладают способностью вступать в реакции комплексообразования, окисления-восстановления, а также способностью к физической сорбции ряда соединений.
Важнейшим показателем ионообменных смол является влажность, так как в силу гидрофильности функциональных групп ионообменных смол влага, содержащаяся в смоле, является «химически связанной». Причем специальное удаление этой влаги приведет при последующем использовании смолы только к физическому разрушению гранул. «Внешняя» же влага, не связанная химически с функциональной группой смолы, как правило, удаляется перед упаковкой или с помощью центрофугирования или фильтрования.
Следующей важной характеристикой ионообменных смол является ионообменная емкость — весовая, объемная и рабочая.
Весовая и объемная емкости являются стандартными показателями, определяются в лабораторных условиях по стандартным методикам и указываются в паспортных данных на готовую продукцию.
В то же время, рабочая ионообменная емкость не может быть измерена в лабораторных условиях, так как зависит от геометрических размеров слоя смолы и от конкретных характеристик обрабатываемых растворов (уровня регенерации, скорости потоков, концентрации растворенных веществ, требуемых показателей качества обрабатываемого раствора, точного размера частиц).
Классификация
В соответствии с общей классификацией ионитов ионообменные смолы делят на катионообменные (поликислоты), анионообменные (полиоснования) и амфотерные, или биполярные (полиамфолиты). Катионообменные смолы бывают сильно- и слабокислотные, анионообменные — сильно- и слабоосновные. Если носителями электрических зарядов молекулярного каркаса ионообменной смолы являются фиксированные ионы (функциональные, или ионогенные, группы) только одного типа, например сульфогруппы, то такие ионообменные смолы называются монофункциональными. Если же смолы содержат разнотипные ионогенные группы, они называются полифункциональными. По структурному признаку различают микропористые, или гелевидные, и макропористые ионообменные смолы. Частицы гелевидных смол гомогенны; ионный обмен в системе гелевидная смола — раствор электролита возможен лишь благодаря диффузии обменивающихся ионов сквозь молекулярную сетку набухшего ионита.
Иониты имеют гелевую, макропористую и промежуточную структуру.
Гелевые иониты лишены истинной пористости и способны к ионному обмену только в набухшем состоянии.
Макропористые иониты обладают развитой поверхностью из-за наличия пор и поэтому способны к ионному обмену как в набухшем, так и в ненабухшем состоянии.
Гелевые иониты характеризуются большей обменной емкостью, чем макропористые , но уступают им по осмотической стабильности, химической и термической стойкости.
Иониты представлены анионитами — материалами, способными к обмену анионов, и катионитами — материалами, обменивающими катионы.
Ионообменные смолы относятся к следующим классам:
- Катионнообменные смолы (катиониты) — содержат кислотные группы
- Анионообменные смолы (аниониты) — содержат основные группы
- Амфотерные ионообменные смолы — содержат одновременно и кислотные, и основные группы
- Селективные ионообменные смолы — содержат комплексообразующие группы
- Окислительно-восстановительные смолы — содержат функциональные группы, способные к изменению зарядов ионов
АНИОНИТЫ подразделяются на:
- сильноосновные, способные к обмену анионов любой степени диссоциации в растворах при любых значениях рН;
- слабоосновные, способные к обмену анионов из растворов кислот при рН 1-6;
- промежуточной и смешанной активности.
КАТИОНИТЫ подразделяются на:
- сильнокислотные, обменивающие катионы в растворах при любых значениях рН;
- слабокислотные, способные к обмену катионов в щелочных средах при рН > 7.
Кроме того, ионообменные смолы могут содержать группы различных классов, относясь к полифункциональным смолам.
По структуре матрицы ионообменные смолы делятся на:
- гелевые — микропоры имеют молекулярные размеры. Они представляют собой гомогенные поперечносвязанные полимеры. Фиксированные ионы равномерно распределены по всему объему полимера. Гелевые ионообменные смолы обладают высокой обменной емкостью, однако характеризуются невысокой скоростью обмена
- макропористые — размеры пор смолы имеют размеры в десятки нанометров. Имеют фиксированную систему пор и каналов, определяемую условиями синтеза. Обменная ёмкость таких смол меньше, чем гелевых при высокой скорости обмена
Методы получения ионообменных смол
Получают ионообменные смолы полимеризацией, поликонденсацией или путём полимераналогичных превращений, так называемой химической обработкой полимера, не обладавшего до этого свойствами ионита. Среди промышленных ионообменных смол широкое распространение получили смолы на основе сополимеров стирола и дивинилбензола. В их числе сильнокислотные катиониты, сильно- и слабоосновные аниониты. Основным сырьём для промышленного синтеза слабокислотных катионообменных смол служат акриловая и метакриловая кислоты и их эфиры. В больших количествах производят также ионообменные смолы на основе феноло-альдегидных полимеров, полиаминов и др. Направленный синтез ионообменных смол позволяет создавать материалы с заданными технологическими характеристиками.
Как правило, ионообменные смолы получают методами полимеризации или полимераналогичных превращений.
Для получения ионообменных смол методом полимеризации используют мономеры, содержащие ионогенные группы. В случае полимераналогичных превращений ионогенные группы вводятся в инертный полимер.
Возможен синтез ионообменных смол способом поликонденсации, однако эти ионообменные смолы имеют менее однородную структуру, меньшую осмотическую стабильность и химическую стойкость.
Чаще всего используются сетчатые полимеры. Их получают суспензионной полимеризацией стирола, производных акриловой кислоты, винилпиридинов с диенами.
Как правило, иониты выпускаются в солевых (натриевая, хлористая) или смешанно-солевых формах (натрий-водородная, гидроксильно-хлоридная). Кроме того, выпускаются иониты, практически полностью переведенные в рабочую форму (водородную, гидроксильную и др.). Выпускаются также готовые смеси ионитов для использования в фильтрах смешанного действия.
Применение
Ионообменные смолы применяются в водоочистке с 60-х годов XX века, но особенное распространение получили в конце 80-х — в 90-х годах.
Ионообменные смолы используют для обессоливания воды, извлечения и разделения редких элементов, очистки продуктов органического и неорганического синтеза и др.
Ионообменные смолы в основном применяются:
- для умягчения и обессоливания воды в теплоэнергетике и других отраслях;
- для разделения и выделения цветных и редких металлов в гидрометаллургии;
- при очистке возвратных и сточных вод;
- для регенерации отходов гальванотехники и металлообработки;
- для разделения и очистки различных веществ в химической промышленности;
- в качестве катализатора для органического синтеза.
Ионообменные смолы используются в котельных, теплоэлектростанциях, атомных станциях, пищевой промышленности (при производстве сахара, алкогольных, слабоалкогольных и других напитков, пива, бутилированной воды), фармацевтической промышленности и других отраслях.
Источник
Способы получения ионообменных смол
Методы синтеза ионообменных смол условно можно разделить на три группы:
• Поликонденсация с участием содержащих соответствующие фрагменты соединений;
• Полимеризация мономеров, содержащих ионогенные функциональные группы;
• Химическая модификация основных типов синтетических смол.
Несмотря на кажущуюся привлекательность простоту и экономическую привлекательность первого метода, базирующегося на сырьевой базе наиболее распространенных (фенол- и карбамидоформальдегидных) смол, получаемых методом поликонденсации, этот метод имеет скорее историческое, чем практическое значение. Это связано с недостатками присущими данному методу поликонденсации, к котором участвуют и ионогенные и функциональные группы. Это приводит к тому, что составы исходных мономеров и элементарных звеньев полученных смол не идентичны. Кроме того, технологический синтез ионитов методом поликонденсации в виде сферических гранул осуществить сложно. Химическая стойкость и механическая прочность поликонденсационных ионообменных смол также обычно ниже, чем у полимеризационных.
Второй метод, заключающийся в сополимеризации функционализированных виниловых мономеров с дивиниловыми, обеспечивает прямое получение смол с большой однородностью молекулярной ионогенных групп и хорошим физико-химическим и механическим свойствами. Однако промышленное использование и развитие этого, несомненно, перспективного метода сдерживается трудностями получения соответствующих виниловых мономеров.
Технология получения ионообменных смол путем химической модификации смол путем химической модификации полимеров также связана с рядом трудностей, к которым относятся многостадийность химических превращений и необходимость использования высокотоксичных активных реагентов, таких как монохлордиметиловый эфир, хлористый сульфурил, различные амины, в количествах намного превышающих стехиометрическое соотношение. Кроме этого, в процессе функционализации происходит частичная деструкция макромолекул исходных полимеров и редко достигается полнота химических превращений.
Несмотря на приведенные трудности и недостатки, именно третий метод наиболее широко применяется в мировой практике, поскольку для его осуществления не требуется специальных исходных соединений. Основные типы катионитов и анионитов производятся на базе сополимеров стирола с дивинилбензолом и акрилатов.
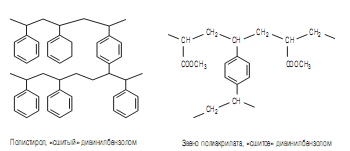
На рисунке 2 показана структура элементарных звеньев соответствующих полимеров.
Рисунок 2
Структура сшитых дивинилбензолом стирольных и акриловых полимеров
Для дальнейшего использования в технологии получения ионообменных смол полимеризация в структуре указанных типов обычно осуществляется суспензионным методом в воде, в процессе которой образуется твердые сферические гранулы полимерной матрицы. Использование специальных технологических приемов на стадиях синтеза и выделения позволяют получать так называемые «монодисперсные» формы ионообменных смол улучшенными физико-химическими и эксплуатационными свойствами. Новое поколение ионитов – смол с однородным гранулометрическим составом зерен, полученных по специальной технологии производства, а не методами тривиального рассева, впервые предложила компания Dow Chemical.
На рисунке 3 приведено распределение размеров и характер упаковки зерен, характерный для моно- и полидисперсных смол.