Получение газообразных веществ. Качественные реакции на газообразные вещества (кислород, водород, углекислый газ, аммиак)
В зависимости от условий получения газов используют различные приборы, простейшие из которых собирают из пробирок (рисунок 3).
Наиболее универсальным прибором для получения больших количеств газа является аппарат Киппа (рисунок 4).
Для того чтобы зарядить аппарат, в шарообразное расширение 4 помещают твёрдый реагент, размер частиц которого должен исключать его попадание в нижний резервуар. Затем реактор 4 закрывают пробкой 3 с газоотводной трубой с краном 2. Кран открывают и через горловину шарообразной воронки 1 заливают соответствующий жидкий реагент. Его наливают в таком количестве, чтобы его уровень при открытом газоотводном кране достигал половины шарообразного расширения. Газ пропускают в течение 55 минут, чтобы вытеснить воздух, затем закрывают газоотводный кран. Жидкий реагент из шарообразного расширения вытесняется газом в нижний резервуар и шарообразную воронку. Для работы с газом открывают кран, а по окончании работы его перекрывают.
Качественная реакция на кислород — яркое загорание тлеющей лучинки.
Качественная реакция на водород — хлопок при поднесении горящей лучинки к сосуду, содержащему смесь водорода и воздуха.
Качественная реакция на углекислый газ — помутнение известковой воды с последующим растворением осадка, а также затухание тлеющей лучины в атмосфере углекислого газа.
Качественная реакция на аммиак — почернение в его парах фильтровальной бумаги, смоченной в растворе соли ртути (I), или образование белого дыма при сближении двух стеклянных палочек, одна из которых смочена раствором аммиака, а другая — раствором соляной кислоты.
Тренировочные задания к разделам
1. Только смеси веществ перечислены в наборе
1) хлорид натрия, железо, песок
2) квас, молоко, уксус
3) воздух, пирит, магний
4) фтор, кальций, железняк
2. Верны ли следующие суждения о чистых веществах и смесях?
А. Воздух является смесью веществ.
Б. Бронза является чистым веществом.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
3. Верны ли следующие суждения о способах очистки веществ?
А. Бромид калия от воды можно отделить выпариванием.
Б. Очистить речной песок от железных опилок можно с помощью магнита.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
4. Верны ли следующие суждения о способах очистки веществ?
А. Очистить воду от нефти можно фильтрованием.
Б. Очистить речной песок от алюминиевых опилок можно фильтрованием.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
5. Верны ли суждения о правилах работы в химической лаборатории?
А. Работы с концентрированной серной кислотой проводят в вытяжном шкафу в защитных перчатках.
Б. Для разделения несмешивающихся жидкостей используют мерный цилиндр.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
6. Верны ли суждения о правилах работы в химической лаборатории?
А. Горючие жидкости запрещено нагревать с помощью газовой горелки.
Б. При попадании на кожу растворов щелочей их немедленно нейтрализуют соляной кислотой.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
7. Верны ли суждения о правилах работы в химической лаборатории?
А. При наливании реактивов нельзя наклоняться над сосудом во избежание попадания брызг на лицо или одежду.
Б. При нагревании пробирки нельзя держать её отверстием к себе или в сторону других лиц.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
8. Верны ли суждения о правилах работы в химической лаборатории?
А. Градуированные пипетки используют для отмеривания различных объёмов жидкостей.
Б. Делительные воронки применяют для разделения растворов.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
9. Верны ли суждения о правилах работы в химической лаборатории?
А. Градуированные пипетки заполняют с помощью груши.
Б. При кратковременном нагревании жидкости в пробирке используют держатели.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
10. Верны ли суждения о правилах работы в химической лаборатории?
А. При длительном нагревании жидкостей используют штативы.
Б. Фильтратом называют раствор, освобождённый от твердых частиц.
1) верно только А
2) верно только Б
3) верны оба суждения
4) оба суждения неверны
11. Лакмус окрасится в красный цвет в растворе
12. Лакмус окрасится в красный цвет в растворе
13. Лакмус окрасится в синий цвет в растворе
14. Лакмус окрасится в синий цвет в растворе
15. Индикатор метиловый оранжевый окрасится в жёлтый цвет в растворе
16. Индикатор метиловый оранжевый окрасится в жёлтый цвет в растворе
17. Индикатор метиловый оранжевый окрасится в розовый цвет в растворе
18. Индикатор метиловый оранжевый окрасится в розовый цвет в растворе
19. Для качественного определения хлорид-иона в растворе применяют реактив
20. Для качественного определения сульфат-иона в растворе применяют реакцию с катионом
1) Al 3+
2) Mg 2+
3) Ba 2+
4) Na +
21. Для качественного определения карбонат-иона в растворе применяют реакцию с катионом
1) Na +
2) Li +
3) Rb +
4) Ca 2+
22. При взаимодействии хлорида натрия и нитрата серебра
1) выпадает осадок жёлтого цвета
2) выпадает осадок коричневого цвета
3) выпадает осадок белого цвета
4) внешних изменений не происходит
23. При взаимодействии нитрата бария с сульфатом калия
1) выпадает кристаллический осадок белого цвета
2) выделяется бесцветный газ
3) выпадает осадок коричнево-красного цвета
4) внешних изменений не происходит
24. При пропускании углекислого газа через известковую воду
1) внешних изменений не происходит
2) выпадает осадок белого цвета, нерастворимый в кислотах
3) выпадает осадок зеленоватого цвета, нерастворимый в кислотах
4) выпадает осадок белого цвета, растворяющийся при дальнейшем пропускании углекислого газа
25. В пробирку с раствором соли добавили концентрированный раствор гидроксида натрия и нагрели. Наблюдалось выделение пузырьков газа, в парах которого влажная лакмусовая бумажка окрасилась в синий цвет. Эта соль
26. Осадок выделится при сливании растворов
27. Осадок выделится при сливании водных растворов
28. Газ выделяется при сливании водных растворов
29. Смесь осадков образуется при взаимодействии водных растворов веществ
30. Осадок и газ образуется одновременно при сливании растворов
Источник
Газообразные вещества

Средняя оценка: 4.3
Всего получено оценок: 334.
Средняя оценка: 4.3
Всего получено оценок: 334.
Соединение, находящееся в одном из основных агрегатных состояний, при котором составные частицы слабо связаны между собой, называется газом или газообразным веществом. Частицы газа движутся хаотично и в некоторых случаях могут переходить в жидкое и твёрдое состояния.
Получение
Существуют вещества, которые при нормальных условиях сохраняются в газообразном агрегатном состоянии. Их можно разделить на две группы:
- простые – азот, кислород, хлор;
- сложные – аммиак, метан, углекислый газ.
Газы выделяют из атмосферы или природного газа путём окисления и адсорбции примесей.
Образованию газообразного состояния веществ способствует изменение нормальных условий. Жидкие или твёрдые вещества нагревают, тем самым разрушая химические связи и высвобождая отдельные молекулы в воздух. Например, жидкая вода при нагревании легко превращается в водяной пар, а твёрдый йод выделяет фиолетовые пары.
В лабораториях газ получают путём разложения (сжигания) сложных веществ или реакцией жидких и твёрдых соединений. Способы получения некоторых газов:
Полученный газ обнаруживают разными способами. Например, пропускают через жидкость и наблюдают за изменением цвета, прозрачности (известковое молочко мутнеет в присутствии углекислого газа). Некоторые газы поддерживают горение или, наоборот, тушат тлеющую лучину.
Физические свойства
Молекулы газообразного вещества постоянно движутся, а расстояние между ними значительно превышает их диаметр. Благодаря такому расположению частиц газы не имеют формы, легко смешиваются и сжимаются.
Газообразные соединения приобретают форму сосуда, в котором находятся. Ударяясь о стенки сосуда с определённой скоростью, газы создают давление. Чем интенсивнее молекулы воздействуют на сосуд, тем выше давление.
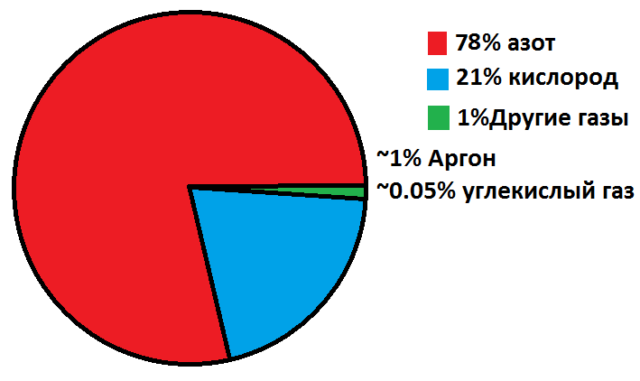
Различные газообразные соединения смешиваются между собой в любых пропорциях. Природный газ – это смесь метана, водорода, сероводорода, углекислого газа, азота, гелия. Атмосфера состоит из смесей простых и сложных газообразных веществ – азота, кислорода, водорода, углекислого газа, водяного пара.
При сжатии объём газов становится значительно меньше. Например, объём кислорода уменьшается в 200 раз.
Описание некоторых газообразных веществ представлено в таблице.
Формула
Физические свойства
Нахождение в природе
Самый лёгкий газ, легче воздуха в 14,5 раз. Не имеет вкуса, запаха, цвета. Плохо растворяется в воде (18,8 мл/100 г), но хорошо растворяется в металлах, особенно в палладии. Сжижается при -252,76°C
В земной коре – 1 %, незначительное количество в атмосфере. Большая часть водорода присутствует в виде соединений
Не имеет вкуса, цвета, запаха. Немного тяжелее воздуха. Плохо растворяется в воде (4,9 мл/100 г) и спирте (2,78 мл/100 г), но хорошо растворяется в жидком серебре. Сжижается при -182,98°C
47 % земной коры состоит из кислорода. Моря и пресные водоёмы содержат 85 % кислорода. В атмосфере – 20 %
Бесцветный газ без запаха. Плохо растворим в воде (2,3 мл/100 г). Атомы азота связаны тройной трудно разрываемой связью. Сжижается при -195,8°C
В атмосфере – 78 %. Один из наиболее распространённых элементов, найденных за пределами Земли. Входит в состав белков
Жёлто-зелёный газ с запахом. Легко сжижается уже при -34°C. При давлении в 0,8 МПа и комнатной температуре становится жидким. Плохо растворяется в воде (1,48 мл/100 г), хорошо растворяется в бензоле и хлороформе
Наиболее распространённый галоген. В природе встречается только в составе минералов
Бесцветный газ, не имеющий запаха при малых концентрациях. В большом количестве имеет кислый запах. В 1,5 раза тяжелее воздуха. Кристаллизуется при -78,3°С. Жидкое состояние получают при комнатной температуре и давлении в 6 МПа
В атмосфере содержится меньше 1 %
Бесцветный газ с резким запахом. В два раза тяжелее воздуха. Хорошо растворяется в воде
Образуется путём разложения азотсодержащих веществ
За счёт свободного движения молекул газ равномерно распространяется в ограниченном пространстве. Такое явление называется диффузией. Яркий пример диффузии – распространение запахов. При приготовлении пищи на кухне запах постепенно распространяется по всей квартире.
Что мы узнали?
Газ – вещество, состоящее из хаотично движущихся частиц – молекул или атомов. Газообразные соединения можно получить выделением из атмосферы путём адсорбции и окисления. Также газ получают из жидких и твёрдых веществ путём изменения условий или взаимодействием простых и сложных веществ. Газы не имеют формы, легко смешиваются между собой и равномерно распределяются в закрытом пространстве. Наиболее распространённый газ в атмосфере – азот. Самый лёгкий газ.
Источник
Краткие теоретические сведения



Практическая работа №2
«Получение и распознавание газов»
Краткие теоретические сведения
Строение газообразных веществ отличается от строения веществ в твердом и жидком состояниях. Газы не имеют собственной формы и расширяются до тех пор, пока не заполнят весь сосуд принимая его форму, по этой же причине газы не имеют собственного объема. Объем газа определяется объемам сосуда. Газ оказывает на стенки сосуда одинаковое во всех направлениях давления. Газы легко сжимаются. Благодаря большому расстоянию между молекулами газы смешиваются друг с другом в любом отношении. Основные газы получаемые и используемые в лабораториях это водород, кислород, углекислый газ.
Лабораторные способы получения этих газов:
Водород получают в аппарате Киппа, при взаимодействии соляной кислоты и металлического цинка (в гранулах) — при комнатной температуре:
Zn + 2HCl = ZnCl2 + H2
Оксид углерода (IV) = углекислый газ можно получить, действуя соляной или разбавленной серной кислотой на мрамор (основное вещество — карбонат кальция) или другой карбонат (при комнатной температуре). Сильная кислота (серная или соляная) будет вытеснять слабую угольную кислоту из её солей; угольная кислота нестойкая, поэтому практически сразу разлагается на углекислый газ и воду:
СаСО3 + 2HCl = CaCl2 + CO2 + H2O
Можно получить углекислый газ, сжигая лучину, бумагу или кусочек угля.
Кислород можно получить разложением при нагревании бертолетовой соли или лучше перманганата калия:
2KClO3 = 2KCl + 3O2 (есть опасность взрыва)
2KMnO4 = K2MnO4 + MnO2 + O2
Собирание газов
В устройстве аппарата Киппа предусмотрена газоотводная трубка с краником; для получения углекислого газа и кислорода реактивы помещают в пробирку и закрывают её пробкой с газоотводной трубкой. Пробирку с перманганатом калия закрепляют в штативе и нагревают пламенем спиртовки.
Водород легче воздуха, поэтому его собирают над воздухом, в перевёрнутую пробирку. Кислород и углекислый газ тяжелее воздуха, поэтому их можно собирать вытеснением воздуха, опустив газоотводную трубку на дно пробирки. Кислород малорастворим в воде, поэтому его можно также собирать над водой, в перевёрнутую пробирку (этот способ лучше, т.к. разница молярных масс кислорода (32 г/моль) и воздуха (29 г/моль) невелика).
Чтобы распознать эти газы, нужно знать их свойства.
Так, кислород поддерживает горение — опущенная в пробирку с кислородом тлеющая лучинка начинает ярко гореть; углекислый газ не поддерживает горение — горящая лучинка, опущенная в пробирку с углекислым газом, гаснет.
Углекислый газ, кроме того, мутит известковую воду: при его взаимодействии с гидроксидом кальция («известковой водой») образуется нерастворимый в воде осадок карбоната кальция:
Са(ОН)2 + СО2 = СаСО3 + Н2О
Чистый водород сгорает с легким звуком «пах», водород с примесью воздуха взрывоопасен «гремучий газ» и в небольшом количестве сгорает с резким лающим звуком.
Водород (Н2) – самый легкий, бесцветный, не имеет запаха.
Кислород (О2) без запаха и цвета,тяжелее воздуха, мало растворим в воде.
Аммиак (NН3) имеет резкий характерный запах, без цвета, хорошо растворим в воде, легче воздуха.
Это оформить в тетради!
Практическая работа №2
Получение и распознавание газов
Цель: изучить процессы и химизм получения газов на примере водорода, кислорода и углекислого газа.
Оборудование:цинк в гранулах, раствор соляной кислоты, мел, раствор пероксида водорода, оксид марганца (II); пробирки, спиртовка, лучинка
Последовательность выполнения работы:
Внимание: Записи о наблюдаемых явлениях по всем опытам внесите в таблицу по форме:
| Что делали | Что наблюдали | Уравнения реакций |
| В пробирку поместить две гранулы цинка. 2. Прилить 2 мл раствора соляной кислоты. Что наблюдаете? Запишите уравнение реакции с точки зрения окислительно-восстановительного процесса. 3. Накрыть пробирку-реактор пробиркой большего диаметра. 4. Через 4 минуты поднимите большую пробирку и, не переворачивая, поднесите её к пламени спиртовки. Что наблюдаете? Запишите уравнение реакции. Что можете сказать о «чистоте» собранного водорода? | ||
| 1. В пробирку прилить 5 мл раствора пероксида водорода. 2. Подготовьте тлеющую лучину. 3. Добавьте в пробирку несколько крупинок оксида марганца (IV). Что наблюдаете? Запишите уравнение реакции с точки зрения окислительно-восстановительного процесса. 4. Внесите тлеющую лучину в пробирку с раствором пероксида водорода. | ||
| 1. В пробирку поместить кусочек мела. 2. Прилить к мрамору 4 мл раствора уксусной кислоты. Что наблюдаете? Запишите уравнение химической реакции в молекулярной и ионной форме. 3. Зажгите лучину. 4. Внесите горящую лучину в пробирку-реактор. |
Контрольные вопросы:
1. Почему водород собирают в перевернутую пробирку?
2. Если через раствор известковой воды посредством стеклянной трубки продувать выдыхаемый воздух, то через некоторое время известковая вода помутнеет. Почему?
3. Какое свойство углекислого газа лежит в основе его применения в углекислотном огнетушителе.
Список литературы
Габриелян О.С., Остроумов И.Г. Химия для профессий и специальностей технического профиля. М. Издательский центр «Академия». 2017
Тема 2. Практическая работа №3
Решение экспериментальных задач по теме «Металлы и неметаллы»
Это для ознакомления, не писать!
Краткие теоретические сведения
Распознавание веществ производится с помощью качественных реакций.
Качественные реакции – это химические реакции, с помощью которых можно определить то, чем одно вещество отличается от другого по элементарному составу, иначе говоря, эти реакции позволяют определить отдельные ионы или молекулы, из которых состоит исследуемое вещество или смесь веществ. В качественном анализе применяют реакции, сопровождающиеся каким-либо эффектом, который можно легко обнаружить органами чувств:
· Изменение окраски раствора;
· Выпадение или растворение осадка;
· Выделение газов (иногда обладающих характерным запахом)
В таблице приведены некоторые из качественных реакций.
| Катион | Воздействие или реактив | Наблюдаемая реакция |
| Na + | Пламя | Желтое окрашивание |
| К + | Пламя | Фиолетовое окрашивание |
| Са 2+ | Пламя | Кирпично-красное окрашивание |
| Аg + | хлорид | Выпадение белого осадка |
| Fe 2+ | гексациано-феррат (III) калия (красная кровяная соль) | Выпадение синего осадка |
| Fe 3+ | роданид | Красное окрашивание |
| Анион | Воздействие или реактив | Наблюдаемая реакция |
| S04 2- | соль бария | Выпадение белого осадка |
| СО3 2- | кислота | вскипание или пузырьки газа |
| Cl — | ионы Аg+ | Выпадение белого осадка, не растворимого в HN03 |
Для выполнения опытов отбирается проба (небольшое количество вещества помещается в чистую пробирку) и исследуется реактивом.
Источник












