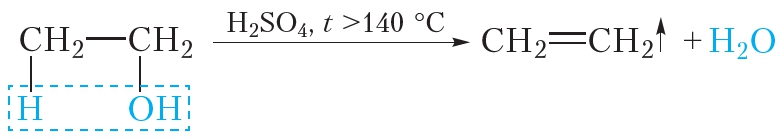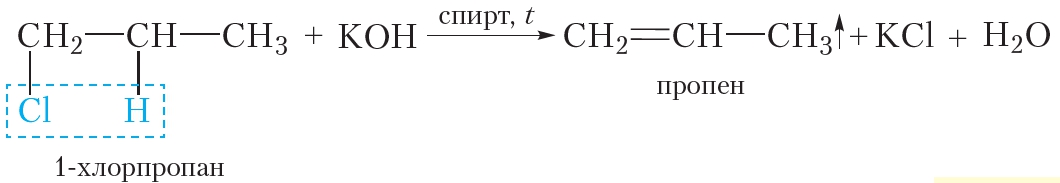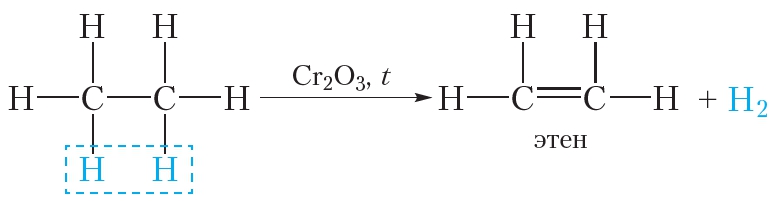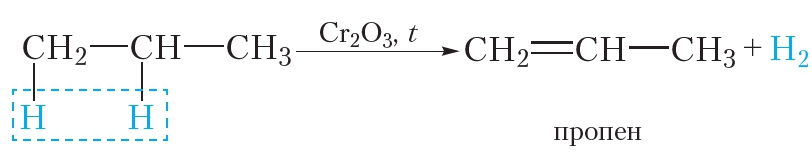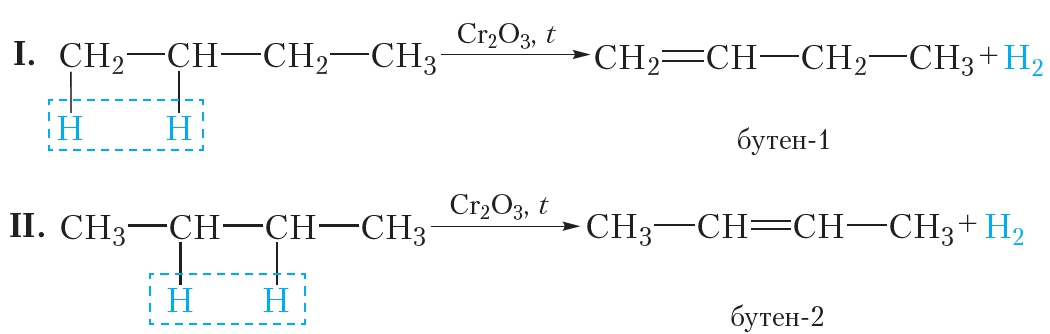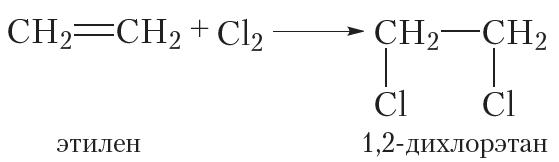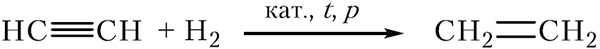- Способы получения алкенов
- Получение алкенов
- 1. Дегидрирование алканов
- 2. Крекинг алканов
- 3. Дегидрогалогенирование галогеналканов
- 4. Дегидратация спиртов
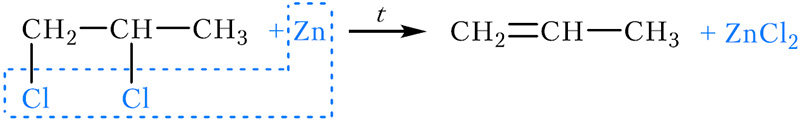
- 5. Дегалогенирование дигалогеналканов
- Алкены
- § 16. Получение и применение алкенов
- Оглавление
- Получение и применение алкенов
- Применение алкенов
- *Получение алкенов
- Вопросы и задания
Способы получения алкенов
Алкены – это непредельные (ненасыщенные) нециклические углеводороды, в молекулах которых присутствует одна двойная связь между атомами углерода С=С.
Наличие двойной связи между атомами углерода очень сильно меняет свойства углеводородов.
Получение алкенов
Рассмотрим промышленные и лабораторные способы получения алкенов.
1. Дегидрирование алканов
При дегидрировании алканов, содержащих от 2 до 4 атомов углерода в молекуле, образуются двойные и тройные связи.
| Например, при дегидрировании этана может образоваться этилен или ацетилен: |
При дегидрировании бутана под действием металлических катализаторов образуется смесь продуктов. Преимущественно образуется бутен-2:

Если бутан нагревать в присутствии оксида хрома (III), преимущественно образуется бутадиен-1,3:

2. Крекинг алканов
Крекинг – это реакция разложения алкана с длинной углеродной цепью на алканы и алкены с более короткой углеродной цепью.
Крекинг бывает термический и каталитический.
Термический крекинг протекает при сильном нагревании без доступа воздуха.
При этом получается смесь алканов и алкенов с различной длиной углеродной цепи и различной молекулярной массой.
| Например, при крекинге н-пентана образуется смесь, в состав которой входят этилен, пропан, метан, бутилен, пропилен, этан и другие углеводороды. |

Каталитический крекинг проводят при более низкой температуре в присутствии катализаторов. Процесс сопровождается реакциями изомеризации и дегидрирования. Катализаторы каталитического крекинга – цеолиты (алюмосиликаты кальция, натрия).
3. Дегидрогалогенирование галогеналканов
Галогеналканы взаимодействуют с щелочами в спиртовом растворе. При этом происходит дегидрогалогенирование – отщепление (элиминирование) атомов водорода и галогена от галогеналкана.
| Например, при взаимодействии хлорэтана с спиртовым раствором гидроксида натрия образуется этилен. |
При отщеплении галогена и водорода от некоторых галогеналканов могут образоваться различные органические продукты. В таком случае выполняется правило Зайцева.
| Правило Зайцева: отщепление атома водорода при дегидрогалогенировании и дегидратации происходит преимущественно от наименее гидрогенизированного атома углерода. |
| Например, при взаимодействии 2-хлорбутана со спиртовым раствором гидроксида натрия преимущественно образуется бутен-2. Бутен-1 образуется в небольшом количестве (примерно 20%). В реакции мы указываем основной продукт. |
4. Дегидратация спиртов
При нагревании спиртов (выше 140 о С) в присутствии водоотнимающих веществ (концентрированная серная кислота, фосфорная кислота) или катализаторов (оксид алюминия) протекает дегидратация. Дегидратация — это отщепление молекул воды.
При дегидратации спиртов образуются алкены.
| Например, при дегидратации этанола при высокой температуре образуется этилен. |

Дегидратация более сложных молекул также протекает по правилу Зайцева.
| Например, при дегидратации бутанола-2 преимущественно образуется бутен-2. |
5. Дегалогенирование дигалогеналканов
Дигалогеналканы, в молекулах которых два атома галогена расположены у соседних атомов углерода, реагируют с активными металлами с образованием алкенов.
Как правило, для отщепления используют двухвалентные активные металлы — цинк или магний.
Источник
Алкены
Алкены — непредельные (ненасыщенные) углеводороды, имеющие в молекуле одну двойную связь С=С. Такая связь содержит одну сигма-связь (σ-связь) и одну пи-связь (π-связь).
Алкены также называют этиленовыми углеводородами, по первому члену гомологического ряда — этилену — CH2=CH2. Общая формула их гомологического ряда — CnH2n.
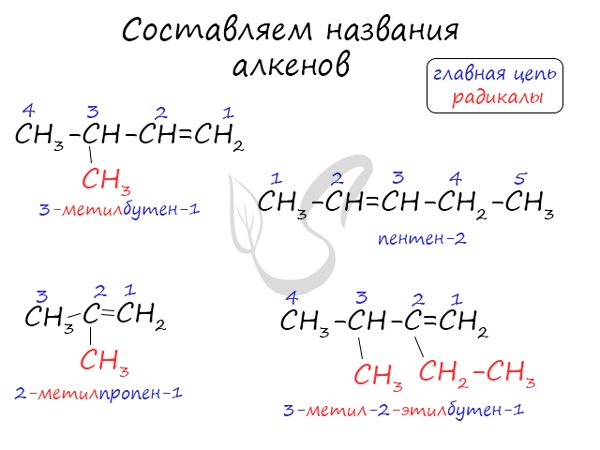
Номенклатура и изомерия алкенов
Названия алкенов формируются путем добавления суффикса «ен» к названию алкана с соответствующим числом: этен, пропен, бутен, пентен и т.д.
При составлении названия алкена важно учесть, что главная цепь атомов углерода должна обязательно содержать двойную связь. Принято начинать нумерацию атомов углерода с того края, к которому ближе двойная связь. В конце названия указывают атом углерода, у которого начинается двойная связь.
Атомы углерода, прилежащие к двойной связи находятся в sp 2 гибридизации.
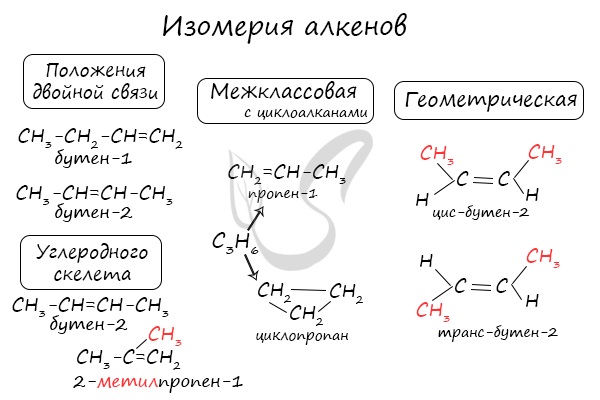
Для алкенов характерна изомерия углеродного скелета, положения двойной связи, межклассовая изомерия с циклоалканами и пространственная геометрическая изомерия в виде существования цис- и транс-изомеров.
Некоторые данные, касающиеся алкены, надо выучить:
- Длина связи между атомами углерода составляет 0,134 нм
- Тип гибридизации атомов углерода (прилежащих к двойной связи) — sp 2
- Валентный угол (между химическими связями) составляет 120°
Получение алкенов
Алкены получают несколькими способами:
- Крекинг нефти
В результате крекинга нефти образуется один алкан и один алкен.
При наличии катализатора и повышенной температуры от молекул алканов отщепляется водород. Наиболее легко водород отдает третичный атом, чуть труднее — вторичный и заметно труднее — первичный.
В реакции галогеналкана со спиртовым(!) раствором щелочи образуется алкен. По правилу Зайцева, водород отщепляется от соседнего наименее гидрированного атома углерода.
В подобных реакциях применяется цинк (цинковая пыль) — двухвалентный металл, который связывает расположенные рядом атомы галогенов. Между атомами углерода, которым принадлежали галогены, завязывается двойная связь.
При нагревании спиртов c серной кислотой — H2SO4, обладающей выраженными водоотнимающими свойствами, происходит отщепление воды от спирта по правилу Зайцева. В результате образуется алкен.
Внутримолекулярная дегидратация спиртов происходит при t > 140 °C.
Химические свойства алкенов
Алкены — ненасыщенные углеводороды, охотно вступающие в реакции присоединения. Реакции замещения для них не характерны.
Водород присоединяется к атомам углерода, образующим двойную связь. Пи-связь (π-связь) рвется, остается единичная сигма-связь (σ-связь).
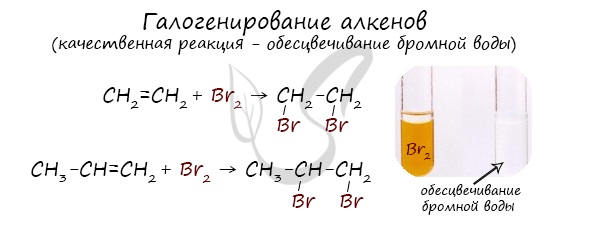
Реакция с бромной водой является качественной для непредельных соединений, содержащих двойные (и тройные) связи. В ходе такой реакции бромная вода обесцвечивается, что указывает на присоединение его по кратным связям к органическому веществу.
Реакция с хлором на свету протекает по свободнорадикальному механизму, так как на свету молекулы хлора расщепляются, образуя свободные радикалы.
Алкены вступают в реакции гидрогалогенирования, протекающие по типу присоединения.
Гидрогалогенирование протекает по правилу Марковникова, в соответствии с которым атом водорода присоединяется к наиболее гидрированному, а атом галогена — к наименее гидрированному атому углерода.
Присоединение воды, гидратация, происходит по правилу Марковникова. Водород присоединяется к наиболее гидрированному атому углерода, гидроксогруппа — к наименее гидрированному.
При горении алкены, как и все органические соединения, сгорают с образованием углекислого газа и воды — полное окисление. При неполном окислении образуются окиси.
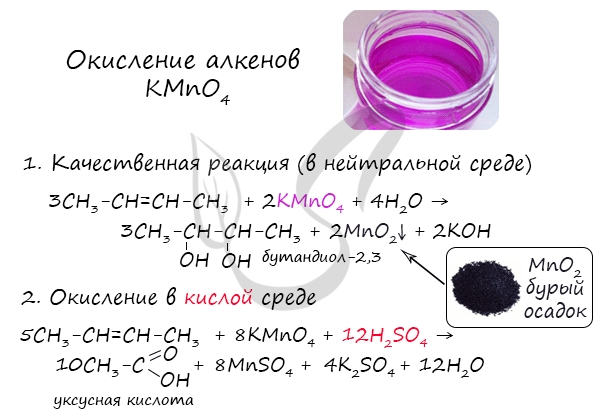
Окисление алкенов перманганатом калия (марганцовкой) в нейтральной среде является качественной реакцией на алкены в частности, и непредельные углеводороды в целом. В результате реакции фиолетовый раствор марганцовки обесцвечивается и выпадает осадок бурого цвета — MnO2.
В более жестких условиях — при подкислении раствора серной кислотой, реакция идет с полным разрывом в самом слабом месте молекулы — двойной связи.
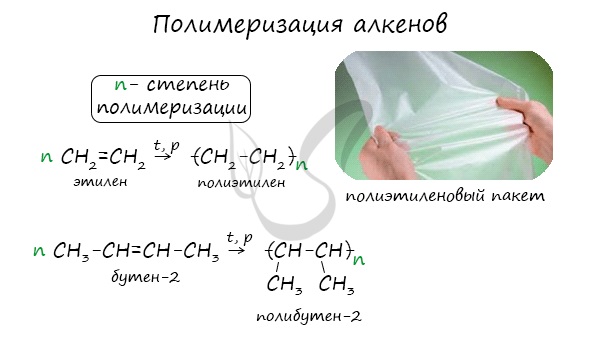
Полимеризация — цепная реакция синтеза полимеров, при котором молекула полимера образуется путем последовательного соединения молекул мономеров.
Индекс «n», степень полимеризации, обозначает число мономерных звеньев, которые входят в состав полимера.
© Беллевич Юрий Сергеевич 2018-2021
Данная статья написана Беллевичем Юрием Сергеевичем и является его интеллектуальной собственностью. Копирование, распространение (в том числе путем копирования на другие сайты и ресурсы в Интернете) или любое иное использование информации и объектов без предварительного согласия правообладателя преследуется по закону. Для получения материалов статьи и разрешения их использования, обратитесь, пожалуйста, к Беллевичу Юрию.
Источник
§ 16. Получение и применение алкенов
| Сайт: | Профильное обучение |
| Курс: | Химия. 10 класс |
| Книга: | § 16. Получение и применение алкенов |
| Напечатано:: | Гость |
| Дата: | Пятница, 19 Ноябрь 2021, 11:19 |
Оглавление
Получение и применение алкенов
Алкены являются химически более активными веществами, чем алканы, поэтому в составе природных источников углеводородов (нефти и природном газе) их содержание невелико.
Основная область применения алкенов — получение полимеров посредством реакции полимеризации. Промышленное производство алкенов и полимеров на их основе занимает важное место в экономике многих стран. В нашей стране полиэтилен и полипропилен получают в Новополоцке (ОАО «Нафтан»).
Рассмотрим способы получения этилена и других алкенов.
1. Дегидратация спиртов
Алкены можно получить в результате реакции отщепления воды от спиртов. Реакция отщепления молекулы воды называется реакцией дегидратации (приставка де- означает отщепление).
Этилен образуется в результате реакции дегидратации этилового спирта. Для этого смесь этилового спирта с концентрированной серной кислотой нагревают в пробирке с газоотводной трубкой (см. видео 15.1). При этом от молекулы спирта отщепляется молекула воды и образуется этилен. Уравнение реакции:
Выделяющийся этилен легко обнаружить с помощью качественных реакций на алкены. Если этилен пропустить через бромную воду либо разбавленный водный раствор перманганата калия, они обесцветятся.
В предыдущем параграфе мы изучали обратную реакцию — присоединение воды к молекуле этилена с образованием этилового спирта. Катализатором и прямой и обратной реакции является серная кислота, но условия их протекания различны. Для протекания реакции дегидратации требуется более высокая температура и концентрированная (практически не содержащая воды) серная кислота. Для реакции гидратации алкенов используют избыток воды. Напомним, что условия протекания реакции принято указывать над стрелкой в уравнении реакции. Из приведённого примера видно, что в зависимости от условий реакция может протекать в прямом либо в обратном направлении. Поэтому следует обязательно указывать условия протекания химических реакций.
2. Дегидрогалогенирование галогенпроизводных алканов
Дегидрогалогенированием называется реакция отщепления галогеноводородов от молекул органических веществ. Таким способом можно получить алкены из галогенпроизводных алканов. При действии спиртового раствора щелочи от молекулы галогенпроизводного отщепляется молекула галогеноводорода и образуется алкен:

3. Дегидрирование алканов
Дегидрированием называется реакция отщепления от органического вещества молекулы водорода (H2). Два атома водорода отщепляются от двух соседних атомов углерода, при этом образуется алкен. Уравнение реакции дегидрирования этана:
Напомним, что над стрелкой в уравнении принято указывать условия протекания реакции. Большинство органических реакций не могут протекать при обычных условиях, поэтому следует обязательно указывать условия их протекания! Так, реакция дегидрирования алканов протекает при температуре около 500 °С и на катализаторе Cr2O3. В предыдущем параграфе мы изучали обратную реакцию — присоединение водорода к этилену. Напомним, что обратная реакция — гидрирование алкенов, протекает на платиновом или никелевом катализаторе при 100–200 °С.
Рассмотрим дегидрирование других алканов. В случае пропана реакция протекает согласно уравнению:
В данном случае может получиться только один алкен — пропен. При дегидрировании бутана образуется смесь алкенов:
Алкены получают также в результате переработки нефти. С этой темой вы познакомитесь далее.
Применение алкенов
Основная область применения алкенов — получение полимеров. Из этилена и пропилена получают полиэтилен и полипропилен, из которых изготавливают самые разнообразные изделия, используемые в быту и промышленности.
Реакцией гидратации этилена получают этиловый спирт.
В результате присоединения хлора к этилену получают 1,2-дихлорэтан, который применяют в качестве растворителя:
Этилен ускоряет созревание различных плодов (груш, дынь, помидоров и т. д.). С целью лучшего сохранения плоды можно транспортировать неспелыми и доводить их до созревания на месте, вводя в воздух хранилищ этилен.
Кроме этого, алкены применяются для синтеза различных органических веществ.
Интересно знать
Яблоки при хранении выделяют этилен, поэтому для ускорения созревания некоторых фруктов, например бананов, в ёмкость, где они хранятся, помещают несколько кусочков яблока. Попробуйте осуществить этот эксперимент дома с зелёными бананами.
В отличие от алканов, содержание алкенов в природных источниках невелико, поэтому их необходимо получать с помощью химических реакций.
Алкены получают дегидратацией спиртов, дегидрогалогенированием галогенпроизводных алканов, дегидрированием алканов.
Алкены используются в качестве мономеров при производстве полимеров и для синтеза различных органических веществ.
*Получение алкенов
Алкены в лаборатории можно получить в результате нагревания дигалогенпроизводных алканов с цинком:
Обратите внимание, что атомы галогена должны располагаться у соседних атомов углерода. Так как в результате реакции от молекулы органического вещества отщепляется молекула галогена, такая реакция называется реакцией дегалогенирования.
Ещё одним методом получения алкенов является гидрирование углеводородов, молекулы которых содержат тройную связь С 
Вопросы и задания
1. Напишите уравнения реакций получения: а) этилена из этилового спирта; б) пропилена из 2-бромпропана; в) пропилена из пропана. Укажите условия протекания этих реакций. Все указанные реакции можно провести в обратном направлении. Запишите уравнения обратных реакций и укажите условия их протекания.
2. Предложите два способа получения хлорэтана из этилена. Напишите уравнения протекающих реакций.
3. Сколько алкенов может быть получено при дегидрировании 2-метилбутана? Напишите уравнения реакций и укажите условия их протекания.
4. При полном сгорании углеводорода А образовалось 27 г воды и 33,6 дм 3 (н. у.) углекислого газа.
а) Установите простейшую формулу углеводорода А.
б) В результате пропускания данного углеводорода в смеси с избытком водорода над никелевым катализатором при нагревании получен углеводород Б, имеющий плотность 1,964 г/дм 3 (н. у.).
Выведите молекулярные формулы углеводородов А и Б.
5. В результате гидрирования алкена X образуется алкан, при хлорировании которого можно получить только два изомерных монохлорсодержащих вещества. При взаимодействии алкена X с бромной водой образуется вещество состава C6H12Br2, имеющее симметричное строение. Приведите структурную формулу алкена X и составьте уравнения всех протекающих реакций.
6. Алкан и алкен содержат одинаковое количество атомов углерода в молекулах. Массовая доля (%) водорода в алкане на 2,38 единицы больше, чем в алкене. Установите молекулярную формулу алкена.
7. Вычислите массу полиэтилена, который может быть получен из 200 м 3 (н. у.) этана, если выход продукта реакции дегидрирования составляет 96 %, а полимеризации 98 %.
8. Напишите уравнения реакций, с помощью которых можно осуществить следующие превращения:
Источник