- Трансплантация костного мозга и стволовых клеток
- Общие принципы
- Как пересаживают костный мозг?
- Что такое пересадка костного мозга?
- Противопоказания
- Выбор донора
- Забор клеток
- Подготовка: химиотерапия и лучевая терапия перед пересадкой костного мозга
- Процедура ТКМ
- Восстановление после пересадки
- Восстановление детей
- Жизнь после трансплантации
- Риск рецидива
- Отзывы пациентов
Трансплантация костного мозга и стволовых клеток
Общие принципы
Трансплантация костного мозга (ТКМ) / стволовых кроветворных клеток периферической крови (ТСКК) — метод лечения гематологических, онкологических и аутоиммунных заболеваний, при котором пациенту после проведения интенсивной иммуносупрессивной терапии с применением больших дозы цитостатических препаратов (иммуносупрессантов), вводят предварительно заготовленный костный мозг или стволовые кроветворные клетки периферической крови (СКК). Ежегодно в мире выполняется около 150 000 ТКМ и ТСКК, причем количество операций постоянно увеличивается.
ОБЩАЯ ИНФОРМАЦИЯ О СТВОЛОВЫХ КРОВЕТВОРНЫХ КЛЕТКАХ
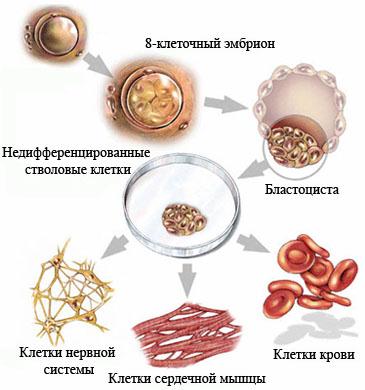
Недифференцированная стволовая клетка, происходящая из бластоцисты, является родоначальницей всех клеток организма, в том числе и стволовой кроветворной клетки (СКК).
Основными свойствами стволовой кроветворной клетки являются возможность дифференцироваться в направлении любого из ростков кроветворения и способность к самоподдержанию.
 Колонии стволовых кроветворных клеток (электронная микроскопия) | 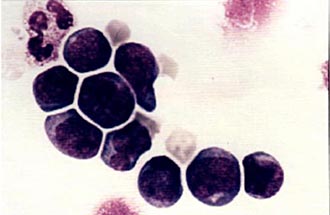 Мононуклеарная фракция, обогащенная клетками CD34, окрашена по Маю-Грюнвальду с докраской по Гимзе. Стволовые клетки, несущие маркер CD34, внешне напоминают малые и средние лимфоциты. |
ИСТОРИЧЕСКАЯ СПРАВКА
Первые работы, посвященные терапевтическому использованию костного мозга, были выполнены в последней декаде XIX века, независимо друг от друга Brown-Sequard, d»Arsonval, Fraser, Billings и Hamilton, которые применяли экстракт костного мозга животных для лечения больных различными видами анемий. Несмотря на положительный эффект, отмеченный всеми авторами, в течение последующих пятидесяти лет использование данной методики носило спорадический характер и не выходило за рамки клинического эксперимента до 1937 года когда Schretzenmayr впервые произвел парентеральное (внутримышечное) введение костного мозга, а в 1939 году Osgood выполнил первое внутривенное введение костного мозга.
Результаты экспериментальных исследований привели клиницистов к идее использования ТКМ при заболеваниях, связанных с поражением костного мозга (лейкозы, апластическая анемия), а также при радиационных воздействиях и проведении химиотерапии, однако основные теоретические и практические проблемы проведения ТКМ удалось преодолеть в 60-е годы. С этого времени ТКМ является одним из методов лечения различных заболеваний крови и иммунной системы.
ВИДЫ ТРАНСПЛАНТАЦИИ КОСТНОГО МОЗГА
Выделяют два основных вида ТКМ:
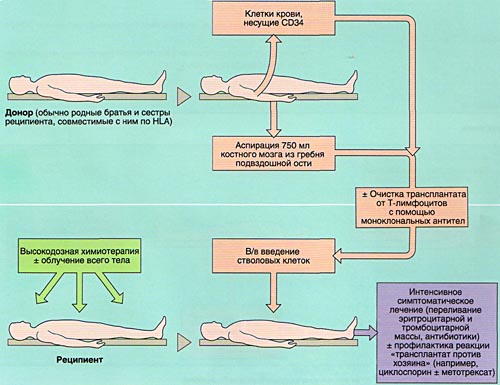
- 1)аллогенную (АллоТКМ) — при которой больному вводится костный мозг от родственного или неродственного совместимого донора;
Разновидностью АллоТКМ является сингенная ТКМ (трансплантация от однояйцевого близнеца).
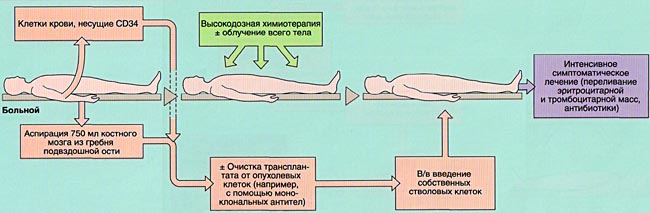
- 2)аутологичную (АутоТКМ) — когда реципиент получает предварительно заготовленный собственный костный мозг;
ПОКАЗАНИЯ К ТРАНСПЛАНТАЦИИ КОСТНОГО МОЗГА
Аллогенная трансплантация костного мозга:
- 1) острые лейкозы;
- 2) хронический миелолейкоз;
- 3) тяжелая апластическая анемия;
- 4) гемоглобинопатии;
- 5) врожденные иммунодефициты и нарушения метаболизма.
Аутологичная трансплантация костного мозга:
- 1) злокачественные лимфомы;
- 2) некоторые солидные опухоли;
- 3) аутоиммунные заболевания.
В связи с ограниченным количеством родственных гистосовместимых доноров, которые имеются лишь у 20- 25% больных, в последние годы нашла применение АлТКМ от неродственных HLA-идентичных доноров. Для этих целей созданы международные регистры, позволяющие подобрать потенциального донора костного мозга и оптимизировать прогноз у пациентов, для которых АллоТКМ предпочтительнее (острые лейкозы, хронический миелолейкоз) или является методом выбора (апластическая анемия, гемоглобинопатии, иммунодефициты, нарушения метаболизма). Общее число зарегистрированных доноров в мире превышает 5 миллионов человек, в том числе в России — около 10 тысяч.
С развитием появлением колониестимулирующих факторов и развитием технологий клеточной сепарации с 70-х годов для получения гемопоэтических клеток крови вмести костного мозга стали использовать стволовые клетки периферической крови.
Применение клеточных сепараторов значительно упростило проведение процедуры получения стволовых клеток крови, уменьшило число осложнений связанных с дачей наркоза и травматическим повреждения костной ткани.
Еще одним потенциальным источником СКК является пуповинная кровь, основным преимуществом которой является меньшая иммуногенность, однако малое количество стволовых клеток в материале ограничивает ее применение и используется преимущественно в педиатрии или у пациентов с массой тела до 50 кг.
Методика проведения миелотрансплантации различается в зависимости от ее вида (аллогенная или аутологичная), нозологической формы заболевания и ряда других факторов.
ПРАКТИЧЕСКИЕ АСПЕКТЫ МИЕЛОТРАНСПЛАНТАЦИИ
При любой методике ТКМ/ТСКК можно выделить следующие этапы:
- 1) определение показаний и противопоказаний;
- 2) выбор донора (при аллогенной трансплантации);
- 3) получение костного мозга/стволовых клеток их обработка, хранение и введение;
- 4) кондиционирование (иммуносупрессивная терапия);
- 5) профилактика и лечение осложнений периода цитопении;
- 6) профилактика и лечение поздних осложнений.
ОПРЕДЕЛЕНИЕ ПОКАЗАНИЙ И ПРОТИВОПОКАЗАНИЙ
Наиболее частыми показаниями к ТКМ/ТСКК являются онкогематологические и гематологические заболевания (лейкозы, злокачественные лимфомы, апластическая анемия, врожденные иммунодефициты и нарушения метаболизма).
Чаше всего ТКМ или ТСКК проводится во время полной ремиссии (ПР), частичной ремиссии (ЧР) или при рецидиве опухоли, чувствительном к химиотерапии. При первичной резистентности к цитостатической терапии результаты ТКМ резко ухудшаются, поэтому в этих случаях операция выполняется относительно редко.
При некоторых заболеваниях трансплантация является методом выбора (тяжелые формы апластической анемии, гемоглобинопатии, врожденных иммунодефицитов и нарушений метаболизма). В ряде случаев ТКМ/ТСКК проводится при солидных опухолях и аутоиммунных заболеваниях. Данная методика имеет возрастные ограничения: АутоТКМ/ТСКК может быть выполнена у лиц моложе 65 лет, АллоТКМ от HLA-идентичного родственника — моложе 55 лет, неродственная АллоТКМ — моложе 50 лет.
Проведение трансплантации противопоказано при:
- 1) нарушении функции внутренних органов (почек, печени, легких, сердечно-сосудистой системы);
- 2) активной инфекции;
- 3) плохом общесоматическом статусе (индекс ВОЗ > I)
- 4) резистентном к химиотерапии рецидиве солидной опухоли или
- онкогематологического заболевания;
- 5) рефрактерности к трансфузиям тромбоцитов.
ВЫБОР ДОНОРА
Совместимость костного мозга определяет результаты АллоТКМ. Родственными донорами считаются совместимые по системе HLA братья или сестры реципиента (сибсы). Родители и дети гаплоидентичны (имеют одну общую хромосому из каждой пары, т. е. совпадают между собой на 50%) и не могут быть донорами аллогенного костного мозга. Совместимые сибсы имеются лишь у 20-25% больных, в связи с чем в последние 10 лет активно внедряется АллоТКМ от неродственных HLA-идентичных доноров или частично совместимых родственных доноров.
МОБИЛИЗАЦИЯ, ОБРАБОТКА И ИНФУЗИЯ СТВОЛОВЫХ КРОВЕТВОРНЫХ КЛЕТОК
Аспирация костного мозга производится под эндотрахеальным наркозом из задних гребней подвздошной кости, при необходимости — также из передних гребней и грудины. Для этого используют удлиненные иглы типа иглы Кассирского и шприцы объемом 20 см3, содержащие гепарин. Во избежание значительного разведения периферической кровью из каждого прокола кости аспирируют не более 5-6 мл костномозговой взвеси, которую фильтруют и помещают в специальные контейнеры. В каждом контейнере подсчитывают количество ядросодержащих клеток. Для восстановления кроветворения при АутоТКМ требуется получить не менее 1,5×106 ядросодержащих клеток на кг массы тела реципиента, при родственной АллоТКМ — не менее 2х106/кг (у больных апластической анемией — не менее 3х106/кг), при неродственной АлТКМ — не менее 3х106/кг. Объем аспирируемой костномозговой взвеси составляет около 1,5 л.
Для сохранения жизнеспособного костного мозга перед АутоТКМ (между аспирацией и инфузией клеток проходит от 2-3 недель до нескольких лет) после фракционирования его консервируют в жидком азоте под защитой криопротектора (чаще всего — диметилсульфоксида).
 А) |  Б) |
А) специальный сосуд (дюар) с жидким азотом для транспортировки контейнеров с костным мозгом
Б) извлеченный из сосуда контейнер с костным мозгом
Инфузия аллогенного, размороженного аутологичного костного мозга или СКК периферической крови проводится внутривенно, капельно после предварительного введения антигистаминных препаратов для предотвращения аллергических реакций.
ИММУНОСУПРЕССИВНАЯ ТЕРАПИЯ (КОНДИЦИОНИРОВАНИЕ)
Задача кондиционирования — обеспечить глубокую депрессию иммунной системы, а при онкологических заболеваниях и уничтожение оставшихся опухолевых клеток при умеренной токсичности для других органов и систем, а также создании условий для успешного приживления трансплантата.
Для проведения кондиционирования используются стандартные протоколы, в которых указываются дни, часы, дозы и длительность введения цитостатиков, симптоматических препаратов (антибактериальных, седативных, противорвотных и др., объем и характер инфузии), при необходимости — порядок проведения лучевой терапии. Протоколы кондиционирования различаются в зависимости от характера заболевания и типа трансплантации.
ПРОФИЛАКТИКА И ЛЕЧЕНИЕ ОСЛОЖНЕНИЙ ПЕРИОДА ЦИТОПЕНИИ
Вскоре после окончания кондиционирования и введения СКК у больного развивается аплазия костного мозга (период отсутствия костного мозгового кроветворения), которая проявляется практически полным отсутствием клеток крови (панцитопенией) и продолжается в среднем 4 недели. Этот период опасен развитием тяжелых осложнений (инфекции, кровоточивость и т.д.).
Основную опасность в периоде цитопении представляют инфекционные осложнения, поэтому их профилактика, своевременное и адекватное лечение являются необходимым условием успешной ТКМ.
Профилактика инфекционных осложнений начинается в среднем за 2 недели до трансплантации и включает:
- 1) помещение больного в стерильный бокс и проведение необходимых санитарно-гигиенических мероприятий (обработка кожи, слизистых оболочек и перианальной области дезинфицирующими растворами);
- 2) подавление микрофлоры кишечника с помощью антибактериальных и противогрибковых препаратов.
Также по показаниям проводится переливание компонентов крови (эритроцитарная масса, тромбомасса, плазма).
Приживление костного мозга или СКК периферической крови констатируют по результатам анализа костного мозга. Вскоре количество нейтрофилов достигает > 0,5*109/л, а тромбоцитов > 20>
Источник
Как пересаживают костный мозг?
Пересадка костного мозга – это последняя надежда для пациентов с раком крови. Это хирургически прсотая процедура, однако она требует длительной реабилитации в стерильных условиях. Если костный мозг пересадили успешно, человек побеждает рак и получает второй шанс на жизнь. Доверить такую ответственность можно только самым опытным врачам. Доктора из зарубежных клиник имеют большой опыт в подобных операциях. В среднем за рубежом проводят более 18,000 трансплантаций.
Что такое пересадка костного мозга?
Трансплантация костного мозга— это пересадка здоровых стволовых клеток для возобновления процесса кроветворения. Эти клетки называются гемопоэтическими – они являются предшественницами клеток крови.
Различают несколько видов пересадки гемопоэтических клеток. Самый простой – пересадка больному его же клеток (аутологичная пересадка). Если такой вид процедуры невозможен, назначают аллогенную пересадку – от ближайшего родственника или от донора с идентичным фенотипом, не являющегося родственником.
Костный мозг трансплантируют при лечении болезней крови: лимфомы, лейкозов (лейкемия), анемии, миеломы, диспластических синдромов, аплазии костного мозга.
Противопоказания
Для пациента. Костный мозг не пересаживают пациентам, которые страдают от серьезных заболеваний почек или печени в терминальной стадии. Категорически противопоказана процедура людям с инфекционными заболеваниями и беременным женщинам. Также пересадку не проводят в случаях, если пациент физически не способен выдержать такую процедуру.
Для донора. Не допускаются к донорству кандидаты с аутоиммунными, онкологическими и инфекционными болезням, а также расстройствами психики.
Выбор донора
Донировать свой костный мозг может любой человек, не имеющий медицинских противопоказаний, в возрасте 18-55 лет. Кандидаты сдают анализы крови для определения фенотипа, проходят общее обследование для занесения в базу. На территории Европы самой крупной базой является Европейский банк доноров, который содержит данные о более чем 4 миллионах потенциальных доноров из всего ЕС. Также существуют и локальные регистры, ограничивающиеся одной страной.
Поиск донора по европейской базе занимает до одного месяца, поиск в местных базах – 1-2 недели.
Все потенциальные кандидаты, которые находятся в базе донируют свой костный мозг исключительно бесплатно. Поэтому кандидат может отказаться от донорства в любой момент, не позднее 10 дней перед пересадкой.
Также потенциальный донор может болеть на момент своей необходимости или отсутствовать в стране. В связи с этим обычно пациенту подыскивается несколько доноров. Для родственной трансплантации используют материал брата/сестры больного при условии совместимости. Реже используется костный мозг одного из родителей. Однако совместимость в таком случае не превышает 50%.
Забор клеток
Процедура забора проводится под общим наркозом. Доктор делает разрез в области бедра, а затем получает материал с помощью шприца.Иногда кроветворные клетки получают из периферической крови. Для этого донору необходимо в течение нескольких дней принимать препараты, заставляющие гемопоэтические клетки костного мозга мигрировать в периферическую кровь. Донора на несколько часов подключают к специальному аппарату, который прогоняет кровь сквозь сепаратор. Таким образом отфильтровываются стволовые клетки.
Если используются аутологичные клетки, то после получения их замораживают до момента окончания химиотерапии.
Подготовка: химиотерапия и лучевая терапия перед пересадкой костного мозга
В случаях раковых заболеваний крови, протокол лечения включает высокодозные радио- и химиотерапию. Стандартные дозировки при лейкозах неэффективны. Такая терапия губит злокачественные клетки крови и костный мозг пациента, освобождая место новым клеткам, которые будут трансплантированы. Этот процесс называют кондиционированием.
В случае аутотрансплантации, у больного сперва делают забор гемопоэтических клеток. В лабораторных условиях из полученного материала отделяют пораженные и недееспособные клетки. После кондиционирования – костный мозг снова вводят для восстановления системы кроветворения.
Процедура ТКМ
Процесс пересадки костного мозга больному заключается во внутривенном переливании материала. Процедура не отличается от обычного переливания крови, не требует анестезии.
Восстановление после пересадки
Самый сложный этап — период приживления трансплантата. Обычно он длится от двух недель до месяца. Это критический период, после прохождения которого можно судить об успешности процедуры. Приживаемость пересаженного материала прежде всего зависит от степени совместимости донора с реципиентом. Пациенты тяжело переносят этот период, т.к. появляется множество побочных эффектов:
тошнота и рвота;
общая слабость и жар;
кровотечения;
расстройства ЖКТ
После пересадки высок риск отторжения трансплантата или такой реакции как “трансплантат против хозяина” — атаки пересаженных клеток на организм пациента. Чтобы исключить эти осложнения, пациенту назначают иммуносупрессоры — препараты, снижающие иммунитет больного, а также противоинфекционную терапию и антибиотики. Поскольку в этот период организм больного беззащитен перед инфекциями, его помещают в особые условия — стерильный бокс. Это палата, оснащенная специальным фильтром, который препятствует проникновению инфекции. Пациенту запрещено принимать подарки, еду и цветы от близких, т.к. это может нарушить стерильные условия его пребывания.
Такая изоляция серьезно воздействует на психику и без того ослабленного больного. Поэтому крайне важно не пренебрегать помощью профессиональных психологов, которые работают во всех онкогематологических центрах зарубежных клиник.
Восстановление детей
Ребенку переносить такие тяжелые последствия процедуры в условиях изоляции особенно сложно. Поэтому зарубежные клиники стараются воссоздать в детских центрах пересадки костного мозга максимально уютную домашнюю атмосферу. В детских палатах есть книги и игровые приставки.
Жизнь после трансплантации
В течение месяца после выписки из больницы следует придерживаться следующих рекомендаций:
придерживаться личной гигиены (мыть руки до и после еды/туалета/гигиенических процедур; пользоваться только личными предметами гигиены, ежедневно менять белье и одежду);
надевать маску при контакте с другими людьми;
не контактировать с больными людьми, с животными, не менять памперсы детям;
нельзя разводить растения в своей комнате, работать в саду;
следует ежедневно делать легкую зарядку;
запрещено курение и прием алкоголя;
необходимо избегать прямых солнечных лучей.
Дальнейшие рекомендации будут зависеть от состояния здоровья пациента по истечению месяца после выписки.
Риск рецидива
Показатель риска зависит от множества факторов — от первоначального диагноза, совместимости донора, соблюдения рекомендаций врача и общего состояния здоровья пациента. Риск возникновения рецидива тем ниже, чем больше времени прошло с момента пересадки. Больные, пережившие рубеж 5 лет, считаются полностью излечившимися.
Отзывы пациентов
Где проводилось: клиника Лив
Какая процедура: Пересадка костного мозга
Возраст пациента: 45 лет
Пациент из: Киева
Денис: “Для меня диагноз лейкемия был просто как гром среди ясного неба.. Я даже не думал, с таким диагнозом у меня вообще есть шансы. Благо, что моя семья паниковать не стала, родители по рекомендации обратились к ребятам из Mediglobus. Уже через месяц я летел в Стамбул, особо не надеясь ни на что хорошее… Турецкие доктора так спокойно отнеслись к моему диагнозу — я даже не сразу понял в чем дело.. Оказывается, статистика в клинике такова, что более 90% таких же пациентов, как и я — выздоравливают! Мне очень повезло, моим донором был мой брат. Многие ищут доноров среди чужих людей, а мне не пришлось.. Вот уже несколько месяцев, как я вернулся домой. Уж не буду говорить сколько всего мне пришлось пережить за время лечения, главное — я жив! Спасибо за это моей семье и турецким докторам.”
Рак крови – опасное заболевание, которое быстро прогрессирует. Если вам требуется срочная пересадка костного мозга – пишите врачам-координаторам MediGlobus. Мы быстро запишем вас в клинику и отправим на лечение за рубеж.
Источник