Характер свечения пламени



Основы возникновения и развития пожара
ПОСОБИЕ ПО ВЫПОЛНЕНИЮ
Содержание
1. Общие сведения. 3
2. Определение характеристик горения. 4
2.1 Характер свечения пламени. 5
2.2 Теоретический и практический расход водуха на горение. 10
2.3 Объем и состав продуктов полного сгорания. 21
2.4 Низшая теплота горения. 30
2.5 Стехиометрическая концентрация в паровоздушной смеси. 32
2.6 Расчет температуры горения. 33
2.7 Максимальное давление взрыва. 35
Общие сведения
По данным справочной литературы выписываются основные сведения о веществе:
Название вещества, структурная формула, область применения. Агрегатное состояние. Внешний вид, цвет и запах. Плотность. Относительная плотность пара по воздуху. Температура плавления. Температура кипения. Коэффициент молекулярной диффузии пара. Растворимость в воде. Химические свойства. Воздействие на человека.
Определение характеристик горения
Характер свечения пламени
Характер свечения пламени при горении веществ зависит от процентного содержания элементов в веществе, главным образом, углерода, водорода, кислорода и азота.
Свечение пламени связано с наличием несгоревших раскаленных твердых частиц углерода С, а также трехатомных молекул.
Если в горючем веществе при термическом разложении углерод не образуется, то вещество горит бесцветным пламенем как, например, в случае горения водорода Н2.
При термическом разложении веществ с массовой долей углерода менее 50 % и содержащих в своем составе кислород (более 30 %) несгоревших частиц углерода образуется очень мало, и в момент образования они успевают окислиться до СО.
СН3ОН 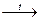
Такие вещества имеют голубоватые пламена (пламя угарного газа СО, метанола СН3ОН и этанола С2Н5ОН).
При горении веществ, содержащих более 75 % углерода (ацетилен С2Н2, бензол С6Н6), в зоне горения образуется настолько много частиц С, что поступающего путем диффузии воздуха не хватает для полного окисления всего углерода.
С6Н6 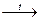
Не окислившийся в пламени углерод выделяется в виде копоти, и пламя при горении таких веществ будет ярким и коптящим.
Если кислород в веществе отсутствует или его содержание не превышает 30 %, но, в свою очередь, и массовая доля углерода не очень велика (менее 75 %), то при термическом разложении будет выделяться значительное количество частиц углерода, но при нормальном доступе воздуха в зону горения они успевают окислиться до СО2.
Возможная реакция при термическом разложении ацетона :
СН3СОСН3 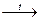
В подобных случаях пламя будет яркое, но не коптящее.
Сопоставляя значения процентного содержания углерода и кислорода в горючих веществах, можно приблизительно судить о характере свечения пламени (таблица 1.).
Таблица 1 Характер свечения пламени
| Содержание углерода в горючем веществе, w (С) % | Содержание кислорода в горючем веществе, w (О) % | Характер свечения пламени | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 30 | пламя бесцветное или голубоватое | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 75 | отсутствует или 2BaCl + Cl2 Монохлорид ВаСl излучает в зеленой линии спектра. Это свойство солей некоторых металлов используется при изготовлении самых разнообразных пиротехнических составов. Пример: Определить характер свечения пламени метаналя НСОН, фенола С6Н5ОН и пентанола С5Н11ОН. 1. Массовые доли углерода и кислорода в молекуле метаналя составляют: w (С) = Массовая доля углерода 30 %, следовательно, при горении метаналя наблюдается голубоватое пламя.
2. Массовые доли углерода и кислорода в молекуле фенола составляют: w (С) = Массовая доля углерода > 50 %, а массовая доля кислорода Источник Определение характера свечения пламениХарактер свечения пламени веществ при их горении зависит от процентного содержания углерода и кислорода в горючем веществе. При горении веществ в зоне горения происходит процесс их термического разложения. Наличие углерода в зоне горения будет придавать пламени яркость. О характере свечения пламени можно судить по процентному содержанию углерода и кислорода в горючем веществе (табл. 18).
Процентное содержание углерода рассчитывается по формуле, % где АrС – атомный вес углерода; МrГВ – молекулярная масса горючего вещества; nС – количество атомов углерода в формуле горючего вещества. Процентное содержание кислорода рассчитывается по формуле, % где АrО – атомный вес кислорода; МrГВ – молекулярная масса горючего вещества; nО – количество атомов кислорода в формуле горючего вещества. ПРИМЕР. Определить характер свечения пламени этилового спирта. Решение: 1. Рассчитываем содержание углерода в этиловом спирте (С2Н5ОН). Ответ: поскольку содержание кислорода в этиловом спирте превышает 30 %, пламя будет бесцветным. Источник 5.5. Характер свечения пламениХарактер свечения пламени при горении веществ зависит от процентного содержания элементов в веществе, главным образом, углерода, водорода, кислорода и азота. Свечение пламени связано с наличием несгоревших раскаленных твердых частиц углерода С, а также трехатомных молекул. Если в горючем веществе при термическом разложении углерод не образуется, то вещество горит бесцветным пламенем как, например, в случае горения водорода Н 2 . При термическом разложении веществ с массовой долей углерода менее 50 % и содержащих в своем составе кислород (более 30 %) несгоревших частиц углерода образуется очень мало, и в момент образования они успевают окислиться до СО. СН 3 ОН t → СО + 2Н 2 Такие вещества имеют голубоватые пламена (пламя угарного газа СО, метанола СН 3 ОН и этанола С 2 Н 5 ОН). При горении веществ, содержащих более 75 % углерода (ацетилен С 2 Н 2 , бензол С 6 Н 6 ), в зоне горения образуется настолько много частиц С, что поступающего путем диффузии воздуха не хватает для полного окисления всего углерода. С 6 Н 6 t → 6С + 3Н 2 Не окислившийся в пламени углерод выделяется в виде копоти, и пламя при горении таких веществ будет ярким и коптящим. Если кислород в веществе отсутствует или его содержание не превышает 30 %, но, в свою очередь, и массовая доля углерода не очень велика (менее 75 %), то при термическом разложении будет выделяться значительное количество частиц углерода, но при нормальном доступе воздуха в зону горения они успевают окислиться до СО 2 . Возможная реакция при термическом разложении ацетона : СН 3 СОСН 3 t → СО + 2С + 3Н 2 . В подобных случаях пламя будет яркое, но не коптящее. Сопоставляя значения процентного содержания углерода и кислорода в горючих веществах, можно приблизительно судить о характере свечения пламени (таблица 5.2). Источник ОПРЕДЕЛЕНИЕ ХАРАКТЕРА СВЕЧЕНИЯ ПЛАМЕНИХарактер свечения пламени веществ при их горении зависит от процентного содержания углерода и кислорода в горючем веществе. При горении веществ в зоне горения происходит процесс термического разложения их. Наличие углерода в зоне горения будет придавать пламени яркость. О характере свечения пламени приблизительно можно судить по процентному содержанию углерода и кислорода в горючем веществе (табл. 3).
Процентное содержание углерода (кислорода) рассчитывается по формуле: где АrС(О) – атомный вес углерода (кислорода); МrГВ – молекулярная масса горючего вещества; nС(О) – количество атомов углерода(кислорода) в формуле горючего вещества. ПРИМЕР: Определить характер свечения пламени этилового спирта. РЕШЕНИЕ: 1. Рассчитываем содержание углерода в этиловом спирте (С2Н5ОН). ОТВЕТ: поскольку содержание кислорода в этиловом спирте превышает 30 %,пламя будет бесцветным. ЗАДАЧИ ДЛЯ САМОСТОЯТЕЛЬНОГО РЕШЕНИЯ 1.Определить объём воздуха, необходимого для сгорания 50 м 3 ацетилена при α=1, 7. 2.Определить объёмы воздуха, продуктов горения и процент содержания продуктов горения 2 м 3 этана. Температуру продуктов горения принять 1200 К, давление 101, 3 кПа, избыток воздуха α=1, 2. 3.Определить объём воздуха, необходимого для сгорания 15 м 3 бутана при температуре 10С и давлении 750 мм рт. ст., если горение протекает с коэффициентом избытка воздуха, равным 1, 4 (α=1,4). 4.Рассчитать объём и состав (в %) продуктов горения при сгорании сероводорода объёмом 12 м 3 при температуре 30 о С и давлении 106 кПа. Коэффициент избытка воздуха составил 1, 1. 5.Рассчитать объём воздуха, объём продуктов горения и процентное содержание в них диоксида углерода при полном сгорании 5 м 3 этилена, если горение протекает с избытком воздуха (коэффициент избытка воздуха 1, 7). 6.Рассчитать количество амилбензола, которое может сгореть в закрытом помещении объёмом 200 м 3 , если горение прекратилось при остаточном содержании кислорода 12 %. Начальная температура в помещении 24 о С, давление 98 кПа. 7.Определить, какое количество бутилацетата может сгореть в помещении объёмом 200 м 3 , если его горение прекращается при содержании кислорода воздуха, равном 13, 8 % (условия нормальные). 8.Определить объёмы продуктов горения и воздуха при сжигании 7 кг гексана. Процесс горения протекал при температуре 33 о С и давлении 730 мм. рт. ст. Температура продуктов горения принять равной 1300 К. 9.Определить объёмы продуктов горения и воздуха при сжигании 11 кг ацетона. Процесс горения протекал при температуре 30 о С и давлении 720 мм рт. ст. Температуру продуктов горения принять равной 1300 К. 10.Определить объём продуктов горения и воздуха при сжигании 17 кг толуола. Процесс горения протекал при температуре 30 о С и давлении 745 мм рт. ст. Температуру продуктов горения принять равной 1100 К. 11.Рассчитать объём воздуха и объём продуктов горения при полном сгорании 6 кг целлюлозы, состоящей из 80 % углерода, 13 % водорода и 7 % кислорода, если горение протекает при температуре 25 о С и давлении 95 кПа. Коэффициент избытка воздуха равен 1, 4. 12.Определить объём воздуха, необходимого для сгорания 6 кг диэтилового эфира при температуре 15 о С и давлении 750 мм рт. ст. Коэффициент избытка воздуха составил 1, 3. 13.Определить, какое количество бензола сгорело в закрытом помещении объёмом 180 м 3 , если известно, что горение его прекратилось при содержании кислорода в воздухе, равном 14, 6 %. Температура до пожара была 19 о С и давление 100 кПа. 14.Рассчитать количество сгоревшего аллилового спирта и процентное содержание воды в продуктах горения, если на его сгорание при температуре 23 о С и давлении 99 кПа израсходовано 110 м 3 воздуха. 15.Определить коэффициент избытка воздуха, если для сгорания 8 кг этилацетата израсходовано 212 м 3 воздуха при температуре 25 о С и давлении 760 мм рт. ст.
16.Рассчитать коэффициент избытка воздуха и процентное содержание в продуктах горения диоксида углерода, если на полное сгорание 4 кг этилпропилового эфира (С5Н12О) при температуре 22 о С и давлении 92 кПа израсходовано 70 м 3 воздуха. 17.Сгорает 3 кг акролеина при температуре 21 о С и давлении 98 кПа. Рассчитать объём воздуха, перешедшего в продукты горения, и процентное содержание в них воды, если горение протекает с избытком воздуха (коэффициент избытка воздуха равен 1, 2). 18.Рассчитать объём воздуха и продуктов горения, образующихся при сгорании 10 кг глицерина, если горение протекало при 25 о С и давлении 102 кПа. Коэффициент избытка воздуха составил 1, 3. 19.Рассчитать объём и состав (в %) продуктов горения, образующихся при сгорании 8 кг пропилацетата, если горение протекало при 20 о С и давлении 103 кПа. Коэффициент избытка воздуха составил 1,4. 20.Рассчитать объём газовой смеси, состоящей из 45 % бутана, 30 % метана, 20 % ацетилена и 5 % кислорода, если на её сгорание при нормальных условиях израсходовано 80 м 3 воздуха. Коэффициент избытка воздуха равен 1,6. 21.Рассчитать количество угля, состоящего из 70 % углерода, 20 % водорода и 10 % серы и объём образовавшихся при этом продуктов горения, если на сгорание угля при нормальных условиях израсходовано 100 м 3 воздуха. 22.Рассчитать объём воздуха и объём продуктов горения при полном сгорании 7 м 3 газовой смеси, состоящей из 57 % водорода, 18 % окиси углерода и 25 % метана, если горение протекает с избытком воздуха (коэффициент избытка воздуха равен 1,3). 23.Рассчитать объём воздуха и объём продуктов горения при полном сгорании 6 кг церезина, состоящего из 80 % углерода, 15 % водорода и 5 % кислорода, если горение протекает при температуре 25 о С и давлении 95 кПа. Коэффициент избытка воздуха равен 1, 5. 24.Рассчитать концентрацию пропанола, сгоревшего в закрытом помещении объёмом 150 м 3 , если горение прекратилось при остаточном содержании кислорода 9 %. Начальная температура в помещении 21 о С, давление 99 кПа. 25.Определить объём и состав продуктов горения (в об. %) смеси газов (табл. 4), если горение происходит при коэффициенте избытка воздуха α(см. табл. 4). 26. Рассчитать объём воздуха и продуктов горения при сгорании горючего вещества заданной массы при заданных условиях (см. табл. 5)
27. Определить характер свечения пламени этилбензола. 28. Определить характер свечения пламени уксусной кислоты. 29. Определить характер свечения пламени гексана. 30. Определить характер свечения пламени амилового спирта. 31. Определить характер свечения пламени бутана. 32. Определить характер свечения пламени бензола. Источник |


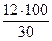 = 40 %; w (О) =
= 40 %; w (О) = 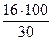 = 53 %
= 53 %
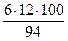 = 77 %; w (О) =
= 77 %; w (О) = 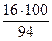 = 17 %
= 17 % , (26)
, (26)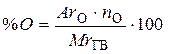 , (27)
, (27)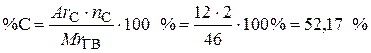 ;
; , следовательно пламя бесцветное.
, следовательно пламя бесцветное.
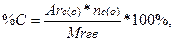
 , следовательно пламя бесцветное
, следовательно пламя бесцветное



