- Способы определения группы крови стандартными сыворотками
- Определение групп крови
- Определение групп крови по стандартным изогемагглютинирующим сывороткам
- Методика определения групп крови.
- Определение группы крови цоликлонами
- Методика проведения анализа
- Результаты реакции
- Определение группы крови
- Система группы крови AB0
- Групповая принадлежность по системе AB0
- Методика определения групп крови A2 и A2B
- Методика определения групп крови
- Алгоритм выявления группы крови гемагглютинирующими сыворотоками
- Техника определения группы крови цоликлонами
- Непрямой метод типирования: алгоритм действий
- Заключение о групповой принадлежности
- Система Резус
- Техника выявления резус-фактора с использованием цоликлона Анти-D-Супер
- Методика определения резус-фактора D u в пробирочном тесте
- Определение резус-принадлежности стандартным универсальным реагентом
Способы определения группы крови стандартными сыворотками
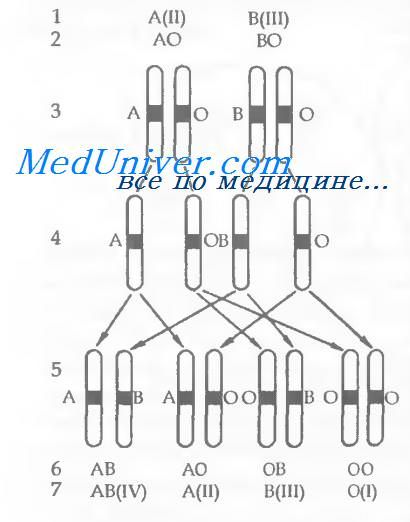
Группа крови (фенотип) наследуется по законам генетики и определяется набором генов (генотипом), получаемых с материнской и отцовской хромосомой. Человек может иметь только те антигены крови, которые имеются у его родителей. Наследование групп крови по системе АВО определяется тремя генами — А, В и О. В каждой хромосоме может быть только один ген, поэтому ребенок получает от родителей только два гена (один от матери, другой от отца), которые и вызывают появление в эритроцитах двух антигенов системы АВО. На рис. 2 представлена схема наследования групп крови по системе АВО.
Антигены крови появляются на 2—3-м месяце внутриутробной жизни и к рождению ребенка хорошо определяются. Естественные антитела выявляются с 3-го месяца после рождения и к 5—10 годам достигают максимального титра.
Определение групп крови
В настоящее время существует два метода определения группы крови.
Простой — определение антигенов крови по стандартным изогемагглютинирующим сывороткам и цоликлонам анти — А и анти — В. Цоликлоны, в отличие от стандартных сывороток, не являются продуктами клеток человека, поэтому исключена контаминация препаратов вирусами гепатита и ВИЧ (вирус иммунодефицита человека). Второй метод — перекрестный, заключающийся в определении агтлютиногенов одним из указанных способов с дополнительным определением агглютининов с помощью стандартных эритроцитов.
Определение групп крови по стандартным изогемагглютинирующим сывороткам
Для определения групп крови применяют стандартные изогемагглютинирующие сыворотки. В сыворотке имеются агглютинины, являющиеся антителами всех 4 групп крови, а их активность определяется титром.
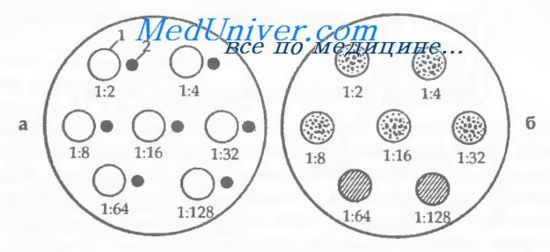
Техника получения сывороток и определения титра заключается в следующем. Для их заготовки используют донорскую кровь. После отстаивания крови, сливания и дефибриллирования плазмы необходимо определить титр (разведение), т. е. активность изогемагглютинирующих сывороток. С этой целью берется ряд центрифужных пробирок, в которых разводится сыворотка. Вначале в чистые пробирки добавляется по 1 мл физиологического раствора поваренной соли. В 1-ю пробирку с физиологическим раствором добавляют 1 мл испытуемой сыворотки, жидкости смешиваются, соотношение жидкостей в 1-й пробирке 1:1. Далее 1 мл смеси из 1-й пробирки переносится во 2-ю, все это смешивается, получается соотношение 1:2. Затем 1 мл жидкости из 2-й пробирки переносится в 3-ю пробирку, смешивается, получается соотношение 1:4. Таким образом разведение сыворотки продолжают до 1:256.
На следующем этапе производят определение титра разведенной сыворотки. Из каждой пробирки на плоскость наносят по 2 крупные капли. В каждую каплю добавляют заведомо иногруппные эритроциты (в соотношении 1 к 10), смешивают, ждут 3—5 минут. Далее определяют последнюю каплю, где произошла агглютинация. Это наибольшее разведение и является титром гемагтлютинирующей сыворотки. Титр не должен быть ниже чем 1:32. Хранение стандартных сывороток допускается в течение 3 месяцев при температуре от +4° до +6 °С с периодическим контролем через 3 недели.
Методика определения групп крови.
На тарелку или любую белую пластину со смачиваемой поверхностью необходимо нанести цифровое обозначение группы сыворотки и ее серологическую формулу в следующем порядке слева направо: I II, III. Это потребуется для определения исследуемой группы крови.
Стандартные сыворотки системы АВО каждой группы двух различных серий наносят на специальную планшетку или тарелку под соответствующими обозначениями, чтобы получилось два ряда по две большие капли (0,1 мл). Исследуемую кровь наносят по одной маленькой капле (0,01 мл) рядом с каждой каплей сыворотки и перемешивают кровь с сывороткой (соотношение сыворотки и крови 1 к 10). Реакция в каждой капле может быть положительной (наличие агглютинации эритроцитов) и отрицательной (отсутствие агглютинации). Результат оценивается в зависимости от реакции со стандартными сыворотками I, II, III. Оценивают результат через 3—5 минут. Различные сочетания положительных и отрицательных результатов дают возможность судить о групповой принадлежности исследуемой крови по двум сериям стандартных сывороток.
Источник
Определение группы крови цоликлонами
Методика проведения анализа
Алгоритм определения группы крови AB0 и резус-фактора цоликлонами облегчает и стандартизирует процедуру типирования. Позволяет однозначно интерпретировать результат реакции антиген/антитело. Для каждого исследования по системе AB0 достаточно одной серии реагентов. Объект исследования – цельная кровь, эритроцитарная масса, отмытые эритроциты, клетки крови в сыворотке или физрастворе.
В качестве примера приводим схему проведения типирования крови человека по системе антигенов AB0.
- Обеспечьте яркое освещение помещения и температуру воздуха 15 – 25 °C.
- Промаркируйте лунки планшета: Анти-A, Анти-B, Анти-AB.
- Добавьте в подписанные лунки по одной капле (приблизительно 0,1 мл) реагентов Анти-A, Анти-B, Анти-AB.
- Поместите по одной маленькой капле концентрированной эритроцитосодержащей среды (0,01 – 0,03 мл) рядом с большой каплей каждого реагента.
- В каждой из трех лунок отдельной стерильной стеклянной палочкой смешайте моноклональный реагент с кровью.
- Плавно покачивайте планшет 2,5 – 3 минуты. Обычно агглютинация формируется в течение 5 – 10 секунд. Запас времени необходим для обнаружения слабых вариантов антигенов.
- Проведите визуальную оценку результатов реакции в каждой лунке. Результат реакции свидетельствует об обнаружении соответствующего агглютиногена.
Результаты реакции
Таблица результатов типирования крови с помощью цоликлонов.
| Групповая принадлежность | Моноклональный реагент | ||
|---|---|---|---|
| Анти-A | Анти-B | Анти-AB | |
| 0(I) | — | — | — |
| A(II) | + | — | + |
| B(III) | — | + | + |
| AB(IV) | + | + | + |
«+» — положительный результат реакции;
«-» — отсутствие агглютинации.
- Отрицательный результат реакции во всех трех лунках свидетельствует об отсутствии агглютиногенов. Группа: 0(I).
- Агглютинация с Анти-A и Анти-AB говорит о наличии агглютиногена A. Групповая принадлежность: A(II).
- Реакция в лунках с Анти-B и Анти-AB указывает на наличие антигена B. Групповая принадлежность: B(III).
- Реакция во всех трех лунках говорит о присутствии обоих антигенов. Группа: AB(IV).
Методика проведения исследования с помощью цоликлонов требует обязательного подтверждения результатов реакции выявлением агглютининов α и β стандартными эритроцитами.
Алгоритм определения резус-фактора представлен в соответствующей статье.
Источник
Определение группы крови
В 1901 году выдающийся ученый Карл Ландштейнер открыл группы крови и заложил основы современной трансфузиологии. Исследователь выявил три группы на основании различных вариантов реакции агглютинации эритроцитов и сывороток крови. Материал для исследования был взят у сотрудников собственной лаборатории. Ученики Ландштейнера Декастелло и Стюрли несколькими годами позже открыли четвертую группу, но посчитали ее сомнительной и исключили из результатов исследований. В 1906 году психиатр из Праги Ян Янский подтвердил существование группы AB (IV). Публикация исследования в местном издании оказалась практически незамеченной. В 1910 году после повторного обнаружения четвертой группы Моссом Ян Янский был вынужден доказывать первенство открытия. Чешский ученый предложил цифровое обозначение групп крови: I, II, III, IV.
В трансфузиологии группами крови называют различные сочетания антигенов эритроцитов. Антигены являются генетическими признаками: наследуются от родителей и остаются неизменными на протяжении жизни. В 1980 году Международное сообщество переливания крови разработало числовую терминологию для антигенов эритроцитов. Выделены 23 системы группы крови, включающие 194 антигена. Нумерация в большинстве случаев соответствует порядку обнаружения. Входящие в каждую из 23 систем антигены кодируются шестизначным номером: первые три цифры являются номером системы, оставшиеся три – указывают на специфичность антигена внутри системы.
| № системы | Наименование | Обозначение | Наименование генов | Хромосомная локализация |
|---|---|---|---|---|
| 001 | AB0 | AB0 | AB0 | 9q34.1—q34.2 |
| 002 | MNS | MNS | GYPA, GYPB, GYPE | 4q28—q31 |
| 003 | P | P1 | P1 | 22q11.2—qter |
| 004 | Rh | RH | RHD, RHCE | 1p36.2—p34 |
| 005 | Lutheran | LU | LU | 19q12—q13 |
| 006 | Kell | KEL | KEL | 7q33 |
| 007 | Lewis | LE | FUT3 | 19p33 |
| 008 | Duffy | FY | FY | 1q22—q23 |
| 009 | Kidd | JK | JK | 18q11—q12 |
| 010 | Diego | DI | AE1 | 17q12—q21 |
| 011 | Yt | YT | ACHE | 7q22 |
| 012 | Xg | XG | XG | Xp22.32 |
| 013 | Scianna | SC | SC | 1p36.2—p22 |
| 014 | Dombrock | DO | DO | неизвестна |
| 015 | Colton | CO | AQP1 | 7p14 |
| 016 | Landsteiner-Wiener | LW | LW | 19p13.2—cen |
| 017 | Chido/Rogers | CH/RG | C4A, C4B | 6p21.3 |
| 018 | Hh | H | FUT1 | 19q13 |
| 019 | Kx | XK | XK | Xp21.1 |
| 020 | Gerbich | GE | GYPC | 2q14—q21 |
| 021 | Cromer | CROM | DAF | 1q32 |
| 022 | Knops | KN | CR1 | 1q32 |
| 023 | Indian | IN | CD44 | 11p13 |
Система группы крови AB0
Групповая принадлежность по системе AB0
| Агглютиногены | Агглютинины |
|---|---|
| 0 | α и β |
| A | β |
| B | α |
| AB | нет |
- 0(I): антигены A и B отсутствуют, антитела α и β – обнаружены (35 — 40 % населения в мире);
- A(II): присутствует антиген A и антитела β (35 %);
- B(III): обнаружен агглютиноген B и агглютинин α (15 – 20 %);
- AB(IV): наличие агглютиногенов A и B, отсутствие агглютининов α и β (5 – 10 %).
По мере движения с запада на восток Евразии частота обнаружения антигена A падает, а антигена B возрастает. Антиген 0 редко встречается в Азии, но имеет широкое распространение у коренных народов Южной Америки, Полинезии и Австралии. Причина – эпидемии инфекционных заболеваний.
Результат типирования крови записывают в историю болезни или в карту донора. Врач-трансфузиолог указывает дату и ставит подпись.
В отдельных случаях во время типирования наблюдается слабовыраженная агглютинация эритроцитов. Недостаточно выраженная реакция объясняется наличием слабых вариантов антигенов A и B. Наибольшее клиническое значение представляют подгруппы A1 и A2. Впервые слабые варианты были обнаружены в 1911 году учеными Dungern и Hirszeld. Позднее в 1930 году Landsteiner и Levine предложили названия подгруппы – A1 и A2. A2 встречается до 20 % в группе A и до 35 % в группе AB. Сыворотка лиц из образцов крови A2 может содержать анти-A1-антитела: в 2 % случаев в группе A2 и в 30 % в A2B. Антитела анти-A1 представляют опасность ввиду агглютинации эритроцитов группы A.
Методика определения групп крови A2 и A2B
Частота выявления эритроцитов A2 существенно варьируется в зависимости от применяемых реагентов. Приводим сравнение результатов исследования при использовании различных методик типирования групп крови A2 и A2B.
- Анти-A1 (лектин, фитогемагглютинин). Диагностикум явно выраженно (на +++/++++) агглютинирует A1 эритроциты сразу после смешения с образцом. Не агглютинирует A2 или вызывает мелкую агглютинацию на пятой минуте и позднее.
- Стандартные изогемагглютинирующие сыворотки.
- Цоликлоны анти-A и анти-AB.
- Цоликлон анти-A слабый.
| Число проанализированных образцов | Группа крови A (II) | Группа крови AB (IV) | ||
|---|---|---|---|---|
| Число проанализированных образцов | Группа A2 (II) в % | Число проанализированных образцов | Группа A2B (IV) в % | |
| Анти-A1 (лектин, фитогемагглютинин) | 1592 | 14,7 | 357 | 23,5 |
| Цоликлоны: анти-A, анти-AB | 3599 | 2,1* | 357 | 7,03* |
| Цоликлон анти-А — слабый | 3587 | 4,5* | 357 | 11,2* |
| Стандартные изогемагглютинирующие сыворотки | 1592 | 17,4 | 344 | 34,2 |
Примечание: * — агглютинация выражена слабо, присутствуют мелкие агглютинаты на розовом фоне.
Наибольшую точность исследования обеспечивает Анти-A1 (лектин, фитогемагглютинин). Тест рекомендован для выявления подгрупп антигена A у детей младше двух лет. Причина – физиологическая незрелость эритроцитов новорожденных, влекущая ошибочные результаты исследования со стандартными изогемагглютинирующими сыворотками.
В 1930 году Landsteiner и Levine обнаружили подтип Aint: промежуточный вариант между A1 и A2. Данный антиген характерен для негроидов и достигает 8,5 % у лиц с группой крови A. У европеоидов Aint наблюдался лишь у 1 % людей со второй группой крови. В крайне редких случаях у человека отсутствуют все антигены системы AB0. Фенотип «Бомбей» обусловлен генотипом hh. При отсутствии антигена H у лиц данной категории обнаруживаются анти-A и анти-B антитела.
Методика определения групп крови
Алгоритм выявления группы крови гемагглютинирующими сыворотоками
Для определения группы крови AB0 прямым методом используют две серии стандартных изогемагглютинирующих сывороток. Подготовьте две серии сывороток трех групп с титром 1:32 или выше. Для забора каждой сыворотки используйте отдельную маркированную пипетку. Подготовьте сыворотку AB(IV) для контроля.
- Обеспечьте хорошее освещение и температуру воздуха 18 – 25 °C.
- Промаркируйте планшет: 0(I) – слева, A(II) – по центру, B(III) – справа. Вверху по центру укажите фамилию донора или номер анализируемой крови.
- Нанесите в лунки 1 – 2 капли (приблизительно 0,1 мл) сывороток в два ряда в соответствии с маркировкой планшета.
- Пипеткой или стеклянной палочкой поместите по одной маленькой капле исследуемых эритроцитов рядом с каплями сыворотки. Объем сыворотки должен примерно в 10 раз превышать объем эритроцитосодержащей жидкости.
- Перемешайте капли в лунках палочкой.
- Для ускорения реакции произведите легкое покачивание планшета.
- Спустя три минуты в лунки планшета, в которых началась агглютинация, добавьте по одной капле NaCl. Подождите еще две минуты.
- Спустя пять минут оцените результаты реакции в проходящем сете. В случае невыраженной агглютинации добавьте еще по одной капле NaCl.
- Отрицательная реакция в трех лунках свидетельствует об отсутствии антигенов на эритроцитах исследуемого образца. Кровь относится к группе 0(I).
- Агглютинация в лунках с сыворотками 0(I) и B(III) говорит о наличии агглютиногена A и принадлежности к группе A(II).
- Наступление реакции с сыворотками 0(I) и A(II) свидетельствует о присутствии антигена B и групповой принадлежности B(III).
- Результаты реакции во всех лунках указывают на присутствие агглютиногенов A и B и соответствуют четвертой группе AB(IV).
В последнем случае следует удостовериться в отсутствии неспецифической реакции: нанесите на планшет 2 – 3 капли соответствующей группе AB(IV) сыворотки и добавьте одну каплю анализируемых эритроцитов. Перемешайте жидкости и оцените результат спустя пять минут. Отсутствие агглютинации свидетельствует о принадлежности к группе AB(IV), наличие – признак неспецифической реакции. В этом случае, а также при слабовыраженной агглютинации повторите исследование с другими сериями сывороток.
Техника определения группы крови цоликлонами
Моноклональные антитела к антигенам эритроцитов пришли на смену изогемагглютинирующих сывороток. Для каждого типирования достаточно одной серии реагентов анти-A, анти-B, анти-AB. Внедрение моноклональных реагентов позволило значительно упростить и стандартизировать методику типирования по системе AB0. Приводим краткое пошаговое руководство проведения исследования на планшете.
- Обеспечьте хорошее освещение. Работайте при комнатной температуре воздуха.
- Объект исследования – эритроцитосодержащие среды.
- Промаркируйте лунки планшета: анти-A, анти-B, анти-AB или используйте планшет с маркированной наклейкой.
- Нанесите примерно по 0,1 мл соответствующего моноклонального реагента в каждую из трех подписанных лунок.
- Добавьте приблизительно по 0,03 мл анализируемых эритроцитов рядом с каждой каплей диагностикума.
- Смешайте реагент с эритроцитами в лунках отдельными индивидуальными стеклянными палочками.
- Покачивайте планшет около трех минут.
- Проверьте наличие агглютинации в лунках.
Обычно реакция обнаруживается уже в первые секунды после смешивания. При этом слабые варианты антигенов A и B могут давать более позднюю агглютинацию.
Непрямой метод типирования: алгоритм действий
Методика определения основана на взаимодействии эритроцитов от предварительно типированных лиц групп 0, A, B или смеси эритроцитов от нескольких одногруппных доноров с изогемагглютининами α и β в исследуемой сыворотке.
При работе с каждым типирующим реагентом используйте сухие чистые пипетки. Промывание палочек для перемешивания и пипеток осуществляйте в 0,9 % растворе NaCl.
- Подготовьте пластину или планшет. Обеспечьте хорошее освещение помещения.
- Выполните забор 3 – 5 мл крови без стабилизатора в пробирку. Дайте сыворотке отстояться 1,5 – 2 часа при комнатной температуре.
- Отмойте тест-эритроциты в 0,9 % физиологическом растворе. Подготовьте 5 % взвесь.
- Промаркируйте секции на планшете: 0(I), A(II), B(III).
- Поместите по 2 капли (приблизительно 0,1 мл) анализируемой плазмы в каждую из трех лунок.
- Добавьте в лунки примерно по 0,03 мл тест-эритроцитов.
- Отдельными палочками смешайте типированные эритроциты с сывороткой.
- Аккуратно покачивайте планшет в течение 5 минут.
- Проведите визуальную оценку результатов реакции агглютинации в проходящем свете.
Заключение о групповой принадлежности
| Результаты анализа плазмы со стандартными эритроцитами | Групповая принадлежность | ||
|---|---|---|---|
| 0(I) | A(II) | B(III) | |
| — | + | + | 0(I) |
| — | — | + | A(II) |
| — | + | — | B(III) |
| — | — | — | AB(IV) |
+ — наличие агглютинации, — — отрицательный результат реакции.
- 0(I): реакция в лунках A(II), B(III) (обнаружены антитела α и β).
- A(II): агглютинация с эритроцитами B(III) (выявлены агглютинины β).
- B(III): агглютинация в лунке A(II) (определены агглютинины α).
- AB(IV): отсутствие результатов реакции во всех лунках (антитела в плазме не обнаружены).
Система Резус
Levine и Stetson обнаружили антигены системы Резус в 1939 году. Ученые изучали причины развития гемолитических реакций у рожениц при трансфузиях женщинам идентичных по системам AB0, MN и P. эритроцитов мужей. Годом позже Landsteiner и Wiener продуцировали выработку антител посредством иммунизации кроликов эритроцитами обезьян макака-резус. Антитела получили название анти-RH антитела. Полученные агглютинины вступали в реакцию агглютинации с эритроцитами макак-резус и с эритроцитами 85 % граждан Нью-Йорка белой расы. Вызвавший образование антител антиген получил название RH-фактор (D-фактор).
В редких случаях эритроциты людей не содержат ни одного антигена резус. Фенотип обозначают Rhnull. Ген Xro в этом случае представлен в гомозиготной форме и подавляет продуцирование всех антигенов. Обладатели фенотипа Rhnull не проявляют агглютиногеной активности, но имеют возможность передавать антигены по наследству.
Среди европейцев частота резус-положительных по антигену D лиц составляет 85 %. На мембране красных кровяных телец обычно расположено около 10 000 – 30 000 молекул D. При этом существуют два особых типа D-положительных лиц: D u (слабый) и D partial (частичный). Иммунная система D u и D partial способна вырабатывать анти-D-антитела.
Слабый антиген встречается у 1,5 % резус-положительных лиц и характеризуется низким числом (100 – 500) молекул D на мембране. Является иммуногенным для резус-отрицательных лиц. При этом переливание D-положительных эритроцитов больным со слабым D может вызвать сенсибилизацию кровяных телец донора. Эритроциты с D u слабо агглютинируются или совсем не вступают в прямую реакцию агглютинации с полными анти-резус антителами. Определение резус-принадлежности производят в непрямом антиглобулиновом тесте. Носителей D u считают резус-положительными донорами и резус-отрицательными реципиентами.
Частичный D имеет дефицит одного или нескольких эпитопов белковой молекулы. Иммунная система людей с D partial способна продуцировать антитела к недостающим эпитопам. Среди носителей частичного антигена выделяют семь групп лиц. Наибольшее клиническое значение имеет носительство D VI (присутствует только эпитоп Z): обладатели данной категории продуцируют антитела к неизмененному антигену и к частичным антигенам D I – D V , D VII . Техника выявления резус-фактора D VI заключается в последовательном применении двух диагностикумов: моноклональных IgM анти-D-антител (цоликлона Анти-D-Супер или Анти-D IgM) и поликлональных или моноклональных IgG антител анти-D (стандартного универсального реагента или цоликлона Анти-D). Отрицательный результат реакции на первом и положительный результат на втором этапе исследования свидетельствует об обнаружении D VI . Обычно категории D VI соответствует генотип CcDee. Беременным женщинам с D VI при вынашивании плода с полным D назначают антирезусный иммуноглобулин.
Антитела против антигенов резус являются иммунными. Возникают вследствие изосенсибилизации. Специфичность определяется спровоцировавшими образование антител антигенами. Выделяют полные и неполные антитела.
Полные являются IgM антителами. Отличаются большим молекулярным весом, обнаруживаются реже по сравнению с неполными антителами. Способны агглютинировать резус-положительные эритроциты. Имеют меньшее значение при трансфузиях.
Неполные преимущественно относятся к классу IgG. Закрепляются на поверхности резус-положительных эритроцитов без образования агглютинатов. Склеивание кровяных телец осуществляется при наличии коллоидных растворов и протеолитических ферментов или после обработки антиглобулиновой сывороткой. Обладают меньшим в сравнении с полными антителами молекулярным весом. Способны проходить через плаценту. Во время сенсибилизации сперва продуцируются полные антитела, далее в большей мере вырабатываются неполные (иммуноглобулины IgG) антитела.
Техника выявления резус-фактора с использованием цоликлона Анти-D-Супер
Цоликлон Анти-D-Супер — это полные анти-D IgM антитела человека. Для получения достоверных результатов анализируемый образец должен содержать достаточное количество эритроцитов.
- Обеспечьте хорошее освещение и комнатную температуру воздуха в помещении.
- Поместите одну большую каплю (приблизительно 0,1 мл) Анти-D IgM на пластину.
- Рядом расположите одну маленькую каплю (примерно 0,03 мл) исследуемых эритроцитов.
- Перемешайте две капли стерильной палочкой.
- Спустя 10 – 15 секунд плавно покачивайте пластинку на протяжении 20 – 30 секунд.
- Проверьте наличие агглютинации спустя три минуты после перемешивания.
В случае наступления реакции кровь оценивается как резус-положительная (Rh+), при отсутствии реакции – как резус-отрицательная (Rh-). При отрицательной либо слабо выраженной агглютинации необходимо повторно провести исследование с неполными анти-D IgG антителами с целью выявления слабого или частичного антигена D.
Методика определения резус-фактора D u в пробирочном тесте
Параллельно с анализом выполняют постановку трех контрольных проб: реагента цоликлон Анти-D (анти-D IgG) со стандартными резус-положительными и резус-отрицательными эритроцитами, анализируемых эритроцитов с раствором желатина без диагностикума анти-D IgG.
- Поместите в пробирку 0,05 – 0,1 мл (одну каплю) эритроцитов из сгустка свернувшейся крови или отмытых от консерванта.
- Добавьте 0,1 мл (две капли) подогретого до разжижения при 45 – 50 °C 10 % желатина.
- Добавьте одну каплю цоликлона Анти-D (анти-D IgG).
- Выполните перемешивание.
- Инкубируйте пробирку на водяной бане 10 – 15 минут или в термостате при 48 °C на протяжении получаса.
- Добавьте 5 – 6 мл изотонического раствора.
- Переверните пробирку 1 – 2 раза.
- Оцените наличие агглютинации в проходящем свете.
Отсутствие результатов реакции с анти-D IgM и выраженная агглютинация с анти-D IgG свидетельствуют об обнаружении слабых форм антигена D. При слабо выраженной агглютинации следует повторить исследование в непрямой пробе Кумбса.
Определение резус-принадлежности стандартным универсальным реагентом
Стандартный реагент антирезус Rh0D содержит поликлональные неполные анти-D-антитела. Параллельно с анализом образца осуществляется контрольное исследование реагента Rh0D со стандартными резус-положительными (одногруппными или группы 0) и резус-отрицательными (одногруппными) эритроцитами.
- Поместите на дно пробирки одну каплю диагностикума Rh0D.
- Добавьте одну каплю анализируемых эритроцитов.
- Несколько раз встряхните пробирку.
- Наклоните пробирку практически до горизонтального положения и медленно поворачивайте не менее 3 минут. Растекание содержимого по стенкам обеспечит более выраженный результат реакции. Обычно агглютинация наступает в первые 60 секунд. Запас времени необходим для выявления слабого антигена D u .
- Добавьте 2 – 3 мл изотонического раствора NaCl и 2 – 3 раза переверните пробирку без взбалтывания.
- Визуально оцените наличие агглютинации. Явно выраженные хлопья на фоне прозрачного раствора свидетельствуют о наличии антигена D. Равномерно окрашенная жидкость говорит об отсутствии антигена.
Результат считается достоверным только после проверки контрольных образцов: наступлении реакции со стандартными резус-положительными и отсутствии реакции – с резус-отрицательными эритроцитами.
Информацию о пошаговой постановке непрямого теста Кумбса с использованием неполных анти-D-антител читайте в разделе сайта «Реакция Кумбса».
Источник


















