- Определение экспрессии гена PCA3. Ранняя диагностика рака предстательной железы
- Диагностика рака предстательной железы
- Причины повышения ПСА
- Результаты теста на ПСА
- РСА3 (Prostate cancer antigen 3)
- Выбор и оптимизация условий ОТ/ПЦР для высокоэффективного анализа уровня экспрессии мРНК гена C-MYC
- Определение экспрессии гена FLT3 (кровь) в Москве
- Приём и исследование биоматериала
- Когда нужно сдавать анализ Определение экспрессии гена FLT3 (кровь)?
- Подробное описание исследования
- Использованная литература
- Подготовка к исследованию
- Противопоказания и ограничения
- Интерпретация результата
- Эпигенетика: теоретические аспекты и практическое значение
- Структура генома человека
- Эпигенетические механизмы регуляции генов
Определение экспрессии гена PCA3.
Ранняя диагностика рака предстательной железы
Эффективный метод определения рака предстательной железы
Диагностика рака предстательной железы
- Пальцевое ректальное исследование (ПРИ)
- Трансректальное ультразвуковое исследование (ТРУЗИ)
- Компьютерная томография (КТ)
- Магнитно-резонансная томография (МРТ)
- Простатспецифический антиген (ПСА)
Причины повышения ПСА
Результаты теста на ПСА
Золотым стандартом диагностики РПЖ является мультифокальная биопсия. Однако число «излишних», отрицательных биопсий у пациентов с повышенным ПСА (4-10 нг/мл) достигает 70-80%, а РПЖ диагностируется только у каждого четвертого.
В связи с тем, что биопсия простаты является достаточно неприятной процедурой и может сопровождаться осложнениями, сокращение числа ненужных биопсий является важной задачей, стоящей перед урологами. Анализ РНК-продукта гена PCA3 является одним из перспективных методов диагностики РПЖ, позволяющим определить показания для биопсии простаты.
РСА3
(Prostate cancer antigen 3)
Новый диагностический маркер, независимый предиктор Рака предстательной железы
Источник
Выбор и оптимизация условий ОТ/ПЦР для высокоэффективного анализа уровня экспрессии мРНК гена C-MYC
Работа призёра открытой городской научно-практической конференции «Старт в медицину» в секции «Биохимия»
Актуальность
Разработка препаратов, направленных на ингибирование онкогенов семейства Myc, является важным направлением в противоопухолевой терапии. Для этого необходимо иметь высокоточные инструменты, позволяющие отследить уровень экспрессии генов этого семейства. Гиперэкспрессия гена C-MYC наблюдается в опухолях миеломы, лимфомы, карциномы и нейробластомы. В силу короткого времени жизни как мРНК, так и белка, довольно важным представляется высокоточное определение уровня экспрессии мРНК гена C-MYC.
Цель
Оптимизировать условия проведения ОТ/ПЦР для определения экспрессии гена C-MYC.
Задачи
1. Получить кДНК из РНК, выделенной из клеточной линии меланомы человека (Bro), с помощью реакции обратной транскрипции.
2. Провести ПЦР на полученной кДНК с праймерами на ген C-MYC при различном количестве циклов.
3. Провести анализ полученных ПЦР-продуктов методом электрофореза в агарозном геле.
4. Сфотографировать гель и провести цифровую обработку полученного изображения.
Оснащение и оборудование, использованное в работе
• Установка для электрофореза нуклеиновых кислот
• Система гель-документирования Syngene G:BOX
• Компьютер с программным обеспечением GeneTools 4.3.8
Описание
Автор провёл ОТ/ПЦР для гена C-MYC с целью определения уровня экспрессии его мРНК в разных условиях. Для этого был использован специальный лабораторный блок, а очищенные гуанидинизотиоционатным методом препараты тотальной клеточной РНК предоставлены Сеченовским Университетом.
Реакцию ПЦР проводили в смеси объёмом 50 мкл, содержащей 67 мМ Tris-HCl (рН 8,8), 16,6 мМ (NH4)2SO4, 0,01% (в/о) Tween 20, 1,5 мМ МgCl2, 0,2 мМ каждого dNTP, 15 пкмоль каждого из пары праймеров, 2,5 ед. рекомбинантной Taq ДНК-полимеразы, 5 мкл реакционной ОТ-смеси, содержащей кДНК.
Реакция образования первой цепи: комплементарная ДНК (cDNA) образуется на матрице мРНК из dNTP ферментом обратной транскриптазой. Компоненты реакции смешиваются с ДНК-праймером (комплементарным исследуемой мРНК) и буфером с обратной транскриптазой на один час при +37 °C.
Реакция образования второй цепи: после того как обратная транскрипция закончена и образована cDNA на матрице мРНК, следующие циклы производятся по стандартной методике ПЦР.
После проведения 25–35 циклов ПЦР образуются миллионы копий нужной последовательности.
Автор провёл электрофорез продуктов ОТ/ПЦР в 2%-м агарозном геле, содержащем 0,5 мкг/мл бромистого этидия. В качестве РНК-матрицы на стадии ОТ использовали 1 мкг тотальной клеточной РНК, полученной из клеточной линии Bro (меланома человека). Затем выполнили окрашивание, фотографирование и анализ изображения геля после электрофореза. Гели снимали на цифровую фотокамеру в системе гель-документирование, анализ изображения проводили на компьютере с помощью специализированного программного обеспечения GeneTools 4.3.8.
Уровни экспрессии исследуемых генов нормализовали по отношению к уровню экспрессии конститутивного гена (β-актина), который принимали за единицу.
Работа с РНК (добавление РНК в смесь ОТ/ПЦР) проводилась под ламинаром, в перчатках и в маске.
Результаты
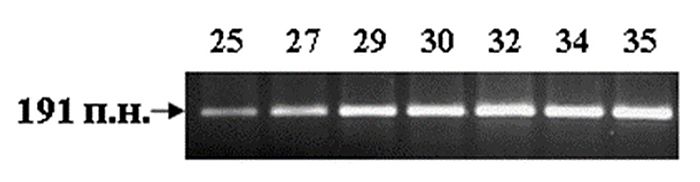
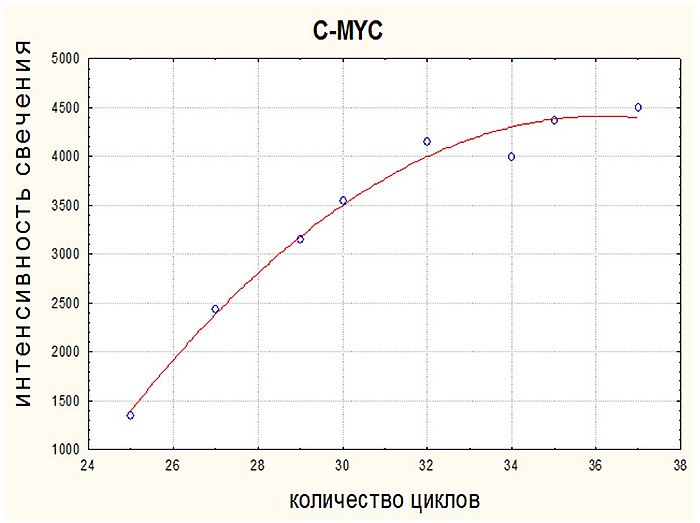
1. Интенсивность свечения окрашенного продукта реакции для гена C-MYC различная в зависимости от количества циклов реакции ОТ/ПЦР. Цифрами над дорожками указано количество циклов ПЦР, стрелкой – положение и размер специфического продукта ОТ/ПЦР.
2. Уровень экспрессии исследуемого гена C-MYC расценивали следующим образом:
— ниже 0,15 отн. ед. – очень низкий;
— от 0,15 до 0,29 отн. ед. – низкий;
— от 0,3 до 0,54 отн. ед. – средний;
— от 0,55 до 0,99 отн. ед. – высокий;
— выше 1 отн. ед. – очень высокий (гиперэкспрессия).
Выводы
1. Анализ экспрессии мРНК гена C-MYC можно проводить с помощью метода ОТ/ПЦР с высокой эффективностью, используя при этом 1 мкг тотальной клеточной РНК. Более того, кроме специфического продукта ОТ/ПЦР, указывающего на присутствие мРНК C-MYC в образце, отсутствуют неспецифические фрагменты ДНК, что говорит о высокой специфичности анализа.
2. Для гена C-MYC при проведении ОТ/ПЦР оптимальным при выбранных условиях будет 35 циклов, т. к. в этом случае накапливается наибольшее количество продуктов.
3. Анализ изображений на компьютере с помощью программы GeneTools v.4.3.8. позволил нормализовать уровень экспрессии гена C-MYC по отношению к уровню экспрессии конститутивного гена β-актина.
4. Для подтверждения полученных результатов разработанную тест-систему необходимо проверить на большем количестве образцов.
Перспективы использования результатов работы
Разработанную тест-систему можно использовать для оценки уровня экспрессии онкогенов семейства Myc.
Сотрудничество с вузом при создании работы
ФГАОУ ВО Первый МГМУ им. И. М. Сеченова Минздрава России (Сеченовский Университет)
Мнение автора
«Конференция «Старт в медицину» дала мне возможность познакомиться с научной медициной. Работа над проектом была сложная, но результаты этого стоили. Было интересно работать с такой важной и очень интересной темой»
Источник
Определение экспрессии гена FLT3 (кровь) в Москве
Исследование предназначено для определения прогноза и подбора оптимального лечения при остром миелоидном лейкозе. Исследование не следует использовать для оценки минимальной остаточной болезни после проведенной терапии.
Приём и исследование биоматериала
Когда нужно сдавать анализ Определение экспрессии гена FLT3 (кровь)?
Определение прогноза и подбор оптимальной терапии при остром миелоидном лейкозе.
Подробное описание исследования
Ген FLT3 относится к семейству рецепторных тирозинкиназ (RTK) третьего класса (III), которые преимущественно определяются в клетках-предшественниках гемопоэза (стволовые и плюрипотентные). Они являются наиболее ранними клетками, из которых впоследствии образуются все кровяные клетки — лейкоциты, эритроциты, тромбоциты.
Ген FLT3 кодирует одноименный белок FLT3, выступающего в качестве клеточного рецептора. Основной функцией этого рецептора является передача сигнала извне клетки к её ядру с использованием специальных молекул-посредников. При помощи этих сигналов белок-рецептор FLT3 регулирует рост, деление и развитие кроветворных клеток. При развитии мутации в гене FLT3 процесс клеточного деления становится автономным и перестает зависеть от сигналов рецептора FLT3. Это способствует неконтролируемому росту кроветворной клетки, которая впоследствии превращается в опухоль.
Известно, что наибольшее прикладное значение генетические мутации FLT3 имеют у пациентов с острым миелоидным лейкозом.
Острый миелоидный лейкоз (ОМЛ) – это злокачественное поражение миелоидного ростка кроветворения, которое проявляется в виде аномального и бесконтрольного размножения незрелых лейкоцитов. Заболевание преимущественно протекает у людей старше 60-65 лет. Основными факторами риска развития ОМЛ являются радиационное/ионизирующее излучение, курение, предшествующая химио- или лучевая терапия. Острый миелоидный лейкоз развивается в результате приобретенных генетических мутаций, которые не передаются по наследству (мутация в гене FLT3 не исключение).
Согласно классификации, ВОЗ пациенты с острым миелолейкозом и мутацией гена FLT3 не выделяются в отдельную подгруппу, однако выявление этой аномалии имеет важное клиническое значение — на основании уровня экспрессии мутировавшего гена FLT3 можно судить о прогнозе ОМЛ.
К часто встречающимся мутациям FLT3 относятся 2 вида — FLT3-ITD и FLT3-TKD. Первая мутация, также именуемая как внутренняя тандемная дупликация, встречается у 30% больных с ОМЛ. В определенных отделах гена (экзонах) происходит удвоение нескольких участков ДНК — нуклеотидов. Данная мутация ассоциирована с негативным прогнозом и высоким риском рецидива лейкоза. Мутация FLT3-TKD осуществляется иным способом, в виде точечной генетической аномалии с заменой аминокислоты аспаргина в особом участке гена FLT3 (835 положение в домене). Данная мутация встречается у порядка 10% пациентов с острым миелоидным лейкозом и не имеет однозначной прогностической роли.
Предполагается, что в присутствии мутаций генов NPM1 или CEBRA данная аномалия преимущественно связана с благоприятным прогнозом. При сочетании мутации FLT3-ITD с FLT3-TKD или MLL-PTD — прогноз неблагоприятный.
В лаборатории «Гемотест» анализ экспрессии гена FLT3 проводится при помощи современного метода молекулярной диагностики — ПЦР (полимеразной цепной реакции). Результат анализа представлен в виде количественного значения уровня экспрессии гена FLT3 в изучаемых клетках. Результат данного исследования помимо определения прогноза ОМЛ также позволяет определить группу пациентов с последующим назначением им химиотерапии. Следует учитывать, что данный анализ не рекомендуется использовать для мониторинга минимальной остаточной болезни после проведенного лечения.
Использованная литература
- Зайкова Е.К., Белоцерковская Екатерина Васильевна, Зайцев Д.В., Петухов А.В., Федорова О.А., Моторин Д.В., Иванов В.В., Зарицкий А.Ю., Гиршова Л.Л. Молекулярная диагностика мутаций гена flt3 у пациентов с острыми миелоидными лейкозами // Клиническая онкогематология. 2020. №2. 2.
- Раджабова А.М., Волошин С.В., Мартынкевич И.С., Кузяева Аа., Шуваев Ва., Мотыко Е.В., Кувшинов А.Ю., Фоминых М.С., Шмидт А.В., Полушкина Л.Б., Бакай М.П., Тиранова С.А., Потихонова На., Зенина М.Н., Кудряшова Са., Балашова Ва., Чубукина Ж.В., Успенская О.С., Карягина Е.В., Богданов А.Н., Чечеткин А.В. Роль мутаций гена flt3 при острых миелоидных лейкозах: влияние на течение заболевания и результаты терапии // Гены и клетки. 2019. 3.
- Национальные клинические рекомендации по острому миелоидному лейкозу, 2020 4. Patnaik MM. The importance of FLT3 mutational analysis in acute myeloid leukemia. Leuk Lymphoma. 2018 Oct;59(10):2273-2286. doi: 10.1080/10428194.2017.1399312. Epub 2017 Nov 22. PMID: 29164965. 5.
- Daver, N., Schlenk, R.F., Russell, N.H. et al. Targeting FLT3 mutations in AML: review of current knowledge and evidence. Leukemia 33, 299–312 (2019). https://doi.org/10.1038/s41375-018- 0357-9
Подготовка к исследованию
- Кровь рекомендуется сдавать утром натощак (между последним приемом пищи и взятием крови должно пройти не менее 8-ми часов, воду можно пить в обычном режиме), накануне исследования легкий ужин с ограничением приема жирной пищи.
- Накануне исследования (в течение 24 часов) исключить алкоголь, интенсивные физические нагрузки, прием лекарственных препаратов (по согласованию с врачом).
- За 1-2 часа до сдачи крови воздержаться от курения, не употреблять сок, чай, кофе, можно пить негазированную воду. Исключить физическое напряжение (бег, быстрый подъем по лестнице), эмоциональное возбуждение. За 15 минут до сдачи крови рекомендуется отдохнуть, успокоиться.
- Не следует сдавать кровь для лабораторного исследования сразу после физиотерапевтических процедур, инструментального обследования, рентгенологического и ультразвукового исследований, массажа и других медицинских процедур.
- При контроле лабораторных показателей в динамике рекомендуется проводить повторные исследования в одинаковых условиях – в одной лаборатории, сдавать кровь в одинаковое время суток и пр.
Противопоказания и ограничения
Абсолютных противопоказаний нет.
Интерпретация результата
Результат анализа не является диагнозом и должен быть интерпретирован только врачом.
Источник
Эпигенетика: теоретические аспекты и практическое значение
В данной статье освещаются современные представления о эпигенетике как новой науке, механизмах эпигенетической регуляции и ее нарушениях, приводящих к развитию заболеваний.
This article highlights the modern views on epigenetics as a new science, the mechanisms of epigenetic regulation and their disorders, leading to the development of diseases.
Эпигенетика — сравнительно недавнее направление биологической науки и пока не так широко известно, как генетика. Под ней понимают раздел генетики, который изучает наследуемые изменения активности генов во время развития организма или деления клеток.
Эпигенетические изменения не сопровождаются перестановкой последовательности нуклеотидов в дезоксирибонуклеиновой кислоте (ДНК).
В организме существуют различные регуляторные элементы в самом геноме, которые контролируют работу генов, в том числе в зависимости от внутренних и внешних факторов. Долгое время эпигенетику не признавали, т. к. было мало информации о природе эпигенетических сигналов и механизмах их реализации.
Структура генома человека
В 2002 г. в результате многолетних усилий большого числа ученых разных стран закончена расшифровка строения наследственного аппарата человека, который заключен в главной молекуле ДНК. Это одно из выдающихся достижений биологии начала ХХI века.
ДНК, в которой находится вся наследственная информация о данном организме, называется геномом. Гены — это отдельные участки, занимающие очень небольшую часть генома, но при этом составляют его основу. Каждый ген отвечает за передачу в организме человека данных о строении рибонуклеиновой кислоты (РНК) и белка. Структуры, которые передают наследственную информацию, называют кодирующими последовательностями. В результате проекта «Геном» были получены данные, согласно которым геном человека оценивался в более чем 30 000 генов. В настоящее время, в связи с появлением новых результатов масс-спектрометрии, геном предположительно насчитывает около 19 000 генов [1].
Генетическая информация каждого человека содержится в ядре клетки и расположена в особых структурах, получивших название хромосомы. Каждая соматическая клетка содержит два полных набора (диплоидный) хромосом. В каждом единичном наборе (гаплоидном) присутствует 23 хромосомы — 22 обычные (аутосомы) и по одной половой хромосоме — Х или Y.
Молекулы ДНК, содержащиеся во всех хромосомах каждой клетки человека, представляют собой две полимерные цепи, закрученные в правильную двойную спираль.
Обе цепи удерживают друг друга четырьмя основаниями: аденин (А), цитозин (Ц), гуанин (Г) и тиамин (Т). Причем основание А на одной цепочке может соединиться только с основанием Т на другой цепочке и аналогично основание Г может соединяться с основанием Ц. Это называется принципом спаривания оснований. При других вариантах спаривание нарушает всю целостность ДНК.
ДНК существует в виде тесного комплекса со специализированными белками, и вместе они составляют хроматин.
Гистоны — это нуклеопротеины, основная составляющая хроматина. Им свойственно образование новых веществ путем присоединения двух структурных элементов в комплекс (димер), что является особенностью для последующей эпигенетической модификации и регуляции.
ДНК, хранящая генетическую информацию, при каждом клеточном делении самовоспроизводится (удваивается), т. е. снимает с самой себя точные копии (репликация). Во время клеточного деления связи между двумя цепями двойной спирали ДНК разрушаются и нити спирали разделяются. Затем на каждой из них строится дочерняя цепь ДНК. В результате молекула ДНК удваивается, образуются дочерние клетки.
ДНК служит матрицей, на которой происходит синтез разных РНК (транскрипция). Этот процесс (репликация и транскрипция) осуществляется в ядрах клеток, а начинается он с области гена, называемой промотором, на котором связываются белковые комплексы, копирующие ДНК для формирования матричной РНК (мРНК).
В свою очередь последняя служит не только носителем ДНК-информации, но и переносчиком этой информации для синтеза белковых молекул на рибосомах (процесс трансляции).
В настоящее время известно, что зоны гена человека, кодирующие белки (экзоны), занимают лишь 1,5% генома [2]. Большая часть генома не имеет отношения к генам и инертна в плане передачи информации. Выявленные зоны гена, не кодирующие белки, называются интронами.
Первая копия мРНК, полученная с ДНК, содержит в себе весь набор экзонов и интронов. После этого специализированные белковые комплексы удаляют все последовательности интронов и соединяют друг с другом экзоны. Этот процесс редактирования называется сплайсингом.
Эпигенетика объясняет один из механизмов, с помощью которого клетка способна контролировать синтез производимого ею белка, определяя в первую очередь, сколько копий мРНК можно получить с ДНК.
Итак, геном — это не застывшая часть ДНК, а динамическая структура, хранилище информации, которую нельзя свести к одним генам.
Развитие и функционирование отдельных клеток и организма в целом не запрограммированы автоматически в одном геноме, но зависят от множества различных внутренних и внешних факторов. По мере накопления знаний выясняется, что в самом геноме существуют множественные регуляторные элементы, которые контролируют работу генов. Сейчас это находит подтверждение во множестве экспериментальных исследований на животных [3].
При делении во время митоза дочерние клетки могут наследовать от родительских не только прямую генетическую информацию в виде новой копии всех генов, но и определенный уровень их активности. Такой тип наследования генетической информации получил название эпигенетического наследования.
Эпигенетические механизмы регуляции генов
Предметом эпигенетики является изучение наследования активности генов, не связанной с изменением первичной структуры входящей в их состав ДНК. Эпигенетические изменения направлены на адаптацию организма к изменяющимся условиям его существования.
Впервые термин «эпигенетика» предложил английский генетик Waddington в 1942 г. Разница между генетическими и эпигенетическими механизмами наследования заключается в стабильности и воспроизводимости эффектов [4].
Генетические признаки фиксируются неограниченное число, пока в гене не возникает мутация. Эпигенетические модификации обычно отображаются в клетках в пределах жизни одного поколения организма. Когда данные изменения передаются следующим поколениям, то они могут воспроизводиться в 3–4 генерациях, а затем, если стимулирующий фактор пропадает, эти преобразования исчезают.
Молекулярная основа эпигенетики характеризуется модификацией генетического аппарата, т. е. активации и репрессии генов, не затрагивающих первичную последовательность нуклеотидов ДНК.
Эпигенетическая регуляция генов осуществляется на уровне траскрипции (время и характер транскрипции гена), при отборе зрелых мРНК для транспорта их в цитоплазму, при селекции мРНК в цитоплазме для трансляции на рибосомах, дестабилизации определенных типов мРНК в цитоплазме, избирательной активации, инактивации молекул белков после их синтеза.
Совокупность эпигенетических маркеров представляет собой эпигеном. Эпигенетические преобразования могут влиять на фенотип.
Эпигенетика играет важную роль в функционировании здоровых клеток, обеспечивая активацию и репрессию генов, в контроле транспозонов, т. е. участков ДНК, способных перемещаться внутри генома, а также в обмене генетического материала в хромосомах [5].
Эпигенетические механизмы участвуют в геномном импритинге (отпечаток) — процессе, при котором экспрессия определенных генов осуществляется в зависимости от того, от какого родителя поступили аллели. Импритинг реализуется через процесс метилирования ДНК в промоторах, в результате чего транскрипция гена блокируется.
Эпигенетические механизмы обеспечивают запуск процессов в хроматине через модификации гистонов и метилирование ДНК. За последние два десятилетия существенно изменились представления о механизмах регуляции транскрипции эукариот. Классическая модель предполагала, что уровень экспрессии определяется транскрипционными факторами, связывающимися с регуляторными областями гена, которые инициируют синтез матричной РНК. Гистонам и негистоновым белкам отводилась роль пассивной упаковочной структуры для обеспечения компактной укладки ДНК в ядре.
В последующих исследованиях была показана роль гистонов в регуляции трансляции. Был обнаружен так называемый гистоновый код, т. е. модификация гистонов, неодинаковая в разных районах генома. Видоизмененные гистоновые коды могут приводить к активизации и репрессии генов [6].
Модификациям подвергаются различные части структуры генома. К концевым остаткам могут присоединяться метильные, ацетильные, фосфатные группы и более крупные белковые молекулы.
Все модификации являются обратимыми и для каждой существуют ферменты, которые ее устанавливают или удаляют.
Метилирование ДНК
У млекопитающих метилирование ДНК (эпигенетический механизм) было изучено раньше других. Показано, что он коррелирует с репрессией генов. Экспериментальные данные показывают, что метилирование ДНК является защитным механизмом, подавляющим значительную часть генома чужеродной природы (вирусы и др.).
Метилирование ДНК в клетке контролирует все генетические процессы: репликацию, репарацию, рекомбинацию, транскрипцию, инактивацию Х-хромосомы. Метильные группы нарушают ДНК-белковое взаимодействие, препятствуя связыванию транскрипционных факторов. Метилирование ДНК влияет на структуру хроматина, блокирует транскрипционные репрессоры [7].
Действительно, повышение уровня метилирования ДНК коррелирует с относительным увеличением содержания некодирующей и повторяющейся ДНК в геномах высших эукариот. Экспериментальные данные показывают, что это происходит потому, что метилирование ДНК служит главным образом как защитный механизм, чтобы подавлять значительную часть генома чужеродного происхождения (реплицированные перемещающиеся элементы, вирусные последовательности, другие повторяющиеся последовательности).
Профиль метилирования — активирование или угнетение — меняется в зависимости от средовых факторов. Влияние метилирования ДНК на структуру хроматина имеет большое значение для развития и функционирования здорового организма, чтобы подавлять значительную часть генома чужеродного происхождения, т. е. реплицированные перемещающиеся элементы, вирусные и другие повторяющиеся последовательности.
Метилирование ДНК происходит путем обратимой химической реакции азотистого основания — цитозина, в результате чего метильная группа СН3 присоединяется к углероду с образованием метилцитозина. Этот процесс катализируется ферментами ДНК-метилтрансферазами. Для метилирования цитозина необходим гуанин, в результате образуется два нуклеотида, разделенные фосфатом (СрG).
Скопление неактивных последовательностей СрG называется островками СрG. Последние представлены в геноме неравномерно [8]. Большинство из них выявляются в промоторах генов. Метилирование ДНК происходит в промоторах генов, в транскрибируемых участках, а также в межгенных пространствах.
Гиперметилированные островки вызывают инактивацию гена, что нарушает взаимодействие регуляторных белков с промоторами.
Метилирование ДНК оказывает огромное влияние на экспрессию генов и, в конечном счете, на функцию клеток, тканей и организма в целом. Установлена прямая зависимость между высоким уровнем метилирования ДНК и количеством репрессированных генов.
Удаление метильных групп из ДНК в результате отсутствия метилазной активности (пассивное деметилирование) реализуется после репликации ДНК. При активном деметилировании участвует ферментативная система, превращающая 5-метилцитозин в цитозин независимо от репликации. Профиль метилирования меняется в зависимости от средовых факторов, в которых находится клетка.
Утрата способности поддерживать метилирование ДНК может приводить к иммунодефициту, злокачественным опухолям и другим заболеваниям [9].
Долгое время механизм и ферменты, вовлеченные в процесс активного деметилирования ДНК, оставались неизвестными.
Ацетилирование гистонов
Существует большое число посттрансляционных модификаций гистонов, которые формируют хроматин. В 1960-е годы Винсент Олфри идентифицировал ацетилирование и фосфорилирование гистонов из многих эукариот [8].
Ферменты ацетилирования и деацетилирования (ацетилтрансферазы) гистонов играют роль в ходе транскрипции. Эти ферменты катализируют ацетилирование локальных гистонов. Деацетилазы гистонов репрессируют транскрипцию.
Эффект ацетилирования это ослабление связи между ДНК и гистонами из-за изменения заряда, в результате чего хроматин становится доступным для факторов транскрипции.
Ацетилирование представляет собой присоединение химической ацетил-группы (аминокислоты лизин) на свободный участок гистона. Как и метилирование ДНК, ацетилирование лизина представляет собой эпигенетический механизм для изменения экспрессии генов, не влияющих на исходную последовательность генов. Шаблон, по которому происходят модификации ядерных белков, стали называть гистоновым кодом.
Гистоновые модификации принципиально отличаются от метилирования ДНК. Метилирование ДНК представляет собой очень стабильное эпигенетическое вмешательство, которое чаще закрепляется в большинстве случаев.
Подавляющее большинство гистоновых модификаций более вариативно. Они влияют на регуляцию экспрессии генов, поддержание структуры хроматина, дифференциацию клеток, канцерогенез, развитие генетических заболеваний, старение, репарацию ДНК, репликацию, трансляцию. Если гистоновые модификации идут на пользу клетки, то они могут продолжаться довольно долго [8].
Одним из механизмов взаимодействия между цитоплазмой и ядром является фосфорилирование и/или дефосфорилирование транскрипционных факторов. Гистоны были одними из первых белков, фосфорилирование которых было обнаружено. Это осуществляется с помощью протеинкиназ.
Под контролем фосфорилируемых транскрипционных факторов находятся гены, в том числе гены, регулирующие пролиферацию клеток. При подобных модификациях в молекулах хромосомных белков происходят структурные изменения, которые приводят к функциональным изменениям хроматина.
Помимо описанных выше посттрансляционных модификаций гистонов имеются более крупные белки, такие как убиквитин, SUMO и др., которые могут присоединяться с помощью ковалентной связи к боковым аминогруппам белка-мишени, оказывая воздействие на их активность.
Эпигенетические изменения могут передаваться по наследству (трансгенеративная эпигенетическая наследственность). Однако в отличие от генетической информации, эпигенетические изменения могут воспроизводиться в 3–4 поколениях, а при отсутствии фактора, стимулирующего эти изменения, исчезают. Передача эпигенетической информации происходит в процессе мейоза (деления ядра клетки с уменьшением числа хромосом вдвое) или митоза (деления клеток).
Модификации гистонов играют фундаментальную роль в нормальных процессах и при заболеваниях.
Регуляторные РНК
Молекулы РНК выполняют в клетке множество функций. Одной из них является регуляция экспрессии генов. За эту функцию отвечают регуляторные РНК, к которым относятся антисмысловые РНК (aRNA), микроРНК (miRNA) и малые интерферирующие РНК (siRNA)
Механизм действия разных регуляторных РНК схож и заключается в подавлении экспрессии генов, реализующейся путем комплементарного присоединения регуляторной РНК к мРНК, с образованием двухцепочечной молекулы (дцРНК). Само по себе образование дцРНК приводит к нарушению связывания мРНК с рибосомой или другими регуляторными факторами, подавляя трансляцию. Также после образования дуплекса возможно проявление феномена РНК-интерференции — фермент Dicer, обнаружив в клетке двухцепочечную РНК, «разрезает» ее на фрагменты. Одна из цепей такого фрагмента (siRNA) связывается комплексом белков RISC (RNA-induced silencing complex) [10].
В результате деятельности RISC одноцепочечный фрагмент РНК соединяется с комплементарной последовательностью молекулы мРНК и вызывает разрезание мРНК белком семейства Argonaute. Данные события приводят к подавлению экспрессии соответствующего гена.
Физиологические функции регуляторных РНК разнообразны — они выступают основными небелковыми регуляторами онтогенеза, дополняют «классическую» схему регуляции генов.
Геномный импритинг
Человек обладает двумя копиями каждого гена, один из которых унаследован от матери, другой от отца. Обе копии каждого гена имеют возможность быть активной в любой клетке. Геномный импритинг это эпигенетически избирательная экспрессия только одного из аллельных генов, наследуемых от родителей. Геномный импритинг затрагивает и мужское и женское потомство. Так, импритингованный ген, активный на материнской хромосоме, будет активным на материнской хромосоме и «молчащим» на отцовской у всех детей мужского и женского пола. Гены, подверженные геномному импритингу, в основном кодируют факторы, регулирующие эмбриональный и неонатальный рост [11].
Импритинг представляет сложную систему, которая может ломаться. Импритинг наблюдается у многих больных с хромосомными делециями (утраты части хромосом). Известны заболевания, которые у человека возникают в связи с нарушением функционирования механизма импритинга.
Прионы
В последние десятилетие внимание привлечено к прионам, белкам, которые могут вызывать наследуемые фенотипические изменения, не изменяя нуклеотидной последовательности ДНК. У млекопитающих прионный белок расположен на поверхности клеток. При определенных условиях нормальная форма прионов может изменяться, что модулирует активность этого белка.
Викнер выразил уверенность в том, что этот класс белков является одним из многих, которые составляют новую группу эпигенетических механизмов, требующих дальнейшего изучения. Он может находиться в нормальном состоянии, а в измененном состоянии прионные белки могут распространяться, т. е. стать инфекционными [12].
Первоначально прионы были открыты как инфекционные агенты нового типа, но сейчас считают, что они представляют собой феномен общебиологический и являются носителями информации нового типа, хранимой в конформации белка. Феномен прионов лежит в основе эпигенетической наследственности и регуляции экспрессии генов на посттрансляционном уровне.
Эпигенетика в практической медицине
Эпигенетические модификации контролируют все стадии развития и функциональную активность клеток. Нарушение механизмов эпигенетической регуляции напрямую или косвенно связано с множеством заболеваний.
К заболеваниям с эпигенетической этиологией относят болезни импринтинга, которые в свою очередь делятся на генные и хромосомные, всего в настоящее время насчитывают 24 нозологии.
При болезнях генного импринтинга наблюдается моноаллельная экспрессия в локусах хромосом одного из родителей. Причиной являются точечные мутации в генах, дифференцированно экспрессирующихся в зависимости от материнского и отцовского происхождения и приводящих к специфическому метилированию цитозиновых оснований в молекуле ДНК. К ним относят: синдром Прадера–Вилли (делеция в отцовской хромосоме 15) — проявляется черепно-лицевым дисморфизмом, низким ростом, ожирением, мышечной гипотонией, гипогонадизмом, гипопигментацией и задержкой умственного развития; синдром Ангельмана (делеция критического района, находящегося в 15-й материнской хромосоме), основными признаками которого являются микробрахицефалия, увеличенная нижняя челюсть, выступающий язык, макростомия, редкие зубы, гипопигментация; синдром Беквитта–Видемана (нарушение метилирования в коротком плече 11-й хромосомы), проявляющийся классической триадой, включающей макросомию, омфалоцеле макроглоссию и др. [13].
К числу важнейших факторов, влияющих на эпигеном, относятся питание, физическая активность, токсины, вирусы, ионизирующая радиация и др. Особенно чувствительным периодом к изменению эпигенома является внутриутробный период (особенно охватывающий два месяца после зачатия) и первые три месяца после рождения. В период раннего эмбриогенеза геном удаляет большую часть эпигенетических модификаций, полученных от предыдущих поколений. Но процесс репрограммирования продолжается в течение всей жизни [14].
К заболеваниям, где нарушение генной регуляции является частью патогенеза, можно отнести некоторые виды опухолей, сахарный диабет, ожирение, бронхиальную астму, различные дегенеративные и другие болезни [15, 16].
Эпигоном при раке характеризуется глобальными изменениями в метилировании ДНК, модификации гистонов, а также изменением профиля экспрессии хроматин-модифицирующих ферментов.
Опухолевые процессы характеризуются инактивацией посредством гиперметилирования ключевых генов-супрессоров и посредством гипометилирования активацией целого ряда онкогенов, факторов роста (IGF2, TGF) и мобильных повторяющихся элементов, расположенных в районах гетерохроматина [17].
Так, в 19% случаев гипернефроидные опухоли почки ДНК островков СрG была гиперметилированной, а при раке груди и немелкоклеточной карциноме легких выявлена взаимосвязь между уровнями гистонового ацетилирования и экспрессией супрессора новообразований — чем ниже уровни ацетилирования, тем слабее экспрессия гена.
В настоящее время уже разработаны и внедрены в практику противоопухолевые лекарственные препараты, основанные на подавлении активности ДНК-метилтрансфераз, что приводит к снижению метилирования ДНК, активации генов-супрессоров опухолевого роста и замедлению пролиферации опухолевых клеток. Так, для лечения миелодиспластического синдрома в комплексной терапии применяют препараты децитабин (Decitabine) и азацитидин (Azacitidine) [18]. С 2015 г. для лечения множественной миеломы в сочетании с классической химиотерапией применяют панобиностат (Panibinostat), являющийся ингибитором гистоновой деацитилазы [19]. Данные препараты по данным клинических исследований оказывают выраженный положительный эффект на уровень выживаемости и качество жизни пациентов.
Изменения экспрессии тех или иных генов могут происходить и в результате действия на клетку факторов внешней среды. В развитии сахарного диабета 2-го типа и ожирения играет роль так называемая «гипотеза экономного фенотипа», согласно которой недостаток питательных веществ в процессе эмбрионального развития приводит к развитию патологического фенотипа [20]. На моделях животных был выявлен участок ДНК (локус Pdx1), в котором под влиянием недостаточности питания снижался уровень ацетилирования гистонов, при этом наблюдались замедление деления и нарушения дифференцировки B-клеток островков Лангерганса и развития состояния, схожего с сахарным диабетом 2-го типа [21].
Активно развиваются и диагностические возможности эпигенетики. Появляются новые технологии, способные анализировать эпигенетические изменения (уровень метилирования ДНК, экспрессию микроРНК, посттрансляционные модификации гистонов и др.), такие как иммунопреципитация хроматина (CHIP), проточная цитометрия и лазерное сканирование, что дает основания полагать, что в ближайшее время будут выявлены биомаркеры для изучения нейродегенеративных заболеваний, редких, многофакторных болезней и злокачественных новообразований и внедрены в качестве методов лабораторной диагностики [22].
Итак, в настоящее время эпигенетика бурно развивается. С ней связывают прогресс в биологии и медицине.
Литература
- Ezkurdia I., Juan D., Rodriguez J. M. et al. Multiple evidence strands suggest that there may be as few as 19,000 human protein-coding genes // Human Molecular Genetics. 2014, 23 (22): 5866–5878.
- International Human Genome Sequencing Consortium. Initial sequencing and analysis of the human genome // Nature. 2001, Feb. 409 (6822): 860–921.
- Xuan D., Han Q., Tu Q. et al. Epigenetic Modulation in Periodontitis: Interaction of Adiponectin and JMJD3-IRF4 Axis in Macrophages // Journal of Cellular Physiology. 2016, May; 231 (5): 1090–1096.
- Waddington C. H. The Epigenotpye // Endeavour. 1942; 18–20.
- Бочков Н. П. Клиническая генетика. М.: Гэотар.Мед, 2001.
- Jenuwein T., Allis C. D. Translating the Histone Code // Science. 2001, Aug 10; 293 (5532): 1074–1080.
- Коваленко Т. Ф. Метилирование генома млекопитающих // Молекулярная медицина. 2010. № 6. С. 21–29.
- Элис Д., Дженювейн Т., Рейнберг Д. Эпигенетика. М.: Техносфера, 2010.
- Taylor P. D., Poston L. Development programming of obesity in mammals // Experemental Physiology. 2006. № 92. P. 287–298.
- Льюин Б. Гены. М.: БИНОМ, 2012.
- Plasschaert R. N., Bartolomei M. S. Genomic imprinting in development, growth, behavior and stem cells // Development. 2014, May; 141 (9): 1805–1813.
- Wickner R. B., Edskes H. K., Ross E. D. et al. Prion genetics: new rules for a new kind of gene // Annu Rev Genet. 2004; 38: 681–707.
- Мутовин Г. Р. Клиническая генетика. Геномика и протеомика наследственной патологии: учеб. пособие. 3-е изд., перераб. и доп. 2010.
- Романцова Т. И. Эпидемия ожирения: очевидные и вероятные причины // Ожирение и метаболизм. 2011, № 1, с. 1–15.
- Bégin P., Nadeau K. C. Epigenetic regulation of asthma and allergic disease // Allergy Asthma Clin Immunol. 2014, May 28; 10 (1): 27.
- Martínez J. A., Milagro F. I., Claycombe K. J., Schalinske K. L. Epigenetics in Adipose Tissue, Obesity, Weight Loss, and Diabetes // Advances in Nutrition. 2014, Jan 1; 5 (1): 71–81.
- Dawson M. A., Kouzarides T. Cancer epigenetics: from mechanism to therapy // Cell. 2012, Jul 6; 150 (1): 12–27.
- Kaminskas E., Farrell A., Abraham S., Baird A. Approval summary: azacitidine for treatment of myelodysplastic syndrome subtypes // Clin Cancer Res. 2005, May 15; 11 (10): 3604–3608.
- Laubach J. P., Moreau P., San-Miguel J..F, Richardson P. G. Panobinostat for the Treatment of Multiple Myeloma // Clin Cancer Res. 2015, Nov 1; 21 (21): 4767–4773.
- Bramswig N. C., Kaestner K. H. Epigenetics and diabetes treatment: an unrealized promise? // Trends Endocrinol Metab. 2012, Jun; 23 (6): 286–291.
- Sandovici I., Hammerle C. M., Ozanne S. E., Constância M. Developmental and environmental epigenetic programming of the endocrine pancreas: consequences for type 2 diabetes // Cell Mol Life Sci. 2013, May; 70 (9): 1575–1595.
- Szekvolgyi L., Imre L., Minh D. X. et al. Flow cytometric and laser scanning microscopic approaches in epigenetics research // Methods Mol Biol. 2009; 567: 99–111.
В. В. Смирнов 1 , доктор медицинских наук, профессор
Г. Е. Леонов
ФГБОУ ВО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
Источник