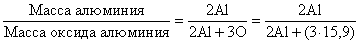- Способы определения атомной массы
- Физические методы определения атомной массы химического элемента
- Старт в науке
- Способы определения атомной массы
- — метод Канниццаро
- — метод, основанный на явлении изоморфизма
- Задачи для самостоятельного решения
- АТОМНАЯ МАССА
- МЕТОДЫ ОПРЕДЕЛЕНИЯ
- Химические методы.
- Физические методы.
- Плотность газа.
- Масс-спектроскопия.
- Ядерные реакции.
- Рентгенография.
- Уточнение атомных масс.
Способы определения атомной массы
- Главная
- Список секций
- Физика
- Физические методы определения атомной массы химического элемента
Физические методы определения атомной массы химического элемента
Автор работы награжден дипломом победителя III степени
Цель работы: О пределить экспериментально относительную атомную массу химического элемента неизвестного вещества в условиях школьной лаборатории.
Экспериментально определить относительную атомную массу химического элемента вещества с помощью физическ их метод ов измерения .
Используя калькулятор CASIO CLASSWIZ, оценить границы случайной погрешности.
1. Повторите основные понятия и термины, используемые в работе.
Относительная атомная масса – показывает во сколько раз масса данного атома химического элемента больше 1/12 массы изотопа 12 С.
Изотопы – атомы одного химического элемента, имеющие разное количество нейтронов и одинаковое число протонов в ядре, следовательно, имеющие разные относительные атомныемассы.
Удельная теплоемкость вещества – это физическая величина, которая показывает, какое количество теплоты необходимо сообщить телу массой 1кг, чтобы изменить его температуру на1 0 С.
Масса Эквивалента — такая масса вещества, которая вступает в реакцию или замещает 1 моль «H».
В 181 Дюлонг совместно с Пти , установили закон теплоёмкости твёрдых тел, согласно которому произведение удельных теплоёмкостей простых твёрдых тел на относительную атомную массу образующих элементов есть величина приблизительно постоянная.
В современных единицах измерения эта величина примерно равна 25,12 Дж/(г • 0 С) .
Значит Ar = 25,12/c , где с — удельная теплоемкость вещества.
2. Практическая часть
Оборудование: рычажные весы, н аборгирь, м ензурка, лабораторный стаканчик с водой, электрический чайник, к алориметр, исследуемое цилиндрическое твердое тело, термометр, калькулятор CASIO CLASSWIZ.
3. Порядок выполнения работы:
1. С помощью рычажных весов определите массу твердого тела цилиндрической формы.
2. Определите начальную температуру твердого тела (т.к. тело длительное время находилось в классе, то его температура равна температуре воздуха в помещении)
3. Определите с помощью мензурки объем горячей воды.
4. Зная плотность воды (1000кг/м³), рассчитайте ее массу.
5. Перелейте воду в калориметр и определите ее начальную температуру.
6. Привяжите к телу нить и опустите его в калориметр с горячей водой.
7. Определите установившуюся температуру (как только показания
термометра более изменяться не будут)
8. Составьте уравнение теплового баланса.
Q 1 =c 1 m 1 (t-t 1 ), где Q 1 — количество теплоты, отданное водой в результате теплообмена, с 1 –удельная теплоемкость воды (табличная величина),
m 1 – масса воды, t –конечная температура, t 1 – начальная температура воды,
Q 2 =c 2 m 2 (t-t 2 ), где Q 2 — количество теплоты, полученное твердым телом в результате теплообмена, с 2 –удельная теплоемкость вещества (нужно определить), m 2 – масса вещества, t 2 – начальная температура исследуемого тела.
Потерями энергии на обмен с окружающей средой пренебрежем.
Следовательно, уравнение теплового баланса в данном случае имеет вид:
Результаты измерений и вычислений, запишите в таблицу:
Результаты вычислений запишем в таблицу:
4. Воспользуемся калькулятором для оценки границ случайной погрешности
Результаты измерений вносим в калькулятор:
1. Включим калькулятор, клавиша «ON».
2. Нажмем клавишу «MODE» . Войдем в режим статистики.
На дисплее видно указание « 2: STAT».
3. Для входа в режим статистики нажмем клавишу с цифрой «2».
4. На дисплее найдем указание о расчете параметров экспериментов, в которых проводятся многократные измерения одной и той же величины «1: 1-VAR» , нажмем клавишу с цифрой «1».
5. Откроется таблица с одной колонкой.
Внесем в таблицу результаты опытов:
набираете результат 25,12
набираете результат 25,33
набираете результат 23,03
Расчет погрешности измерения
1. Входим в режим расчетов, нажимаем клавишу «АС».
2. Для входа в режим статистических расчетов нажимаем сначала «OPTN» , затем нажимаем клавишу с цифрой «2» (функция этой клавиши — статистика).
3. На дисплее видим:
Округлим до сотых
Среднее значение = 24,50 а.е.м. (верхняя строчка)
С реднеквадратичное отклонение = 1, 04 а.е.м.
Среднеквадратичное отклонение измеряется в единицах измерения самой случайной величины и используется при расчёте стандартной ошибки среднего арифметического.
Рассчитаем погрешность среднего
Вывод: относительная атомная масса исследуемого вещества равна
Аr = 24, 50 ± 0,60 (а.е.м.)
8. Хомченко И.Г. Общая химия, М, Химия, 1990;
9. Энциклопедический словарь юного химика. Сост Крицман В.А., Станцо В.В., М, Педагогика, 1996
Старт в науке
Учредителями Конкурса являются Международная ассоциация учёных, преподавателей и специалистов – Российская Академия Естествознания, редакция научного журнала «Международный школьный научный вестник», редакция журнала «Старт в науке».
Источник
Способы определения атомной массы
Атомная теплоемкость – это произведение молярной массы элемента на удельную теплоемкость простого вещества. Согласно правилу атомных теплоемкостей эта величина для большинства простых веществ в твердом состоянии приблизительно одинакова и в среднем равна 25 Дж/моль×К (правило Дюлонга-Пти). Этот метод используется только для металлов и дает Приближенное значение искомой величины.
Пример 9. 0,5 г металла, реагируя с избытком кислоты, вытесняют при н. у. 100 мл водорода. Удельная теплоемкость металла равна 0,23 Дж/г×К. рассчитать точное значение атомной массы металла.
Решение .
Вначале определяют приближенное значение атомной массы металла:

Затем вычисляют эквивалент металла:
0,5 г вытесняют при н. у. 0,1 л


Находят валентность металла, а затем его точную атомную массу:


— метод Канниццаро
Находят массовую долю элемента в нескольких его соединениях и молекулярные массы этих соединений, а затем рассчитывают, какая масса элемента содержится в 1 моль каждого вещества. Наименьшая из найденных величин в большинстве случаев, когда хотя бы одно из выбранных веществ содержит в молекуле один атом элемента, представляет собой атомную массу элемента.
Возможные значения 

— метод, основанный на явлении изоморфизма
Изоморфными называют соединения, имеющие одинаковую кристаллическую структуру.
Пример 10. Оксид одного из редкоземельных элементов изоморфен хлориду натрия и содержит 9,52 % кислорода по массе. Определите 
Решение .
Оксид, полиморфный 

Атомную массу находим из пропорции:
В оксиде на 9,52 г кислорода приходится (100 – 9,52) г элемента
В оксиде на 16 г кислорода приходится Х г элемента


Задачи для самостоятельного решения
1.5.1. Найти относительную атомную массу кремния и серы по следующим экспериментальным данным для ряда их соединений:
Источник
АТОМНАЯ МАССА
АТОМНАЯ МАССА. Понятие об этой величине претерпевало длительные изменения в соответствии с изменением представления об атомах. Согласно теории Дальтона (1803), все атомы одного и того же химического элемента идентичны и его атомная масса – это число, равное отношению их массы к массе атома некоего стандартного элемента. Однако примерно к 1920 стало ясно, что элементы, встречающиеся в природе, бывают двух типов: одни действительно представлены идентичными атомами, а у других атомы имеют одинаковый заряд ядра, но разную массу; такие разновидности атомов были названы изотопами. Определение Дальтона, таким образом, справедливо только для элементов первого типа. Атомная масса элемента, представленного несколькими изотопами, есть средняя величина из массовых чисел всех его изотопов, взятых в процентном отношении, отвечающем их распространенности в природе.
В 19 в. в качестве стандарта при определении атомных масс химики использовали водород или кислород. В 1904 за стандарт была принята 1/16 средней массы атома природного кислорода (кислородная единица) и соответствующая шкала получила название химической. Масс-спектрографическое определение атомных масс проводилось на основе 1/16 массы изотопа 16 О, и соответствующая шкала называлась физической. В 1920-х годах было установлено, что природный кислород состоит из смеси трех изотопов: 16 О, 17 О и 18 О. В связи с этим возникли две проблемы. Во-первых, оказалось, что относительная распространенность природных изотопов кислорода немного варьирует, а значит, в основе химической шкалы лежит величина, не являющаяся абсолютной константой. Во-вторых, у физиков и химиков получались разные значения таких производных констант, как молярные объемы, число Авогадро и др. Решение вопроса было найдено в 1961, когда за атомную единицу массы (а.е.м.) была принята 1/12 массы изотопа углерода 12 С (углеродная единица). (1 а.е.м., или 1D (дальтон), в СИ-единицах массы составляет 1,66057Ч10 –27 кг.) Природный углерод также состоит из двух изотопов: 12 С – 99% и 13 С – 1%, но новые величины атомных масс элементов связаны только с первым из них. В результате была получена универсальная таблица относительных атомных масс. Изотоп 12 С оказался удобным и для физических измерений.
МЕТОДЫ ОПРЕДЕЛЕНИЯ
Атомную массу можно определить либо физическими, либо химическими методами. Химические методы отличаются тем, что на одном из этапов в них фигурируют не сами атомы, а их комбинации.
Химические методы.
Согласно атомной теории, числа атомов элементов в соединениях относятся между собой как небольшие целые числа (закон кратных отношений, который открыт Дальтоном). Поэтому для соединения известного состава можно определить массу одного из элементов, зная массы всех других. В некоторых случаях массу соединения можно измерить непосредственно, но обычно ее находят косвенными методами. Рассмотрим оба этих подхода.
Атомную массу Al недавно определили следующим образом. Известные количества Al были превращены в нитрат, сульфат или гидроксид и затем прокалены до оксида алюминия (Al2O3), количество которого точно определяли. Из соотношения между двумя известными массами и атомными массами алюминия и кислорода (15,9)
нашли атомную массу Al. Однако прямым сравнением с атомной массой кислорода можно определить атомные массы лишь немногих элементов. Для большинства элементов их определяли косвенным путем, анализируя хлориды и бромиды. Во-первых, эти соединения для многих элементов можно получить в чистом виде, во-вторых, для их точных количественных определений в распоряжении химиков имеется чувствительный аналитический метод, основанный на сравнении их масс с массой серебра. Для этого точно определяют массу анализируемых соединений и массу серебра, необходимого для взаимодействия с ними. Атомную массу нужного элемента рассчитывают исходя из атомной массы серебра – эталонной величины в подобных определениях. Атомную массу серебра (107,870) в углеродных единицах определяли косвенным химическим методом.
Физические методы.
В середине 20 в. существовал только один физический метод определения атомных масс, сегодня наиболее широко применяют четыре.
Плотность газа.
Самый первый физический метод основывался на определении плотности газа и на том, что в соответствии с законом Авогадро равные объемы газов при одинаковых температуре и давлении содержат одинаковое число молекул. Следовательно, если определенный объем чистого СО2 имеет массу, в 1,3753 большую, чем такой же объем кислорода в тех же условиях, то молекула СО2 должна быть в 1,3753 раза тяжелее молекулы кислорода (мол. масса О2 = 31,998), т.е. масса молекулы СО2 по химической шкале равна 44,008. Если из этой величины вычесть массу двух атомов кислорода, равную 31,998, мы получим атомную массу углерода – 12,01. Чтобы получить более точное значение, необходимо ввести ряд поправок, что усложняет этот метод. Тем не менее с его помощью были получены некоторые весьма ценные данные. Так, после открытия благородных газов (He, Ne, Ar, Kr, Xe) метод, основанный на измерении плотности, оказался единственно пригодным для определения их атомных масс.
Масс-спектроскопия.
Вскоре после Первой мировой войны Ф.Астон создал первый масс-спектроскоп для точного определения массовых чисел различных изотопов и тем самым открыл новую эру в истории определения атомных масс. Сегодня существует два основных типа масс-спектроскопов: масс-спектрометры и масс-спектрографы (последним является, например, прибор Астона). Масс-спектрограф предназначен для изучения поведения потока электрически заряженных атомов или молекул в сильном магнитном поле. Отклонение заряженных частиц в этом поле пропорционально отношению их масс к заряду, а регистрируют их в виде линий на фотопластинке. Сравнивая положения линий, отвечающих определенным частицам, с положением линии для элемента с известной атомной массой, можно с достаточной точностью определить атомную массу нужного элемента. Хорошей иллюстрацией метода является сравнение массы молекулы СН4 (метана) с массовым числом самого легкого изотопа кислорода 16 О. Одинаково заряженные ионы метана и 16 О одновременно впускают в камеру масс-спектрографа и регистрируют их положение на фотопластинке. Различие в положении их линий отвечает разности масс 0,036406 (по физической шкале). Это значительно более высокая точность, чем может дать любой химический метод.
Если исследуемый элемент не имеет изотопов, то определение его атомной массы не составляет особого труда. В противном случае необходимо определить не только массу каждого изотопа, но и их относительное содержание в смеси. Эту величину не удается определить с достаточной точностью, что ограничивает применение масс-спектрографического метода для нахождения атомных масс изотопических элементов, особенно тяжелых. Недавно с помощью масс-спектрометрии удалось установить с высокой точностью относительное содержание двух изотопов серебра, 107 Ag и 109 Ag. Измерения были выполнены в Национальном бюро стандартов США. Используя эти новые данные и более ранние измерения масс изотопов серебра, уточнили значение атомной массы природного серебра. Теперь эта величина считается равной 107,8731 (химическая шкала).
Ядерные реакции.
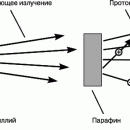
Для определения атомных масс некоторых элементов можно использовать соотношение между массой и энергией, полученное Эйнштейном. Рассмотрим реакцию бомбардировки ядер 14 N быстрыми ядрами дейтерия с образованием изотопа 15 N и обычного водорода 1 Н:
14 N + 2 H = 15 N + 1 H + Q
В результате реакции выделяется энергия Q = 8 615 000 эВ, которая в соответствии с уравнением Эйнштейна эквивалентна 0,00948 а.е.м. Значит, масса 14 N + 2 H превышает массу 15 N + 1 H на 0,00948 а.е.м., и если мы знаем массовые числа трех любых изотопов – участников реакции, то можем найти массу четвертого. Метод позволяет определить разность массовых чисел двух изотопов с большей точностью, чем масс-спектрографический.
Рентгенография.
Этим физическим методом можно определять атомные массы веществ, которые при обычной температуре образуют регулярную кристаллическую решетку. Метод основан на связи между атомной (или молекулярной) массой кристаллического вещества, его плотностью, числом Авогадро и неким коэффициентом, который определяют из расстояний между атомами в кристаллической решетке. Необходимо провести прецизионные измерения двух величин: постоянной решетки рентгенографическими методами и плотности методом пикнометрии. Применение метода ограничивается трудностями получения чистых совершенных кристаллов (без вакансий и дефектов любого рода).
Уточнение атомных масс.
Все измерения атомных масс, которые были выполнены более 20 лет назад, проводились химическими методами или методом, основанным на определении плотности газов. В последнее же время данные, получаемые масс-спектрометрическими и изотопными методами, совпадают с такой высокой точностью, что Международная комиссия по атомным массам решила скорректировать атомные массы 36 элементов, причем 18 из них не имеют изотопов.
См. также АВОГАДРО ЧИСЛО.
Кравцов В.А. Массы атомов и энергии связи. М., 1965
Воронцова Е.Р. Атомный вес. М., 1984
Эмсли Дж. Элементы (справочник). М., 1993
Источник