Методы очистки коллоидных растворов.



Методы очистки коллоидных растворов.
Коллоидные растворы, полученные одним из рассмотренных методов, содержат примеси растворенных низкомолекулярных веществ и грубодисперсных частиц, наличие которых может отрицательно сказываться на свойствах золей, снижая их устойчивость (см. раздел 12.5).
Для очистки коллоидных растворов от примесей используют фильтрацию, диализ, электродиализ, ультрафильтрацию.
Фильтрация (от лат. filtrum — войлок) основана на способности коллоидных частиц проходить через поры обычных фильтров. При этом более крупные частицы задерживаются. Фильтрацию используют для очистки коллоидных растворов от примесей грубодисперсных частиц.
Диализ (от греч. dyalisis — отделение) — удаление с помощью мембран низкомолекулярных соединений из коллоидных растворов и растворов ВМС. При этом используют свойство мембран пропускать молекулы и ионы малого размера и задерживать коллоидные частицы и макромолекулы. Жидкость, подвергаемую диализу, отделяют от чистого растворителя соответствующей мембраной. Малые молекулы и ионы диффундируют через мембрану в растворитель и при его достаточно частой замене почти нацело удаляются из диализуемой жидкости.
Проницаемость мембраны по отношению к низкомолекулярным веществам обусловливается или тем, что малые молекулы и ионы, свободно проходят через капилляры, пронизывающие мембраны, или растворяются в веществе мембраны. В качестве мембран для диализа применяют различные пленки, как естественные— бычий или свиной мочевой пузырь, плавательный пузырь рыб, так и искусственные—из нитроцеллюлозы, ацетилцеллюлозы, целлофана, желатина и других материалов.
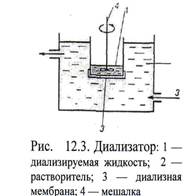
Существует большое разнообразие диализаторов — приборов для проведения диализа. Все диализаторы построены по общему принципу: диализируемая жидкость («внутренняя жидкость») находится в сосуде, в котором она отделена от воды или другого растворителя («внешняя жидкость») мембраной (рис. 12.3). Скорость диализа возрастает с увеличением поверхности мембраны, ее пористости и размера пор, с повышением температуры, интенсивности перемешивания диализируемой жидкости, скоростью смены внешней жидкости и уменьшается с ростом толщины мембраны.
Электродиализ используют для увеличения скорости диализа низкомолекулярных электролитов.
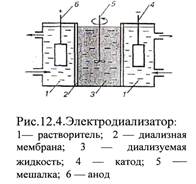
С этой целью в диализаторе создают постоянное электрическое поле с падением потенциала, 20—250 В/см и выше. Принципиальная схема электродиализа-, тора представлена на рис. 12.4. Проведение диализа в электрическом поле позволяет ускорить очистку коллоидного раствора в несколько десятков раз.
Компенсационный диализ применяют, когда необходимо освободить коллоидный раствор лишь от части низкомолекулярных примесей. В диализаторе растворитель заменяют раствором низкомолекулярных веществ, которые необходимо оставить в коллоидном растворе.
Ультрафильтрация (от лат. — ultra — сверх, filtrum — войлок) применяется для очистки систем, содержащих частицы коллоидных размеров (золи, растворы ВМС, взвеси бактерий и.вирусов) . В основе метода лежит продавливание разделяемой смеси через фильтры с порами.
Источник
1.8. Очистка золей от примесей
Очистка коллоидных систем от примесей присутствующих в них электролитов осуществляется при помощи мембран или фильтров, пропускающих ионы, но задерживающих коллоидные частицы. Эти методы называют соответственно диализом и фильтрацией. Для ускорения процесса диализа часто используют электрический ток; в этом случае метод называется электродиализом. Электродиализаторпредставляет собой сосуд, разделенный на три части полупроницаемыми перегородками, задерживающими коллоидные частицы. Разделение сосуда только одной перегородкой может привести к тому, что присутствующий электролит, например сульфат натрия, разделится на два раствора — серную кислоту и гидроксид натрия в анодной и катодной частях. Это может вызвать нарушение устойчивости золя. В средней части электродиализатора обычно помещается золь, а в боковых, приэлектродных пространствах, устанавливается постоянный поток дистиллированной воды для удаления прошедших через мембрану ионов. Природа мембран оказывает существенное влияние на ход процесса электродиализа. В последнее время часто используют мембраны с ионообменной смолой.
Коллоидные системы — золи или латексы — содержат загрязняющие вещества: золи — соли, латексы — соли, продукты распада инициатора и избыточное количество эмульгатора. Эти вещества обычно искажают коллоидно-химические свойства золей и латексов, поэтому в ряде случаев они должны быть удалены. Очистка золей и латексов проводится одним из методов диализа: периодическим или непрерывным.
Источник
Получение и способы очистки коллоидных систем
Получение коллоидных систем
Для получения коллоидных систем, применяют, в основном, 2 метода:
- Дисперсионный метод – используют дробление твердого вещества до частиц, размером, соответствующих коллоидам. Измельчение производят:
- механически при помощи шаровых мельниц, гомогенизаторов или ультразвуковых дезинтеграторов;
- с помощью физико-химических способов, таких как пептизация, добавление поверхностно–активных веществ.
- Конденсационный метод — укрупнение частиц путем агрегации молекул или ионов, до размеров, соответствующих коллоидам. Это можно реализовать следующими способами:
- испарение растворителя;
- замена растворителя;
- осуществление реакций, в результате которых образуются малорастворимые или нерастворимые вещества – реакции окисления – восстановления, разложения, гидролиза и др.
Способы очистки коллоидных систем
Коллоидные растворы могут содержать примеси, снижающие их стабильность, вследствие чего производят их очистку. Для этого используют такие методы, как диализ, электродиализ, фильтрация и ультрафильтрация.
- Диализ — удаление низкомолекулярных соединений с помощью мембран, способных задерживать коллоидные частицы и пропускать частицы меньшего размера. Прибор, используемый в этих целях, называют диализатором:
Диализатор
Коллоидный раствор наливают в сосуд, в нижней части которого находится мембрана и помещенный в емкость с водой. В растворитель проникают лишь ионы и молекулы низкомолекулярных примесей.
Процесс диализа протекает медленно и для его ускорения используют электрическое поле.
- Электродиализ – используется для увеличения скорости диализа посредством электрического поля. Прибор, используемый для проведения электродиализа, называют электродиализатором. Он состоит из трех частей: средняя часть отделена полупроницаемыми мембранами от соседних частей, соединенных с электродами. Коллоидный раствор помещается в среднюю часть электродиализатора. При создании электрического поля, находящиеся в коллоидном растворе катионы, начинают движение через мембрану к катоду, а анионы – к аноду.
Электродиализатор
- Фильтрация и Ультрафильтрация – это процесс отделения примесей от коллоидных частиц путем фильтрования коллоидного раствора через полупроницаемые мембраны под давлением.
Ультрафильтрация
Источник
Методы очистки золей: диализ, электродиализ, ультрафильтрация
6. Методы очистки золей: диализ, электродиализ, ультрафильтрация
Диализ. Очищаемый золь, заливают в сосуд, дном которого служит мембрана, задерживающая коллоидные частицы или макромолекулы и пропускающая молекулы растворителя и низкомолекулярные примеси. Внешней средой, контактирующей с мембраной, является растворитель. Низкомолекулярные примеси, концентрация которых в золе или макромолекулярном растворе выше, переходят сквозь мембрану во внешнюю среду (диализат). Очистка идет до тех пор, пока концентрации примесей в золе и диализате не станут близкими по величине. Если обновлять растворитель, то можно практически полностью избавиться от примесей.
Такое использование диализа целесообразно, когда цель очистки – удаление всех низкомолекулярных веществ, проходящих сквозь мембрану. Однако в ряде случаев задача может оказаться сложнее – необходимо освободиться только от определенной части низкомолекулярных соединений в системе. Тогда в качестве внешней среды применяют раствор тех веществ, которые необходимо сохранить в системе. Именно такая задача ставится при очистке крови от низкомолекулярных шлаков и токсинов (солей, мочевины и т.п.). Если удалять подряд все низкомолекулярные компоненты крови, то начинается разрушение клеток, что, в свою очередь, может привести к гибели организма.
Электродиализ. Очистку от электролитов можно значительно ускорить действием приложенной разности потенциалов (электромиграцией). Такой метод очистки называется электродиализом. Его используют для очистки различных биологических объектов (растворы белков, сыворотка крови и пр.).
Ультрафильтрация. Ультрафильтрация – метод очистки коллоидных систем путем продавливания дисперсионной среды вместе с низкомолекулярными примесями через ультрафильтры. Ультрафильтрами служат мембраны того же типа, что и для диализа. В мешочек из ультрафильтра наливают очищаемый золь или раствор высокомолекулярного вещества. К золю прилагают давление, избыточное по сравнению с атмосферным. Дисперсионную среду обновляют, добавляя к золю чистый растворитель.
Ультрафильтрация используется не только для удаления низкомолекулярных компонентов смеси, но и для концентрирования систем и разделения веществ с различной молекулярной массой. Этим методом очищают сточные воды, отделяют культуральные жидкости от продуктов микробиологического синтеза, концентрируют биологически активные вещества: белки, ферменты, антибиотики и т.д.
В последние годы ультрафильтрация наряду с диализом получила распространение в клинике для обработки крови. Этот метод применяется для выведения из организма токсических веществ и, если это необходимо, для удаления избытка жидкости.
II. Раздел «Оптические свойства коллоидных систем»
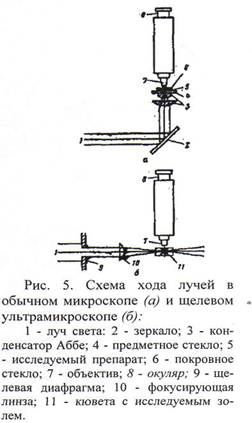
1. Оптические свойства коллоидных систем. Опалесценция и флуоресценция
Прохождение света через коллоидную систему вызывает три оптических эффекта: поглощение, отражение и рассеивание лучей. Поглощение свойственно всем системам, тогда как отражение более характерно для грубодисперсных систем (эмульсий и суспензий), где размер частиц больше, чем длина волны облучения. Поэтому, в отличие от молекулярных и ионных растворов, которые не имеют поверхности раздела фаз и оптически однородны, коллоидные растворы рассеивают свет.
Это проявляется опалесценцией в виде голубоватого матового свечения при освещении боковым светом. При пропускании параллельного пучка света через коллоидный раствор наблюдается конус рассеянного света – эффект Тиндаля. По способности рассеивать свет можно определять концентрацию коллоидных частиц в растворе — метод нефелометрии.
Опалесценция (светорассеяние) наблюдается только тогда, когда длина световой волны больше размера частицы дисперсной фазы. Если длина световой волны много меньше диаметра частицы, происходит отражение света, проявляющееся в мутности.
Рассеянный свет имеет ту особенность, что он распространяется во всех направлениях. Интенсивность рассеянного света в различных направлениях различна.
С опалесценцией внешне сходна, флуоресценция, характерная для истинных растворов некоторых красителей. Она заключается в том, что раствор при наблюдении в отраженном свете имеет иную окраску, чем в проходящем, и в нем можно видеть такой же конус Тиндаля, что и в типичных коллоидных системах. Однако по существу это совершенно различные явления. Опалесценция возникает в результате рассеяния света, при этом длина волны рассеянного света та же, что и падающего. Флуоресценция же представляет собой внутримолекулярное явление, заключающееся в селективном поглощении молекулой вещества светового луча и в трансформировании его в световой луч с другой, большей длиной волны.
2. Поглощение света дисперсными системами. Зависимость поглощения от концентрации. Закон Бугера-Ламберта-Бера
В 1760г. Ламберт, а еще ранее Бугер установили следующую зависимость между интенсивностью прошедшего света и толщиной среды, через которую этот свет прошел:
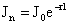
где 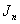
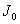
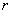

Согласно закону Бугера-Ламберта – каждый последующий слой поглощает ту же долю проходящего света, что и предыдущий.
Бер показал, что коэффициент поглощения растворов с абсолютно бесцветным и прозрачным растворителем пропорционален молярной концентрации 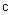
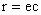
Вводя значение молярного коэффициента поглощения 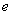
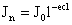
Закон устанавливает зависимость интенсивности прошедшего света от толщины слоя и концентрации растворенного вещества.
Логарифмируя уравнение, получим:
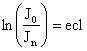
где 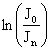
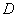
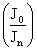
Если 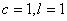
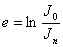
Если 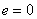

т.е. интенсивность прошедшего света будет равна интенсивности падающего.
Молярный коэффициент поглощения 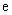
Закон Бугера-Ламберта-Бера приложим для золей высокой дисперсности, если слой жидкости не слишком толст, а концентрация раствора не слишком большая.
Для металлических золей уравнение светопоглощения должно учитывать дисперсность системы:
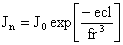
Источник