- Способы образования названий алканов греческие числительные
- Способы образования названий алканов греческие числительные
- Номенклатура алканов. Рациональная номенклатура
- Номенклатура алканов
- Алканы
- Гомологический ряд алканов
- Строение алканов
- Изомерия алканов
- Структурная изомерия
- Оптическая изомерия
- Номенклатура алканов
- Химические свойства алканов
- 1. Реакции замещения
- 1.1. Галогенирование
- 1.2. Нитрование алканов
- 2. Реакции разложения
- 2.1. Дегидрирование и дегидроциклизация
- 2.2. Пиролиз (дегидрирование) метана
- 2.3. Крекинг
- 3. Реакции окисления алканов
- 3.1. Полное окисление – горение
- 3.2. Каталитическое окисление
- 4. Изомеризация алканов
- Получение алканов
- 1. Взаимодействие галогеналканов с металлическим натрием (реакция Вюрца)
- 2. Электролиз солей карбоновых кислот (электролиз по Кольбе )
- 4. Декарбоксилирование солей карбоновых кислот (реакция Дюма)
- 5. Гидрирование алкенов, алкинов, циклоалканов, алкадиенов
- 6. Синтез Фишера-Тропша
- 7. Получение алканов в промышленности
Способы образования названий алканов греческие числительные
2.4.2. Правила построения названий алканов по систематической международной номенклатуре ИЮПАК
- Для простейших алканов (С 1 -С 4 ) приняты тpивиальные названия:
метан, этан, пpопан, бутан, изобутан. - Начиная с пятого гомолога, названия нормальных (неpазветвленных) алканов стpоят в соответствии с числом атомов углеpода, используя гpеческие числительные и суффикс -ан : пентан, гексан, гептан, октан, нонан, декан и далее.
- В основе названия разветвленного алкана лежит название входящего в его конструкцию нормального алкана с наиболее длинной углеродной цепью. При этом углеводоpод с pазветвленной цепью pассматpивают как пpодукт замещения атомов водоpода в ноpмальном алкане углеводоpодными pадикалами.
рассматривается как замещенный пентан , в котором два атома водорода замещены на радикалы –СН 3 ( метил ).
Порядок построения названия разветвленного алкана
Выбрать в молекуле главную углеродную цепь. Во-первых, она должна быть самой длинной. Во-вторых, если имеются две или более одинаковые по длине цепи, то из них выбирается наиболее разветвленная.
Например, в молекуле есть 2 цепи с одинаковым числом (7) атомов С (выделены цветом):
В случае (а) цепь имеет 1 заместитель, а в (б) – 2. Поэтому следует выбрать вариант (б).
Пронумеровать атомы углерода в главной цепи так, чтобы атомы С, связанные с заместителями, получили возможно меньшие номера. Поэтому нумерацию начинают с ближайшего к ответвлению конца цепи. Например:
Таким образом, в названии разветвленного алкана корень+суффикс – название нормального алкана
( греч. числительное+суффикс «ан» ),
приставки – цифры и названия углеводородных радикалов .
Пример построения названия:
Другой пример последовательного построения названия по шагам приведен в разделе 2.4.3.
Источник
Способы образования названий алканов греческие числительные
- Главная
- Обучение
- Предварительный просмотр
- Мероприятия / ВИШР
- Обучение
- Тренажер ЕГЭ
- Учебные пособия
- Игры
- 120 лет ТПУ. Викторина онлайн
- Университетские субботы
- Высшая инженерная школа России
Химия
3.3. Классификация органических веществ. Номенклатура органических веществ (тривиальная и международная)
Номенклатура алканов. Рациональная номенклатура
Первые четыре алкана названы метан, этан, пропан и бутан. Эти названия наряду с названиями изобутан, неопентан считаются случайными или тривиальными. Начиная с пятого члена ряда названия алканов происходят от названия греческих числительных, обозначающих число атомов углерода в молекуле с добавлением общего для всего гомологического ряда алканов окончания –ан, например: С5 – пентан, С8 – октан и т. д.
Приставка н- (н-пентан) используется для обозначения неразветвленных алканов независимо от величины; приставка изо- для алканов с шестью или менее атомами углерода, имеющих только одну метильную группу у второго по счету атома углерода (СН3)2СН–, например изогексан:
Приставка нео- используется, если в составе молекулы присутствует группировка (СН3)3С– на конце неразветвленной прямой цепи, например неогексан:
Существует два способа составления названий алканов: по рациональной номенклатуре и систематической (IUPAC) номенклатуре.
Рациональная номенклатура
Исторически первой возникла рациональная номенклатура. Для алканов её называют метановой. За основу названия любого алкана принимают метан, в котором один или несколько атомов углерода замещены алкильными группами. (названия алкильных групп см.в разд.1.2)
Название алкана начинается с перечисления алкильных групп в порядке в порядке усложнения структуры, если имеется несколько одинаковых радикалов, то число их указывается с помощью приставок- числительных: ди (две)-, три (три)-, тетра (четыре)-; заканчивается название словом «метан». Например:
Источник
Номенклатура алканов
1. Свою номенклатуру имеют радикалы (углеводородные радикалы)
Алкан
— ан
С n H 2n+2
Радикал (R)
— ил
С n H 2n+1
Важнейшие радикалы ряда алканов
2. Число одинаковых заместителей указывают при помощи множительных приставок :
Для названия предельных углеводородов применяют в основном систематическую (международная номенклатура IUPAC) и рациональную номенклатуры
I. По рациональной номенклатуре алканы рассматривают как производные простейшего углеводорода — метана, в молекуле которого один или несколько водородных атомов замещены на радикалы. Эти заместители (радикалы) называют по старшинству (от менее сложных к более сложным). Если эти заместители одинаковые, то указывают их количество. В основу названия включают слово «метан»:
II. Систематическая номенклатура
Правила систематической номенклатуры:
В формуле молекулы алкана выбираем главную цепь — самую длинную.
Э ту цепь нумеруем с того края , к которому ближе и больше разветвлена углеродная цепь . Если заместителей несколько, то поступают так, чтобы цифры, указывающие их положение, были наименьшими . Заместители перечисляем по старшинству в гомологическом ряду (мелил, этил и т.д.) .
Называем углеводород: вначале указываем (цифрой) место расположения заместителя, затем называем этот заместитель (радикал). Если при данном атоме находятся несколько заместителей, то соответствующий номер в названии повторяется столько раз, сколько одинаковых заместителей через запятую ( например, 2,2-ди метил; 2,3,4-триметил ). После номера через дефис указывают количество заместителей (ди — два, три — три, тетра — четыре, пента — пять) и название заместителя (метил, этил, пропил). Затем без пробелов и дефисов — название главной цепи. Главная цепь называется, как углеводород — член гомологического ряда метана (метан, этан, пропан и т. д.), её название определяется количеством атомов углерода в её составе: если углеродных атомов в главной цепи 4 , то оканчивается название словом бутан , если пять — пентан и т.д.
Запомните! Сколько радикалов в формуле — столько цифр в названии! Цифры от слов в названии отделяют дефисом, а друг от друга запятыми.
Источник
Алканы
Алканы – это предельные углеводороды, содержащие только одинарные связи между атомами С–С в молекуле, т.е. содержащие максимальное количество водорода.
Гомологический ряд алканов
Все алканы — вещества, схожие по физическим и химическим свойствам, и отличающиеся на одну или несколько групп –СН2– друг от друга. Такие вещества называются гомологами, а ряд веществ, являющихся гомологами, называют гомологическим рядом.
Самый первый представитель гомологического ряда алканов – метан CH4. , или Н–СH2–H.
Продолжить гомологический ряд можно, последовательно добавляя группу –СН2– в углеводородную цепь алкана.
| Название алкана | Формула алкана |
| Метан | CH4 |
| Этан | C2H6 |
| Пропан | C3H8 |
| Бутан | C4H10 |
| Пентан | C5H12 |
| Гексан | C6H14 |
| Гептан | C7H16 |
| Октан | C8H18 |
| Нонан | C9H20 |
| Декан | C10H22 |
Общая формула гомологического ряда алканов CnH2n+2.
Первые четыре члена гомологического ряда алканов – газы, C5–C17 – жидкости, начиная с C18 – твердые вещества.
Все алканы легче воды, не растворимы в воде и не смешиваются с ней.
Строение алканов
В молекулах алканов встречаются химические связи C–H и С–С.
Связь C–H ковалентная слабополярная, связь С–С – ковалентная неполярная. Это одинарные σ-связи. Атомы углерода в алканах образуют по четыре σ-связи. Следовательно, гибридизация атомов углерода в молекулах алканов – sp 3 :

При образовании связи С–С происходит перекрывание sp 3 -гибридных орбиталей атомов углерода:

При образовании связи С–H происходит перекрывание sp 3 -гибридной орбитали атома углерода и s-орбитали атома водорода:

Четыре sp 3 -гибридные орбитали атома углерода взаимно отталкиваются, и располагаются в пространстве так, чтобы угол между орбиталями был максимально возможным.
Поэтому четыре гибридные орбитали углерода в алканах направлены в пространстве под углом 109 о 28′ друг к другу:

Это соответствует тетраэдрическому строению молекулы.
| Например, в молекуле метана CH4 атомы водорода располагаются в пространстве в вершинах тетраэдра, центром которого является атом углерода |


Молекулам линейных алканов с большим числом атомов углерода соответствует зигзагообразное расположение атомов углерода.
| Наример, пространственное строение н-бутана — зигзагообразное |
Изомерия алканов
Структурная изомерия
Для алканов характерна структурная изомерия – изомерия углеродного скелета.
Структурные изомеры — это соединения с одинаковым составом, которые отличаются порядком связывания атомов в молекуле, т.е. строением молекул.
Изомеры углеродного скелета отличаются строением углеродного скелета.
| Например. Для н-бутана (алкана с линейной цепью) существует изомер с разветвленным углеродным скелетом – изобутан |
| Бутан | Изобутан |
 |  |
С увеличением числа атомов углерода в молекуле увеличивается количество изомеров, соответствующих данной формуле.
Количество изомеров в ряду алканов:
| Молекулярная формула | Число структурных изомеров |
| CH4 | 1 |
| C2H6 | 1 |
| C3H8 | 1 |
| C4H10 | 2 |
| C5H12 | 3 |
| C6H14 | 5 |
| C7H16 | 9 |
| C8H18 | 18 |
| C9H20 | 35 |
| C10H22 | 75 |
Оптическая изомерия
Если атом углерода в молекуле связан с четырьмя различными заместителями (атомами или атомными группами), например:
то возможно существование двух соединений с одинаковой структурой, но различным пространственным строением.Молекулы таких соединений относятся друг к другу, как зеркальные изображение и предмет. При этом никаким вращением нельзя получить одну молекулу из другой.
Номенклатура алканов
В названиях алканов используется суффикс -АН.
| Например, алкан имеет название 2-метилпропан. Для простейших алканов (метан, этан, пропан, бутан и изобутан) используют тривиальные названия. Начиная с пятиатомного углероводорода, в названии неразветвленных (нормальных) алканов используют корень, который показывает число атомов углерода в молекуле, и добавляют соответствующий суффикс (для алканов – ан, для алкенов – ен, и т.д.). Название разветвленных алканов строится по следующим правилам: 1. Выбирают главную углеродную цепь. При этом считают, что углеводородные радикалы, которые не входят в главной цепь, являются в ней заместителями. При этом главная цепь должна быть самой длинной. Например, в молекуле на рисунке главной является цепь, отмеченная на рисунке а:
Главная цепь должна быть самой разветвленной. Например, в молекуле, изображенной на рисунках а и б, выделены цепи с одинаковым числом атомов углерода. Но главной будет цепь, изображенная на рисунке а, т.к. от нее отходит 2 заместителя, а от цепи на рисунке б – только один:
2. Нумеруют атомы углерода в главной цепи так, чтобы атомы углерода, которые соединены с заместителями, получили минимальные возможные номера. Причем нумерацию следует начинать с более близкого к старшей группе конца цепи. 3. Называют все радикалы, указывая впереди цифры, которые обозначают их расположение в главной цепи. Например, 2-метилпропан:
Для одинаковых заместителей эти цифры указывают через запятую, при этом количество одинаковых заместителей обозначается приставками ди- (два), три- (три), тетра- (четыре), пента- (пять) и т.д. Например, 2,2-диметилпропан или 2,2,3-триметилпентан. 4. Названия заместителей со всеми приставками и цифрами располагают в алфавитном порядке. Например: 2,2-диметил-3-этилпентан. 5. Называют главную углеродную цепь, т.е. соответствующий нормальный алкан. Например, название молекулы на рисунке:
Химические свойства алкановАлканы – предельные углеводороды, поэтому они не могут вступать в реакции присоединения. Для предельных углеводородов характерны реакции: Разрыв слабо-полярных связей С – Н протекает только по гомолитическому механизму с образованием свободных радикалов. Поэтому для алканов характерны только радикальные реакции. Алканы устойчивы к действию сильных окислителей (KMnO4, K2Cr2O7 и др.), не реагируют с концентрированными кислотами, щелочами, бромной водой. 1. Реакции замещенияВ молекулах алканов связи С–Н более доступны для атаки другими частицами, чем менее прочные связи С–С. 1.1. ГалогенированиеАлканы реагируют с хлором и бромом на свету или при нагревании. При хлорировании метана сначала образуется хлорметан:
При хлорировании алканов с углеродным скелетом, содержащим более 3 атомов углерода, образуется смесь хлорпроизводных.
Бромирование протекает более медленно и избирательно.
|

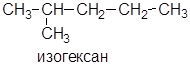
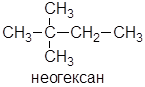









 Хлорметан может взаимодействовать с хлором и дальше с образованием дихлорметана, трихлорметана и тетрахлорметана:
Хлорметан может взаимодействовать с хлором и дальше с образованием дихлорметана, трихлорметана и тетрахлорметана:

























