Коллоидные растворы (золи) Методы получения
Коллоидные системы по степени дисперсности занимают промежуточное положение между грубодисперсными системами и истинными растворами. Поэтому их можно получать двумя путями:
а) методами диспергирования – дроблением более крупных частиц до коллоидной степени дисперсности – механическим, электрическим, ультразвуком, пептизацией (превращение осадков в коллоидный раствор под влиянием химических веществ – пептизаторов);
б) методами конденсации – укрупнением частиц в агрегаты коллоидной степени дисперсности (получение нерастворимых веществ в результате реакций различных типов);
в) ультрафильтрацией через полупроницаемые мембраны.
Строение коллоидных частиц
Образование нерастворимого вещества в результате химической реакции – это лишь одно из условий получения коллоидного раствора. Другим не менее важным условием является неравенство исходных веществ, взятых в реакцию. Следствием этого неравенства является ограничение роста величины частиц коллоидах растворов, которое привело бы к образованию грубодисперсной системы.
Механизм образования коллоидной частицы рассмотрим на примере образования золя иодистого серебра, который получается при взаимодействии разбавленных растворов азотнокислого серебра и йодистого калия.
Ag + + NO3 ¯ +K + + I ¯ = AgI ↓ + NO3 ¯ + K +
Нерастворимые нейтральные молекулы йодистого серебра образуют ядро коллоидной частицы.
Сначала эти молекулы соединяются в беспорядке, образуя аморфную, рыхлую структуру, которая постепенно превращается в высокоупорядоченную кристаллическую структуру ядра. В рассматриваемом нами примере ядро это кристаллик йодистого серебра, состоящий из большого числа (m) молекул AgI:
m[Agl] — ядро коллоидной частицы
На поверхности ядра происходит адсорбционный процесс. По правилу Пескова-Фаянса, на поверхности ядер коллоидных частиц адсорбируются ионы, входящие в состав ядра частицы, т.е. адсорбируются ионы серебра (Аg + ) или ионы иода (I – ). Из этих двух видов ионов адсорбируютcя те, которые находятся в избытке.
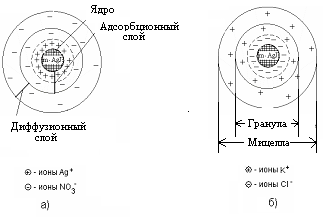
Так, если получать коллоидный раствор в избытке йодистого калия, то адсорбироваться на частицах (ядрах) будут ионы иода, которые достраивают кристаллическую решетку ядра, естественно и прочно входя в его структуру. При этом образуется адсорбционный слой, который придает ядру отрицательный заряд:
Ионы, адсорбирующиеся на поверхности ядра, придавая ему соответствующий заряд, называются потенциалобразующими ионами.
При этом в растворе находятся и противоположно заряженные ионы, их называют противоионами. В нашем случае это ионы калия (K + ), которые электростатически притягиваются к заряженному ядру (величина заряда может достигать I в). Часть противоионов К + прочно связывается электрическими и адсорбционными силам и и входит в адсорбционный слой. Ядро с образовавшимся на нем двойным адсорбционным слоем ионов называется гранулой.
Оставшаяся часть противоионов (обозначим их числом «х К + «) образует диффузный слой ионов.
Ядро с адсорбционным и диффузным слоями называется мицеллой:
При пропускании постоянного электрического тока через коллоидный раствор гранулы и противоионы двинутся к противоположно заряженным электродам соответственно.
Наличие одноименного заряда на поверхности частиц золей является важным фактором его устойчивости. Заряд препятствует слипанию и укрупнению частиц. В устойчивой дисперсной системе частицы удерживаются во взвешенном состоянии, т.е. не происходит выпадения в осадок коллоидного вещества. Это свойство золей называется кинетической устойчивостью.
Строение мицелл золя иодистого серебра, полученного в избытке AgNO3, представлено на рис. 1а, в избытке KCI — 1б.
Рис.1.5. Строение мицелл золя иодистоого серебра, полученного в избытке:
а) азотнокислого серебра; б) хлорида калия.
Источник
Получение коллоидных растворов



Гидрофобными золями являются золи благородных металлов, малорастворимых в воде гидроксидов, карбонатов, сульфатов и др. Переход свежеосажденного осадка в золь называется пептизацией.
Коллоидные растворы (золи) образуются при распределении в дисперсионной среде малорастворимых веществ дисперсной фазы. Они состоят из частиц очень малых размеров, поэтому суммарная поверхность всех частиц S очень велика. В системе возникает огромная свободная поверхностная энергия GS = σS. В соответствии со вторым началом термодинамики такие системы термодинамически неустойчивы; в них самопроизвольно протекают процессы, направленные на снижение поверхностной энергии (GS
Таким образом, для образования устойчивых лиофобных коллоидных растворов необходимо выполнение следующих условий: 1) малая растворимость дисперсной фазы в дисперсионной среде; 2) определенные размеры частиц дисперсной фазы (10 -9 — 10 -7 м); 3) наличие в системе стабилизатора.
При выполнении этих условий в коллоидном состоянии можно получить любое вещество. Первое условие выполняется правильным выбором растворителя. Если вещество хорошо растворимо в данном растворителе, то самопроизвольно получается истинный раствор, однако при использовании растворителя, в котором оно плохо растворимо, можно получить коллоидный раствор. Например, при растворении в воде хлорида натрия всегда получается истинный раствор, однако введение хлорида натрия в бензол, где он плохо растворим, может привести к образованию коллоидного раствора. И наоборот, невозможно получить коллоидный спиртовой раствор канифоли, поскольку она хорошо растворима в спирте, однако при определенных условиях образуется коллоидный раствор канифоли в воде, где она растворима плохо.
Второе условие — получение частиц определенного размера — можно выполнить разными способами. Поскольку коллоидные растворы по размерам частиц дисперсной фазы занимают промежуточное положение между грубодисперсными системами и истинными растворами, коллоидные частицы можно получить двумя путями: 1) измельчением крупных частиц до размеров коллоидных — диспергационные методы; 2) объединением молекул и ионов в истинных растворах в более крупные коллоидные частицы — конденсационные методы.
ИстинныйКоллоидный Грубодисперсная
раствор ¾¾¾¾¾¾® раствор¾¾¾¾¾¾ система
d -9 м конденсирование 10 -9 -7 м диспергирование d>10 -7 м
Конденсационные методы получения коллоидных растворов делят на физические и химические. Основным физическим методом служит замена растворителя. Если приготовить истинный раствор канифоли в спирте и добавлять его к воде, в которой канифоль очень плохо растворима, то вследствие понижения растворимости молекулы канифоли конденсируются в частицы коллоидных размеров. При необходимости спирт можно удалить нагреванием.
При химической конденсации для получения коллоидных растворов используют реакции, приводящие к образованию малорастворимых соединений, например:
Эти реакции надо проводить при избытке одного из реагентов, который выполняет роль стабилизатора образующихся коллоидных частиц.
Диспергационные методы весьма разнообразны. Чаще всего используют:
— механическое дробление с помощью шаровых и коллоидных мельниц в присутствии жидкой дисперсионной среды и стабилизатора;
— ультразвуковое измельчение под действием ультразвуковых колебаний на смесь нерастворимого вещества и растворителя;
— электрическое диспергирование, при котором с помощью электрической дуги, возникающей между двумя электродами, опущенными в воду, получают золи металлов;

— химическое диспергирование (пептизация), которое заключается в химическом воздействии на осадок.
Коллоидные растворы, полученные одним из этих методов, содержат примеси растворенных низкомолекулярных веществ и грубодисперсных частиц, наличие которых снижает устойчивость полученных систем. Для очистки коллоидных растворов от примесей используют:
— фильтрацию через обычные бумажные фильтры; коллоидные растворы проходят через их поры, а примеси грубодисперсных частиц задерживаются фильтром;
— диализ — удаление низкомолекулярных соединений с помощью мембран, пропускающих молекулы и ионы малого размера и задерживающих коллоидные частицы и макромолекулы большого размера (рис.21а); малые молекулы и ионы диффундируют через мембрану в непрерывно заменяемый растворитель и удаляются от диализируемого коллоидного раствора;
— электродиализ, при котором для увеличения скорости диализа создают постоянно электрическое поле, способствующее движению ионов из коллоидного раствора в растворитель (рис.21б);









 |
 |









 |















 |  |
Рис.21. Схема диализатора (а) и электродиализатора (б):
1 — диализируемый раствор; 2 — поток растворителя;
3 — диализная мембрана; 4 — мешалка; 5 — электроды.
— компенсационный диализ, который применяют для удаления не всех присутствующих низкомолекулярных веществ, а только их части; вместо чистого растворителя применяют раствор низкомолекулярных веществ, которые необходимо оставить в коллоидной системе, при этом диффундируют через мембрану в этот раствор все ионы кроме тех, которые в нем содержатся;
— ультрафильтрация — продавливание разделяемой смеси под давлением через фильтры с узкими порами, пропускающими только молекулы и ионы низкомолекулярных веществ.
Непременным условием получения устойчивого коллоидного раствора является наличие в нем стабилизатора. Роль стабилизатора могут выполнять: избыток одного из реагентов, используемых для получения вещества дисперсной фазы, ПАВ, белки, полисахариды и другие вещества.
Источник