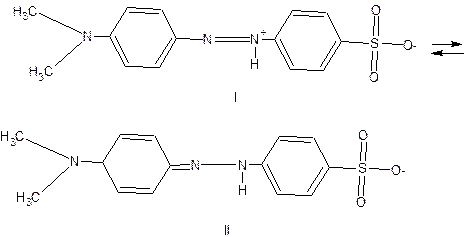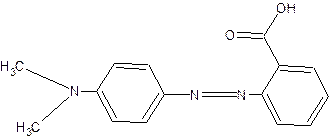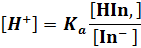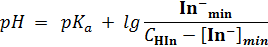Способы обнаружения точки эквивалентности. Кислотно-основные индикаторы. Интервал перехода индикатора. Выбор индикатора. Ошибки титрования.
Способы фиксирования точки эквивалентности в методе кислотно-основного титрования основаны на использовании резкого изменения pH вблизи точки эквивалентности. Определить точку эквивалентности можно двумя способами 1) визуально (индикаторный способ) и 2) инструментально (потенциометрическое, кондуктометрическое, спектрофотометрическое и другие виды титрования). При визуальном определении применяют кислотно-основные индикаторы, представляющие собой слабые органические кислоты или основания, окраска которых изменяется при изменении pH среды.
Индикаторы — это слабые органические кислоты, у которых недиссоциированные молекулы, и образуемые ими ионы имеют различную окраску. Поэтому они носят общее название кислотно-основных индикаторов. Индикаторы, обладающие свойством присоединения протонов, называют основным индикаторами. Такие индикаторы диссоциируют по схеме: IndOH+H+=Ind++H2O.
Индикаторы, обладающие свойством отдавать протоны, называют кислотными индикаторами. Молекула такого индикатора играет роль донора протона, то-есть дает при диссоциации катион H+ и анион Ind-. Перемена окраски у индикаторов — результат изменений в их внутреннем строении. У одноцветных индикаторов это связано с появлением или исчезновением хромофоров. У двухцветных индикаторов эти изменения обусловлены превращением одних хромофоров в другие.
Типичный одноцветный индикатор — фенолфталеин. При pH 4,5 жёлтую окраску. Объясняется это тем, что азот в индикаторе обладает свойством присоединять катионы водорода кислоты и превращаться в ион красного цвета. Таким образом, при действии кислот наблюдается переход жёлтой окраски индикатора в красную. Переход из одной формы индикаторов в другую происходит под действием Ионов H+ и OH-, поскольку одна из форм индикатора является слабой органической кислотой или слабым основанием. Выбор индикатора. Интервал перехода окраски выбранного индикатора должен по возможности совпадать со скачком pH, наблюдаемым в данной системе. При выборе индикатора сначала вычисляют область pH раствора, в которой наблюдается скачок pH, а затем подбирают такой индикатор, у которого интервал перехода окраски совпадает с вычисленным скачком pH. Тип ошибки Условия возникновения ошибки Ошибки титрования:
Водородная- Недотитрованная сильная кислота сильным основанием (проба, в которой не достигнута точка эквивалентности и вещество пробы находится в избытке)
Гидроксидная— Недотитрованное сильное основание сильной кислотой
Кислотная -Недотитрованная слабая кислота сильным основанием
Основная -Недотитрованное слабое основание сильной кислотой
Перетитрованное сильное основание сильной кислотой (проба, в которой находится избыток титранта)
Перетитрованная сильная кислота сильным основанием
Поможем написать любую работу на аналогичную тему
Способы обнаружения точки эквивалентности. Кислотно-основные индикаторы. Интервал перехода индикатора. Выбор индикатора. Ошибки титрования.
Способы обнаружения точки эквивалентности. Кислотно-основные индикаторы. Интервал перехода индикатора. Выбор индикатора. Ошибки титрования.
Способы обнаружения точки эквивалентности. Кислотно-основные индикаторы. Интервал перехода индикатора. Выбор индикатора. Ошибки титрования.
Источник
Способы обнаружения точки эквивалентности
Индикаторы. Для фиксирования конца титрования используют визуальные (титрование с индикатором, цветным или флуоресцентным) и инструментальные методы (потенциометрическое, амперометрическое, фотометрическое титрование). Цветные индикаторы в кислотно-основном титровании — это слабые органические кислоты и основания, протониро-ванные и непротонированные формы которых различаются по структуре и окраске. Существуют одноцветные (например, фенолфталеин) и двухцветные (например, метиловый оранжевый) индикаторы.
Изменение окраски индикатора связано с таутомерией органических молекул, содержащих хромофор. Такие соединения обладают подвижными электронами, и в зависимости от распределения электронной плотности молекуле можно приписать несколько структур; предельные структуры называются таутомерами. На распределение электронной плотности влияет наличие ауксохромных групп (например, 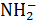
Цепь сопряжения в таутомере II, а следовательно, и подвижность π-электронов увеличивается, в результате энергия возбуждения молекулы уменьшается и свет поглощается в красной области спектра. Метиловый оранжевый — двухцветный индикатор. Он относится к классу азоинди-каторов, имеющих в кислой среде красную, а в щелочной среде желтую окраску. Сюда относятся также метиловый красный.
Однако существуют соединения, не содержащие хромофоров, у которых под влиянием среды структура изменяется так, что появляются хромофорные группы. Таковы фталеины. Например, фенолфталеин в кислой среде бесцветен. В щелочной среде в результате перераспределения электронной плотности в его молекуле образуется хиноидная структура (хромофор), находящаяся в равновесии со своей таутомерной формой. Вещество приобретает красную окраску.
Группу индикаторов, схожую с фталеинами, составляют сулъфофталеины: бромкрезоловый зеленый, феноловый красный, тимоловый синий и другие соединения. Например, в растворе фенолового красного в равновесии находятся красная и желтая формы.
Отдельную группу составляют трифенилметановые красители: кристаллический фиолетовый, метиловый фиолетовый, малахитовый зеленый и др.
Известно большое число разных кислотно-основных индикаторов, сведения о которых есть в литературе
| Индикатор | Область пе- | pKa | Изменение окраски |
| рехода рН | (I=0) | ||
| Метиловый фиолетовый | 0-1,8 | — | Желтая — фиолетовая |
| Тимоловый синий | 1,2—2,8 | 1,65 | Красная — желтая |
| Метиловый оранжевый | 3,1-4,4 | 3,36 | Красная — желтая |
| Бромкрезоловый зеленый | 3,9—5,4 | 4,90 | Желтая — синяя |
| Метиловый красный | 4,4-6,2 | 5,00 | Красная — желтая |
| Бромтимоловый синий | 6,0—7,6 | 7,3 | Желтая — синяя |
| Феноловый красный | 6,4—8,2 | 8,00 | Желтая — красная |
| Тимоловый синий | 8,0—9,6 | 9,20 | Желтая— синяя |
| Фенолфталеин | 8,2—9,8 | 9,53 | Бесцветная — красная |
| Тимолфталеин | 9,3—10,5 | 9,6 | Бесцветная — синяя |
| Ализариновый желтый______ | 9,7—10,8 | — | Желтая — красная |
Из константы кислотности индикатора, пренебрегая влиянием ионной силы и побочными взаимодействиями, получаем
Схематически равновесие в растворе индикатора можно представить как кислотно-основную реакцию
HIn + H20= In — + H3O +
Человеческий глаз воспринимает окраску одной из форм при определенной концентрации ее в растворе. Для двухцветного индикатора присутствие одной из форм заметно, если концентрация ее в несколько раз превышает концентрацию другой формы. Пусть глаз замечает форму In — при 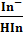
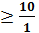
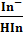
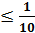
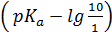
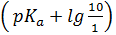
Очевидно, что, если глаз улавливает окраску одной из форм на фоне другой при большем или меньшем соотношении, 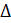
Для одноцветных индикаторов при изменении рН нарастает или уменьшается концентрация окрашенной формы. При определенной концентрации глаз замечает появление или исчезновение окраски. Пусть окрашенная форма 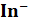
Как видно, рН появления окраски зависит от концентрации индикатора в растворе.
К индикаторам предъявляют ряд требований.
1. Индикатор должен обладать высоким светопоглощением так, чтобы окраска даже его небольшого количества была заметна для глаза. Большая концентрация индикатора может привести к расходу на него титранта.
2. Переход окраски должен быть контрастным.
3. Область перехода окраски должна быть как можно уже.
Середина области перехода окраски индикатора (при этом рН = рКа) называется показателем индикатора (рТ) и фактически отождествляется с конечной точкой титрования. Выбирают индикатор для титрования так, чтобы область перехода входила в скачок титрования. Границы скачка титрования определяются заданной точностью. Чем жестче требования к точности титрования, тем уже скачок, тем более ограничен выбор индикатора.
Для сужения области перехода окраски и увеличения контрастности применяют смешанные индикаторы, которые составляют из индикатора и красителя. При определенном значении рН цвет красителя является дополнительным к цвету индикатора — в результате в этой точке окраска будет серой, а переход от окрашенного раствора к серому — контрастным.
На область перехода окраски индикатора (положение и интервал) влияют все факторы, от которых зависит константа равновесия (ионная сила, температура, посторонние вещества, растворитель), а также концентрация индикатора.
Ионная сила по-разному влияет на индикаторы разных групп в зависимости от того, заряженной или незаряженной является кислотная или щелочная форма:
где
Погрешности титрования.
При титровании возможны случайные и систематические погрешности (ПТ). Случайные погрешности связаны с измерением объема и массы навески, систематические — с несовпадением ТЭ и конца титрования.
Случайные погрешностиобрабатываются по законам математической статистики. Они тем меньше, чем больше индекс крутизны кривой титрования, поскольку стандартное отклонение объема титранта sT связано с крутизной соотношением
где s ( V ) — стандартное отклонение объема в конечной точке титрования.
Индекс крутизны при титровании слабых электролитов меньше, чем при титровании сильных, поэтому случайные погрешности в последнем случае имеют меньшие значения.
Систематические погрешностимогут быть положительными (пере-титровывание) и отрицательными (недотитровывание).
Для оценки систематической погрешности можно воспользоваться графическим и расчетным способами.
Графический способявляется лишь ориентировочным. Опустим перпендикуляр из точки с ординатой рТ на ось абсцисс. Отрезок между полученным значением f и f в ТЭ и есть погрешность титрования.
При расчетном способепогрешность вычисляют, используя формулы , связывающие рН и f. При недотитровьшании ПT=-(1- f), при
перетитровывании ПТ = f -1. При титровании сильных кислот, для которых
Источник
Физико-химические методы обнаружения точки эквивалентности

Физико-химические методы обнаружения точки эквивалентности
- Методы обнаружения точек физической и химической эквивалентности Использование цветовых индикаторов является широко распространенным и простым, но это не единственный способ определения эквивалентности.
- Наряду с цветом используются также флуоресцентные и хемилюминесцентные индикаторы. Различные физико-химические методы также были использованы и были очень успешными.
Потенциометрия, измерение проводимости, фотометрия, измерение температуры и т. Д. Людмила Фирмаль
- С помощью потенциометрических измерений вы можете отслеживать изменения pH. В течение всего процесса титрования, экспериментально получать кривые титрования и определять точки эквивалентности по скачкам pH.
Во время кислотно-основных реакций электропроводность раствора существенно изменяется, поэтому во многих случаях измерения проводимости используются для определения точки эквивалентности. Кислотно-основной метод эффективно использует фотометрическое и температурное титрование.
Физико-химические методы коррекции эквивалентности описаны в части 2 учебника. Людмила Фирмаль





















































Образовательный сайт для студентов и школьников
Копирование материалов сайта возможно только с указанием активной ссылки «www.lfirmal.com» в качестве источника.
© Фирмаль Людмила Анатольевна — официальный сайт преподавателя математического факультета Дальневосточного государственного физико-технического института
Источник