- Способы наполнения ампул(шприцевой, вакуумный, пароконденсационный)
- Стадия ампулирования
- Лекарственные формы в ампулах
- Ампулы как сосуды для лекарственных веществ и их изготовление
- Процесс ампулирования
- Современная номенклатура ампулированных растворов и особенности частной технологии некоторых из них
- Шприц-тюбики как форма упаковки инъекционных растворов
- Глазные лекарственные формы
- Глазные капли
- Глазные пленки
Способы наполнения ампул(шприцевой, вакуумный, пароконденсационный)
Шприцевой– с помощью поршневого дозатора или мемрного. Несколько полых игл опускаются внутрь ампул, расположенных на конвейере, происходит их заполнение раствором. Легкоокисляющинся – по принципу газовой защиты. Вначале подается инертный газ и вытесняется воздух, затем наливается раствор, затем снова ин.газ и запайка. Высокая точность дозирования, капилляры не загрязняются-важно для густых и вязких растворов. Недостаток – малая производительность, сложное аппарат оформление.
Вакуумный– в аппаратах, как вакууммоечные.. Кассету с ампулами капиллярами вниз устанавливают внутрь, создают вакуум.-воздух из ампул выходит, и после сброса, р-р заполняет ампулы В емкость подают раствор по трубопроводу, создают расчетное разряжение. Дозирование создается с помощью измеренной глубины разрежения. , предварительно определяют. После наполнения ампул вакуум гасят подачей стерильного фильтрованного воздуха. Достоинство-высокопроизв, минус-не точно, неэкономичный расод р-ра, его загрязнение, вода остается в капиллярах- что приведет к некач. запайке.
Пароконденсационный – ампулы, наполненные паром, опускаются в ванночки-дозаторы, содержащие точно отмерянный объем раствора, капиллярами вниз, за счет конденсации пара внутри ампулы создается вакуум и раствор наполняет их. После наполнения в капиллярах остается раствор, который можно удалить отсасыванием под вакуумом или продавливанием стерильным воздухом или инертным газом.
140. Запайка ампул. Контроль качества ампул. Маркировка. Упаковка. Бракераж ампулированных растворов.
Запайка: а) оплавление кончиков капилляров б) их оттяжка-отпаивание с оттяжкой части капилляра и впроцессе отпайки происходит запаивание. в) электрический нагрев. Оплавление – машина для запайки ампул АП-6М. Ампулы поступают в ячейки трансп. Ленты, ампулы достигают зоны горелок. Начинают вращаться вокруг оси и ,кончик капилляра нагревается, стекло смягчается и само заплавляет отверстие капилляра. Далее в укладчик в кассету. Недостатки оплавления- наплывы,напряжение, трещины
Оттяжка-капилляр разогревается, у вращ-ся ампулы, затем щипцами оттягивается , отпаивается и в отходы, затем горелка подводится для пережога стекл. нити.
Автомат для наполнения и запайки ампул типа 541 осуществляет наполнение шприцевым методом. НА участке запайки с пневматической оттяжкой капилляра ампула, вращается, горелки разогревают участок капилляра в месте запайки, а струи сжатого воздуха оттягивают отпаявшуюся часть. Запаянная ампула по транспортеру подается в приемник..
Амп со взрывоопасн р-рами запаивают электр. нихромовым нагревателем.
сущ-ет запайка пластмассой.
Контроль запайки: 1. ампулы помещают капиллярами вниз. Создают разрежение, из плохо запаянных раствор выливается. 2.Горячие ампулы в ванну с м\с, при резком остывании в ампулах создается разрежение и окраш. р-р поступает внутрь.3. Визуальное наблюдение за свечением газовой среды внутри ампулы под действием высокочастотного эл. Поля.
Бракераж: после запайки и стерилизации ампулы помещают в р-р м\с комн. темп. Если есть трещины, внутрь засасывается краситель.
Контроль на механич.включения: вращают, просматривают на черном фоне для проверки прозрачности и механических включений. На светлом – цвет раствора, отс-ие мех.вкл. черного цвета, целостность свекла. Также используют проекторы, линзы. Мембранно-микроскопические методы, проточные (механические частицы изменяют силу тока, прибор регистрирует микроимпульс).
Стерильность: на тест-микроорганизмах устанавливается наличие или отсутствие антимикробного действия.При обнаружении антимикробного действия используют инактиваторы. Если активатора нет, исп-т метод мембранного фильтрования для отделения антимикробных веществ. Далее растворы высеивают на тест-среды. Просматривают. Если рост хотя бы в 1 пробирке , повторяют испытание.
Маркировка, упаковка. В бункер загружают ампулы и барабаном подачи направляют к офсетному цидиндру, на который подается краска из ванны,на нем вдавлены буквы и цифры. При контакте надпись наносится на ампулу, ампулы передаются на упаковку. М.Б. одновременно маркировка и упаковка.
141. Неводные ампулированные растворы. Номенклатура. Требования к неводным растворителям и их характеристика.
Требования к растворителям: высокая растворяющая способность, химическая чистота, индифферентность, хим.совместимость, устойчивость при хранении, дешевизна. Дополнительные требования: малотоксичные, прозрачные, с небольшой вязкостью, не вызывать раздражения. Класс-ия: жирные масла, спирты, эфиры, амиды, сульфоны и сульфоксиды И их смеси. Номенклатура: гормоны, витамины, мнтибиотики, камфора, барбитураты, сера. Растит.масла: Прозрачные масл. Ж-ти, с запахом, нераств. В воде. Должны быть получены из свежих семян, не содержать влаги. Минусы: высокая вязкость, болезненные ин-ии, плохое рассасывание. Исп-т персиовое, миндальное, оливковое масла и др.. Предварительно стерилизуют. Спирты. Этиловый спирт – растворы гидрокортизона, сердечные гликозиды. Минусы: вызывает анестезию, болезненные уколы. Пропиленгликоль – сульфамиды, барбитураты, витамины а и д, анестезин. Используют смеси с водой. Пролонгирует действие. Глицерин – целанид, дибазол. В смесях с водой или спиртом. ПЭГ – нейтральны, физиологически индифф., растворимы в воде и спирте, устойчивы, не гидролизуются. Обычно исп. ПЭО 400. Р-ры дигоксина, левомицетина. Эфиры: этиловый эфир олеиновой, линолевой кислот и др. Бензилбензоат – для стероидных гормонов. ИСп-т всмеси с персик.маслом. Диоксаны и диоксаланы: солькеталь – стабильная при хранении бесцв. Жидкость. Смешивается с водой и спиртом. Растворы тетрациклина. Амиды: N,N – диметилацетамид – прозр. Нейтр. Жидкость. Р-р Тетрациклина. Сульфоксиды и сульфоны: диметилсульфоксид. НЕзначит.токсичность, смешив-ся со многими растворителями.
142. Природа пирогенных веществ. Пути загрязнения инъекционных растворов пирогенными веществами. Методы обнаружения пирогенных веществ.
Пирогены – липополисахаридные комплексы наружных мембран микроорганизмов, могут быть в виде агрегатов с кальцием или магнием, мицелл. Вызывают лихорадку через 30-60 мин, повышая синтез простагландинов. Термостойки. Попадают из воды при перегонке путем переброски капель воды. В паре их нет.
Обнаружение: хим.-цветные реакции, физ- измерение электропроводности, биологический метод –основан на троекратном измерении т тела тела кролика после в\в введения иссл препарата. повышение на 0.6С и более свидетельствует о наличии пирогенов. Недостатки метода: индивидуальность кролика))) высокие затраты. Лал-тест: чувствительный, быстрее результат, можно определить пироген количественно.В основе реакция гелирования лизата амебоцитов крови подковообразных крабов Лимулюс. Если есть пироген – образуется гель. минус-не определяет грамм отриц бактерии.
143. Требования, предъявляемые к физиологическим и кровозамещающим растворам. Р-ры Рингер-Локка, полиглюкина, реополиглюкина.
Физрастворы – по составу растворенных веществ способны поддерживать жизнедеятельность клеток и органов, не вызывая существенных сдвигов физиологического равновесия в организме.
Рры максим. приближ к плазме крови нз-ся кровезамещающими ж-тями.
Гемодинамические(противошоковые) – для лечения шока, восполнения объема крови. Полиглюкин, реополиглюкин,. Иногда добавляют этанол, бромиды, наркотические в-ва, глюкозу.
Регуляторы водно-солевого баланса и кислотно-щелочного равновесия – коррекция состава крови при обезвоживании, диарее, отеках мозга, токсикозе. Р-ры натрия хлорида, РИнгера, РИнгер-Локка,
Дезинтоксикационные- их компоненты связ-ся с токсинами-гемодез
Для парнт питанияр-р глюкозы 40%,
Еще сущ-ют с функцией переноса крови и полифункциональные.
Требования: апирогенность, стерильность, стабильность, отсутствие мех.вкл. Дополнительно: должны выполнять свои функции, не кумулировать, не повреждать ткани, не нарушать функции органов, быть не токсичными, не вызывать сенсибилизацию и эмболию, не раздражать сосуды. Изотоничность, изоионичность, изогидричность. Вязкость д.б. как у плазмы крови.
Раствор Рингер-Локка: изотонический по отношению к крови водный раствор хлорида натрия, хлорида кальция, однозамещенного карбоната натрия и глюкозы.
№ 1:Раствор NаС1 0,9 % — 500 мл; № 2:Раствор NаНСО3 — 0,2
КС1 — 0,2 Н2О для инъекций до 500,0
Полиглюкин плазмозамещающее, противошоковое. коллоидный раствор полимера глюкозы — декстрана бактериального происхождения, содержащий среднемолекулярную фракцию декстрана, молекулярная масса,обеспечивающего нормальное коллоидно-осмотическое давление крови человека. Препарат представляет собой 6% раствор декстрана в изотон растворе хлорида натрия; рН 4,5-6,5. Выпускают в стерильном виде во флпо 400 мл.
реополиглюкин: Реополиглюкин-10% раствор низкомолекулярного декстрана в изотоническом растворе хлорида натрия. дезагрегирующее действие, ,улучшает реологические свойства крови и микро- циркуляцию.
144. Противошоковые растворы. Растворы специального назначения (гемодез, дисоль, трисоль, ацесоль).
1. Гемодинамечские или противошоковые. для лечения шока, восполнения объема крови. Полиглюкин, реополиглюкин, желатиноль. Иногда добавляют этанол, бромиды, наркотические в-ва, глюкозу.
2. Дезинтоксикационные – для лечения интоксикаций, вызванных ожогами, инфекциями, отравлениями. Компоненты растворов должны связываться с токсинами и быстро выводиться из организма. Р-ры поливинилпирролидона, спирт поливиниловый, гемодез, полидез неогемодез, глюконеодез, энтеродез.
3. Регуляторы водно-солевого баланса и кислотно-щелочного равновесия – коррекция состава крови при обезвоживании, отеках, токсикозе. Р-ры натрия хлорида, Рингера, Рингер-Локка, Петрова, калия хлорида и др.
4. Препараты для парентерального питания. Глюкоза 40%, гидролизат казеина, аминопептид, аминокровин, липидин.
5. Растворы с функцией переноса кислорода – для восстановл дыхат.ф-ии крови.
6. Растворы комплексного действия. Требования:апирогенность, стерильность, стабильность, отсутствие мех.вкл. Дополнительно: должны выполнять свои функции, не кумулировать, не повреждать ткани, не нарушать функции органов, быть не токсичными, не вызывать сенсибилизацию и эмболию, не раздражать сосуды. Изотоничность, изоионичность, изогидричность. Вязкость д.б. как у плазмы крови.
Дисоль: натрия хлорида 6 г, натрия ацетата 2 г, воды до 1 л
Трисоль: натрия хл 5 г, калия хлорида 1 г, натрия гидрокарбоната 4 г, воды до 1 л.
Источник
Стадия ампулирования
Этапы ампулирования:
наполнение ампул раствором;
стерилизация ампулированных растворов;
бракераж ампулированных растворов;
Наполнение ампул раствором
Нормы наполнения ампул устанавливаются Государственной фармакопеей. Для того чтобы обеспечить нужную дозу при наполнении шприца, фактический объем наполнения ампул должен быть больше номинального. Процесс наполнения ампул должен проводиться с соблюдением всех правил асептики в помещениях I класса чистоты.
Существует три способа наполнения ампул:
Вакуумный способ. Аппараты имеют схожую конструкцию и принцип действия с вышеупомянутыми вакуумомоечными. Отличие состоит в том, что в случае наполнения ампул аппараты обеспечивают только продвижение ламинарного потока раствора в ампулы. На производстве чаще других встречается полуавтомат АП-4 М 2.
Пароконденсационный способ чрезвычайно редко встречается на производстве.
Шприцевой способ. Поршневой дозатор посредством нескольких игл, расположенных на конвейере, заполняет ампулы необходимым объемом раствора, для легкоокисляющихся растворов заполнение происходит по принципу газовой защиты. Для проверки точности объема наполнения берется рекомендуемое Государственной фармакопеей количество ампул от партии и в сосудах до 50 мл объем замеряется калибровочным шприцем, 50 мл и более замеряется калибровочными цилиндрами при температуре 202 °С. Объем раствора после вытеснения воздуха и наполнения иглы и мерного цилиндра не должен быть меньше номинального.
Источник
Лекарственные формы в ампулах
В 1885 г. петербургский фармацевт проф. А. В. Пель впервые предложил специальные стеклянные сосуды-ампулы, рассчитанные на разовый прием помещенного в них стерильного раствора лекарственного вещества. С этого времени производство стерильных и асептически приготовленных лекарственных форм получило свое дальнейшее развитие. Основное преимущество ампулирования заключается в том, что оно позволяет приготовлять инъекционные лекарственные формы в запас и притом в дозированном виде. В настоящее время масштабы ампулирования лекарственных форм растут необыкновенно быстро — ежегодный выпуск ампул исчисляется миллиардами штук.
Промышленное изготовление лекарственных форм в ампулах оказывает очень большую помощь аптеке, освобождая ее от изготовления многих прописей и давая возможность немедленно выдать лекарственный препарат по рецепту. На долю аптек остаются только индивидуальные прописи, а также прописи, перевод которых в условиях заводского производства из-за недостаточной массовости нерентабелен. В заводских условиях производство стерильных и асептически приготовленных лекарственных форм в ампулах сосредоточено в особом цехе — ампульном, в специализированных отделениях которого осуществляется проведение отдельных операций.
Ампулы как сосуды для лекарственных веществ и их изготовление
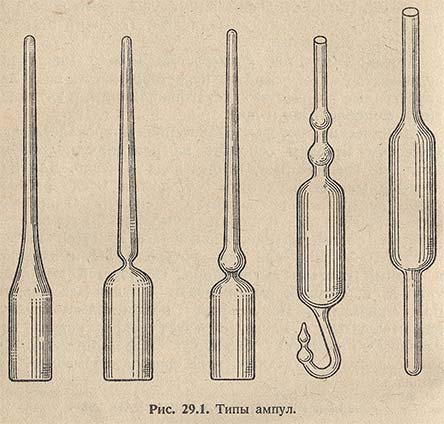
Ампулы представляют собой стеклянные сосуды различной вместимости и формы (рис. 29.1), состоящие из расширенной части — корпуса (пульки), куда помещают лекарственные вещества (в растворе или другой форме), и капилляра, который служит для наполнения и опорожнения ампул. Капилляр запаивается, изолируя таким образом лекарственные вещества, находящиеся в ампуле, от внешнего воздействия. Наиболее распространенными являются ампулы с цилиндрическим корпусом вместимостью от 1 до 10 мл. Наиболее рациональными являются ампулы с перехваченной шейкой, так как жидкость благодаря перехвату не может попасть в оттянутый капилляр, что важно при запаивании и вскрытии ампул. Фармацевтические предприятия могут пользоваться готовыми ампулами, изготовленными стекольными заводами, или выделывают их сами в стеклодувных отделениях, работающих в одном потоке с другими отделениями ампульного цеха.
Стекло представляет собой твердый раствор, полученный в результате охлаждения расплавленной смеси силикатов и оксидов металлов и обладающий механическими свойствами твердых тел. В состав стекла входят различные оксиды SiO, К2O, CaO, MgO, В2O3, Al2O3. Особенно большая роль в фармацевтическом производстве принадлежит силикатным стеклам, т. е. стеклам, полученным на основе кремнезема. Вводя в состав этих стекол определенные оксиды, получают стекла с заранее заданными физико-химическими свойствами, в том числе специальные сорта (марки) ампульного стекла: НС-1, НС-2, НС-3 (нещелочные стекла — марки 1, 2, 3) и АБ (безборное стекло).
К наиболее важным показателям качества стекла относится его химическая стойкость. Ампульное стекло НС-3 как содержащее относительно большее количество В2O3 (6%) при наименьшем содержании щелочных оксидов (8,5%) является наиболее химически стойким. Стекло марки АВ-1 как не содержащее оксиды бора и содержащее наибольшее количество оксидов щелочных металлов (14,5%) является наименее химически стойким.
Химическая устойчивость характеризует сопротивляемость стекол разрушающему действию агрессивных сред. На стекло воздействуют различные химические агенты, растворяя его составные части и вызывая коррозию. Одним из самых вредных агентов для стекла является вода, переводящая силикаты в щелочи и создающая благодаря этому затруднения при изготовлении многих инъекционных растворов. Способность воды растворять отдельные составные части стекла начинает проявляться уже в первые минуты контакта водного раствора со стеклом даже при комнатной температуре и усиливается при хранении. Стерилизация оказывает очень сильное влияние на устойчивость стекла и вызывает сдвиг pH.
Явления, происходящие в результате воздействия различных водных растворов на стекло ампул, станут понятными, если учесть, что поверхностный слой стекла всегда насыщен ионами щелочных и щелочноземельных металлов. По этой причине ион натрия даже при комнатной температуре может замещаться другими ионами. Ионы щелочных металлов легко перемещаются из внутренних слоев стекла на место ионов, вступивших в реакцию.
При воздействии на стекло растворов кислот происходит нейтрализация щелочи, причем, если раствор содержит относительно много кислоты (pH 3,0 и ниже), то выщелачивание поверхности стекла происходит без заметного изменения концентрации водородных ионов. Если же на стекло действуют растворы с pH выше 3,0 и вода, то реакция нейтрализации весьма заметно отражается на концентрации водородных ионов, и pH резко возрастает. При воздействии растворов кислот и воды реакции выщелачивания сопровождаются образованием на поверхности стекла кремнеземистой пленки.
Щелочные растворы, воздействуя на поверхность стекла, смывают его поверхностный слой, разрывая при этом связи Si — О — Si и приводя к образованию групп Si — О — Na. В результате такого воздействия самый верхний слой стекла полностью переходит в раствор, подвергается гидролизу и приводит к увеличению pH раствора.
Вещества, растворенные в воде, воздействуют на стекло в зависимости от своих свойств. Соли сильных оснований и слабых кислот, отщепляющие при гидролизе щелочи, действуют аналогично щелочам. Соли слабых оснований и сильных кислот действуют так же, как кислоты, ибо гидролизуются с образованием кислот. При выщелачивании в раствор выделяется чистый кремнезем, который в виде тончайшей взвеси находится в растворе и может оказать вредное воздействие на организм. Кремнеземистая пленка также может отделяться и загрязнять раствор. Продукты выщелачивания в свою очередь могут воздействовать на лекарственные вещества, растворы которых омывают стекло.
В свете сказанного становится ясным, почему при оценке качества ампульного стекла на заводах проверяют прежде всего его химическую стойкость. Для этого отобранные ампулы промывают горячей водой, дважды ополаскивают дистиллированной водой, наполняют свежеперегнанной дистиллированной водой (pH 6,0 ±0,2) до номинальной вместимости и запаивают. Ампулы автоклавируют в течение 30 мин при давлении 2 ата, а затем после их охлаждения определяют при помощи рН-метра сдвиг pH воды, извлеченной из ампул, по отношению к pH исходной дистиллированной воды. Сдвиг pH должен быть выше 4.5 для ампул, изготовленных из стекла марки АБ-1 и 1,8 для марки НС-3.
Производство ампул (вместилища). Ампулы изготавливают из стеклянных трубок длиной около 1.5 м, называемых дротами. До изготовления ампул дрот калибруют (сортируют) по внешнему диаметру и толщине стенок для того, чтобы все ампулы изготовляемой серии имели одинаковую вместимость. Дрот сортируется на семь групп по номинальной вместимости изготовляемых ампул (1, 2, 5, 10, 20, 25, 50 мл).
После калибровки стеклодрот отмывается от механических загрязнений, что в значительной степени облегчит последующую промывку ампул перед их наполнением. Промывка осуществляется в герметически закрывающихся цилиндрических камерах, в которых вертикально стоящие пучки дрота замачиваются в горячей воде (с использованием моющих средств), затем душируются горячей водой и под конец горячей дистиллированной водой. По окончании промывки в камеру подают профильтрованный подогретый воздух для сушки дрота.
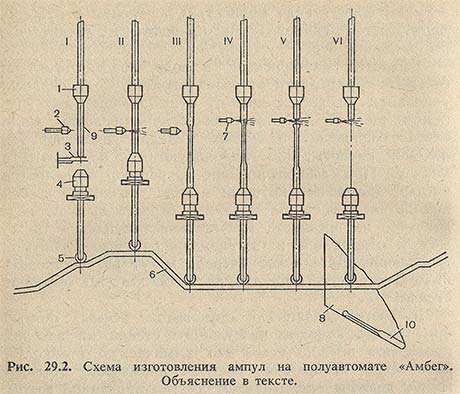
Ампулы всех размеров изготовляются на карусельных полуавтоматах, которые работают по следующей принципиальной схеме (рис. 29.2): в верхний патрон (1) вставляется дрот (9), который в позиции I опускается до ограничителя длины (3). Нижний патрон (4), опираясь на шток и ролик (5), двигается по копиру (6). В позиции II нижний патрон зажимает конец дрота, который, вращаясь вокруг своей оси, разогревается в пламени горелки (2) до размягчения. В Позиции III горелки (2) тушатся, патрон опускается и растягивает трубку, образуя капилляр, В позиции IV зажигаются горелки (7), дающие острое пламя, которое отрезает капилляр, одновременно запаивая дно следующей ампулы (позиция V). После этого разжимается патрон (4) и готовая ампула (10) выпадает (позиция VI) на приемный лоток (8). Далее по поднимающемуся копиру патрон (4) вновь возвращается в позицию I и цикл начинается сначала.
Процесс ампулирования
Процесс заполнения ампул растворами лекарственных веществ (ампулирование) складывается из следующих последовательно протекающих операций: вскрытия ампул (резка капилляров); набора ампул в кассеты; мойки и сушки ампул; наполнения, запайки, стерилизации, бракеража, этикетировки, упаковки и заключительного анализа.
Вскрытие ампул производится на автомате и состоит из двух операций: нанесения риски на наружной поверхности капилляра и облома его по месту надреза. Надрез производится при помощи алмазных или карборундовых дисков (брусков). Вскрытые ампулы набирают в кассеты, представляющие собой алюминиевые диски, в которых имеются многочисленные гнезда — отверстия для ампул (от 300 до 1000 в зависимости от вместимости ампул).
Промывка ампул является одной из самых ответственных операций ампульного производства. Она складывается из наружной и внутренней мойки ампул. Для наружной мойки кассеты с ампулами помещают в ванну на подставку и душируют горячей водопроводной водой (50-60° С), затем дистиллированной водой. Известно несколько способов внутренней промывки, например, шприцевой, который используется для промывки крупноемких ампул. При этом ампулы надевают на полые иглы, через которые последовательно пропускают под давлением горячую водопроводную воду, дистиллированную воду, пар.
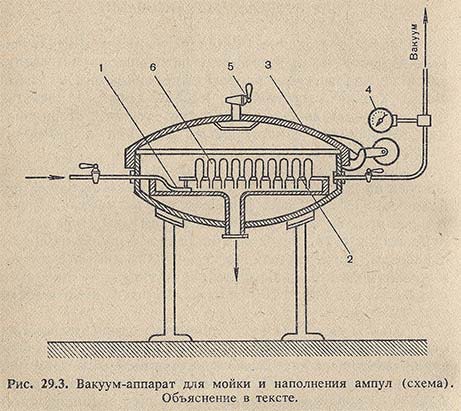
Наиболее распространенным является вакуумный способ (рис. 29.3). На кювету (1) помещают кассету (2), затем закрывают крышку (3) и из герметически закрытого аппарата отсасывают воздух. При этом кювета заполняется требуемым количеством дистиллированной воды и одновременно в аппарате и ампулах создается разрежение. После достижения необходимого разрежения, определяемого по манометру (4), открывают воздушный кран (5) с фильтром для воздуха, и в аппарат под атмосферным давлением поступает воздух. При этом вода быстро наполняет ампулы. Затем кассету с заполненными водой ампулами вынимают из аппарата и переносят в другой аппарат с пустой кюветой, из которого отсасывают воздух. В результате разрежения вода вытекает из ампул (6). Эти операции (наполнения и опорожнения ампул) проводят несколько раз. Дальнейшим усовершенствованием явилась конструкция, которая позволяла проводить операции наполнения и выливания в одном и том же аппарате.
В крупных ампульных цехах промывку ампул проводят пароконденсационным способом, предложенным проф. Ф. А. Коневым. Воздух в ампуле замещается паром (1-я стадия), капилляр ампулы погружается в жидкость. В это время пулька ампулы охлаждается, пар конденсируется, в ампуле создается разрежение и она наполняется жидкостью (2-я стадия). Затем нагревается пулька ампулы. Внутри последней образуется пар, вытесняющий из ампулы жидкость (3-я стадия). Ампула остается заполненной паром и готова к повторению процесса.
После проверки чистоты ампул их высушивают в шкафах при температуре 120-130° С в течение 15-20 мин. При необходимости стерилизации (в случае ампулирования в асептических условиях) температуру в шкафах повышают до 160-170° С и увеличивают экспозицию до 1 ч. Сушильный шкаф устанавливают в стене между отделениями мойки и наполнения ампул. Он открывается с обеих сторон: для загрузки и выгрузки кассет с ампулами. После сушки и стерилизации ампулы охлаждают в этих шкафах стерильным или фильтрованным воздухом.
Изготовление растворов для ампулирования проводят в специальных помещениях, выкрашенных масляной краской и периодически облучаемых бактерицидными лампами. Для растворения используют фарфоровые, эмалированные или стеклянные реакторы, имеющие при необходимости мешалки и паровые обогреватели. При приготовлении растворов с веществами, легко окисляющимися кислородом воздуха, растворение ведут в атмосфере углекислого газа или азота.
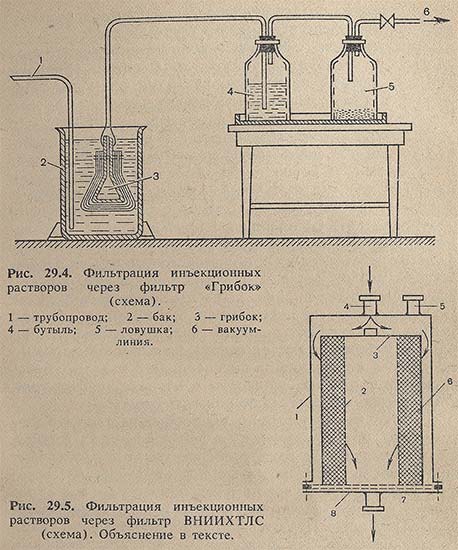
Фильтрование небольших количеств инъекционных растворов проводят с помощью фильтра «Грибок», принцип работы которого показан на рис. 29.4. При фильтровании больших количеств инъекционных растворов большое распространение получил фильтр ВНИИХТЛС (рис. 29.5). Он состоит из корпуса (1) и перфорированной трубки (2), на которую между ограничителями (3 и 8) плотно и ровно наматывают марлю (6). Через патрубок (5) удаляют воздух. Фильтруемая жидкость поступает в патрубок (4), через слой фильтрующего материала и отверстия в перфорированной трубке проходит внутрь нее и удаляется через патрубок (7). Корпус фильтра изготовлен из органического стекла или нержавеющей стали. Зарядку фильтра производят, с таким расчетом, чтобы толщина слоя марли равнялась 3-4 см. По окончании намотки марли на перфорированную трубку ее вставляют в корпус фильтра и закрепляют. Фильтр устанавливают на специальной подставке в вертикальном положении и присоединяют к нему трубопроводы, подающие жидкость и отводящие фильтрат. Фильтрацию осуществляют под вакуумом.
Необходимая чистота инъекционных растворов в значительной степени зависит от чистоты воздуха в помещениях ампульного цеха, особенно там, где происходит приготовление растворов и наполнение ампул. Фильтрация воздуха в ампульном цехе осуществляется с помощью мощных фильтров, заряжаемых комбинированным слоем хлопчатобумажной или синтетической ткани со стеклотканью. Эти фильтры вместе с вентиляторами устанавливаются в чердачном помещении.
Наполнение ампул может производиться двояким способом: 1) раствором наполняют каждую ампулу отдельно (шприцевой способ); 2) раствором наполняют одновременно большое количество ампул (вакуумный, пароконденсационный способы).
При шприцевом способе инъекционная жидкость под давлением чистого профильтрованного воздуха поступает в бюретку. На конец бюретки надевают полую иглу (от шприца), которую вводят в шейку ампулы. Преимуществом шприцевого способа является то, что шейки ампул остаются чистыми и запаивание не представляет трудности даже при работе с такими жидкостями, как масла, эмульсии, растворы глюкозы и т. д.
Вакуумное наполнение ампул проводят в аппаратах, аналогичных применяемым при мойке, с той лишь разницей, что в этом случае определяют степень разрежения, благодаря чему в ампулы поступает требуемое количество жидкости. Для освобождения шеек от жидкости кассеты с ампулами переносят в герметически закрываемый шкаф открытыми шейками вверх и, подавая профильтрованный воздух, прогоняют жидкость в корпус ампул. Вакуумный метод наполнения ампул высокопроизводителен.
При пароконденсационном способе заполнение ампул происходит следующим образом. После промывки ампулы остаются заполненными паром, капилляры ампул опускают в ячейки-дозаторы, содержащие точные объемы раствора для одной ампулы, корпусы ампул охлаждают, после чего они. заполняются раствором.
После наполнения капилляры ампул обмывают струей дистиллированной воды или обрабатывают паром для того, чтобы смыть с капилляра пленку раствора, которая при запаивании высыхает и в случае обугливания может загрязнить содержимое ампулы.
Запайку ампул осуществляют возможно быстро, чтобы содержимое ампул не успело нагреться. Запайку производят в специальных аппаратах, работа которых основана на принципе движения ампул в гнездах вращающегося диска или транспортера, проходящего мимо горелок, которые запаивают капилляры.
В заводских условиях стерилизацию ампул проводят в горизонтальном автоклаве, установленном в стене между двумя помещениями: в одном — автоклав загружается, а в другом — из него выгружаются простерилизованные ампулы. Пар в автоклав поступает из котельной завода.
После стерилизации, проведенной в установленном тепловом режиме, еще горячие ампулы проверяют на герметичность. С этой целью их погружают в подкрашенную метиленовым синим холодную воду. Когда ампулы остынут, давление в них снижается, и если в стенках имелись трещины, то окрашенная вода проникает внутрь ампул. Это позволяет легко отобрать негодные ампулы. Далее ампулы промывают горячей водой под душем. Что касается ампул, наполненных масляными растворами, то их вначале тщательно моют горячей мыльной водой, а затем горячей водой под душем.
Вымытые ампулы вытирают мягкими полотенцами и направляют на бракераж. Бракераж проводят визуально в темной комнате с помощью щелевидного рефлектора, дающего луч от электрической лампы мощностью 40-60 Вт. Каждую ампулу просматривают в этом луче света на темном фоне, несколько раз ее переворачивая. При этом не должно обнаруживаться видимых невооруженным глазом частиц, т. е. частиц размером 10 мкм и более.
Ампулы, прошедшие контроль, поступают в этикетировочную машину. Название и концентрация раствора печатается непосредственно на стекле ампулы. Готовые ампулы упаковывают в коробки с гнездами для каждой ампулы. На коробки наклеивают этикетки с указанием препарата, количества и концентрации раствора, числа ампул в коробке, серии и номеров химического и бактериологического анализов.
Современная номенклатура ампулированных растворов и особенности частной технологии некоторых из них
Общее число официнальных ампулированных растворов превышает 100 наименований и список их непрерывно увеличивается по мере внедрения в медицинскую практику новых лекарственных средств. Подавляющее большинство ампулированных растворов предназначено для инъекций. Из растворов, применяемых наружно, в ампулах выпускаются: 5% спиртовый раствор йода, 10% раствор аммиака и 2% раствор грамицидина. Основная масса инъекционных растворов представляет собой водные растворы лекарственных веществ. Все они, как правило, нуждаются в ампулах из нейтрального стекла соответствующей марки.
Если в основу классификации этой группы растворов положить важнейший признак их качества — стабильность, то все их множество можно разделить на две группы: 1) растворы лекарственных веществ, которые при ампулировании и хранении не нуждаются в специальной стабилизации; 2) растворы лекарственных веществ, которые при ампулировании и хранении нуждаются в стабилизаторах и других формах защиты от деструкции.
Ампулирование растворов первой группы лекарственных веществ протекает по типовой схеме, с учетом предусмотренных ГФХ, pH раствора, вида и режима стерилизации, повышенной чистоты исходных веществ, изотонирования и других требований. На некоторые из них уже обращалось внимание, когда описывалось изготовление инъекционных растворов в аптечных условиях.
Что касается водных растворов, требующих стабилизации, то они отличаются большим разнообразием. Так, например, растворы малостабильных веществ ампулируют в токе инертных газов: азота, углекислого газа, аргона. Сам раствор также предварительно насыщают инертным газом. Надежность тазовой защиты доказана на растворах папаверина гидрохлорида, алкалоидов спорыньи, тиамина хлорида и глюкозы с аскорбиновой кислотой.
Растворы солей алкалоидов и некоторых других органических оснований в большинстве случаев нуждаются в стабилизации хлористоводородной кислотой.
С добавлением этой кислоты (разных количеств) изготавливают растворы: атропина сульфата, стрихнина нитрата, скополамина гидрохлорида, цититона, омнопона, новокаина, текодина, тетацин-кальция.
Стабилизация хлористоводородной кислотой в сочетании с хлоридом натрия применяется для растворов глюкозы всех концентраций. Глюкоза в растворе устойчива при pH 3-4. В более кислой среде образуется гетероциклический альдегид — оксиметилфурфурол, обусловливающий окрашивание раствора в желтый цвет. С повышением pH (более 5) наблюдается разрыв цепи в молекуле глюкозы и образование органических кислот. Процесс разложения глюкозы в растворах ускоряют следы тяжелых металлов.
С добавлением натрия хлорида изготовляют растворы желатина для инъекций. Натрия, хлорид вводят с целью несколько понизить температуру плавления студня желатина, что позволяет пользоваться его раствором.
К помощи едкого натра и натрия гидрокарбоната прибегают для стабилизации растворов солей слабых кислот и сильных оснований (никотиновой кислоты, кофеин-бензоата натрия, натрия тиосульфата). Прибавлением щелочей подавляется реакция гидролиза, к которой склонны эти соли в водных растворах.
Большую роль в стабилизации многих инъекционных растворов играют факторы, тормозящие процессы окисления и самоокисления. Эти реакции протекают под влиянием атмосферного кислорода. В результате наблюдаются изменение цвета раствора, выпадение осадков и др. Подбор оптимального значения pH, предохранение от действия света, уменьшение количества растворенного кислорода в жидкой фазе — вот способы предохранения лабильных лекарственных веществ от самоокисления.
Широко практикуется также применение веществ, прерывающих цепь самоокисления, так называемых антиоксидантов. Действие антиоксидантов основано на том, что они обладают более подвижными атомами водорода, чем вещества, которые следует предохранить от окисления, и поэтому они в первую очередь окисляются, расходуя на эту окислительно-восстановительную реакцию кислород воздуха, присутствующий в ампуле. К антиоксидантам относятся: неорганические серные соединения (сульфиты, пиросульфиты), алкоголи и энолы (хлорбутанолгидрат, аскорбиновая кислота), фенолы (гидрохинон, пирогаллол). Добавления антиоксидантов требуют, в частности, растворы адреналина, этазола натрия, новокаинамида, аминазина и дипразина.
Растворы некоторых лекарственных веществ не могут приобрести необходимую стабильность при использовании какой-либо одной формы защиты. В этом случае прибегают к комбинированным формам защиты. Например, стабилизация 30% раствора сульфацил-натрия достигается оптимальным сочетаниям pH среды (7,5-8,5) антиоксиданта (натрия метабилсульфит) и режима стерилизации.
Для стабилизации раствора морфина гидрохлорида применяют сочетания: pH среды (3,0-3,5), стекло НС-3, газовая защита (СО2) и щадящая стерилизация (текучим паром). Аскорбиновая кислота благодаря наличию в молекуле энольной группы обладает сильно выраженными восстановительными свойствами. Поэтому в растворах под влиянием кислорода она легко окисляется, превращаясь в дигидроаскорбиновую кислоту. В кислых растворах (pH 1-4) аскорбиновая кислота разлагается с образованием альдегида фурфурола, что обусловливает желтую окраску разложившихся растворов. Раствор аскорбиновой кислоты изготовляют в присутствии натрия гидрокарбоната, который повышает pH до 6-7 (образуется соль аскорбиновой кислоты — натрия аскорбинат) и натрия сульфата или натрия метабисульфита. Раствор ампулируют в токе углекислого газа и стерилизуют текучим паром 15 мин.
Лекарственные вещества, находящиеся в ампулах в виде масляных растворов (например, растворы камфоры, препаратов гормонов и их синтетических аналогов, жирорастворимых витаминов), стабилизации не требуют, так как масло не взаимодействует со стеклом и влияние ампульного стекла в данном случае исключается. В связи с этим масляные растворы можно помещать в ампулы, изготовленные, например, из стекла марки АБ-1. Требования асептики полностью сохраняют свое значение.
Шприц-тюбики как форма упаковки инъекционных растворов
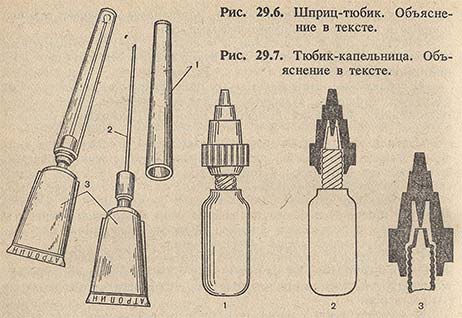
Шприц-тюбики, содержащие стерильный раствор лекарственного вещества, очень удобны для одноразового использования в полевых условиях и при оказании неотложной помощи. Шприц-тюбик (рис. 29.6) состоит из ампулы (3) из полиэтилена, в которую запрессована игла (2). В иглу вставляют мандрен и герметически закрывают ампулу колпачком (1).
При использовании шприц-тюбика для инъекций снимают колпачок, вынимают мандрен и вводят лекарственное вещество подкожно или внутримышечно.
Шприц-тюбики заполняют растворами лекарственных веществ в асептических условиях с помощью дозирующих полуавтоматов, которые находятся в стерильном помещении — боксе. В этом же помещении производят запайку ампул шприц-тюбиков. Заполненные раствором лекарственного вещества шприц-тюбики вставляют в тюбикодержатель и запаивают. Одновременно на нижнюю, запаиваемую часть шприц-тюбика наносят тисненую надпись с наименованием лекарственного вещества. Заполненные шприц-тюбики подвергают тиндализации. Кроме химического и бактериологического контроля, готовые шприц-тюбики проверяют на герметичность. Упаковывают в коробки по 100 штук.
Глазные лекарственные формы
Глазные капли
Рациональная упаковка глазных капель — одно из важнейших условий, обеспечивающих продление срока их стабильности и, следовательно, возможности и целесообразности перевода часто встречающихся прописей в заводское производство.
Такой рациональной упаковкой для глазных капель явились тюбики-капельницы вместимостью 1,5-2 мл, изготавливаемые из индифферентных высокополимеров, обеспечивающих герметичность упаковки и точность дозирования капель (рис. 29.7). Отросток (1), после заполнения тюбика запаивается и закрывается колпачком (2), навинчивающимся на отросток. Внутри колпачка вверху имеется упор — шип (3). Если одной рукой взять тюбик, а другой повернуть колпачок до упора, то последний прокалывает отросток. После этого колпачок снимается, и легким нажатием корпуса тюбика откапывают раствор.
Прописи глазных капель, выпускаемые промышленностью, включают добавки веществ, обеспечивающие изотоничность капель (натрия хлорид), устойчивость к кислороду воздуха (антиоксиданты — метабисульфит и др.), микрофлоре (консерванты — нипагин и др.) и в ряде случаев пролонгирование действия (МЦ, натрий-КМЦ, поливиниловый спирт). Промышленностью выпускаются глазные капли, представляющие собой растворы: сульфацил-натрия 30%, атропина сульфата 0,1%, пилокарпина гидрохлорида 1%, скополамина гидробромида 0,25%, гоматропина гидробромида 0,25% и др.
Глазные пленки
При применении глазных капель практически невозможна точная дозировка лекарственных веществ, так как они довольно быстро эвакуируются из конъюнктивальной полости со слезой, выделение которой обычно интенсифицируется в момент инстилляции (закапывания). Исследования показали, что водные глазные капли задерживаются в конъюнктивальной полости только 5-10 мин, при этом высокая концентрация лекарственных веществ наблюдается только первые 29 с, а через 20 мин остаются лишь следы препарата. Часто для достижения терапевтического эффекта проводится 5-8, а иногда и большее число инстилляций, что является причиной побочных неблагоприятных реакций. Например, в результате многократных инстилляций раствора атропина, часть его, попадая через слезные каналы на слизистые оболочки носовой части глотки, вызывает не только ощущение сухости во рту, но и явления интоксикации, психосиндрома и нарушения нервной деятельности.
Другая традиционная глазная лекарственная форма — мази — также имеет свои отрицательные стороны, в частности компоненты мазевых основ часто служат причиной аллергических реакций, сенсибилизации, раздражения слизистой оболочки глаза и т. п.
В результате проведенных научных исследований по изысканию более совершенных глазных лекарственных форм была предложена новая глазная лекарственная форма — глазная пленка (membranula ophthalmica).
К настоящему времени разработаны растворимые в слезной жидкости глазные лекарственные пленки на основе сополимера акриламида, винилпирролидона и этилакрилата. Эти пленки представляют собой твердые пластинки, имеющие размеры: длина 6-8 мм, ширина 2-5 мм, толщина 0,2-0,6 мм; масса 10-30 мг. После закладывания за веко пленки смачиваются слезной жидкостью, становятся эластичными и постепенно растворяются в течение 10-40 мин. Пленки не вызывают ни раздражения, ни токсических изменений тканей глаза. Они обеспечивают точное дозирование и позволяют значительно увеличить продолжительность нахождения и концентрацию лекарственных веществ в тканях глаза. Пленки можно стерилизовать.
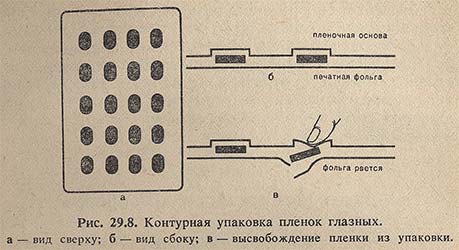
Процесс изготовления глазных пленок складывается из 4 стадий: изготовление раствора лекарственных веществ в растворе полимера; отлива пленочного полотна; получения элементарных пленок; упаковки пленок и их стерилизации. Вначале изготавливают водный раствор полимера, в котором растворяются лекарственные вещества. Далее проводятся гомогенизация раствора, деаэрация (освобождение смеси от пузырьков воздуха) и фильтрация. На второй стадии производится отлив пленочного полотна. Для этой цели служит металлическая лента длиной примерно 3 м, вращающаяся на барабанах и находящаяся в закрытой (сушильной) камере. Поступая с одного конца из загрузочной воронки, раствор полимера, проходя всю камеру, успевает просохнуть и образовать тонкий сплошной слой полимера необходимой толщины. Далее полученное полотно продольно разрезается на ленты (заготовка). На третьей стадии продольные ленты направляют в резальную машину, вырубающую из ленты элементарные пленки необходимых размеров, которыми фактически определяется разовая доза в пленке лекарственного вещества. Вырубленные пленки досушиваются в сушилке, после чего они проходят галтовку, т. е. операцию отборки для сглаживания острых краев, кромок и разных шероховатостей. На заключительной стадии пленки упаковывают в одноячейковые контурные упаковки из поливинилхлоридной пленки и фольги по 20 штук (рис. 29.8). Готовые упаковки подвергаются радиационной стерилизации.
По описанной технологии промышленность выпускает глазные пленки с атропина сульфатом, пилокарпина гидрохлоридом, дикаином, неомицина сульфатом, сульфапиридазина-натрием и флореналем.
Источник