Особенности культивирования анаэробных бактерий
Важным условием, которое необходимо соблюдать на всех этапах выделения и идентификации анаэробов, является защита этих микробов от токсического действия молекулярного кислорода. Время между взятием материала и его посевом на питательные среды должно быть максимально коротким.
Анаэробные бактерии можно культивировать только на специальных бескислородных средах с низким окислительно-восстановительным потенциалом (10 — 150мВ). Для контроля за степенью насыщения этих сред кислородом используют специальные редокс — индикаторы (метиленовый синий, резазурин), восстановленные формы которых бесцветны. При возрастании окислительно-восстановительного потенциала (ОВП) метиленовый синий окрашивает среды в синий, а резазурин — в розовый цвет, что указывает на непригодность таких сред для культивирования облигатных анаэробов. Для сохранения низкого ОВП питательные среды должны быть агаризированы. Добавление даже 0,05% агара повышает их вязкость и уменьшает аэрацию.
Анаэробный тип энергетического метаболизма во много раз менее продуктивный, чем аэробный, поэтому питательные среды для анаэробов должны быть богаче питательными субстратами и витаминами. В практических лабораториях для выделения анаэробов из патологического материала чаще всего используют среду для контроля стерильности крови (СКС), среду Китта-Тароцци, анаэробный кровяной агар (на основе эритрит-агара или агара Д), среду Вильсона — Блера, среду Шедлера и др. Эти свежеприготовленные питательные среды должны быть использованы для посева в течение 2-х часов во избежание насыщения кислородом.
Методы создания анаэробных условий. Создание анаэробных условий достигается с помощью физических, химических, биологических и смешанных методов.
Физические методы. Основаны на выращивании микроорганизмов в безвоздушной среде, что достигается:
1. посевом в среды, содержащие редуцирующие и легко окисляемые вещества; В качестве редуцирующих веществ обычно используют кусочки (около 0,5 г) животных тканей (печень, мозг, почки, селезенка, кровь). Эти ткани связывают растворенный в среде кислород и адсорбируют бактерии. Чтобы уменьшить содержание кислорода в питательной среде, ее перед посевом кипятят 10-15 мин, а затем быстро охлаждают и заливают сверху небольшим количеством стерильного вазелинового масла. В качестве легко окисляемых веществ используют глюкозу, лактозу и муравьинокислый натрий. Лучшей жидкой питательной средой с редуцирующими веществами является среда Китта-Тароцци, которая используется для накопления анаэробов при первичном посеве из исследуемого материала и для поддержания роста выделенной чистой культуры анаэробов.
2. посевом микроорганизмов в глубину плотных питательных сред. Посев микроорганизмов в глубину плотных сред производят по методу Вейнберга
Метод Вейнберга. 1-2 капли материала со среды Кита-Тароцци вносят в пробирку с МПБ для разведения. Затем пастеровской пипеткой с запаянным концом переносят материал последовательно в 3-5 узких пробирок с сахарным МПА, предварительно расплавленным и прокипяченным в течение 20 мин и остуженным до 50°С, погружая капилляр пипетки в расплавленный агар до дна пробирки. Засеянные пробирки быстро охлаждают под струей холодной воды, при этом агар застынет и зафиксирует разобщенное положение отдельных микробных клеток. Инкубируют в анаэробных условиях. Через сутки отбирают колонии, на уровне колонии пробирку распиливают, колонию отсасывают пипеткой и переносят в среду Китта-Троцци для накопления и идентификации.
3. механическим удалением воздуха из сосудов, в которых выращиваются анаэробные микроорганизмы; Удаление воздуха производят путем его механического откачивания их специальных приборов — анаэростатов, в которые помещают чашку с посевом анаэробов. Переносной анаэростат представляет собой толстостенный металлический или пластиковый цилиндр с хорошо притертой крышкой (с резиновой прокладкой), снабженный отводящим краном и вакуумметром. После размещения засеянных чашек или пробирок воздух из анаэростата удаляют с помощью вакуумного насоса.
4. заменой воздуха в сосуде каким-либо индифферентным газом. Замену воздуха индифферентным газом (азотом, водородом, аргоном, С02) можно производить в анаэростатах путем вытеснения его газом из баллона.
Приборы и среды для культивирования анаэробов:
Микроанаэростат — используется для создания вакуума с дозированным содержанием кислорода. Прибор представляет собой герметически закрывающийся сосуд, снабженный манометром, в который помещают посевы и откачивают воздух. Микроанаэростат помещают в термостат.
Эксикатор — стеклянный лабораторный сосуд с притертой крышкой. В его донной части имеется дополнительная емкость, куда наливается смесь пирогаллола и едкого натра или гидросульфита натрия и двууглекислой соды. На сетку-подставку помещают посевы и притирают крышку с помощью вазелина. Эксикатор помещают в термостат.

Винтовой зажим с герметичной прокладкой
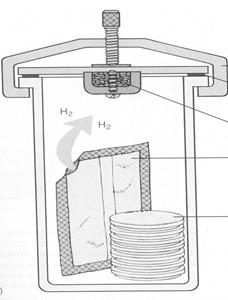
Рис. 9 Газогенераторные пакеты
Система Generbag anaer состоит из воздухонепроницаемых емкостей, изготовленных из прозрачной пластмассы и генераторов, содержащих смесь веществ, поглощающих кислород (рис. 9). При применении GasPak Plus необходимо увлажнить таблетку боргидрида натрия, при этом выделяется водород и в присутствии палладиевого катализатора он соединяется с кислородом с образованием воды. Последовательность работы: вынуть генератор из пакета, поместить в нижнюю часть воздухонепроницаемого пакета, затем поместить чашки (или пробирки) с посевами и закрыть пакет. Инкубация при 37°С.
Анаэробный бокс — прозрачная плексиглассовая камера со шлюзом, отверстиями для рук с рукавами, заканчивающимися резиновыми перчатками. В нем создаются стерильные условия, его заполняют газовой смесью и поддерживают температуру 37°С.
Среда Китта-Тароцци. Содержит мясо-пептонный бульон (МПБ), 0,5% глюкозы и 0,15% агара. На дно пробирки для адсорбции О2 помещают кусочки вареной печени или фарша слоем 1-1,5 см и заливают 6-7 мл среды. Среду перед посевом регенерируют (прогревают 15-20 мин на водяной бане для удаления воздуха, а затем быстро охлаждают). После посева среду заливают вазелиновым маслом и помещают в термостат.
Полужидкий сахарный агар (высокий столбик). В пробирку с 6-7 мл расплавленного и охлажденного до 40-45 0 полужидкого питательного агара, содержащего 0,5-1% глюкозы, вносят исследуемый материал и перемешивают. Посевы помещают в термостат.
Химические методы. Основаны на поглощении кислорода воздуха в герметически закрытом сосуде (анаэростате, эксикаторе) такими веществами, как пирогаллол или гидросульфит натрия.
1. Применение щелочных растворов пирогаллола для поглощения кислорода в замкнутой воздушной среде.
2. Можно применять гидросульфит натрия. Для связывания кислорода в 1 л объема берут 100 мл свежеприготовленного 20% раствора Na2S204и 16 мл 50% КОН.
3. Использование веществ — редуцентов, к которым относятся тиогликолевая кислота или тиогликолат натрия (0,01-0,02%), аскорбиновая кислота (0,1%), различные сахара (0,1-3%), цистин и цистеин (0,03-0,05%), муравьинокислый натрий (0,25-0,75%) и др.
Применение газогенерирующих систем для создания анаэробных условий в замкнутой воздушной среде (микроанаэростатах, эксикаторах, прозрачных газонепроницаемых пластиковых пакетах). Для образования водорода и двуокиси углерода, необходимых для роста облигатных анаэробов, используют специальные таблетки, которые активируются добавлением воды. Водород, генерируемый таблетками боргидрида натрия, связывает кислород воздуха в присутствии палладиевого катализатора с образованием воды. Углекислый газ вырабатывается при взаимодействии лимонной кислоты с бикарбонатом натрия.
Биологические методы
1. Совместное выращивание анаэробов и аэробов (метод Фортнера). При этом на одну половину чашки Петри с плотной питательной средой засевают исследуемый материал, а на другую — культуру аэробного микроорганизма, способного энергично поглощать кислород. После посева чашку закрывают крышкой, края которой для герметизации заливают парафином или заклеивают пластилином. В качестве активного поглотителя кислорода из замкнутого пространства часто используют культуру “чудесной палочки” (Serratia marcescens), которая является своеобразным индикатором качества анаэробиоза. При недостаточной герметизации чашки этот микроорганизм образует ярко-красный пигмент, а при сохранении строго анаэробных условий вырастают бесцветные или бледно-розовые колонии.
2. Помещение в питательную среду кусочков печени, головного мозга, почек и других внутренних органов. При этом тканевые клетки активно поглощают и адсорбируют на себе кислород, в результате чего в среде создаются анаэробные условия. Примером питательной среды, сконструированной по этому принципу, является содержащая кусочки печени среда Китта — Тароцци. К тому же в печеночной ткани содержится большое количество веществ с SH-группой (цистеин, глютатион и др.), обладающих сильным редуцирующим действием.
3. Культуры некоторых облигатных анаэробов можно поддерживать путем пассажа на лабораторных животных, однако в настоящее время этот метод используется достаточно редко.
Комбинированные методы основаны на сочетании физических, химических и биологических методов создания анаэробиоза, и используются в большинстве практических лабораторий. Для работы с наиболее чувствительными к молекулярному кислороду анаэробами используют строгую анаэробную технику (метод Хангейта). Принцип метода заключается в использовании лишенных кислорода питательных сред, воздух над которыми удаляется и замещается бескислородным газом.
III. План практической работы
1. Изучить аппаратуру для стерилизации, культивирования бактерий аэробов и анаэробов, зарисовать схему устройства микроанаэростата
2. Изучить технику и зарисовать схемы посевов исследуемого материала на питательные среды с целью получения изолированных колоний
3. Выписать цель и схему бактериологического метода исследования
4. Ознакомиться с питательными средами и заполнить таблицу «Питательные среды».
5. Заполните таблицу «Основные методы стерилизации»
6. Посеять смесь бактерий истощающим штрихом на МПА с целью выделения чистой культуры
7. Решить ситуационные задачи
IV. Примеры ситуационных задач
Ситуационная задача № 1
Из материала больного выделили кишечную палочку. Какие питательные среды используют для того, чтобы выделить чистую культуру и отличить ее от других представителей кишечной микрофлоры:
1. Дифференциально-диагностические среды
2. Универсальные среды
3. Среды обогащения
4. Синтетические среды
Ситуационная задача № 2
Для проведения бактериологических исследований необходимо подготовить стерильные чашки Петри, пипетки, колбы и др. посуду. Какой метод стерилизации используют:
1. Стерилизацию сухим жаром
2. Стерилизацию облучением
3. Химическую стерилизацию
4. Стерилизацию текучим паром
Ситуационная задача № 3
Из больного с опасением на анаэробную инфекцию взяли материал (раневой экссудат). Какие среды используют для культивирования возбудителя:
1. Среду Китта-Тароцци
2. Среду Вильсона — Блера
3. Среду Плоскирева
Ситуационная задача № 4
Врач-бактериолог в мазке из исследуемого материала выделил смесь нескольких микроорганизмов. Что необходимо для дальнейшей идентификации возбудителя:
1. Получение чистых культур микроорганизмов
2. Посев исследуемого материала на среду накопления
3. Произвести реакцию агглютинации с поливалентными сыворотками
4. Произвести посев материала на ряд Гиса
Опора деревянной одностоечной и способы укрепление угловых опор: Опоры ВЛ — конструкции, предназначенные для поддерживания проводов на необходимой высоте над землей, водой.
Папиллярные узоры пальцев рук — маркер спортивных способностей: дерматоглифические признаки формируются на 3-5 месяце беременности, не изменяются в течение жизни.
Источник
Методы культивирования анаэробов.
Для культивирования анаэробов необходимо понизить окислительно-восстановительный потенциал среды, создать условия анаэробиоза, т. е. пониженного содержания кислорода в среде и окружающем ее пространстве. Это достигается применением физических, химических и биологических методов.
Физические методы. Основаны на выращивании микроорганизмов в безвоздушной среде, что достигается:
1) посевом в среды, содержащие редуцирующие и легко окисляемые вещества;
2) посевом микроорганизмов в глубину плотных питательных сред;
3) механическим удалением воздуха из сосудов, в которых выращиваются анаэробные микроорганизмы;
4) заменой воздуха в сосудах каким-либо индифферентным газом.
В качестве редуцирующих веществ обычно используют кусочки (около 0,5 г) животных или растительных тканей (печень, мозг, почки, селезенка, кровь, картофель, вата). Эти ткани связывают растворенный в среде кислород и адсорбируют бактерии. Чтобы уменьшить содержание кислорода в питательной среде, ее перед посевом кипятят 10—15 мин, а затем быстро охлаждают и заливают сверху небольшим количеством стерильного вазелинового масла. Высота слоя масла в пробирке около 1 см.
В качестве легко окисляемых веществ используют глюкозу, лактозу и муравьинокислый натрий.
Лучшей жидкой питательной средой с редуцирующими веществами является среда Китта — Тароцци, которая используется с успехом для накопления анаэробов при первичном посеве из исследуемого материала и для поддержания роста выделенной чистой культуры анаэробов.
Посев микроорганизмов в глубину плотных сред производят по способу Виньяль — Вейона, который состоит в механической защите посевов анаэробов от кислорода воздуха. Берут стеклянную трубку длиной 30 см и диаметром 3—6 мм. Один конец трубки вытягивают в капилляр в виде пастеровской пипетки, а у другого конца делают перетяжку. В оставшийся широкий конец трубки вставляют ватную пробку. В пробирки с расплавленным и охлажденным до 50°С питательным агаром засевают исследуемый материал. Затем насасывают засеянный агар в стерильные трубки Виньяль — Вейона. Капиллярный конец трубки запаивают в пламени горелки и трубки помещают в термостат. Так создаются благоприятные условия для роста самых строгих анаэробов. Для выделения отдельной колонии трубку надрезают напильником, соблюдая правила асептики, на уровне колонии, ломают, а колонию захватывают стерильной петлей и переносят в пробирку с питательной средой для дальнейшего выращивания и изучения в чистом виде.
Удаление воздуха производят путем его механического откачивания из специальных приборов — анаэроста-тов, в которые помещают чашки с посевом анаэробов. Переносный анаэростат представляет собой толстостенный металлический цилиндр с хорошо притертой крышкой (с резиновой прокладкой), снабженный отводящим краном и вакуумметром. После размещения засеянных чашек или пробирок воздух из анаэростата удаляют с помощью вакуумного насоса.
Замену воздуха индифферентным газом (азотом, водородом, аргоном, углекислым газом) можно производить в тех же анаэростатах путем вытеснения его газом из баллона.
Химические методы. Основаны на поглощении кислорода воздуха в герметически закрытом сосуде (анаэро-стате, эксикаторе) такими веществами, как пирогаллол или гидросульфит натрия Na2S204.
Биологические методы. Основаны на совместном выращивании анаэробов со строгими аэробами. Для этого из застывшей агаровой пластинки по диаметру чашки вырезают стерильным скальпелем полоску агара шириной около 1 см. Получается два агаровых полудиска в одной чашке. На одну сторону агаровой пластинки засевают аэроб, например часто используют S. aureus или Serratia marcescens. На другую сторону засевают анаэроб. Края чашки заклеивают пластилином или заливают расплавленным парафином и помещают в термостат. При наличии подходящих условий в чашке начнут размножаться аэробы. После того, как весь кислород в пространстве чашки будет ими использован, начнется рост анаэробов (через 3—4 сут). В целях сокращения воздушного пространства в чашке питательную среду наливают возможно более толстым слоем.
Комбинированные методы. Основаны на сочетании физических, химических и биологических методов создания анаэробиоза.
№ 18 Типы и механизмы питания бактерий.
Типы питания. Микроорганизмы нуждаются в углеводе, азоте, сере, фосфоре, калии и других элементах. В зависимости от источников углерода для питания бактерии делятся на аутотрофы, использующие для построения своих клеток диоксид углерода С02 и другие неорганические соединения, и гетеротрофы, питающиеся за счет готовых органических соединений. Аутотрофными бактериями являются нитрифицирующие бактерии, находящиеся в почве; серобактерии, обитающие в воде с сероводородом; железобактерии, живущие в воде с закисным железом, и др.
Гетеротрофы, утилизирующие органические остатки отмерших организмов в окружающей среде, называются сапрофитами. Гетеротрофы, вызывающие заболевания у человека или животных, относят к патогенным и условно-патогенным. Среди патогенных микроорганизмов встречаются облигатные и факультативные паразиты (от греч. parasitos — нахлебник). Облигатные паразиты способны существовать только внутри клетки, например риккетсии, вирусы и некоторые простейшие.
В зависимости от окисляемого субстрата, называемого донором электронов или водорода, микроорганизмы делят на две группы. Микроорганизмы, использующие в качестве доноров водорода неорганические соединения, называют литотрофны-ми (от греч. lithos — камень), а микроорганизмы, использующие в качестве доноров водорода органические соединения, — органотрофами.
Учитывая источник энергии, среди бактерий различают фототрофы, т.е. фотосинтезирующие (например, сине-зеленые водоросли, использующие энергию света), и хемотрофы, нуждающиеся в химических источниках энергии.
Механизмы питания. Поступление различных веществ в бактериальную клетку зависит от величины и растворимости их молекул в липидах или воде, рН среды, концентрации веществ, различных факторов проницаемости мембран и др. Клеточная стенка пропускает небольшие молекулы и ионы, задерживая макромолекулы массой более 600 Д. Основным регулятором поступления веществ в клетку является цитоплазматическая мембрана. Условно можно выделить четыре механизма проникновения питательных веществ в бактериальную клетку: это простая диффузия, облегченная диффузия, активный транспорт, транслокация групп.
Наиболее простой механизм поступления веществ в клетку — простая диффузия, при которой перемещение веществ происходит вследствие разницы их концентрации по обе стороны цитоплазматической мембраны. Вещества проходят через липид-ную часть цитоплазматической мембраны (органические молекулы, лекарственные препараты) и реже по заполненным водой каналам в цитоплазматической мембране. Пассивная диффузия осуществляется без затраты энергии.
Облегченная диффузия происходит также в результате разницы концентрации веществ по обе стороны цитоплазматической мембраны. Однако этот процесс осуществляется с помощью молекул-переносчиков, локализующихся в цитоплазматической мембране и обладающих специфичностью. Каждый переносчик транспортирует через мембрану соответствующее вещество или передает другому компоненту цитоплазматической мембраны — собственно переносчику. Белками-переносчиками могут быть пермеазы, место синтеза которых — цитоплазматическая мембрана. Облегченная диффузия протекает без затраты энергии, вещества перемещаются от более высокой концентрации к более низкой.
Активный транспорт происходит с помощью пермеаз и направлен на перенос веществ от меньшей концентрации в сторону большей, т.е. как бы против течения, поэтому данный про цесс сопровождается затратой метаболической энергии (АТФ), образующейся в результате окислительно-восстановительных реакций в клетке.
Перенос (транслокация) групп сходен с активным транспортом, отличаясь тем, что переносимая молекула видоизменяется в процессе переноса, например фосфорилируется.
Выход веществ из клетки осуществляется за счет диффузии и при участии транспортных систем.
№ 19 Основные принципы культивирования бактерий.
Универсальным инструментом для производства посевов является бактериальная петля. Кроме нее, для посева уколом применяют специальную бактериальную иглу, а для посевов на чашках Петри — металлические или стеклянные шпатели. Для посевов жидких материалов наряду с петлей используют пастеровские и градуированные пипетки. Первые предварительно изготовляют из стерильных легкоплавких стеклянных трубочек, которые вытягивают на пламени в виде капилляров. Конец капилляра сразу же запаивают для сохранения стерильности. У пастеровских и градуированных пипеток широкий конец закрывают ватой, после чего их помещают в специальные пеналы или обертывают бумагой и стерилизуют.
При пересеве бактериальной культуры берут пробирку в левую руку, а правой, обхватив ватную пробку IV и V пальцами, вынимают ее, пронося над пламенем горелки. Удерживая другими пальцами той же руки петлю, набирают ею посевной материал, после чего закрывают пробирку пробкой. Затем в пробирку со скошенным агаром вносят петлю с посевным материалом, опуская ее до конденсата в нижней части среды, и зигзагообразным движением распределяют мате риал по скошенной поверхности агара. Вынув петлю, обжигают край пробирки и закрывают ее пробкой. Петлю стерилизуют в пламени горелки и ставят в штатив. Пробирки с посевами надг писывают, указывая дату посева и характер посевного материала (номер исследования или название культуры).
Посевы «газоном» производят шпателем на питательный агар в чашке Петри. Для этого, приоткрыв левой рукой крышку, петлей или пипеткой наносят посевной материал на поверхность питательного агара. Затем проводят шпатель через пламя горелки, остужают его о внутреннюю сторону крышки и растирают материал по всей поверхности среды. После инкубации посева появляется равномерный сплошной рост бактерий.
№ 20 Искусственные питательные среды, их классификация. Требования, предъявляемые к питательным средам.
Питательной средой в микробиологии называют среды, содержащие различные соединения сложного или простого состава, которые применяются для размножения бактерий или других микроорганизмов в лабораторных или промышленных условиях.
Питательные среды готовят из продуктов животного или растительного происхождения. Большое значение имеет наличие в питательной среде ростовых факторов, которые катализируют метаболические процессы микробной клетки (витамины группы В, никотиновая кислота и др.).
Искусственные среды готовят по определенным рецептам из различных настоев или отваров животного или растительного происхождения с добавлением неорганических солей, углеводов и азотистых веществ.
В бактериологической практике чаще всего используют сухие питательные среды, которые получают на основе достижений современной биотехнологии. Для их приготовления используют экономически рентабельное непищевое сырье: утратившие срок годности кровезаменители (гидролизин—кислотный гидролизат крови животных, аминопептид — ферментативный гидролизат крови; продукты биотехнологии (кормовые дрожжи, кормовой лизин, виноградная мука, белколизин). Сухие питательные среды могут храниться в течение длительного времени, удобны при транспортировке и имеют относительно стандартный состав.
По консистенции питательные среды могут быть жидкими, полужидкими, плотными. Плотные среды готовят путем добавления к жидкой среде 1,5—2% агара, полужидкие — 0,3— 0,7 % агара. Агар представляет собой продукт переработки особого вида морских водорослей, он плавится при температуре 80—86 °С, затвердевает при температуре около 40 °С и в застывшем состоянии придает среде плотность. В некоторых случаях для получения плотных питательных сред используют желатин (10—15%). Ряд естественных питательных сред (свернутая сыворотка крови, свернутый яичный белок) сами по себе являются плотными.
По целевому назначению среды подразделяют на основные, элективные и дифференциально-диагностические.
К основным относятся среды, применяемые для выращивания многих бактерий. Это триптические гидролизаты мясных, рыбных продуктов, крови животных или казеина, из которых готовят жидкую среду — питательный бульон и плотную — питательный агар. Такие среды служат основой для приготовления сложных питательных сред — сахарных, кровяных и др., удовлетворяющих пищевые потребности патогенных бактерий.
Элективные питательные среды предназначены для избирательного выделения и накопления микроорганизмов определенного вида (или определенной группы) из материалов, содержащих разнообразную постороннюю микрофлору. При создании элективных питательных сред исходят из биологических особенностей, которые отличают данные микроорганизмы от большинства других. Например, избирательный рост стафилококков наблюдается при повышенной концентрации хлорида натрия, холерного вибриона — в щелочной среде и т. д.
Дифференциально-диагностические питательные среды применяются для разграничения отдельных видов (или групп) микроорганизмов. Принцип построения этих сред основан на том, что разные виды бактерий различаются между собой по биохимической активности вследствие неодинакового набора ферментов.
Особую группу составляют синтетические и полусинтетические питательные среды. В состав синтетических сред входят химически чистые вещества: аминокислоты, минеральные соли, углеводы, витамины. В полусинтетические среды дополнительно включают пептон, дрожжевой экстракт и другие питательные вещества. Эти среды чаще всего применяют в научно-исследовательской работе и в микробиологической промышленности при получении антибиотиков, вакцин и других препаратов.
В последние годы в целях экономии питательных сред и ускоренной идентификации некоторых микроорганизмов (энтеробактерии, стафилококки, стрептококки и др.) применяются так называемые микротест-системы (МТС). Они представляют собой полистироловые пластины с лунками, в которых содержатся стерильные дифференциально-диагностические среды. Стерилизацию МТС проводят УФ-облучением. Микротест-системы особенно удобны при массовых бактериологических исследованиях в практических лабораториях.
Источник