- Лабораторная работа №6 Получение синтез-газа конверсией метана
- Главная > Документ
- Синтез-газ
- Определение
- Получение
- Конверсия метана с паром
- Парциальное окисление метана
- Транспортировка
- Применение
- Получение аммиака
- Получение метанола
- Синтез Фишера-Тропша
- Технология получения синтез-газа паровой конверсией углеводородов
- Выводы
Лабораторная работа №6 Получение синтез-газа конверсией метана
Главная > Документ
| Информация о документе | |
| Дата добавления: | |
| Размер: | |
| Доступные форматы для скачивания: |
ЛАБОРАТОРНАЯ РАБОТА № 6
Получение синтез-газа конверсией метана
Синтез-газ — смесь монооксида углерода и водорода — широко используется в промышленности для производства жидких и газообразных углеводородов (синтез Фишера-Тропша), а также для получения кислородсодержащих продуктов (метанола, высших спиртов, альдегидов и.т.п.)
Основной метод получения синтез-газа — конверсия углеводородов при высоких температурах с водяным паром, со смесью водяного пара и диоксида углерода или водяного пара с кислородом. Чаще всего в качестве сырья используют метан, в некоторых случаях — каменный уголь.
В общем виде основная реакция конверсии углеводородного сырья водяным паром выражается уравнением:
С n Н n +2 + n Н 2 O nСО + (2n+1)Н 2 ; — Q
При конверсии метана протекают следующие реакции:
1. СН 4 + Н 2 O СО + ЗН 2 ; — 206 кДж/моль
2. СО + Н 2 O СО 2 + Н 2 ; + 41 кДж/моль
3. СН 4 +СО 2 2СО+2Н 2 ; — 248,3 кДж/моль
Все они обратимы и идут с увеличением объема. При необходимости получения синтез-газа с мольным соотношением Н 2 :СО = 2:1, которое используется при синтезе метанола, основного продукта, производимого из синтез-газа, к исходному сырью добавляют 5 — 7% СО 2 .
В настоящее время конверсию метана проводят в присутствии катализаторов, наиболее эффективными из которых являются катализаторы на основе оксида никеля.
Отечественные катализаторы марки ГИАП представляют собой цилиндры или кольца размером от 11х11×7 до 20х20х7мм. Они содержат от 4 до 30% оксида никеля (NiO), нанесенного на оксид алюминия Al 2 O 3 . Для повышения активности катализаторов в качестве промоторов используют MgO, Сг 2 O 3 , ТiO 2 , CaO, ZrO 2 и т.д. В частности, катализатор, использованный в данной работе — ГИАП-25 представляет собой кольца размером 15х17х4 мм и содержит 25% NiO, 46%А1 2 O 3 , 14%CuO, 15%MgO.
Оптимальными условиями конверсии метана являются: температура 800 — 900°С, давление до 2 МПа, объемная скорость подачи метана 600ч -1 и мольное соотношение Н 2 O:CH 4 , равное (2-3:1).
Сырье, поступающее на конверсию, должно быть тщательно очищено от соединений серы, которые являются сильными ядами для никелевых катализаторов. Содержание серы в сырье не должно превышать 2— 3 мг серы на 1м 3 .
Получение смеси СО и Н 2 — синтез-газа — паровой каталитической конверсией метана, составление материального баланса опыта и расчет основных показателей процесса: конверсии метана и воды, выходов синтез-газа на пропущенное и разложенное сырье, селективности процесса, соотношения СО:Н 2 .
катализатор ГИАП -25.
Объем катализатора в реакторе составляет 20 см 3 ; объемная скорость газа 600 час -1 (на исходный сухой газ), мольное отношение Н 2 O:СН 4 =2:1, температура опыта 850°С.
После получения задания от преподавателя, студент рассчитывает объемные скорости подачи воды и метана, зная объем загруженного в реактор катализатора, время проведения опыта и мольное отношение метан : вода.
После проверки выполненных расчетов преподавателем, студент приступает к выполнению работы. В конце опыта определяется количество воды, фактически поданное за опыт, на основании которого рассчитываются фактические параметры проведения процесса (объемная скорость и мольное соотношение метан:вода) и результаты опыта (конверсия метана, селективность процесса, выходы).
Конверсию метана проводят на установке, схема которой приведена на рис. 11.
Включают электрообогрев печей 3 сероочистки и 15 реактора 6. Устанавливают температуру на измерителях — регуляторах 350°С и 800°С соответственно. Включают охлаждение водяного холодильника 7. Далее необходимо включить насос-дозатор воды 10, установить на нем рассчитанный расход воды. До выхода установки на рабочий температурный режим газ необходимо пустить в обход реактора. Для этого трехходовой кран 5 поворачивают в положение сброса газа. Затем поворотом вентиля тонкой регулировки 1 устанавливают расход газа по реометру 2. После того как в реакторе установилась постоянная температура реакции, поворотом крана 5 начинают подачу газа в реактор 6 и замеряют уровень воды в мерном цилиндре 16. Спустя некоторое время, (5 мин) из приемной колбы 8 сливают накопившуюся воду. Затем поворотом кранов 12 и 14 (при закрытом кране 11) начинают набирать газ в газометр 13 и с этого момента начинают отсчет времени опыта. Тщательно следят за ходом протекания процесса (температура, расходы метана и воды).
На следующем этапе выполнения работы необходимо произвести отбор газа из газометра 13. Для этого открывают кран 11 на газометре 13, и поворотом крана 9 направляют воду в газометр для создания небольшого избыточного давления. Закрывают кран 11, поворотом крана 12 направляют газ на линию сброса и быстро присоединяют стеклянную бюретку с напорной склянкой к линии сброса газа.
Рис. 11. Схема установки конверсии метана
1 — вентиль тонкой регулировки подачи газа; 2 — реометр; 3 — печь сероочистки; 4 — кварцевая трубка с СuО; 5,9,12 — трехходовые краны; 6 — реактор; 7 — обратный холодильник; 8 — приемная колба для воды; 10 — насос-дозатор для подачи воды; 11, 14 — краны; 13 — газометр; 15 — печь реактора; 16 — мерный цилиндр; 17, 18 -термопары; 19, 20 — измерители-регуляторы температуры;
Ставят напорную склянку ниже бюретки, открывают краны на бюретке и начинают отбор газа на анализ. После того как необходимое количество газа будет находиться в бюретке, закрывают краны и переводят кран 12 в нейтральное положение. Наполненную газом бюретку отдают лаборанту для анализа. Далее открывают кран 11 и кран 12, начинают заполнять водой газометр 13.
После каждого опыта необходимо регенерировать катализатор. Для этого через реометр 2 начинают подавать воздух в реактор 6 с помощью компрессора. Степень регенерации катализатора проверяют спустя 1 час путем пропускания газа через баритовую воду. После завершения процесса регенерации отключают питание печи 15, продолжая подавать воду в реактор 6 еще около 30 минут до снижения температуры в нем до 400°С. Затем прекращают подачу воды, охлаждают реактор до комнатной температуры.
Обработка экспериментальных данных
При подготовке к лабораторной работе студент оформляет таблицу 20, которая заполняется данными по мере их получения во время опыта
Источник
Синтез-газ
Определение
Понятие «синтез-газ» применяют к разным смесям монооксида углерода (СО) и водорода (Н2), которые используются для получения некоторых нефтехимических продуктов. Его в основном получают из природного газа (метана). Действительно, важнейшие вещества — аммиак, метанол и парафиновые углеводороды — получают именно из синтез-газа.
Получение
Существуют два основных метода получения синтез-газа – конверсия метана с водяным паром и парциальное (частичное) окисление. Оба метода довольно просты.
Конверсия метана с паром
Конверсия с паром состоит в пропускании метана или нафты и водяного пара над никелевым катализатором. Реакция протекает за счет разрушительной силы высоких температур и давлений, и ее следует проводить в реакторах, аналогичных печам крекинга. При этом происходят побочные процессы, при водящие к образованию СО2 и углерода. Углерод откладывается на катализаторе и дезактивирует его.
Парциальное окисление метана
Другой метод — это парциальное (частичное) окисление метана. Процесс проводят при высоких температурах без катализатора. Метод парциального окисления обычно используют для превращения более тяжелых видов сырья — от нафты до остаточного топлива — в тех случаях, когда в распоряжении нет природного газа и легких углеводородов (этана, пропана и бутана). В обоих процессах выход суммы СО и Н2 составляет 90 – 95%.
В качестве побочного продукта получают СО2, который можно удалить либо экстракцией растворителем, либо можно ввести в реакцию с водяным паром дополнительное количество метана, что даст СО и Н2. Эта реакция протекает при высоких температурах и давлениях и в присутствии никелевого катализатора.
Транспортировка
Обычно установка по производству синтез-газа бывает интегрирована в структуру завода, на котором он перерабатывается.
Единственным приемлемым способом транспортировки синтез-газа является его транспортировка по трубопроводам.
Применение
Получение аммиака
Наиболее важной областью применения синтез-газа является производство аммиака – NH3.
Смесь азота и водорода пропускают над железным катализатором (который содержит оксид алюминия в качестве промотора). Реакция проходит в очень жестких условиях — при температуре 420 С и давлении 280 атм.
Большая часть установок по производству аммиака снабжена оборудованием для отделения СО от сырья, так как СО может отравлять катализатор. Чаще всего с этой целью СО обрабатывают водяным паром для получения СО и Н2. Диоксид углерода удаляют экстракцией этаноламином, а Н2 направляют на рециркуляцию.
Получение метанола
Метанол часто называют древесным спиртом. Это связано с тем, что первым промышленным способом получения метанола была сухая перегонка свежеспиленной древесины лиственных деревьев. Помимо других соединений в летучей фракции присутствует метанол. Отсюда и произошло название «древесный спирт».
С 1923 г. метанол производится в промышленности из синтез-газа; в настоящее время большую часть метанола получают именно таким методом. По нескольким причинам эти установки обычно строят вблизи установок для производства аммиака или даже объединяют с ними.
Технология и оборудование аналогичны, и в производстве метанола можно использовать СО2, образующийся при синтезе аммиака. В этом случае СО2 вводят в реакцию с метаном и водяным паром над никелевым катализатором, приводящую к образованию дополнительного количества СО и Н2, которые затем взаимодействуют, давая метанол.
Процесс проводят при давлении 67 – 100 атм. И температуре 200 – 260оС на катализаторах на основе оксидов меди и цинка.
Синтез Фишера-Тропша
Каталитическое гидрирование оксида углерода (синтез Фишера-Тропша) для получения углеводородов, в частности парафинов, в основном нормального строения и олефинов, является гетерогенной реакцией. Проводится она преимущественно над кобальтовыми или над железными катализаторами с использованием возможно более чистых смесей оксида углерода и водорода. Оптимальные рабочие температуры синтеза различны для различных катализаторов.
Никелевые и кобальтовые катализаторы дают оптимальные результаты при 170-205, железные — при 200-325°С. Синтез на никелевых катализаторах ведется практически только при нормальном давлении, так как при повышенном давлении резко усиливается образование карбонилов.
На железном и кобальтовом катализаторах можно работать без образования карбонилов при давлениях до 20 атм.
Считается, что при синтезе по Фишеру-Тропшу на железных катализаторах оксид углерода гидрируется с образование метиленовой группа, которая затем полимеризуется. Оксид углерода конвертируется в углекислоту. При этом кислород оксида углерода связывается, образуя воду. Этим реакциям благоприятствуют более высокая температура синтеза на железных катализаторах и активность железа по отношению к реакции конверсии.
С технической точки зрения решающее значение при синтезе Фишера-Тропша имеют, во-первых, очень большая теплота реакции каталитического гидрирования оксида углерода и, во-вторых, необходимость очень точного соблюдения постоянной температуры синтеза. В противном случае значительно возрастает нежелательное образование метана. Кроме того, при высоких температурах наблюдается отложение углерода на катализаторе, приводящее к быстрой его дезактивации.
Источник
Технология получения синтез-газа паровой конверсией углеводородов
Авторы: С.В. Афанасьев (Тольяттинский государственный университет), О.С. Рощенко (ОАО «Тольяттиазот»), С.П. Сергеев (ОАО «ГИАП»).
Опубликовано в журнале Химическая техника №6/2016
Cинтез-газ является смесью водорода и оксида углерода и широко используется в химической промышленности для получения базовых продуктов – аммиака, метанола, уксусной кислоты и др. Кроме того, он применяется в качестве экологически чистого источника тепловой энергии.
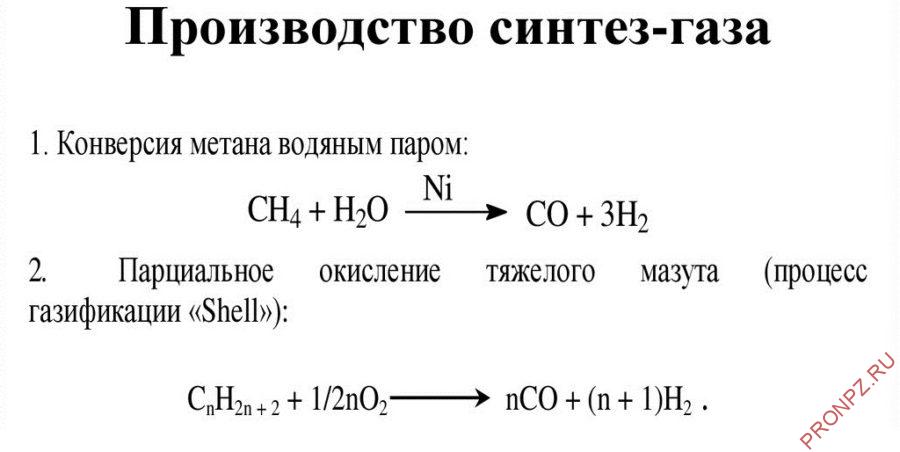
Сегодня существуют три основных метода производства синтез-газа. 1. Газификация угля. Данный процесс основан на взаимодействии каменного угля с водяным паром и протекает по формуле
Приведенная реакция является эндотермической, и равновесие при температуре 900…1000°С сдвигается вправо. Разработаны различные технологические процессы, использующие парокислородное дутье, благодаря которому наряду с упомянутой реакцией параллельно протекает экзотермический процесс сгорания угля, который обеспечивает необходимый тепловой баланс. 2. Конверсия метана – взаимодействие водяного пара и метана при повышенных значениях температуры и давлении в присутствии никелевых катализаторов (Ni–Al2O3):
CH4 + H2O → CO + 3H2.
Вместо метана можно использовать любое сырье, содержащее углеводороды. 3. Парциальное окисление углеводородов. Данный процесс, происходящий при температурах выше 1300°С, заключается в термическом окислении углеводородов:
CnH2n +2 + 1/2nO2 → nCO + (n + 1)H2.
Настоящее исследование посвящено усовершенствованию промышленного способа получения синтез-газа, обогащенного водородом и монооксидом углерода, путем каталитического риформинга углеводородсодержащего сырья в трубчатых реакторах с использованием катализаторов определенной конструктивной формы с целью внедрения на крупнотоннажных производствах аммиака, метанола, уксусной кислоты и водорода.
При осуществлении указанного процесса реализуются следующие эндои экзотермические реакции:
СnHm + nH2O → nCO + (n + m/2)H2 (–ΔHо 298 Способ осуществления парового риформинга
%
Как видно, по сравнению с известным методом наблюдается снижение содержания метана в вырабатываемом синтез-газе, что указывает на повышение активности катализатора.
Согласно выполненным кинетическим и теплофизическим расчетам, установка в печи риформинга реакционных труб с уменьшенным внутренним диаметром (101 мм) позволит снизить температуру конвертированного газа и содержание остаточного метана, существенно повысить производительность установки по синтезгазу (табл. 2).
Параметры работы печи риформинга с реакционными трубами разного диаметра
| Производительность, т/сутки | 1950…2000 | 1750…1800 | 1440 | 1440 (база) |
| Внутренний диаметр трубы, мм | 101 | 101 | 102 | 89 |
| Температура конвертированного газа, °С: | ||||
| в центре трубы | 718,5 | 721,1 | 732,1 | 732,9 |
| у стенки | 743,5 | 745,8 | 755,6 | 752,4 |
| Линейная скорость, м/с: | ||||
| в центре трубы | 2,233 | 2,084 | 1,996 | 2,536 |
| у стенки | 2,288 | 2,126 | 2,002 | 2,549 |
| Содержание метана в сухом газе на выходе из трубы, мол. % | 13,2557 | 12,1942 | 11,7262 | 12,6346 |
| Соотношение пар : газ на выходе из реакционной трубы | 0,8831 | 0,8533 | 0,8009 | 0.8260 |
Выводы
Использование предлагаемого технического решения позволяет улучшить теплоперенос через стенку труб в печи риформинга и как результат снизить разность температур между их наружной поверхностью и выходящим синтез-газом. Одновременно с этим удается уменьшить перепад давления по катализаторному слою, сократить расход топливного газа на проведение конверсии, увеличить выработку синтез-газа на агрегатах аммиака.
Источник