Методы выделения и очистки ферментов — это методы выделения и очистки белков.



Очистка фермента начинается с выделения данного фермента из грубого клеточного экстракта, содержащего множество других компонентов. Небольшие молекулы удаляются диализом или гель-фильтрацией, нуклеиновые кислоты осаждаются путем добавления антибиотиков (стрептомицина) и т.д. Основная проблема—отделить нужный фермент от сотен химически и физически сходных белков. Если контроль за выделяемым белком доставляет довольно много хлопот исследователю, о присутствии фермента и его количестве на всех этапах очистки можно следить по его активности. В общем виде под активностью понимают количество фермента или биологического материла, содержащего фермент, которое при определенных условиях катализирует в единицу времени превращение определенного количества реагента, называемого субстратом. Активность — это изменение количества субстрата под влиянием фермента в единицу времени. Под изменением субстрата понимают снижающееся в единицу времени количество субстрата или же увеличивающееся количество продукта. Понятие «активность фермента» по сути дела идентична понятию «скорость ферментативной» реакции. Ферментативная активность выражается в единицах активности. В связи с существованием различных систем единиц исчисления введена интернациональная (стандартная)единица активности. Она носит символ «U» (unit-единица) и определяется как 1 мкмоль субстрата/мин. В системе СИ в качестве единицы ферментативной активности используют «катал» (kat). Катал определяется как 1 моль/сек.
1kat = 1 моль/сек.
Размерность её слишком велика, на практике пользуются меньшими кратными значениями, начиная с нанокатала (нкат). Это одна миллиардная катала или 10 -9 кат. В сравнении с международной единицей следующее уравнение
В практике лабораторий широко пользуются понятием удельная активность. Для этого число cтандартных единиц пересчитывают на какую-либо единицу сравнения. Это может быть мг белка в пробе или объем исследуемой биологической жидкости. Определение активности ферментов широко распространено в любой современной клинической лаборатории.
При исследовании кинетики реакций используется и такое понятие как молекулярная активность. Она показывает, сколько молекул субстрата в секунду превращаются в продукт 1 молекулой фермента и используется для сравнительной характеристики активности нескольких ферментов.
Пример вычисления активности фермента:
| Исходные данные: | Через 10 мин: |
| 25.0 x 10 -3 моль л —1 пептида-субстрата, объем реакционной смеси 2.5 мл, 0.50 µг химотрипсина[4] | 18.6 x 10 -3 моль л —1 пептида -субстрата, Объем реакционной смеси 2.5 мл, 0.50 µг химотрипсина. |
| Использованный субстрат | = 6.4 x 10 -3 моль л -1 за 10 мин |
| Скорость реакции | = 6.4 x 10 -4 моль л -1 мин -1 |
| Активность Фермента (скорость x объем) | = 6.4 x 10 -4 моль л -1 мин -1 x 2.5 x 10 -3 л = = 1.6 x 10 -6 моль мин -1 |
| Удельная активность (активность / масса) | = 1.6 x 10 -6 моль мин -1 / 0.50 µг = = 3.2 x 10 -6 моль µг -1 мин -1 |
| Число оборотов (уд. акт. x молярная масса) | = 3.2 x 10 -6 моль µг -1 мин -1 x 25,000 x 10 6 µг моль -1 = 8.0 x 10 4 мин -1 =1330 сек -1 |
Если удельная активность, рассчитанная выше, относится к чистому химотрипсину, образец, давший, например, удельную активность 2.0 x 10 -7 моль µг -1 мин -1 — 100 % x 2.0 x 10 -7 / 3.2 x 10 -6 или 6.3 % чистоты. 1.0 µг такого образца на самом деле содержит лишь 0.063 µг химотрипсина и 0.937 µг примесей.
Методы исследования активности определяются механизмом реакции и природой опре
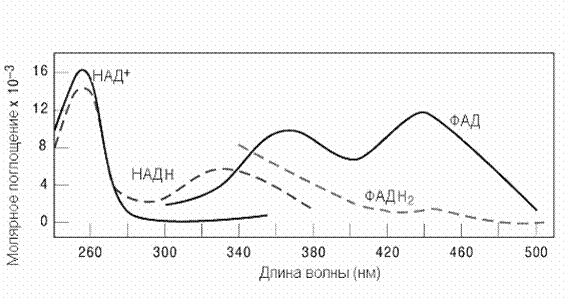
Рис2-4. Молярное поглощение НАД + ,НАДН+Н + , ФАД, ФАДН2 при разных длинах волн поглощаемого света
деляемого вещества. Наиболее широко используются:
· Измерение изменения спектральных свойств (измерение поглощения света в видимой или ультрафиолетовой области, измерение флюоресценции) при помощи спектрофотометров, ФЭКов, спектрофлуориметров. Эти методы применяют и для определения количества продуктов или субстратов реакции, и для изменений количества коферментов, участвующих в реакции. Последнее нашло широкое применение в практике клинических биохимических лабораторий. В основе этих методов лежит закон Beer-Lambert: A = e x c x l = log (I0/I) (e, поглощение 1 M раствора вещества при специфической длине волны или молярный коэффициент экстинкции; c, концентрация ; A, поглощение ; l, длина в см кюветы спектрофотометра ; I0, интенсивность падающего света; I, интенсивность прошедшего света). В случае, если молярный коэффициент экстинкции (e) исследуемого вещества неизвестен, исследователь определяет экспериментально зависимость между поглощением света исследуемого раствора и концентрацией этого вещества и использует полученную закономерность в форме стандартного (калибровочного) графика.

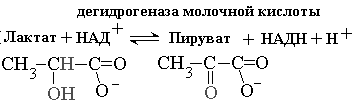
На рисунке 2-4 показаны спектральные характеристики коферментов НАД и ФАД в окисленной и восстановленной форме. Измерение поглощения при 340 нм используется для количественной оценки активности ферментов, катализирующих окислительно-восстановительные реакции c участием НАД. Вот пример такого расчета для реакции, катализируемой лактатдегидрогеназой В этой реакции молочная кислота окисляется, передавая водороды на НАД + . При этом НАД + восстанавливается до НАДН +Н + ., который в отличие от НАД + поглощает свет с длиной волны 340 нм. Допустим, за время проведения реакции поглощение при длине волны 340 нм изменялось на 0.31 единицы в минуту. Измерения проводили в кювете шириной 1 см. Коэффициент молярной экстинкции для НАДН при 340 нм e = 6200 л моль -1 см -1 .
| Увеличение [НАДH] = | Увеличение поглощения e . l | 0.31 | =5.0 х10 -5 моль/л |
Эту величину можно использовать для оценки скорости реакции.
· Измерение изменений концентрации высвобождаемых или поглощаемых во время реакции H + или ОН — при помощи pH-стата (устройство, которое автоматически добавляет кислоту или основание, сохраняя постоянство pH в реагирующей смеси)
· Химический анализ с использованием высокоразрешающей жидкостной или газовой хроматографии, или ЯМР или тонкослойной хроматографии. (АТФазы)
· Изотопный анализ (например, с использованием радиоактивного 32 P)
·
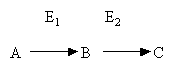 |
Сопряженные реакции – используются в случаях, если нет возможности прямо определить количество продукта исследуемой реакции. В таких случаях в реагирующую смесь добавляется фермент (Е2) катализирующий превращение образующегося продукта в реакции, которую можно оценить количественно, одним из вышеперечисленных методов.
Если фермент Е2 присутствует в избытке, скорость образования C отражает скорость образования В.
Например, сопряженное исследование активности глюкокиназы (используется избыток глюкозо-6-фосфат дегидрогеназы и НАДФ + )
Глюкоза + AТФ → глюкоза 6-Ф + AДФ : (катализируется глюкокиназой –Е1)
Глюкоза-6-Ф + НАДФ + → 6-фосфоглюконолактон + НАДФН + H + : ( катализируется глюкоза-6Ф –дегидрогеназой – Е2):
Скорость образования НАДФH (измеряется по поглощению при 340 нм) пропорциональна активности глюкокиназы (см выше)
Классические методы очистки. Широко используются следующие методы очистки: осаждение различными концентрациями солей щелочно — земельных металлов (чаще всего сульфата аммония или сульфата натрия) или сочетанием их с органическими растворителями (ацетоном, этанолом), дифференциальная денатурация путем нагревания или изменения рН, дифференциалъное центрифугирование, гель-фильтрация и электрофорез.
Для быстрой очистки ферментов успешно применяется избирательная адсорбция и элюция белков с ионобменников (ДЭАЭ или КМ производные целлюлозы или других полимеров). Широко используется также: разделение белков по размерам при помощи гель-фильтрации. Все эти методы являются, однако, относительно мало избирательными (если они не используются в сочетании) для выделения индивидуального белка из сложной смеси клеточных ферментов.Значительно упрощается такая задача при помощи метода аффинной хроматографии.
| Табл 2-1. Типичная процедура очистки одного из ферментов печени | ||||
| Этапы очистки | Суммарная активность ед | Суммарный белок мг | Удельная активность ед/мг | Выход % |
| 1. Водно-солевой экстракт плаценты | 0.408 | (100) | ||
| 2. Осадок ,образующийся после осаждения 65% -ным (NH4)2SO4 | 0.674 | 90.7 | ||
| 3. Осадок ,образующийся после осаждения 35-65% -ным (NH4)2SO4 | 3.781 | 85.2 | ||
| 4. Активная фракция после хроматографии на ДЭАЭ-целлюлозе осадка фракции 3 | 8.252 | 78.5 | ||
| 5. Активная фракция после хроматографии фракции 4 на фосфоцеллюлозе | 59.1 | 58.4 | ||
| 6. Активная фракция после гель фильтрации фракции 5 | 110.8 | 227.2 | 53.4 | |
| 7. Повторение этапа 6. | 88.8 | 216.7 | 40.1 |
Типичная процедура очистки одногоиз ферментов печени с хорошим выходом и 227-кратной степенью очистки препарата описана в табл 2-1. Обратите внимание на изменение при очистке удельной активности и выхода фермента. Процедура направлена на достижение максимальной удельной активности (число единиц активности фермента на 1 мг белка) при возможно большем выходе исходной суммарной активности. Из данных таблицы видно, что уже в процессе очистки решаются проблемы исследования свойств фермента. Повторение этапа 6 привело к снижению удельной активности, что возможно связано с особенностями физико-химических свойств выделяемого фермента.
Источник
Методы выделения ферментов



Процесс выделения какого-либо белка начинается с переведения белков ткани в раствор. Для этого ткань (материал), из которой получают фермент, тщательно измельчают в гомогенизаторе в присутствии буферного раствора. Для лучшего разрушения клеток к материалу добавляют кварцевый песок, если материал растирают в ступке. В результате получают кашицу — гомогенат. Если не проводилось предварительное фракционирование органоидов клетки, гомогенат содержит обрывки клеток, ядра, хлоропласты и другие органоиды клеток, растворимые пигменты и белки.
При выделении ферментов из тканей живых организмов, в том числе растительных, необходимо соблюдать условия, не вызывающие денатурацию белка. Все работы проводят при пониженной температуре (4 0 С) и при оптимальных для данного фермента значениях pH среды буферного раствора.
После перевода ферментов из ткани в растворенное состояние гомогенат подвергают центрифугированию для отделения нерастворимой части материала, а затем в отдельных фракциях экстрата-центрифугата выделяют следуемые ферменты.
Так как все ферменты являются белками, то для получения очищенных препаратов ферментов применяются те же способы выделения, что и при работе с белками.
· осаждение белка органическими растворителями;
· метод ионообменной хроматографии;
· метод аффинной хроматографии, или метод хроматографии по сродству;
Источник
Выделение и очистка ферментов.
Объект, задачи инженерной энзимологии, базовые технологи.
Задачи заключаются в развитии прогрессивных методов выделения ферментов, их стабилизации и иммобилизации; конструировании катализаторов с нужными свойствами и разработке научных основ их применения. Методами белковой инженерии, сущность которых состоит в изменении первичной структуры природной молекулы фермента посредством химической модификации самого; энзима или его гена, удается принципиально трансформировать структуру активного центра и его функцию, модулировать субстратную специфичность и физико-химические свойства фермента. Многие проблемы технологии синтеза органических соединений, пищевой и медицинской промышленности, мониторинга человека и окружающей среды, защиты окружающей среды, энергетики не могут быть решены без использования методов современной инженерной энзимологии.Важным этапом развития инженерной энзимологии стала разработка способов получения и использования иммобилизованных ферментов.
Носители для иммобилизированных ферментов биокатализаторов ( орг полимеры, неорг, полимерные синтетики).
Иммобилизованными ферментами называются ферменты, искусственно связанные с нерастворимым носителем, но сохраняющие свои каталитические свойства.
Носители для иммобилизации ферментов
По Дж. Поратуидеальные материалы, используемые для иммобилизации ферментов, должны обладать следующими основными свойствами: нерастворимостью; высокой химической и биологической стойкостью; значительной гидрофильностью; достаточной проницаемостью как для ферментов, так и для коферментов, субстратов и продуктов реакции; способностью носителя легко активироваться.
В зависимости от природы носители делятся на органические и неорганические материалы.
Органические полимерные носители. Иммобилизация многих ферментов осуществляется на полимерных носителях органической природы. Существующие органические полимерные носители можно разделить на два класса: природные и синтетические полимерные носители. В свою очередь, каждый из классов органических полимерных носителей подразделяется на группы в зависимости от их строения. Среди природных полимеров выделяют белковые, полисахаридные и липидные носители, а среди синтетических — полиметиленовые, полиамидные и полиэфирные.
К преимуществам природных носителей следует отнести их доступность, полифункциональность и гидрофильность, а к недостаткам — биодеградируемостьи достаточно высокую стоимость.
Из полисахаридов для иммобилизации наиболее часто используют целлюлозу,агарозу и их производные. Для придания химической устойчивости линейные цепи целлюлозы и декстрана поперечно сшивают эпихлоргидрином. В полученные сетчатые структуры довольно легко вводят различные ионогенные группировки. Химической модификацией крахмала сшивающими агентами (формальдегид, глиоксаль) синтезирован новый носитель — губчатый крахмал, обладающий повышенной устойчивостью к гликозидазам.
Из природных аминосахаридов в качестве носителей для иммобилизации применяют хитин, который в значительных количествах накапливается в виде отходов в процессе промышленной переработки крабов и креветок. Хитин химически стоек и имеет хорошо выраженную пористую структуру.
Среди белков практическое применение в качестве носителей нашли структурные протеины, такие, как кератин, фиброин, коллаген и продукт переработки коллагена — желатина. Эти белки широко распространены в природе, поэтому доступны в значительных количествах, дешевы и имеют большое число функциональных групп для связывания фермента. Белки способны к биодеградации, что очень важно при конструировании иммобилизованных ферментов для медицинских целей. К недостаткам белков как носителей в этом случае следует отнести их высокую иммуногенность.
Синтетические полимерные носители. Благодаря разнообразию и доступности материалы этой группы широко используются как носители для иммобилизации. К ним относятся полимеры на основе стирола, акриловой кислоты, поливинилового спирта; полиамидные и полиуретановые полимеры. Большинство синтетических полимерных носителей обладают механической прочностью, а при образовании обеспечивают возможность варьирования в широких пределах величины пор, введения различных функциональных групп. Некоторые синтетические полимеры могут быть произведены в различных физических формах.
Носители неорганической природы. В качестве носителей наиболее часто применяют материалы из стекла, глины, керамики, графитовой сажи, силикагеля, а также оксиды металлов. Их можно подвергать химической модификации, для чего носители покрывают пленкой оксидов алюминия, титана, гафния, циркония или обрабатывают органическими полимерами. Основное преимущество неорганических носителей — легкость регенерации. Подобно синтетическим полимерам неорганическим носителям можно придать любую форму и получать их с любой степенью пористости.
Методы иммобилизации: а) физические (адсорбция, включения в гель, вкл в полупроницаемые структуры; б) химические (ковалентная связь с ОН-группой, NH2-группой, СООН-группой, SH-группой)
Существуют два принципиально различных метода иммобилизации ферментов: без возникновения ковалентных связей между ферментом и носителем (физические методы иммобилизации) и с образованием ковалентной связи между ними (химические методы иммобилизации).
Адсорбция.К недостаткам адсорбционного метода следует отнести невысокую прочность связывания фермента с носителем. При изменении условий иммобилизации могут происходить десорбция фермента, его потеря и загрязнение продуктов реакции. Существенно повысить прочность связывания фермента с носителем может предварительная его модификация (обработка ионами металлов, полифункциональными агентами — полимерами, белками, гидрофобными соединениями, монослоем липида).
Иммобилизация ферментов путем включения в гель. Способ иммобилизации ферментов путем включения в трехмерную структуру полимерного геля широко распространен благодаря своей простоте и уникальности. Метод применим для иммобилизации не только индивидуальных ферментов, но и мультиэнзимных комплексов и даже интактных клеток. Иммобилизацию ферментов в геле осуществляют двумя способами. В первом случае фермент вводят в водный раствор мономера, а затем проводят полимеризацию, в результате которой возникает пространственная структура полимерного геля с включенными в его ячейки молекулами фермента. Во втором случае фермент вносят в раствор уже готового полимера, который впоследствии переводят в гелеобразное состояние. Для первого варианта используют гели полиакриламида, поливинилового спирта, силикагеля, для второго — гели крахмала, агар-агара, агарозы, фосфата кальция. Иммобилизация ферментов в гелях обеспечивает равномерное распределение энзима в объеме носителя. Однако метод непригоден для иммобилизации ферментов, действующих на водонерастворимые субстраты.
Иммобилизация ферментов в полупроницаемые структуры. Сущность этого способа иммобилизации заключается в отделении водного раствора фермента от водного раствора субстрата с помощью полупроницаемой мембраны, пропускающей низкомолекулярные молекулы субстратов и кофакторов, но задерживающей большие молекулы фермента. Разработано несколько модификаций этого метода, из которых интерес представляет микрокапсулирование и включение ферментов в липосомы.
Первый способ предложен Т.Чангом и состоит в том, что водный раствор фермента включается внутрь замкнутой микрокапсулы, стенки которой образованы полупроницаемым полимером. Один из механизмов возникновения мембраны на поверхности водных микрокапсул фермента заключается в реакции межфазной поликонденсации двух соединений, одно из которых растворено в водной, а другое — в органической фазе. Достоинства метода микрокапсулирования — простота, универсальность, возможность многократного использования нативного фермента.
Близким к инкапсулированию методом иммобилизации можно считать включение водных растворов ферментов в липосомы, представляющие собой сферические или ламеллярные системы двойных липидных бислоев. Впервые данный способ был применен для иммобилизации ферментов Дж. Вайсманом и Дж. Сессом в 1970 г. Для получения липосом из растворов липида упаривают органический растворитель. Оставшуюся тонкую пленку липидов диспергируют в водном растворе, содержащем фермент. В процессе диспергирования происходит самосборкабислойных липидных структур липосомы, содержащий включенный раствор фермента.
Химические методы иммобилизации ферментов. Иммобилизация ферментов путем образования новых ковалентных связей между ферментом и носителем — наиболее массовый способ получений промышленных биокатализаторов. В отличие от физических методов этот способ иммобилизации обеспечивает прочную и необратимую связь фермента с носителем и часто сопровождается стабилизацией молекулы энзима.
Иммобилизация ферментов на носителях, обладающих гидроксогруппами. Наиболее распространенным методом образования ковалентной связи между ферментом и полисахаридным носителем или синтетическим диольнымсоединением является бромциановый метод, который был предложен Аксеном, Поратом и Эрнбаком. При обработке носителя бромцианом возникают реакционноспособныецианаты и имидокарбонаты, которые при взаимодействии с нуклеофильными аминогруппами фермента образуют производные изомочевины и уретанов.Иммобилизация путем химического присоединения биокатализатора к носителю отличается высокой эффективностью и прочностью связи.
Остальное на листке.
4) Виды каталитических систем: а) ферменты, б) клетки, в) субклеточные структуры, г) комбинир препараты.
Методы иммобилизации универсальны для всех видов иммобилизованных биокатализаторов — индивидуальных ферментов, клеток, субклеточных структур, комбинированных препаратов.
Наряду с иммобилизацией ферментов в последнее время все большее внимание уделяется иммобилизации клеток и субклеточных структур. Это объясняется тем, что при использовании иммобилизованных клеток отпадает необходимость выделения и очистки ферментных препаратов, применение кофакторов; создается возможность получения полиферментных систем, осуществляющих многостадийные непрерывно действующие процессы. В промышленных процессах чаще используют покоящиеся клетки. Растущие клетки нарушают структуру носителя. Образующиеся при делении дочерние клетки, покидая носитель, загрязняют целевой продукт. Для подавления роста иммобилизованных клеток растений используют дефицит фитогормонов, а рост клетки бактерий тормозят добавлением антибиотиков.
Иммобилизованные клетки микроорганизмов применяют для биотрансформации органических соединений, разделения рацемических смесей, гидролиза ряда сложных эфиров, инверсии сахарозы, восстановления и гидроксилирования стероидов. Разрабатывается реактор на основе иммобилизованных клеток дрожжей для получения этанола из мелассы, в котором дрожжи сохраняли бы способность к спиртовому брожению в течение 1800 ч. Из более чем 2000 известных в настоящее время ферментов иммобилизована и используется для целей инженерной энзимологии 1/10 часть (преимущественно оксидоредуктазы, гидролазы и трансферазы).
1) оксидоредуктазы — катализируют окислительно- восстановительные реакции;
2) трансферазы — катализируют реакции переноса целых атомных групп от одного соединения к другому; 3) гидролазы — катализируют реакции расщепления сложных соединений на более простые при участии воды;4) лиазы — катализируют реакции отщепления от субстратов отдельных групп с образованием двойных связей или присоединение групп к двойным связям;
5) изомеразы — катализируют реакции изомеризации; 6) лигазы (синтетазы) — катализируют реакции синтеза с участием АТФ или аналогичных трифосфатов.
Выделение и очистка ферментов.
Выделение и очистка фермента весьма трудоемкая и дорогостоящая процедура, поэтому, если фермент можно использовать в виде неочищенного препарата, его не очищают. Для успешного выделения ферментов из клеточного содержимого необходимо очень тонкое измельчение исходного материала вплоть до разрушения субклеточных структур: лизосом, митохондрий, ядер, которые имеют в своем составе многие индивидуальные ферменты. Для этого используют специальные мельницы и гомогенизаторы, а также ультразвук, метод попеременного замораживания и оттаивания ткани. Для высвобождения ферментов из мембранных структур клетки к гомогенатам добавляют небольшие количества детергентов (твин, тритон Х-100) или обрабатывают их энзимами — лизоцимом, целлюлазой, лецитиназой. Особое внимание при выделении ферментов уделяют проведению всех операций в условиях, исключающих денатурацию белка. При выходе ферментов из ферментера от культуральной жидкости посредством центрифугирования и последующее разрушение клеток в гомогенизаторе высокого давления. Для освобождения белков от нуклеиновых кислот полученный гомогенат обрабатывают сульфатом марганца до конечной концентрации этой соли в смеси. Осадок нуклеиновых кислот отделяется с помощью ротационной вакуум-фильтрации, а в образовавшийся фильтрат добавляют сульфат аммония до 45 % от его насыщения. Возникший осадок белков собирают с помощью центрифугирования или вакуум-фильтрации. Вся процедура очистки энзима от момента подачи бактерий в систему до момента получения осадка 3-галактозидазы занимает всего 1 ч.
В зависимости от свойств выделяемого фермента и сопутствующих ему балластных веществ при получении очищенных препаратов ферментов комбинируют различные приемы и методы, такие, как термическое фракционирование, осаждение органическими растворителями, солями и тяжелыми металлами, фильтрация на молекулярных ситах, ионообменная хроматография, электрофорез.На заключительных этапах очистки часто используют аффинную хроматографию, которая основана на способности ферментов избирательно связывать те или иные лиганды — субстраты, коферменты, конкурентные ингибиторы, аллостерические эффекторы. Такое связывание весьма специфично, что позволяет выделить тот или иной энзим из множества других белков. Очищенные ферментные препараты хранят при низкой температуре (до -80 °С). Для стабилизации ферментов в их препараты добавляют коферменты и субстраты.
Гель-фильтрация
С помощью метода гельфильтрации можно быстро разделить белки в соответствии с их размерами. Носителем для хроматографии является гель, который состоит из поперечно-сшитой трехмерной молекулярной сетки, сформированной в виде гранул. Чем больше поперечных сшивок, тем меньше размеры отверстий. Гель играет роль молекулярного сита. При пропускании раствора через колонку, наполненную гранулами сефадекса, крупные частицы, размер которых превышает размер пор сефадекса, будут двигаться быстро. Мелкие молекулы будут двигаться медленно, поскольку в процессе движения будут проникать внутрь гранул
Тепловая денатурация
На начальном этапе очистки для разделения белков иногда используют тепловую обработку. Она эффективна, если белок относительно устойчив в условиях нагревания, в то время как сопутствующие белки денатурируют. При этом варьируют рН раствора, продолжительность обработки и температуру.
После проведения первых этапов очистки белки в экстракте отличаются друг от друга растворимостью, молекулярной массой, величиной суммарного заряда молекулы, относительной стабильностью. Эти различия используют для дальнейшего разделения белков.
Дата добавления: 2018-05-12 ; просмотров: 1189 ; Мы поможем в написании вашей работы!
Источник