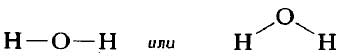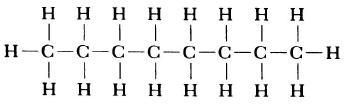- Урок 3. Схема образования молекул
- Молекулы состоят из атомов
- Связь атомов в молекулах
- Ковалентная химическая связь
- Молекулярная и структурная формула
- Относительная молекулярная масса вещества
- Способы отображения строения молекул. Формулы. Модели
- § 21. Способы изображения органических соединений
- 1. Какую информацию можно получить из молекулярной формулы органического соединения?
- 2. Приведены названия и формулы различных веществ: а) оксид углерода(IV) $\mathrm;$ б) дихлорметан $\mathrm;$ в) метан $\mathrm;$ г) карбонат натрия $\mathrm.$ Какие из них относятся к органическим веществам? К органическим веществам относят: б) дихлорметан $\mathrm;$ в) метан $\mathrm;$ к неорганическим — а) оксид углерода(IV) $\mathrm;$ г) карбонат натрия $\mathrm.$ 3. Назовите различия между шаростержневыми и масштабными моделями органических соединений. В шаростержневых моделях атомы изображают в виде трубок из пластмассы и отражают взаимное расположение атомов в пространстве. В масштабных моделях атомы изображают в виде сферы с размерами, пропорциональными их радиусу. 4. Раскройте сущность понятия «химическое строение вещества». Химическое строение — последовательность соединения атомов в молекулах органических соединений; в молекуле этана, например: атомы углерода соединены друг с другом, а атомы водорода связаны с атомами углерода. 5. Химическую связь между какими атомами указывает черточка в сокращенной структурной формуле этана $\mathrm<СН_3 - СН_3>?$ В сокращённой структурной формуле этана чёрточка показывает связь между атомами углерода. 6. Укажите общее число атомов в молекуле метана: а) 2; б) 3; в) 4; г) 5. Общее число атомов в молекуле метана $\mathrm$ равно 5 (г). 7. Попытайтесь написать структурную формулу органического соединения c молекулярной формулой $\mathrm,$ являющегося производным углеводорода этана. Структурная формула соединения $\mathrm$ 8. Изобразите соединение, показанное на рисунке 88, в виде структурной формулы. Структурная формула отображает порядок (последовательность) соединения атомов в молекулах. 9. На основании пространственного изображения молекулы этана на рисунке 86 попытайтесь изобразить пространственное строение молекулы с молекулярной формулой $\mathrm.$ Пространственное строение молекулы $\mathrm:$ Источник
- 3. Назовите различия между шаростержневыми и масштабными моделями органических соединений.
- 4. Раскройте сущность понятия «химическое строение вещества».
- 5. Химическую связь между какими атомами указывает черточка в сокращенной структурной формуле этана $\mathrm<СН_3 - СН_3>?$
- 6. Укажите общее число атомов в молекуле метана: а) 2; б) 3; в) 4; г) 5.
- 7. Попытайтесь написать структурную формулу органического соединения c молекулярной формулой $\mathrm,$ являющегося производным углеводорода этана.
- 8. Изобразите соединение, показанное на рисунке 88, в виде структурной формулы.
- 9. На основании пространственного изображения молекулы этана на рисунке 86 попытайтесь изобразить пространственное строение молекулы с молекулярной формулой $\mathrm.$
Урок 3. Схема образования молекул
В уроке 3 «Схема образования молекул» из курса «Химия для чайников» выясним из чего состоят молекулы и как образуется ковалентная химическая связь; кроме того рассмотрим структурную и молекулярную формулы молекулы; научимся вычислять относительную молекулярную массу веществ. Настоятельно рекомендую перед тем, как приступить к прочтению данного урока, внимательно изучить предыдущие, так как они содержат необходимые основы химии для начинающих и буду весьма полезны в изучении курса. Напомню, что в прошлом уроке мы обсуждали изотопы элементов.
Молекулы состоят из атомов
Здесь все просто и понятно: все вещества во вселенной состоят из молекул, в свою очередь молекулы состоят из атомов, а атомы состоят из положительно заряженного ядра и электронных оболочек, на которых расположены отрицательно заряженные электроны.
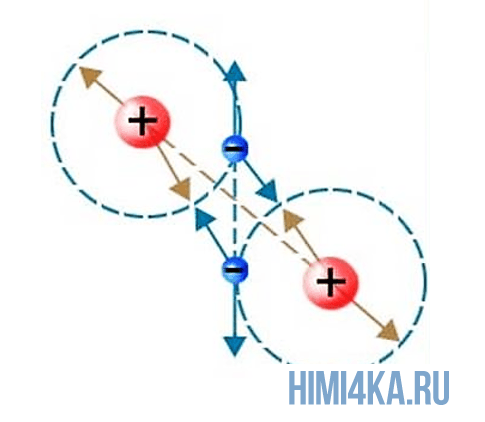
Представьте, что два атома достаточно сблизились друг с другом. В таком случае электроны на внешней оболочке одного атома начинают взаимодействовать с внешними электронами другого. Подобное взаимодействие внешних электронов и образует молекулы, так как оно способно удерживать взаимодействующие атомы вместе, притягивая их друг к другу.
Связь атомов в молекулах
Как было сказано выше, образование молекул происходит из-за внешних электронов взаимодействующих атомов, так как они создают силы притяжения между ними. Когда образуются данные силы притяжения происходит образование химической связи. В природе существует несколько видов химической связи атомов в молекулах, но пока рассмотрим простейший из них.
Ковалентная химическая связь
Химическая связь, возникающая при обобществлении внешних электронов взаимодействующих атомов, называется ковалентной химической связью. Обобществленные электроны называются электронной парой. Объяснение ковалентной химической связи простыми словами: два атома положили в общую копилку по монетке (электрону) и схватились за нее «руками», причем оба атома не хотят отдавать копилку друг другу, поэтому так и продолжают держаться за нее.
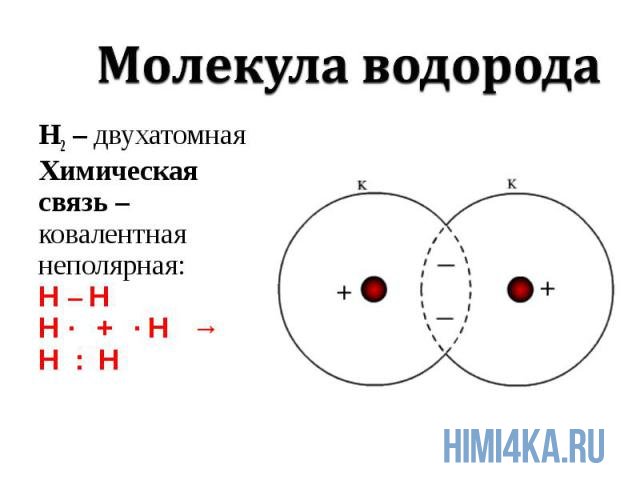
Ковалентная химическая связь подразделяется на два вида: неполярную и полярную. В этом уроке рассмотрим ковалентную неполярную химическую связь, которая возникает, когда в состав молекулы входят два абсолютно одинаковых атома неметалла , потому как одинаковые атомы владеют электронной парой в равной степени. А «Неполярная» — означает что заряд атомов не изменился, после образовании ковалентной связи. Приведем примеры молекул, образованных ковалентной неполярной химической связью: H2, O2, N2, Cl2. В редких случаях ковалентная химическая связь может образовываться между атомами разных неметаллов, но подробнее об этом в следующем уроке, где мы изучим электроотрицательность , и вам станет понятнее механизм образования химических связей атомов в молекулах.
Молекулярная и структурная формула
Графическое изображение структуры молекулы называется структурной формулой. Обычно ковалентная химическая связь в структурных формулах молекул изображается прямой линией, которая соединяет связанные атомы.
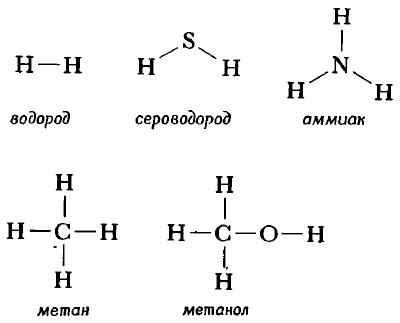
Структурную формулу молекулы воды H2O, к примеру, изображают двумя способами. Второй вариант структурной формулы воды, учитывает тот факт, что на самом деле молекула воды не линейна; две связи Н—О образуют угол 105° друг с другом. Молекулы газообразного водорода, сероводорода, аммиака, метана и метанола (метилового спирта) имеют следующие структурные формулы:
Структурная формула молекулы лишь схематично изображает связи между атомами, но не дает информации о реальной форме молекулы. Заметим, что угол между связями в молекулах, содержащих более двух атомов, может принимать различные значения. Так, угол между связями в молекуле воды равен 105°, а угол в молекуле сероводорода равен 92°; четыре атома, присоединенных к центральному атому углерода в метане и метаноле, направлены к четырем вершинам тетраэдра. Структурная формула неразветвленного октана, одного из компонентов бензина, такова:
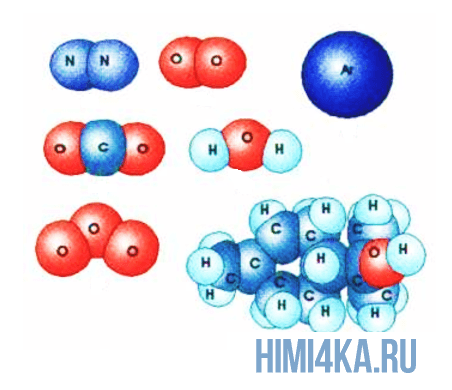
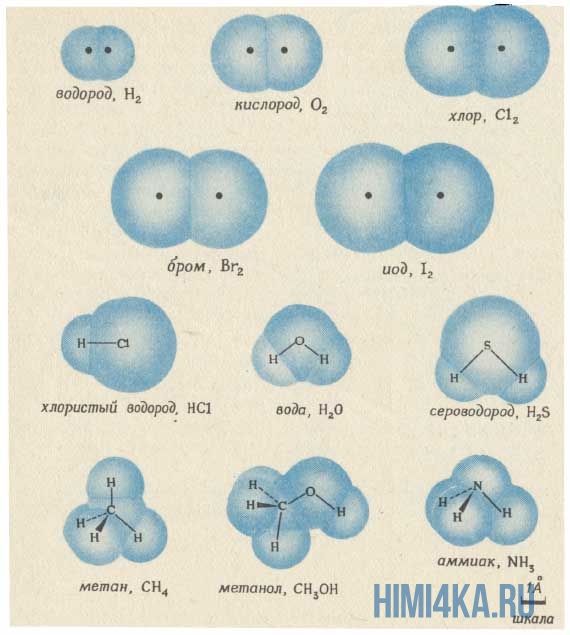
Изображение ниже дает более реальное представление о форме и относительном объеме некоторых простых молекул. Каждая пара связанных атомов как бы проникает друг в друга, потому что их электронные облака перекрываются между собой. Принято изображать молекулы таким образом, что расширяющаяся линия указывает связь, направленную от плоскости рисунка в сторону наблюдателя, а пунктирная линия указывает связь, уходящую за плоскость рисунка в сторону от наблюдателя.
Каждая из указанных выше структурных формул может быть сведена к сжатой молекулярной формуле, которая указывает, сколько атомов каждого элемента имеется в молекуле, но совсем или почти совсем не дает сведений о том, как эти атомы соединены между собой. Молекулярная формула водорода Н2, воды Н2O, сероводорода H2S, аммиака NH3, метана СН4, метанола (метилового спирта) СН3ОН или СН4O, а октана С8Н18. Формула октана может быть также записана в такой форме:
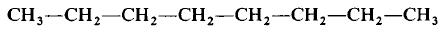
Относительная молекулярная масса вещества
Под молекулярной массой вещества понимается масса молекулы, вычисленная через сумму всех атомных масс, входящих в нее атомов; измеряется, как и атомная масса, в а.е.м. Если молекулярную массу вещества вычислять через относительные атомные массы, то и называться масса молекулы будет относительной молекулярной массой вещества. Относительная молекулярная масса — величина безразмерная.
Пример 1: Какая относительная молекулярная масса у воды?
Решение: Заходим в таблицу Менделеева и выписываем относительные атомные массы водорода и кислорода, округляя до целого значения. У водорода = 1, а у кислорода = 16. Так как молекулярная формула воды имеет вид H2O, то ее молекулярная масса равна:
Ответ: относительная молекулярная масса воды равна 18.
Пример 2: Вычислите молекулярную массу метанола (метилового спирта).
Решение: Молекулярная формула метанола СН3ОН или СН4O. Следовательно,
- 1 углерод: 1 × 12,011 а.е.м. = 12,011 а.е.м.
- 4 водорода: 4 × 1,008 а.е.м. = 4,032 а.е.м.
- 1 кислород: 1 × 15,999 а.е.м. = 15,999 а.е.м.
Ответ: Суммарная молекулярная масса равна 32,04 а.е.м.
В примере 2 следует обратить внимание на то, что естественная атомная масса углерода равна не 12,000, а 12,011 а.е.м., поскольку природный углерод представляет собой смесь, содержащую 98,89% углерода-12 и 1,11% углерода-13, а также следы углерода-14.
Пример 3: Чему равна молекулярная масса чистого октана?
Решение: Молекулярная формула октана С8Н18, поэтому его молекулярная масса равна
Надеюсь урок 3 «Схема образования молекул» был понятным и познавательным. Если у вас возникли вопросы, пишите их в комментарии.
Источник
Способы отображения строения молекул. Формулы. Модели



Теория строения органических соединений М.И. Бутлерова
Основные положения теории химического строения
В 1860-х гг. А. М. Бутлеров сформулировал основные положения, ставшие впоследствии фундаментом теории строения органических соединений. Согласно этой теории:
- атомы в органических молекулах соединены друг с другом в соответствии с валентностью, при этом углерод всегда четырехвалентен;
- порядок соединения атомов в молекуле называется химическим строением;
- свойства веществ определяются не только их составом, но и химическим строением;
- атомы в молекулах оказывают взаимное влияние друг на друга;
- исходя из строения молекулы можно предсказать свойства вещества, и, наоборот, на основании химических свойств можно предсказать строение вещества.
Углеводородные цепи могут быть как открытыми (алициклическими), так и замкнутыми (циклическими), как прямыми, так и разветвленными.
Определение
Гомологи — органические соединения, принадлежащие к одному классу веществ, обладающие сходным строением и свойствами, но отличающиеся друг от друга по составу на одну или несколько групп СНСН2 и отвечающие одной общей формуле.
Способы отображения строения молекул. Формулы. Модели
Структуру вещества, то есть порядок соединения атомов в молекуле, отображает структурная формула, в которой связи между атомами (или группами атомов) изображаются в виде черточек: одна черточка означает одну связь или одну общую электронную пару. Поскольку углерод в органических соединениях всегда четырехвалентен, то каждый атом углерода может образовывать четыре связи (четыре черточки).
По количеству соседних углеродных атомов, атомы углерода в молекуле подразделяются на первичные(один «сосед»), вторичные (два «соседа»), третичные (три «соседа») и четвертичные (четыре «соседа»). Так, концевые атомы в молекуле углеводородов всегда первичные, в линейных молекулах промежуточные атомы — вторичные, а в разветвленных могут появляться третичные и (или) четвертичные атомы углерода.
Для отображения органических молекул используют молекулярные или брутто-формулы, которые представляют собой сокращенную форму записи количественного и качественного состава.
Например, запись СНС2Н6 означает, что молекула вещества состоит из 2 атомов углерода и 6 атомов водорода. Для каждого класса органических соединений можно вывести общую формулу,отвечающую количественному составу всех гомологов. Эту формулу называют общей формулой гомологического ряда.Вещества, принадлежащие к одному классу, отвечают одной общей формуле.
Сравним структурные формулы простейших углеводородов: метана, этана и пропана.
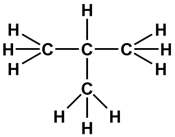
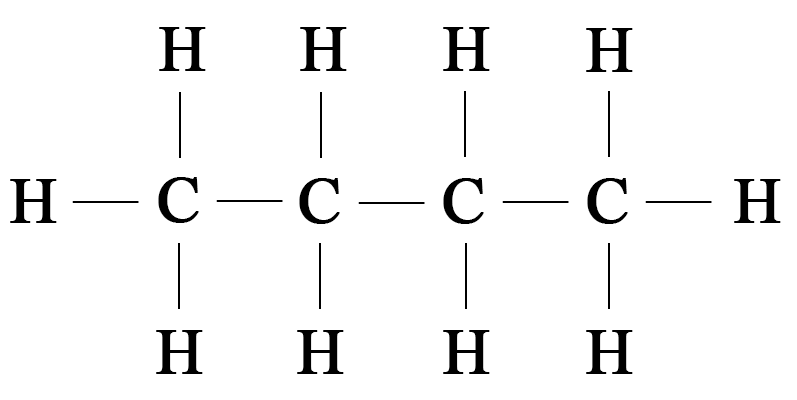
Молекулярная формула метана СН4, этана С2Н6, пропана С3Н8. Видно, что формула этана отличается от формулы метана на одну группу СН2. Аналогично, состав молекул пропана и этана также отличается на одну группу СН2. Следовательно, все эти вещества являются гомологами и относятся к гомологическому ряду метана. Прибавив к формуле пропана указанную гомологическую разницу СН2, получим формулу следующего представителя этого гомологического ряда — С4Н10 (бутан):
Для состава С4Н10 можно изобразить еще одну структурную формулу:
Следовательно, веществ состава С4Н10 должно быть два, каждому из этих веществ соответствует своя структурная формула. Если первое вещество называется бутаном или н-бутаном, то второе — изобутаном. Бутан и изобутан — изомеры, так как у них одинаковый количественный состав, но разный порядок соединения атомов. Подробно с явлением изомерии и изомерами можно познакомиться в теме «Виды изомерии».
Для пространственного отображения структуры молекул органических веществ используют стереохимические формулы.
Стереохимическая формула показывает пространственное расположение атомов в молекулах органических веществ.
Например, пространственное строение этана можно отобразить стереохимической формулой или с помощью проекций Ньюмена, отображающих конформации этана, то есть расположение (поворот) метильных радикалов относительно одинарной С–С-связи:
Более подробно проекции Ньюмена будут рассмотрены в теме «Виды изомерии».

Для наглядности отображения пространственного строения органических молекул используют также разные модели. Наиболее распространенными являются шаростержневые модели, в которых атомы имеют форму шаров, а связи представлены в виде палочек. Одинарная связь — одна палочка, двойная связь — две палочки. Более достоверно истинную структуру молекул отображаютмасштабные (полусферические) модели:
Источник
§ 21. Способы изображения органических соединений
1. Какую информацию можно получить из молекулярной формулы органического соединения?
Молекулярная формула органического соединения показывает, какие атомы и каком количестве присутствуют в данном органическом соединении.
2. Приведены названия и формулы различных веществ: а) оксид углерода(IV) $\mathrm;$ б) дихлорметан $\mathrm;$ в) метан $\mathrm;$ г) карбонат натрия $\mathrm.$ Какие из них относятся к органическим веществам?
К органическим веществам относят: б) дихлорметан $\mathrm
3. Назовите различия между шаростержневыми и масштабными моделями органических соединений.
В шаростержневых моделях атомы изображают в виде трубок из пластмассы и отражают взаимное расположение атомов в пространстве. В масштабных моделях атомы изображают в виде сферы с размерами, пропорциональными их радиусу.
4. Раскройте сущность понятия «химическое строение вещества».
Химическое строение — последовательность соединения атомов в молекулах органических соединений; в молекуле этана, например:
атомы углерода соединены друг с другом, а атомы водорода связаны с атомами углерода.
5. Химическую связь между какими атомами указывает черточка в сокращенной структурной формуле этана $\mathrm<СН_3 - СН_3>?$
В сокращённой структурной формуле этана чёрточка показывает связь между атомами углерода.
6. Укажите общее число атомов в молекуле метана: а) 2; б) 3; в) 4; г) 5.
Общее число атомов в молекуле метана $\mathrm
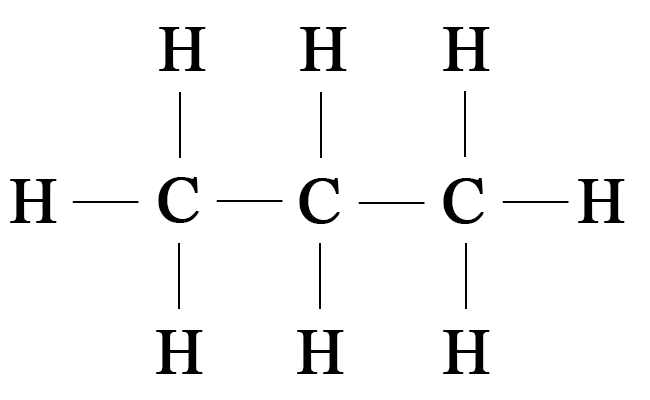
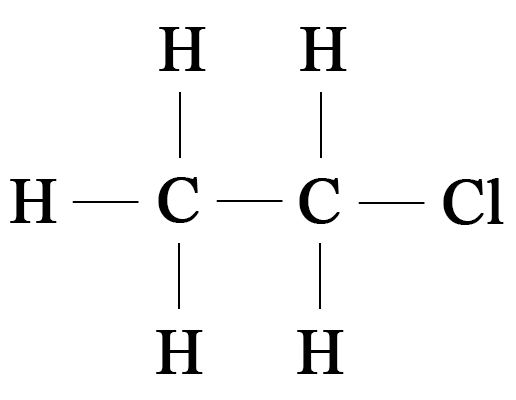
7. Попытайтесь написать структурную формулу органического соединения c молекулярной формулой $\mathrm,$ являющегося производным углеводорода этана.
Структурная формула соединения $\mathrm
8. Изобразите соединение, показанное на рисунке 88, в виде структурной формулы.
Структурная формула отображает порядок (последовательность) соединения атомов в молекулах.
9. На основании пространственного изображения молекулы этана на рисунке 86 попытайтесь изобразить пространственное строение молекулы с молекулярной формулой $\mathrm.$
Пространственное строение молекулы $\mathrm
Источник